Synthèse en solution facile de nanoparticules de phosphore rouge pour les anodes de batteries lithium-ion
Résumé
Le phosphore rouge (RP) a beaucoup attiré l'attention en tant que matériau anodique pour les batteries lithium-ion (LIB) en raison de sa capacité spécifique théorique élevée de 2596 mA h g − 1 et l'abondance de la terre. Cependant, la préparation facile et à grande échelle des nanomatériaux de phosphore rouge via une synthèse de solution reste un défi. Ici, nous développons une méthode de solution simple et facile pour préparer des nanoparticules de phosphore rouge (RP NP). PCl3 réagit facilement avec HSiCl3 en présence d'amines à température ambiante pour produire des NP RP amorphes avec des tailles d'environ 100 à 200 nm avec des rendements élevés. Lorsqu'elle est utilisée comme anode pour batterie lithium-ion rechargeable, l'électrode RP NP présente de bonnes performances électrochimiques avec une capacité réversible de 1380 mA h g − 1 après 100 cycles à une densité de courant de 100 mA g − 1 , et des rendements coulombiens atteignant presque 100 % pour chaque cycle. L'étude montre que cette synthèse de solution est une approche facile et pratique pour la production à grande échelle de matériaux RP NP à utiliser dans des batteries Li-ion hautes performances.
Introduction
On s'est rendu compte depuis longtemps que les combustibles fossiles sont non renouvelables, limités et nocifs pour l'environnement. Les batteries lithium-ion rechargeables (LIB) à haute densité d'énergie et à longue durée de vie ont stimulé un intérêt considérable pour la recherche en raison de leur potentiel en tant que systèmes de stockage d'énergie efficaces et bon marché [1,2,3]. Les demandes croissantes de batteries lithium-ion (LIB) à faible coût avec une densité d'énergie élevée et une longue durée de vie nécessitent le développement de nouveaux matériaux d'électrode [4,5,6,7]. L'anode en graphite traditionnelle, couramment utilisée dans les batteries lithium-ion, est limitée par ses faibles capacités (372 mA h g − 1 ) [8, 9]. Pour résoudre ce problème ou cette question, de nombreux efforts ont été consacrés à l'exploration et au développement de matériaux d'anode alternatifs avec une capacité et une efficacité coulombienne sensiblement améliorées [10,11,12,13,14,15,16,17]. Parmi une large gamme de matériaux d'anode à haute capacité, le phosphore et ses composites présentent des applications potentielles en raison de son faible coût, de son abondance et de sa capacité spécifique théorique élevée (≈ 2600 mA h g − 1 ) [18,19,20,21,22].
Le phosphore a trois allotropes, le P blanc, le P noir et le P rouge [23]. Le blanc P est toxique et chimiquement instable, et ne convient pas à l'application dans les LIB. Le noir P a une bonne stabilité thermodynamique et conductivité, mais le processus de préparation complexe limite ses applications à grande échelle [24,25,26]. Parmi ces trois allotropes différents, le rouge P est le candidat le plus prometteur [27] pour la prochaine génération de matériaux anodiques à haute énergie en raison de sa stabilité et de son abondance. Cependant, le rouge P est en proie à sa mauvaise conductivité électronique (10 − 12 S m − 1 ) et un changement de volume drastique (300 %) au cours du processus de lithiation-délithiation lorsqu'il servait d'anodes pour les LIB rechargeables [28, 29].
Pour contourner ces obstacles, le rouge P a été encapsulé dans différents types de matériaux hôtes en carbone [30,31,32,33,34,35,36] pour améliorer considérablement les performances électrochimiques des anodes rouges P pour les LIB. Par exemple, Li et al. a considérablement amélioré les performances de stockage du lithium et du sodium du P rouge en confinant du P rouge amorphe nanométrique dans une matrice de carbone mésoporeux (P@CMK-3) via un processus de vaporisation-condensation-conversion [37]. Ruan et al. a conçu une nouvelle stratégie pour intégrer des particules de P rouge dans un film de carbone structurel de réticulation (film P-C) à utiliser comme anode flexible sans liant dans les LIB, afin d'améliorer la conductivité électronique et de s'adapter à l'expansion de volume [38]. Néanmoins, le taux de chargement du P rouge dans les matériaux composites préparés par la méthode de vaporisation-condensation est généralement faible, ce qui est défavorable pour l'application pratique [39, 40]. À cette fin, l'utilisation de nanoparticules ou de nanostructures creuses de P rouge préparées par le contrôle de la taille et l'ingénierie morphologique [41, 42] ont été considérées comme des stratégies efficaces pour s'adapter à la grande contrainte induite par l'expansion volumique et éviter la pulvérisation du matériau. Par exemple, Chang et al. développé une synthèse à grande échelle de nanoparticules de phosphore rouge (RPNP) par réduction de PI3 dans l'iodobenzène par l'éthylène glycol en présence de CTAB. Les électrodes RPNP obtenues présentaient une capacité spécifique élevée, une longue durée de vie et une excellente capacité de débit en tant qu'anodes pour les LIB [43]. De plus, Zhou et al. ont rapporté une méthode solvothermique humide pour synthétiser des nanosphères creuses de phosphore rouge avec des coquilles poreuses. Les électrodes à nanosphères creuses P obtenues ont démontré des capacités élevées et d'excellentes performances à long cycle en raison des mérites des structures poreuses et creuses [44]. Même si plusieurs littératures ont rapporté les méthodes de synthèse à grande échelle du phosphore rouge, le développement d'une méthode facile à haut rendement et à faible coût pour préparer le phosphore rouge est toujours hautement souhaitable. En particulier, la préparation du nanomatériau de phosphore rouge via une synthèse en solution reste un défi.
Nous rapportons ici une approche simple, rapide et nouvelle basée sur une solution pour synthétiser des NP RP, en utilisant une réaction à température ambiante de PCl3 avec HSiCl3 en CH2 Cl2 en présence d'amines. Cette nouvelle solution offre une approche rentable pour la production massive de nanoparticules de phosphore rouge à utiliser dans les batteries lithium-ion.
Méthodes
Matériaux
Trichlorosilane (HSiCl3 ) a été acheté auprès de TCI. n-Tripropylamine (Pr3 N) a été obtenu auprès d'Aladdin. Trichlorure de phosphore (PCl3 ) a été acheté auprès de Sinopharm Chemical Reagent Co. Ltd. Dichlorométhane (CH2 Cl2 ) a été séché sur CaH2 Avant utilisation. Tous les autres réactifs chimiques ont été utilisés tels quels sans autre purification.
Synthèse de nanoparticules de phosphore rouge
Dans une préparation typique, 0,55 mL de Pr3 N et 0,5 mL de HSiCl3 ont été ajoutés dans 20 mL de CH2 anhydre Cl2 . La solution incolore formée a été agitée magnétiquement pendant une nuit à température ambiante, pendant laquelle la couleur est devenue jaune clair. Et puis 0,5 mL de PCl3 ont été ajoutés à la solution. Des nanoparticules de phosphore rouge (RP NP) ont été obtenues en quelques secondes. Les produits ont été centrifugés, séparés et lavés avec du CH2 anhydre Cl2 , 1 M de HF et de l'eau distillée pour éliminer le PCl3 n'ayant pas réagi et de la silice.
Mesures électrochimiques
Les propriétés électrochimiques des nanoparticules de phosphore rouge en tant que matériaux d'anode dans les LIB ont été étudiées en utilisant un assemblage de pile bouton 2032 avec des feuilles de lithium métalliques servant de contre-électrodes. Les cellules CR2032 ont été assemblées dans une boîte à gants remplie d'argon (tous deux H2 O et O2 < 0,1 ppm). L'électrode de travail a été préparée en mélangeant un matériau actif (RP NP), du graphite conducteur et de la carboxyméthylcellulose sodique (CMC) dans un rapport pondéral de 5:3:2 dans de l'eau déminéralisée pour former une suspension homogène, qui a ensuite été déposée à la lame sur un Feuille de cuivre. Après séchage à 80 °C pendant 12 h sous vide, la feuille a été découpée en disques de 14 mm de diamètre. La charge massique totale de matériaux actifs sur l'électrode était de ~ 0,5 mg cm − 2 . L'électrolyte était de 1,0 M LiPF6 dans un mélange de 1:1 (v /v ) carbonate d'éthylène/carbonate de diéthyle (Shenzhen Kejingstar Technology Ltd., Chine). Les profils de charge-décharge des demi-cellules ont été enregistrés à l'aide d'un appareil de test de batterie Neware (Shenzhen, Chine) en mode courant constant.
Caractérisation
La diffraction des rayons X sur poudre (PXRD) a été réalisée sur un diffractomètre à rayons X Bruker D8 avec un rayonnement Cu Kα (λ = 1,5418 Å). Des images de microscopie électronique à balayage (MEB) et des spectres de spectroscopie à dispersion d'énergie (EDS) (des plaquettes de silicium comme substrat) ont été obtenues sur un microscope électronique à balayage à émission de champ Hitachi (S-4800). La microscopie électronique à transmission (MET) et la MET à haute résolution (HR) ont été réalisées avec un équipement JEM-2100 (Japon). N2 les isothermes d'adsorption ont été collectés à 77 K (analyseur Micromeritics ASAP 2020) après dégazage sous vide de l'échantillon à 100 °C pendant 10 h. La spectroscopie Raman (LabRAM Aramis, Horiba, équipée d'un laser à 633 nm) a été utilisée pour étudier la structure des NP RP. Les mesures de spectroscopie photoélectronique à rayons X (XPS) ont été enregistrées avec un PHI 5000 VersaProbe. Des analyses thermogravimétriques (TG) ont été effectuées sur un analyseur thermique simultané STA449F3 (Netzche) sous un écoulement de N2 . Les courbes I-V des NP RP ont été mesurées à l'aide de l'instrument de la station de sonde cryogénique Biologic VMP3 (CRX-4K, Lake Shore, USA). Des tests de voltamétrie cyclique (CV) ont été effectués sur une station électrochimique CHI650d (Shanghai Chenhua Instruments Inc., Chine).
Résultats et discussion
Synthèse et caractérisation des RPNP
Les nanoparticules de phosphore rouge (appelées NP RP) ont été synthétisées via une méthode de solution facile, qui est représentée dans le schéma 1. Nous avons constaté que le trichlorure de phosphore (PCl3 ) réagit facilement avec HSiCl3 prémélangé et tripropylamine (Pr3 N) en CH2 Cl2 à température ambiante pour produire des poudres oranges en quelques secondes. La couleur de la solution a viré à l'orange très rapidement lors du mélange d'une solution de HSiCl3 –Pr3 N–CH2 Cl2 avec PCl3 , indiquant la formation de RP NP (Fichier supplémentaire 1 :Figure S1). Nous avons postulé que PCl3 ont été réduits par des chlorures d'oligosilane subvalents pour former les nanoparticules de phosphore. Les chlorures d'oligosilane ont été formés par la réaction de HSiCl3 avec de la tripropylamine (Pr3 N) en CH2 Cl2 résultant de la réaction de dismutation de HSiCl3 en présence de catalyseurs aminés [45,46,47]. Il est à noter que les intermédiaires oligosilanes préformés étaient essentiels pour l'apparition de la réaction. Sans amines (Pr3 N), la réaction de HSiCl3 avec PCl3 n'a pas pu avoir lieu à température ambiante. De même, le Pr3 N n'a pas pu réagir avec PCl3 pour produire des NP RP à température ambiante. Le rendement des NP RP, basé sur la quantité d'atomes de P dans PCl3 , était d'environ 38 %, ce qui est beaucoup plus élevé que la littérature rapportée [43]. De plus, cette approche en phase de solution utilise PCl3 relativement peu coûteux au lieu de PI3 dans l'iodobenzène, qui pourrait être plus économiquement et plus facilement étendu pour obtenir de grandes quantités de NP RP. La couleur des RPNP était orange clair, différente de la couleur rouge foncé du RP commercial (Fichier supplémentaire 1 :Figure S2).
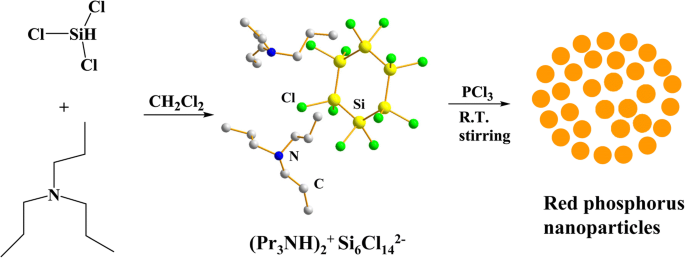
Illustration schématique du processus de synthèse des NPs RP
L'analyse PXRD a montré que le produit était du phosphore rouge. Comme le montre la figure 1a, les trois pics de diffraction élargis à 13-16°, 25-38° et 47-65°, cohérents avec le modèle XRD de RP commercial rapporté dans la littérature [21, 36]. Les images SEM montrent que la majorité des NP RP synthétisées présentaient une forme sphérique irrégulière avec des tailles d'environ 100 à 200 nm de diamètre. Le modèle SAED correspondant des RP NP (image en médaillon de la figure 2b) a révélé que les RP NP étaient de structure amorphe. Les spectres Raman des NP RP présentaient trois pics plissés entre 300 et 500 cm − 1 , ce qui est cohérent avec le spectre Raman de la RP commerciale rapporté dans la littérature [36]. Les trois pics peuvent être bien attribués aux modes de flexion des liaisons (mode fondamental B1), aux vibrations de flexion des liaisons (mouvement d'étirement symétrique A1) et aux vibrations d'étirement (mode dégénéré E1) du rouge amorphe P (Fig. 1b). L'analyse thermogravimétrique (TGA) des RPNP de la figure 3a montre une perte de poids importante entre 380 et 430 °C sous atmosphère d'azote en raison de la sublimation, tandis que le RP commercial montre une perte de poids importante entre 450 et 500 °C. La baisse observée de la température de sublimation des NP RP peut résulter des rapports surface/volume élevés des nanoparticules [43, 48]. Pour obtenir quantitativement l'information de surface, N2 des mesures de sorption (Fig. 3b) ont été effectuées. Les résultats ont révélé que la surface Brunauer-Emmett-Teller (BET) des NP RP était d'environ 37 m 2 g − 1 , ce qui est beaucoup plus important que celui du RP commercial.
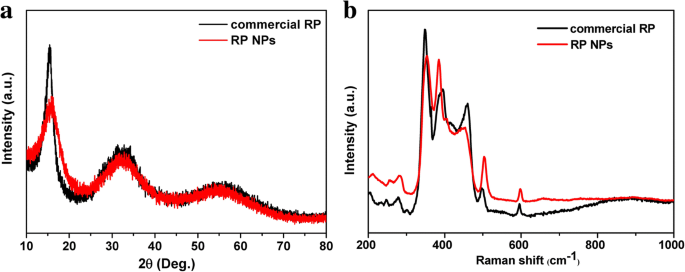
Caractérisation des RPNP. un Modèles XRD de RPNP et RP commercial. b Spectres Raman des RPNP et RP commercial

Morphologie des NP RP. un Images SEM de RP NPs. b Images MET de RP NP. L'image en médaillon est le motif SAED
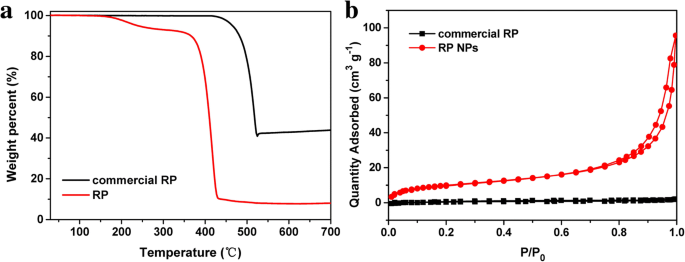
un ATG des NPs RP et RP commerciale. b N2 isothermes d'adsorption des NPs RP et RP commercial
Afin de caractériser davantage les structures, les compositions et les états chimiques des NP RP préparées, des mesures de spectroscopie à rayons X à dispersion d'énergie (EDS) et de spectroscopie photoélectronique à rayons X (XPS) ont été effectuées (Fig. 4). Les spectres EDS montrent que les NP RP sont presque entièrement composées de phosphore élémentaire. Le spectre du relevé XPS (Fig. 4b) confirme en outre que P est l'élément dominant. Le pic principal du spectre P 2p de XPS pourrait être déconvolué en deux pics à 129,74 et 130,74 eV, qui correspondent au 2p3/2 et 2p1/2 de P dans la liaison P–P, respectivement, selon la littérature précédente [49, 50]. De plus, un pic faible à 133,50 eV pourrait être attribué à la liaison P–O qui s'est peut-être formée par oxydation de surface lors de l'exposition à l'air. Par conséquent, les résultats ci-dessus indiquent que les nanoparticules préparées sont des P rouges amorphes. De plus, les courbes courant-tension (I-V) des NP RP ont été mesurées, comme indiqué dans le fichier supplémentaire 1 :Figure S3. La conductivité des RPNP est d'environ 1,7 × 10 − 7 S m − 1 (0–2 V), soit 10 5 fois plus élevé que le RP commercial (10 − 12 S m − 1 ).
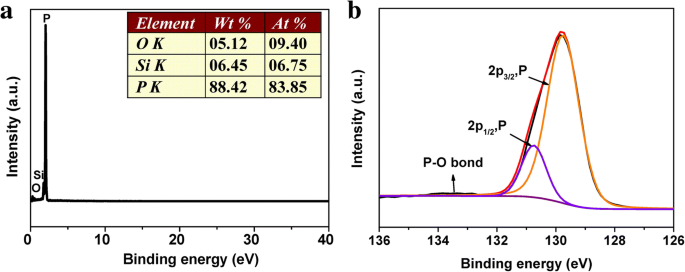
un Spectres EDS des NP RP. b Spectre XPS P 2p des NP RP
Les performances électrochimiques des NP RP en tant que matériaux d'anode dans les LIB ont été testées dans des piles bouton CR2032 en utilisant une feuille de lithium métallique comme contre-électrode dans les tensions de fonctionnement de 0,01 à 2,5 V. La figure 5a illustre les courbes CV typiques des NP RP lors d'un balayage taux de 0,1 mV s − 1 . Il y a un large pic dans le premier cycle de lithiation, qui est attribué au processus d'activation d'insertion d'ions Li dans le phosphore. Quelques pics redox situés à 0,5-0,75 V et 1,0-1,25 V sont attribués respectivement à la lithiation du P et à la délithiation des alliages P-Li [32, 51, 52]. L'écart entre la première et les suivantes courbes cathodiques implique une perte de capacité irréversible, qui pourrait être attribuée à la formation de l'interface d'électrolyte solide (SEI) ainsi qu'à l'apparition de réactions secondaires sur les surfaces des électrodes, telles que des réactions secondaires de défaut sites, l'oxygène de surface et les impuretés de l'eau [36, 37, 53], un comportement couramment observé pour les anodes LIB. La figure 5b montre les profils de tension de décharge-charge typiques de l'électrode RP NPs pour les 3 premiers cycles à une densité de courant de 0,1 A g − 1 . Les plateaux de tension de décharge et de charge courts apparents à environ 0,7 V et 1,1 V sont dus à la lithiation et à la délithiation des composants RP NPs, respectivement, qui sont en bon accord avec les résultats CV. L'électrode a fourni des capacités de décharge et de charge spécifiques de 2818 et 1641 mA h g − 1 , respectivement, pour le premier cycle, donnant un premier rendement coulombien de 58,2%. La diminution de la capacité de charge pourrait être attribuée à la formation irréversible de la membrane SEI. On constate que l'efficacité coulombienne des NPs RP augmente ensuite rapidement jusqu'à 100 % après le deuxième cycle. Les NP RP présentaient une décroissance de capacité évidente au cours des 3 premiers cycles. La capacité irréversible dans les premières étapes de décharge-charge résultait de la décomposition de l'électrolyte, qui a provoqué la formation de SEI sur la surface de l'électrode et la consommation de Li-ion. De plus, les nanoparticules possèdent une grande surface spécifique en contact avec la solution d'électrolyte, ce qui entraînerait plus de réactions secondaires, diminuant l'efficacité coulombienne initiale dans le premier cycle [54].
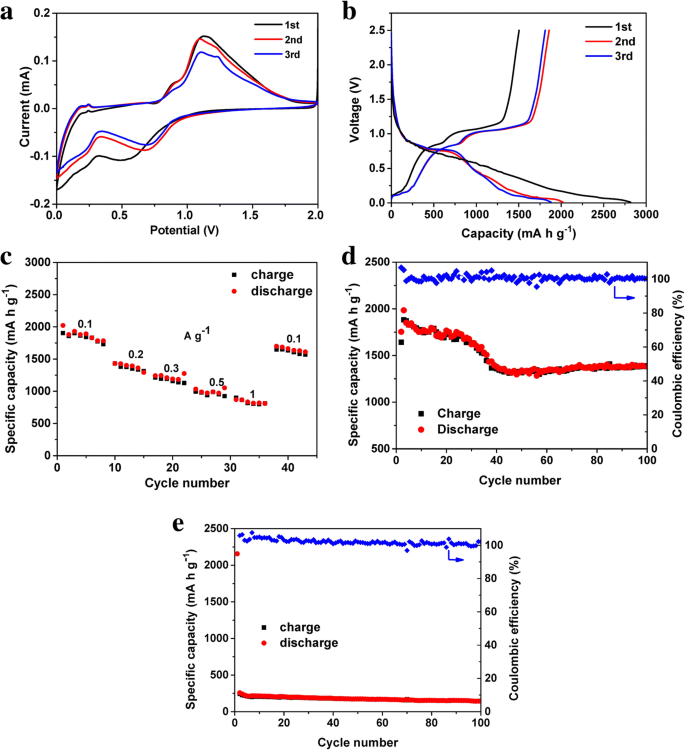
Performances électrochimiques des RPNP. un Courbes CV des RPNP. b Profils de tension des RPNP. c Taux de performance des RPNP cyclés à différentes densités de courant. d Performances de cyclisme des RPNP à un taux de 0,1 A g − 1 . e Performances de cyclisme du RP commercial à un taux de 0,1 A g − 1
La vitesse typique et les performances de stabilité de cycle à long terme de l'électrode RP NPs sont illustrées aux Fig. 5c, d, respectivement. Les RPNP ont fourni les capacités de charge spécifiques de 1801, 1430, 1245, 1227, 1184 et 871 mA h g − 1 aux taux de 0,1, 0,2, 0,3, 0,5 et 1 A g − 1 , respectivement. L'électrode a montré une bonne réversibilité du taux, avec la capacité de décharge spécifique récupérée à la valeur initiale lorsque la densité de courant est revenue à 0,1 A g − 1 après avoir fait du vélo à des densités de courant élevées. Les NP RP ont finalement maintenu une capacité de décharge réversible élevée de 1380 mA h g − 1 , c'est-à-dire la rétention de 89,1 %, après 100 cycles avec des rendements coulombiens proches de 100 % tout au long des mesures. Par rapport au RP commercial (Fig. 5e), les NP RP ont montré une stabilité de cycle à long terme bien améliorée.
Conclusions
En résumé, nous avons développé une nouvelle approche en phase solution facile pour synthétiser des nanoparticules de phosphore rouge par la réaction de PCl3 et HSiCl3 en présence d'amines dans le milieu ambiant. Les RP NP présentaient de bien meilleures performances électrochimiques avec une capacité réversible élevée et une stabilité de cycle à long terme que les RP commerciales lorsqu'elles servaient d'anodes pour une batterie lithium-ion rechargeable. Les électrodes RP NPs ont maintenu une capacité de décharge réversible élevée de 1380 mA h g − 1 (rétention de 89,1 %) après 100 cycles, avec une efficacité coulombienne proche de 100 % pour chaque cycle. Cette méthode de préparation simple ouvre la voie à une production rentable de NP RP en tant qu'anodes hautes performances pour l'industrie des batteries lithium-ion.
Abréviations
- CH2 Cl2 :
-
Dichlorométhane
- CV :
-
Voltamétrie cyclique
- EDS :
-
Spectroscopie à dispersion d'énergie
- HSiCl3 :
-
Trichlorosilane
- PCl3 :
-
Trichlorure de phosphore
- Pr3 N :
-
n-Tripropylamine
- PXRD :
-
Diffraction des rayons X sur poudre
- NPs RP :
-
Nanoparticules de phosphore rouge
- SEM :
-
Microscopie électronique à balayage
- TEM :
-
Microscopie électronique à transmission
- TG :
-
Thermo gravimétrique
- XPS :
-
Spectroscopie photoélectronique aux rayons X
Nanomatériaux
- Nanocristaux d'étain pour la future batterie
- Anode nano et batterie :un examen
- Synthèse facile et propriétés optiques de petits nanocristaux et nanotiges de sélénium
- Synthèse facile de nanoparticules SiO2@C ancrées sur MWNT en tant que matériaux anodiques hautes performances pour batteries Li-ion
- Membranes composites contenant des nanoparticules d'échangeurs d'ions inorganiques pour le dessalement électrodialytique du glycérol
- Synthèse facile de composite CuSCN coloré et conducteur revêtu de nanoparticules CuS
- Croissance directe de structures de ZnO ressemblant à des plumes par une technique de solution facile pour une application de détection photo
- Nanoparticules de silice pour l'administration de protéines intracellulaires :une nouvelle approche de synthèse utilisant la protéine fluorescente verte
- Une solution immersive pour des batteries EV thermiquement plus sûres



