Le poly (acide γ-glutamique) favorise la déchloration améliorée du p-chlorophénol par les nanoparticules de Fe-Pd
Résumé
Le fer à valence nulle à l'échelle nanométrique (nZVI) s'est révélé très prometteur dans le traitement des composés organiques chlorés, mais une agrégation et une inactivation rapides entravent son application. Dans cette étude, des nanoparticules de fer à valence nulle dopées au palladium impliquant de l'acide poly (γ-glutamique) (Fe-Pd@PGA NPs) ont été synthétisées. Les nanoparticules étaient petites (~ 100 nm), uniformément réparties et très stables. Les performances de déchloration des NP Fe-Pd@PGA ont été évaluées à l'aide de p -CP comme modèle. Les résultats ont démontré que les NP Fe-Pd@PGA présentent une activité élevée même dans des conditions faiblement alcalines. La constante de vitesse maximale a atteint 0,331 min − 1 à pH 9,0 avec un Fe à p -Ratio CP de 100. De plus, l'activité de déchloration des NP Fe-Pd@PGA est plus de dix fois supérieure à celle des NP Fe-Pd nues, démontrant le rôle crucial de la PGA dans ce système. De plus, nous avons étudié les performances de déchloration en présence de différents anions. Les résultats ont indiqué que les NP Fe-Pd@PGA peuvent maintenir une activité élevée en présence de Cl − , H2 Bon de commande4 − , et l'acide humique, tandis que HPO4 2− et HCO3 − les ions réduisent légèrement l'activité de déchloration. Nous pensions que le PGA est un stabilisateur et un promoteur prometteur pour les NP Fe-Pd et que les NP Fe-Pd@PGA ont le potentiel pour des applications pratiques.
Contexte
La pollution de l'eau a soulevé des préoccupations mondiales sur la durabilité de l'environnement et de nombreux matériaux de haute performance ont été développés pour les traitements efficaces de la pollution [1,2,3,4,5]. Le fer à valence nulle à l'échelle nanométrique (nZVI) a fait l'objet d'études approfondies et est considéré comme l'un des nanomatériaux les plus prometteurs pour l'assainissement de l'environnement de divers contaminants, tels que les composés organiques chlorés, les ions de métaux lourds, les pesticides et les colorants organiques [1, 6, 7 ]. Il a l'extraordinaire capacité de transformer les contaminants toxiques en formes non toxiques grâce à des processus de réduction chimique, mais les nanoparticules nZVI réagissent facilement avec l'eau et perdent des électrons qui contribuent à la réaction de dégradation [8]. Par conséquent, un autre métal a toujours été utilisé comme dopant pour produire une nanoparticule bimétallique, telle que Fe-Pd ou Fe-Ni, pour augmenter les taux de dégradation [9, 10]. Cependant, il existe des forces de van der Waals et des forces magnétiques attractives entre les particules nZVI, qui conduisent à une agrégation importante, entravant leur transport dans les aquifères contaminés et altérant la réactivité [11, 12]. Les défauts intrinsèques du nZVI, même des systèmes bimétalliques, pourraient affaiblir l'effet d'élimination et limiter la faisabilité de l'utilisation.
Pour inhiber l'agrégation, des efforts considérables ont été faits pour appliquer des stabilisants de surface polymères (par exemple, des polysaccharides, des polyélectrolytes et des tensioactifs). Ces stabilisateurs pourraient fournir à la fois une répulsion électrostatique et stérique pour empêcher l'agrégation des particules [13]. Par exemple, He et al. [14] ont synthétisé du nZVI stabilisé par de la carboxyméthylcellulose (CMC) et les nanoparticules dérivées ont été utilisées avec succès pour la destruction in situ d'éthènes chlorés, tels que le trichloroéthylène (TCE) et les polychlorobiphényles (PCB). Petersen et al. [15] ont produit du nZVI en présence de poly (acide acrylique) (PAA), atteignant un taux de dégradation élevé pour les contaminants chlorés. Liu et al. [16] ont synthétisé le nZVI stabilisé au CMC et au polyacrylamide anionique (APAM) et ont observé que la modification de l'APAM conduisait à l'agrégation de nZVI en suspension, tandis que la modification de CMC permettait de bien disperser le nZVI. Cette étude a fourni la preuve que la structure moléculaire a joué un rôle important dans l'effet de modification de nZVI. De nombreux autres types différents de modificateurs macromoléculaires ont été utilisés pour enrober les particules nZVI. [17] En plus du problème d'agrégation, un autre problème est la passivation de surface due à la formation de couches d'oxyde, telles que la goethite (α-FeOOH), la maghémite (γ-Fe2 O3 ), et l'hématite (α-Fe2 O3 ). Des études antérieures ont démontré que des conditions acides favorisent l'évitement de la passivation de surface du nZVI et le maintien de son activation de surface [18,19,20]. Par conséquent, la valeur du pH est un paramètre crucial qui affecte la formation de la couche d'oxyde. De nombreux rapports ont étudié la réaction dans des conditions acides pour améliorer l'efficacité de la déchloration [21, 22]. De plus, l'inactivation rapide causée par les anions communs et l'acide humique (HA, matière organique couramment trouvée dans l'eau [23]) a également limité l'application sur le terrain de nZVI [24, 25]. Par conséquent, des matériaux à base de nZVI adaptés aux conditions alcalines avec différents anions sont attendus.
Le poly (acide γ-glutamique) (PGA), un polypeptide anionique naturel produit par Bacillus subtilis, est non toxique, hautement soluble dans l'eau et peut être chimiquement, physiquement et enzymatiquement dégradé dans la nature. Il est composé d'unités d'acides l- et d-glutamiques liées à des amides entre l'acide -aminé et l'acide -carboxylique [26]. Il a de larges applications dans les industries alimentaires, chimiques, biologiques et médicales [27,28,29]. De plus, le PGA est un biosorbant potentiel pour l'élimination et la récupération des métaux lourds des eaux usées en raison de sa capacité à lier les ions métalliques. Par exemple, Jamiu et al. [30] ont synthétisé une résine à base de PGA comme sorbant pour séquestrer le Co 2+ ions de la solution aqueuse. Hu et al. [31] ont développé un sorbant biocomposite incorporant du PGA pour l'adsorption et la récupération de Cu 2+ ions. Bodnar et al. [32] ont décrit la préparation de nanoparticules biodégradables basée sur la complexation de PGA avec Pb 2+ ions, démontrant que le PGA était un sorbant prometteur pour l'élimination des métaux lourds dans l'eau polluée. Tenant compte du fait que le PGA anionique a des groupes carboxyle abondants, qui peuvent fournir une répulsion électrostatique et stérique pour empêcher l'agrégation des particules, ainsi qu'une capacité de liaison élevée envers les ions métalliques via la chélation et la liaison électrostatique [33, 34], nous avons tenté de l'utiliser comme un stabilisant et un agent de coordination pour synthétiser les NP Fe-Pd et chélater davantage Fe 2+ /Fe 3+ ions générés par la corrosion des NPs Fe-Pd. Nous supposons que le PGA peut améliorer les performances des NP Fe-Pd dans des conditions alcalines avec différents anions.
Ici, nous avons synthétisé les nanoparticules Fe-Pd modifiées par PGA (notées Fe-Pd@PGA NPs). Les nanoparticules ont été caractérisées par microscopie électronique à balayage (MEB), microscopie électronique à transmission (MET), diffraction des rayons X (XRD) et spectroscopie infrarouge à transformée de Fourier (FTIR). La stabilité colloïdale des NP Fe-Pd@PGA a également été évaluée. De plus, p -Chlorophénol (p -CP) (l'un des dérivés phénoliques les plus toxiques [35,36,37]) a été sélectionné comme polluant modèle pour évaluer l'activité de déchloration des NPs Fe-Pd@PGA. La déchloration de p -CP sur les NPs avec différentes doses de PGA et de charge Pd a été étudiée. Il convient de mentionner que toutes les expériences ont été menées dans des conditions faiblement alcalines sans contrôle du pH (la valeur du pH était d'environ 9). De plus, nous avons également étudié la déchloration de p -CP en présence de différents anions et HA pour évaluer leur utilisation potentielle dans les eaux usées réelles.
Méthodes
Matériaux
PGA (MF 100 000 à 50 000 kDa) a été acheté à Yuanye Bio-Technology (Shanghai, Chine). Sulfate ferreux heptahydraté (FeSO4 ·7H2 O,> 99,0%), borohydrure de potassium (KBH4 , 97%), chloropalladite de potassium (K2 PdCl4 , 98 %), et p -chlorophénol (p -CP, 99%) ont été fournis par Aladdin Reagent Company (Shanghai, Chine). Méthanol (CH3 OH, qualité HPLC, 99,9 %) a été acheté auprès de Concord Technology (Tianjin, Chine). Chlorure de sodium (NaCl, 99%), bicarbonate de sodium (NaHCO3 , 99,7%), hydrogénophosphate disodique (Na2 HPO4 , 99 %), et le dihydrogénophosphate de sodium (NaH2 Bon de commande4 , 99 %) ont été achetés auprès de Chemregeant (Tianjin, Chine). L'acide humique (HA, technique) a été acheté chez Heowins (Tianjin, Chine). Tous les produits chimiques ont été utilisés sans autre purification. Toute l'eau a été purifiée par un système de purification d'eau Sartorius arium pro VF (18,2 MΩ de résistivité).
Préparation des NP Fe-Pd@PGA
Les NP Fe-Pd@PGA ont été synthétisées en utilisant une méthode de réduction chimique dans laquelle le borohydrure de potassium a servi de réactif de réduction. Ensuite, 250 mg de FeSO4 ·7H2 O a été ajouté dans 50 mL de solution de PGA contenant différentes masses de PGA (10, 25, 50 et 70 mg), ce qui a donné les concentrations souhaitées de Fe 2+ et PGA (% en poids). Le mélange a ensuite été purgé à l'argon pendant environ 20 min pour assurer la formation de Fe 2+ -Complexe PGA et pour éliminer l'oxygène dissous (OD). Ensuite, 3 mL de KBH4 (50 mg mL − 1 ) a été injecté dans le mélange à un BH4 -à-Fe 2+ rapport molaire de 3,0 pour former les Fe NPs. Pour assurer l'utilisation efficace du réducteur, la suspension a été purgée avec de l'argon pendant 15 min jusqu'à ce que le dégagement de gaz (hydrogène) cesse. Ensuite, les nanoparticules de Fe ont été testées sous forme de particules monométalliques ou chargées de traces (0,1, 0,2, 0,4 et 0,8 % en poids de Pd/Fe) de Pd pour produire les nanoparticules bimétalliques stabilisées par PGA en ajoutant des quantités connues de solution aqueuse de chloropalladite de potassium. dans la suspension de nanoparticules. De plus, des NP Fe-Pd nues avec différents degrés de charge de Pd ont également été préparées à des fins de comparaison. Le système a été constamment purgé à l'argon pendant la réaction de synthèse et de déchloration. La température de la solution a été maintenue à 25°C par un bain-marie thermostaté.
Test de stabilité
Pour les expériences de sédimentation, les suspensions de Fe-Pd@PGA NPs préparées à la dernière étape ont été transférées du réacteur dans un tube en verre de 50 mL. La suspension a été agitée sans sonication avant l'expérience. Ensuite, le tube de verre de 50 mL a été laissé à décanter et l'étendue de la sédimentation a été enregistrée en prenant des photos des tubes de verre à intervalles réguliers.
Expériences de déchloration par lots
Les 550 mg L − 1 solution mère de p -CP a été préparé en dissolvant p -CP dans l'eau à 25°C. De plus, 2 mL de p -La solution mère de CP a été ajoutée à la suspension Fe-Pd préparée pour obtenir le rapport molaire initial souhaité de Fe à p -CP (105:1) et p initial -Concentration en CP de 20 mg L − 1 . Ensuite, la dégradation de p -CP a été initié et la réaction a été réalisée avec la purge d'argon. Pour la mesure de la concentration de p -CP, 0,8 mL d'échantillon liquide a été prélevé de la solution aux moments sélectionnés souhaités, puis un aimant a été utilisé pour accélérer la sédimentation. Le surnageant liquide a ensuite été filtré à travers un filtre à membrane à seringue (0,22 μm) et encore testé avec une chromatographie liquide à haute performance (HPLC). Tous les points expérimentaux ont été dupliqués dans deux expériences consécutives, et les écarts types ont été calculés.
p -Tests d'élimination de CP dans les eaux souterraines simulées
Dans ces tests, la concentration initiale de p -CP a été défini sur 20 mg L − 1 , identique à la concentration précédente des expériences de déchloration par lots, les concentrations d'anions ont été fixées à 1 mM et 5 mg/L d'acide humique ont été ajoutés à la suspension pour simuler une situation d'eau souterraine naturelle. La recette d'eau souterraine simulée est composée de différents types d'anions après avoir ajouté différents types de sels inorganiques, y compris NaCl (0,1 mM), Na2 HPO4 ·12H2 O (0,1 mM), NaH2 Bon de commande4 (0,1 mM) et NaHCO3 (1 mm). Le pH de la suspension réactionnelle a également été enregistré pendant la réaction.
Caractérisation
La microscopie électronique à balayage (SEM, Hitachi S-4800) et la microscopie électronique à transmission haute résolution (HRTEM, JEM-2100F) ont été utilisées pour étudier la morphologie et la taille des NP Fe-Pd nues et modifiées par PGA. Les échantillons HRTEM ont été dilués et traités aux ultrasons dans de l'éthanol, puis la suspension résultante a été déposée sur les grilles de cuivre recouvertes de carbone et séchées à température ambiante. La mesure par diffraction des rayons X (XRD) a été réalisée à l'aide d'un instrument de mesure Bruker D8-Focus avec une source de rayons X Cu Kα. Des analyses de spectroscopie infrarouge à transformée de Fourier (FTIR, Nicolet Nexus 670) ont été menées pour élucider l'interaction entre les NP Fe-Pd et PGA. Les échantillons mentionnés précédemment pour la section « Caractérisation » ont été lavés trois fois avec de l'eau et de l'alcool, puis séchés dans une étuve sous vide à température ambiante et conservés. Le p -La concentration de CP en solution a été mesurée par HPLC.
Résultats et discussion
Synthèse et caractérisation des NP Fe-Pd@PGA
Comme le montre le schéma 1, les NP Fe de valence zéro (NP Fe@PGA) ont été synthétisées en réduisant Fe 2+ avec KBH4 en présence de PGA. Après cela, les NP Fe-Pd@PGA ont été obtenues via la réaction de remplacement entre Pd 2+ (K2 PdCl4 ) et Fe 0 . Pour évaluer l'activité de déchloration, p -CP a été sélectionné comme polluant modèle, et le processus de déchloration est également montré dans le schéma 1.
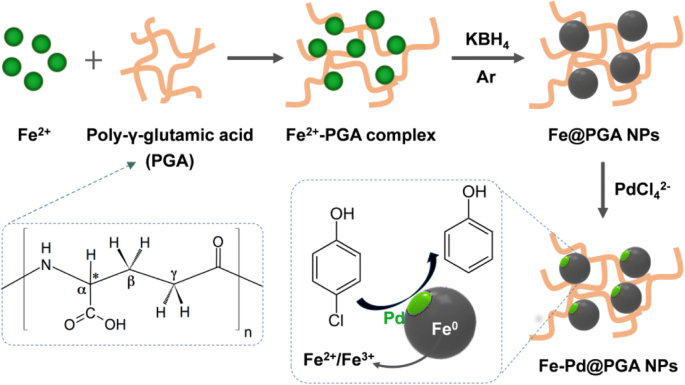
Illustration schématique pour la synthèse des NPs Fe-Pd@PGA et la déchloration de p -CP
Les morphologies et la taille des NP nues Fe-Pd et Fe-Pd@PGA ont été caractérisées par SEM et MET. Comme le montrent les Fig. 1a, b, la majorité des NP Fe-Pd@PGA avaient des formes relativement sphériques dans la plage de taille de 50 à 200 nm et étaient connectées à des structures en forme de puce, ce qui a été attribué à la modification PGA. La structure est similaire à celle précédemment rapportée en utilisant la méthode de réduction chimique [38]. La distribution et la composition des éléments ont été présentées dans le fichier supplémentaire 1 :Figure S1 et le fichier supplémentaire 1 :Tableau S1. L'image SEM montre que les NP Fe-Pd@PGA avaient des surfaces sphériques lisses, tandis que les NP Fe-Pd nus avaient déjà été oxydés, ce qui prouvait que le PGA pouvait inhiber l'agrégation et restreindre l'oxydation (Fig. 1c, d). En général, par rapport au nZVI modifié par d'autres stabilisants dans un travail précédent [16]. Les NP Fe-Pd@PGA avaient une forme et une taille similaires.

un , b TEM et c Micrographies SEM des NP Fe-Pd@PGA. d Micrographie SEM de NP Fe-Pd nus
La figure 2a montre le schéma XRD des NP Fe-Pd@PGA qui s'étaient déposées dans l'air pendant 1 jour. Le pic à 2θ de 44,8 ° et un pic faible à 82,5 ° a indiqué la présence de α-Fe 0 avec une nature mal ordonnée et amorphe dans les NPs [16, 39]. Deux autres pics caractéristiques faibles sont apparus à 2θ de 35,6 ° et 65,2 ° , qui correspond aux produits de corrosion de Fe 0 , magnétite (Fe3 O4 ), et/ou de la magnétite (γ-Fe2 O3 ) [40, 41], suggérant que seule une petite partie de Fe 0 était oxydé. Le modèle XRD a vérifié que nZVI avait été créé avec succès.
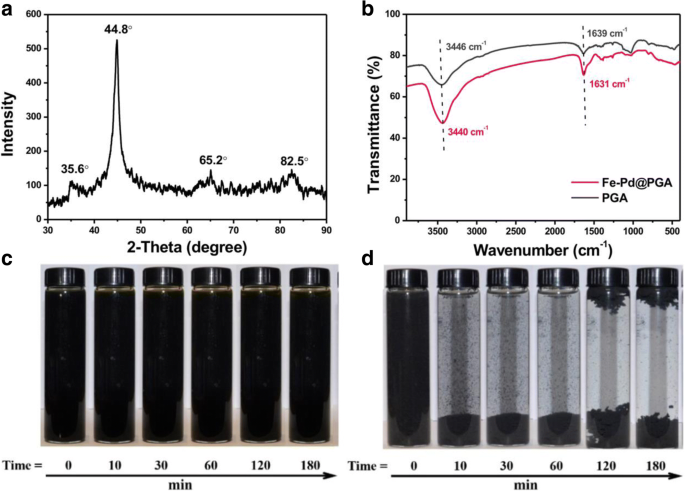
un Modèle XRD des NP Fe-Pd@PGA. b Spectres FTIR des NPs PGA et Fe-Pd@PGA. c , d Photos des NP Fe-Pd@PGA (c ) et des NP Fe-Pd nus (d ) suspension à des moments différents
La figure 2b est les spectres FTIR des NPs PGA et Fe-Pd@PGA dans la plage de 4000 à 400 cm − 1 . Le pic d'absorption à 3440 cm − 1 est une caractéristique de la vibration d'étirement O − H des hydroxyles dans les groupes carboxyle. Le pic d'absorption aux alentours de 1631 cm − 1 est une caractéristique de la vibration d'étirement C=O des groupes carboxyle. Le pic d'absorption entre 900 et 650 cm − 1 vient des groupes amido de PGA [42, 43]. Le léger décalage du pic d'absorption des NP Fe-Pd@PGA indiquait l'interaction des NP Fe-Pd et PGA.
La stabilité colloïdale des NP Fe-Pd@PGA et des NP Fe-Pd nues a été étudiée par des expériences de sédimentation. Les NP Fe-Pd nues se sont agrégées rapidement en 10 min, et le sédiment noir visible peut être observé au fond du tube (Fig. 2d). Après 120 min, le flottage et la floculation générée se sont formés, ce qui pourrait être attribué à la génération d'hydrogène. Comme prévu, les NP Fe-Pd@PGA se sont bien dispersées et se sont à peine déposées au fond du tube de verre pendant plus de 180 min, comme le montre la figure 2c. De plus, nous avons constaté que l'agrégation des NP Fe-Pd@PGA se produisait après une journée de repos (Fichier supplémentaire 1 :Figure S2). La stabilité colloïdale des NP Fe-Pd@PGA est comparative et même meilleure que celle des NP Fe-Pd classiques modifiées par CMC (par exemple, pour 5 g L − 1 de CMC-nZVI, le temps de règlement est de 30 min [44]).
Déchloration de p-CP par Fe-Pd@PGA NPs
L'activité de déchloration des NP Fe-Pd@PGA a été étudiée par lot p -Tests de déchloration CP en conditions faiblement alcalines (pH = 9). La figure 3a–c montre la suppression de p -CP utilisant des NP Fe-Pd et Fe-Pd@PGA nus avec différentes charges de Pd. Les résultats ont indiqué que les NP Fe-Pd nues sans modification PGA ne pouvaient éliminer qu'environ 50 % de p -CP en 4 h, tandis que les NP Fe-Pd@PGA ont une efficacité de dégradation largement améliorée. Plus précisément, les NP Fe-Pd@PGA avec 25 mg de PGA et 0,8 % de charge en Pd pourraient éliminer plus de 90 % de p -CP dans les 30 min. Une nouvelle augmentation de la charge PGA à 50 mg pourrait atteindre 100 % p - Retrait du CP dans les 30 min. Ces résultats ont démontré que le PGA favorise l'activité de déchloration accrue des NP Fe-Pd. Du point de vue d'une réaction médiée par la surface, la réactivité était proportionnelle à la surface disponible [39]. La modification du PGA pouvait empêcher les nanoparticules de s'agglomérer, puis les NP Fe-Pd étaient plus petites et avaient par conséquent une plus grande surface totale par unité de masse. Comme prévu, les NP Fe-Pd@PGA étaient plus efficaces que les NP Fe-Pd nus pour éliminer p -CP.
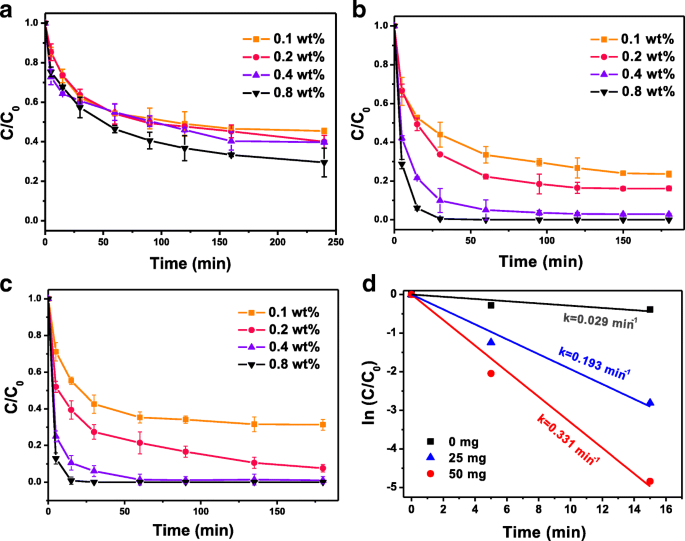
un –c Déroulements temporels de la déchloration utilisant des NP Fe-Pd nus (a ) et les NP Fe-Pd@PGA (b , c ) avec différents chargements PGA (b 25 mg de PGA ; c 50 mg de PGA) et différentes charges de Pt variaient de 0,1 à 0,8 % en poids. d La constante de vitesse (k ) pour la déchloration de p -CP avec différentes charges PGA à pH 9,0 (charge Pd =0,8 % en poids)
Lors de la déchloration de p -CP par les NPs Fe-Pd@PGA, la charge en Pd est également un facteur important pour l'activité de déchloration. Comme le montrent les figures 3b, c, les NP Fe-Pd@PGA avec une teneur en Pd plus élevée ont affiché une activité de déchloration plus élevée. Ce phénomène est cohérent avec celui rapporté dans de nombreuses études antérieures. Une explication est que Fe et Pd peuvent former des cellules galvaniques, et Pd pourrait accepter des électrons de Fe, qui ont joué un rôle catalytique non seulement en accélérant la corrosion du Fe mais aussi en améliorant l'activité de déchloration [45]. Il convient de noter que, sans modification PGA, il est difficile d'atteindre une efficacité de déchloration élevée même avec une charge élevée en Pd. Par conséquent, la modification du PGA est cruciale pour la forte activité de déchloration des NP Fe-Pd@PGA.
Généralement, la déchloration de p -CP par Fe-Pd NPs suit une loi de vitesse de pseudo-premier ordre [46], qui peut être modélisée à l'aide de l'équation suivante :
$$ \mathit{\ln}\left(\frac{C}{C_0}\right)=kt $$ (1)où C et C 0 sont des concentrations chimiques de p -CP parfois t (min) et 0, respectivement, k (min − 1 ) est la constante de vitesse, et t est le temps de réaction. Par conséquent, le k valeur des systèmes de déchloration est la pente de ln(C /C 0 ) contre t heures supplémentaires. Calculs de la constante de vitesse pour la déchloration de p -CP avec différentes charges PGA sont montrés dans la Fig. 3d. La valeur k pour les NP Fe-Pd nus est de 0,029 min − 1 , alors qu'il est passé à 0,331 min − 1 pour les NP Fe-Pd@PGA à 50 mg de charge PGA. La figure 4 montre le p -Constantes de vitesse cinétique de dégradation du CP (k ) des NP Fe-Pd avec divers degrés de charge PGA et Pd. Les constantes de vitesse de pseudo-premier ordre ont augmenté avec l'augmentation de la teneur en Pd, similaire à la tendance de l'efficacité de la déchloration, et, lorsque la charge de PGA a augmenté de 0 à 50 mg, k augmente avec l'augmentation de la charge PGA. Cependant, il est apparu que la réaction de déchloration était restreinte et donc la constante de vitesse a montré une baisse avec une nouvelle augmentation de la charge de PGA de 50 à 70 mg. Comme le montre le fichier supplémentaire 1 :Figure S3, les images SEM montrent l'agrégation significative des NP Fe-Pd@PGA en raison de la couverture excessive de PGA, entraînant une diminution de l'activité de déchloration. Cette diminution de l'activité de déchloration a également été observée dans des études antérieures [47, 48]. Par conséquent, il y avait une charge PGA optimale (~ 50 mg) et la constante de vitesse de réaction d'élimination maximale est de 0,331 min − 1 .
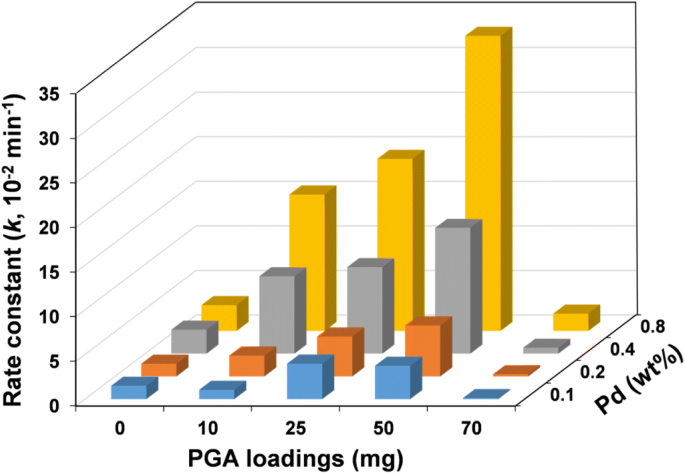
La constante de vitesse de déchloration de p -CP avec différents chargements PGA et Pd
Le tableau 1 résume les différents stabilisants utilisés pour la synthèse de nZVI et les paramètres expérimentaux correspondants et les résultats de la réaction de déchloration pour p -CP. Nous pouvons trouver que k dans notre travail était de plus de 1 ou 2 ordres plus élevé que les valeurs rapportées dans les études précédentes malgré le plus petit rapport de Fe sur p -CP (nFe/p -CP ) et une valeur de pH plus élevée utilisée dans ce travail. En général, un nFe/p élevé -CP (par exemple,> 1000) et des conditions neutres ou acides (par exemple, pH = 3) ont été utilisées pour obtenir une activité de déchloration élevée. Dans cette étude, à un nFe/p -CP de 100 et pH 9, Les NP Fe-Pd@PGA ont présenté une activité de déchloration élevée, ce qui a démontré que le PGA est un stabilisateur prometteur de nZVI pour la déchloration de p -CP.
Déchloration de p -CP dans les eaux souterraines stimulées
Nous avons testé P -Élimination du CP dans les eaux souterraines stimulées pour évaluer les applications pratiques potentielles. L'expérience à blanc a été réalisée en utilisant des NP Fe-Pd@PGA modifiées avec 25 mg de PGA avec une charge de 0,8 % de Pd. L'impact des constituants dissous dans les eaux souterraines stimulées a été évalué en présence de quatre types d'ions (Cl − , H2 Bon de commande4 − , HPO4 2− , et HCO3 − ) et HA. Comme le montre la Fig. 5a–c, en présence de Cl − , H2 Bon de commande4 − , ou HA, le k les valeurs sont très proches de celles de l'expérience à blanc, tandis que HPO4 2− et HCO3 − les ions réduisent l'activité de déchloration, les k les valeurs ont diminué de 0,173 à 0,06 et 0,07 min − 1 . Dans les travaux précédents, l'augmentation du pH après l'ajout d'anions était considérée comme l'une des raisons importantes de l'inhibition de l'activité [49].
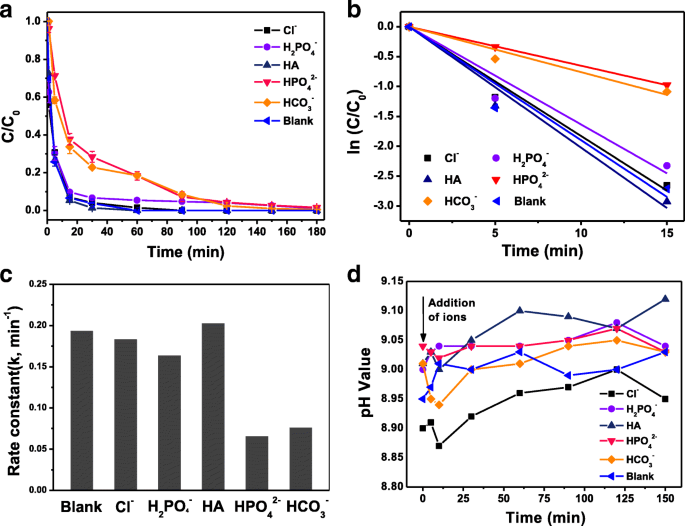
un Cours à temps et (b , c ) constante de vitesse de déchloration de p -CP dans les eaux souterraines simulées avec différents constituants. d Les changements de pH après l'ajout de constituants au cours de la réaction
Le processus de réaction de déchloration de p -CP peut être représenté comme suit [20] :
$$ {\mathrm{Fe}}^0\à {\mathrm{Fe}}^{2+}+2{\mathrm{e}}^{-} $$$$ 2{\mathrm{H}} _2\mathrm{O}+2{\mathrm{e}}^{-}\overset{\mathrm{Pd}}{\to }2{\mathrm{H}}^{\ast }+2{\mathrm {OH}}^{-} $$$$ \mathrm{Pd}+{\mathrm{H}}^{\ast}\to \mathrm{Pd}-\mathrm{H} $$$$ \mathrm{ Pd}-\mathrm{H}+\mathrm{R}-\mathrm{Cl}\à \mathrm{Pd}+\mathrm{R}-\mathrm{H}+{\mathrm{Cl}}^{- } $$Les équations ci-dessus indiquent que la valeur du pH est un paramètre crucial qui affecte le taux de dégradation de p -CP. À un pH plus élevé, moins d'hydrogène ou d'hydrure atomique à la surface des particules est disponible pour attaquer les molécules chlorées. Pendant ce temps, les ions ferreux et hydroxyles forment de l'hydroxyde ferreux et précipitent. La couche de passivation de surface de l'hydroxyde ferreux et du précipité pourrait entraver le transport des molécules chlorées et bloquer les sites réactifs sur Fe et donc diminuer la vitesse de réaction globale. Dans cet esprit, nous avons mesuré les valeurs de pH pendant la réaction de déchloration, comme le montre la figure 5d. Le résultat a montré qu'il n'y a pas de changement évident des valeurs de pH après l'ajout de différents ions, probablement en raison de la présence de PGA. Une légère augmentation des valeurs de pH a été observée avec l'augmentation du temps, et enfin, des valeurs relativement stables ont été observées. Les résultats ont indiqué que le changement de pH n'est pas la raison dominante de l'inhibition des ions. De plus, nous avons également étudié la déchloration de la p-CP à pH 5 (Fichier supplémentaire 1 :Figure S4). Les résultats ont indiqué qu'une condition d'acide faible était en faveur de la réaction de déchloration. Quant à l'inhibition de l'HPO4 2− et HCO3 − , une étude plus approfondie est nécessaire pour comprendre le mécanisme.
Mécanisme de déchloration renforcée de p -CP par Fe-Pd@PGA NPs
Sur la base de nos résultats expérimentaux, un mécanisme possible de la déchloration améliorée par les NP Fe-Pd@PGA a été proposé, comme le montre la figure 6.
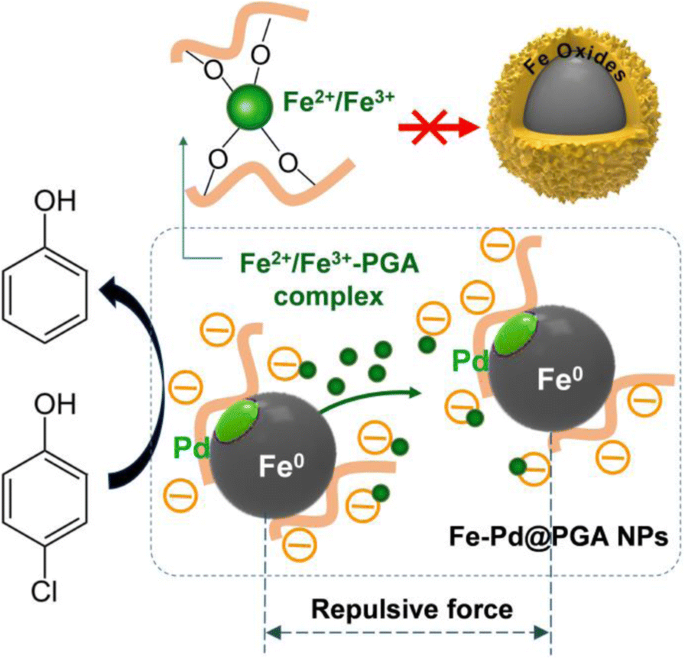
Mécanisme de la déchloration renforcée de p -CP par Fe-Pd@PGA NPs
D'une part, on suppose généralement que nZVI a de l'oxyde/hydroxyde de fer dans la coquille [50], la coquille d'oxyde de fer contribuant à des charges positives [51]. Par conséquent, les molécules de PGA avec des groupes anioniques abondants de carboxyle (COO − ) pourrait facilement être attaché à la surface des NP Fe-Pd avec des charges positives. Les groupes carboxyle de PGA ont été déduits pour se connecter aux surfaces des NP Fe-Pd par le biais de trois méthodes de complexation possibles :(i) chélation monodentée, (ii) chélation bidentée et (iii) pontage bidenté [52]. De plus, l'organisation des nanoparticules polymères fournit un échafaudage efficace avec des dimensions nanométriques, augmentant ainsi la surface spécifique des nanoparticules. La modification des NPs Fe-Pd avec du PGA stabilise non seulement les NPs mais empêche également les NPs de s'agglomérer par répulsion électrostatique et stérique. Par conséquent, l'excellente efficacité de déchloration et la bonne dispersité des NP Fe-Pd@PGA ont été principalement attribuées à la structure complexe des NP Fe-Pd@PGA et à l'interaction de répulsion électrostatique-stérique.
D'autre part, le PGA pourrait lier des ions métalliques (par exemple, Fe 2+ , Fe 3+ ) par chélation et liaison électrostatique. Comme le montre le fichier supplémentaire 1 :Figure S5, les spectres UV-vis de solutions contenant des ions Fe et du PGA ont indiqué la formation de complexes PGA-fer [53]. Pendant le processus de déchloration, Fe 2+ et Fe 3+ dépôt sur les surfaces de Fe NPs, conduisant à la formation d'hydroxydes de fer et à l'épaississement de la coquille d'oxyde de fer. En présence de PGA, les ions Fe issus de la réaction de déchloration formeraient des complexes avec le PGA et limiteraient la formation d'hydroxydes de fer, empêchant ainsi le précipité d'hydroxyde de Fe à la surface, préservant les sites actifs des NPs Fe-Pd et fournissant un microenvironnement favorable au maintien de la réactivité de déchloration. Dans ce cas, p -CP les molécules peuvent facilement accéder aux sites actifs et être rapidement déchlorées par les NP Fe-Pd.
Conclusions
En résumé, nous avons réussi à synthétiser les nanoparticules bimétalliques Fe-Pd en utilisant du PGA comme stabilisant. Les NP Fe-Pd@PGA telles que préparées présentent une bonne dispersité et une bonne stabilité colloïdale. Les performances de déchloration des NP Fe-Pd@PGA ont été évaluées à l'aide de p -CP comme modèle. Les résultats ont indiqué que le PGA favorise de manière significative la déchloration de p -CP, atteignant un k élevé valeur de 0,331 min − 1 . Cette valeur est beaucoup plus élevée que celles rapportées précédemment malgré le plus petit rapport de Fe sur p -CP et une valeur de pH plus élevée ont été utilisés dans ce travail. De plus, nous avons constaté que les NP Fe-Pd@PGA maintiennent une activité élevée en présence de Cl − , H2 Bon de commande4 − , et HA, qui sont généralement présents dans l'eau. Nous avons proposé que la forte activité de déchloration des NP Fe-Pd@PGA est principalement attribuée à l'interaction de répulsion électrostatique-stérique et à la prévention de la formation d'hydroxyde de Fe en raison de la capacité de liaison de PGA à Fe 2+ /Fe 3+ ions. Compte tenu de la bonne stabilité, de l'activité de déchloration élevée et de la tolérance aux ions, les NP Fe-Pd@PGA présentent des applications prometteuses dans la déchloration des composés organiques chlorés.
Abréviations
- APAM :
-
Polyacrylamide anionique
- CMC :
-
Carboxyméthylcellulose
- FAIRE :
-
Oxygène dissous
- Fe-Pd@PGA NP :
-
Nanoparticules de fer à valence nulle dopées au palladium impliquant du poly(acide γ-glutamique)
- FTIR :
-
Spectroscopie infrarouge à transformée de Fourier
- HA :
-
Acide humique
- HPLC :
-
Chromatographie liquide haute performance
- nZVI :
-
Fer à valence zéro à l'échelle nanométrique
- AAP :
-
Poly(acide acrylique)
- PCB :
-
Biphényles polychlorés
- p -CP :
-
p -Chlorophénol
- PGA :
-
Poly(acide γ-glutamique)
- SEM :
-
Microscopie électronique à balayage
- TCE:
-
Trichloroethylene
- TEM :
-
Microscopie électronique à transmission
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- Nanoparticules FePO4 biocompatibles :administration de médicaments, stabilisation de l'ARN et activité fonctionnelle
- Activité de préparation et d'hydrogénation catalytique améliorée des nanoparticules de Sb/Palygorskite (PAL)
- Détection photo-électrochimique améliorée de l'acide urique sur une électrode de carbone vitreuse modifiée par nanoparticules d'Au
- Nanoparticules de chitosane chargées de génistéine et de bioflavonoïdes ciblés sur les récepteurs folates pour un effet anticancéreux amélioré dans les cancers du col de l'utérus
- Activités photocatalytiques renforcées par des nanoparticules Au-Plasmonic sur une photoélectrode de nanotube de TiO2 recouverte de MoO3
- Stabilité améliorée des nanoparticules magnétiques d'or avec du poly(acide 4-styrènesulfonique-co-acide maléique) :propriétés optiques adaptées pour la détection des protéines
- Polyglycérol hyperramifié modifié comme dispersant pour le contrôle de la taille et la stabilisation des nanoparticules d'or dans les hydrocarbures
- Effets synergiques des nanoparticules d'Ag/BiV1-xMoxO4 avec une activité photocatalytique améliorée
- Performances de détection H2 hautement améliorées des hétérojonctions MoS2/SiO2/Si à quelques couches par la décoration de la surface des nanoparticules de Pd



