Effets du fullerène C60 sur l'interaction du diphényl-N-(trichloroacétyl)-amidophosphate avec l'ADN in silico et son activité cytotoxique contre la lignée cellulaire leucémique humaine in vitro
Résumé
Un nouveau représentant des carbacylamidophosphates - le diphényl-N-(trichloroacétyl)-amidophosphate (HL), qui contient deux substituants phénoxy proches du groupe phosphoryle, a été synthétisé, identifié par analyse élémentaire et spectroscopie IR et RMN, et testé en tant qu'agent cytotoxique lui-même et en combinaison avec C60 fullerène.
D'après les résultats de la simulation moléculaire, C60 fullerène et HL pourraient interagir avec l'ADN et former un complexe rigide stabilisé par l'empilement des interactions des groupes phényle HL avec C60 fullerène et nucléotide ADN G, ainsi que par les interactions de HL CCl3 grouper par liaisons ion-π avec C60 molécule et par liaisons électrostatiques avec le nucléotide G de l'ADN.
Avec l'utilisation du test MTT, l'activité cytotoxique de HL contre les cellules leucémiques humaines CCRF-CM avec IC50 la valeur détectée à une concentration de 10 μM à 72 h de traitement des cellules a été montrée. Sous action combinée de 16 μM C60 fullerène et HL, la valeur de IC50 a été détecté à une concentration de HL inférieure de 5 μM et à une période d'incubation de 48 h plus tôt, en plus de l'effet cytotoxique de HL a été observé à une faible concentration de 2,5 μM à laquelle HL en soi n'avait aucune influence sur la viabilité cellulaire. Reliure de C60 fullerène et HL avec un sillon d'ADN mineur avec formation d'un complexe stable est supposé être l'une des raisons possibles de leur inhibition synergique de la prolifération des cellules CCRF-CЕM.
Application de C60 Le fullerène en combinaison avec 2,5 μM de HL n'a eu aucun effet nocif sur la stabilité structurelle de la membrane des érythrocytes sanguins. Ainsi, action combinée de C60 fullerène et HL à faible concentration potentialisaient l'effet cytotoxique du HL contre les cellules leucémiques humaines et n'étaient pas suivis d'un effet hémolytique.
Contexte
Le représentant de la nanostructure de carbone C60 Il a été démontré que le fullerène possède des propriétés physico-chimiques et une activité biologique uniques non seulement en tant qu'antioxydant ou photosensibilisateur, mais également en tant que modificateur de l'effet toxique des médicaments anticancéreux en raison de sa capacité à pénétrer à l'intérieur de la cellule et à fonctionner comme vecteur de médicament [1,2,3,4 ]. C60 La molécule peut interagir avec des médicaments chimiothérapeutiques tels que la doxorubicine, le cisplatine et le paclitaxel et peut former des complexes avec eux améliorant l'effet thérapeutique [5,6,7,8].
Les carbacylamidophosphates (CAPh) sont des molécules organiques qui ont attiré l'attention en raison de leur structure particulière, leur activité biologique et leurs perspectives d'application biomédicale [9,10,11,12]. La présence de groupements peptidiques et phosphoramides réunis dans le fragment C(O)N(H)P(O) de la molécule détermine son interaction avec les molécules biologiques et les membranes cellulaires. La variation des substituants à proximité des groupes phosphoryle et carbonyle permet de moduler les propriétés stéréochimiques et pharmacologiques de CAPh. En particulier, il a été démontré que différents représentants de CAPh possèdent une activité antinéoplasique [13, 14].
Récemment, nous avons confirmé que le diméthyl-N-(benzoyl)-amidophosphate représentatif de CAPh utilisé à des concentrations millimolaires diminuait la viabilité des cellules leucémiques L1210 et que son effet toxique était facilité par le C60 fullerène [15]. Nous avons également montré que l'introduction de substituants aromatiques supplémentaires et CCl électronégatif3 groupe dans la structure CAPh a entraîné une augmentation de sa toxicité [16]. Ainsi, un effet toxique significatif du dimorfolido-N-trichloroacétylphosphoramide a été démontré contre des cellules leucémiques humaines d'origine différente, mais sa concentration efficace était toujours élevée et aucune amélioration de la toxicité après action combinée avec C60 fullerène a été observé. Dans la continuité de ces recherches, nous avons synthétisé un nouveau représentant du diphényl-N-(trichloroacétyl)-amidophosphate (HL) CAPh qui possède deux substituants phénoxy au lieu de groupes morfolido près du groupe phosphoryle (Fig. 1).
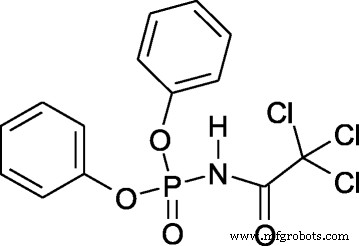
La structure du diphényl-N-(trichloroacétyl)-amidophosphate (HL)
L'objectif de la recherche était d'estimer l'activité biologique du diphényl-N-(trichloroacétyl)-amidophosphate (HL) seul ou en combinaison avec le C60 fullerène avec l'utilisation de l'analyse in silico de leur interaction avec l'ADN et l'étude in vitro des effets cytotoxiques contre la lignée cellulaire leucémique humaine.
Méthodes/Expérimental
Produits chimiques
Milieu liquide RPMI 1640, sérum bovin fœtal (FBS), pénicilline/streptomycine et L-gluthamine (Biochrom, Allemagne), diméthylsulfoxyde (DMSO) (Carl Roth GmbH+Co, Allemagne), MTT [3-(4,5-diméthylthiazol- Bromure de 2-yl)-2,5-diphényl tétrazolium] (Sigma-Aldrich Co, Ltd., États-Unis), HCl (Kharkivreachim, Ukraine).
Caractérisation du composé chimique
Pour augmenter la solubilité, nous avons obtenu le sel de sodium du diphényl-N-(trichloroacétyl)-amidophosphate (HL) selon les réactions suivantes (Fig. 2).
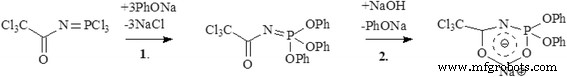
Schéma de solubilité du diphényl-N-(trichloroacétyl)-amidophosphate (HL) dans le sel de sodium
La solution de trichlorophosphazothrichloroacétyle (0,035 M) dans 200 ml de chloroforme a été ajoutée lentement à une suspension de phénolate de sodium bien agitée (0,106 M, 12,3 g) dans 150 ml de chloroforme (Fig. 2 ; étape 1). La température du mélange n'a pas été autorisée à dépasser 40-50 °C. L'agitation a été poursuivie pendant environ 1 h, puis la solution a été chauffée jusqu'à 70 °C et agitée pendant 20 min dans ces conditions. Le produit résultant triphénoxyphosphazothrichloroacétyle a été évaporé. Ensuite, 40 ml de NaOH 1 M ont été ajoutés et chauffés au reflux pendant 90 minutes (Fig. 2; étape 2). Un mélange résultant a été évaporé. Le précipité solide de sodium HL a été lavé trois fois à l'éther diéthylique et recristallisé dans i -propanole sous forme de poudre cristalline blanche (rendement 80 %). Cristaux incolores de NaL·3H2 O convenant à l'analyse aux rayons X ont été obtenus par i -PrOH:H2 O (9:1 v /v ) solution à évaporation lente. Le composé est stable à l'air, très soluble dans l'eau et les alcools. député 215 °С.
HL a été identifié par analyse élémentaire et spectroscopie IR et RMN :les analyses élémentaires (C, H, N) ont été réalisées à l'aide de l'analyseur élémentaire EL III Universal CHNOS. Des mesures spectrales IR ont été effectuées pour des échantillons sous forme de pastilles de KBr sur un spectromètre FT-IR Perkin-Elmer Spectrum BX avec une résolution de 2 cm − 1 et des accumulations de 8 scans, qui sont combinés pour faire la moyenne des artefacts d'absorption aléatoires dans la gamme spectrale 4000-400 cm − 1 . 1 Les spectres RMN H dans des solutions de DMSO-d6 ont été enregistrés sur un spectromètre RMN AVANCE 400Bruker à température ambiante.
HL :IR (cm −1 ) : 1639 vs, sh (νCO); 1353 s, sh (Amide II) ; 1194 s, sh (νPO); 941 s, sh (νPN).
1 RMN H (DMSO-d6 ) : 7,05 (t, 2H, -CH2 ); 7.205, 7.255 (dt, 8H, - et -CH2 ).
Pour CCl3 C(O)N(Na)P(O)(OC6 H5 )2 la composition élémentaire a été déterminée, % :C 40,58, H 2,35, N 3,15; et calculé, % :C 40,37, H 2,42, N 3,36.
Synthèse et caractérisation de C60 Fullerène
Une solution colloïdale aqueuse hautement stable de C60 Le fullerène (200 μM, pureté> 99,5 %, taille moyenne des nanoparticules jusqu'à 50 nm) a été synthétisé à l'Université technique d'Ilmenau (Allemagne) comme décrit dans [17, 18].
Сell Culture
Les expériences ont été réalisées sur une lignée cellulaire CCRF-CM de leucémie aiguë à cellules T humaines. La lignée cellulaire a été achetée auprès du Leibniz Institute DSMZ-Collection allemande de micro-organismes et de cultures cellulaires :CCRF-CM (ACC 240). Les cellules ont été cultivées dans du milieu RPMI 1640 additionné de 10 % de FBS, 1 % de pénicilline/streptomycine et 2 mM de glutamine, en utilisant 25 cm 2 flacons à 37 °C avec 5% de CO2 en incubateur humidifié.
Les cellules dans le milieu RPMI 1640 ont été incubées avec C60 fullerène (16 μM) ou HL (2,5, 5 et 10 μM) séparément et ensemble pendant 24, 48 et 72 h. Survie cellulaire sans ajout de HL ou C60 le fullerène a été reçu à 100 % (l'échantillon de contrôle contenait 0,05 M de DMSO).
Test de viabilité cellulaire (MTT)
La viabilité cellulaire a été évaluée par le test de réduction du MTT [3-(4,5-diméthylthiazol-2-yl)-2,5-diphényl tétrazolium bromure] [19]. Aux moments d'incubation indiqués, 100 μl d'aliquotes (0,5 × 10 4 cellules) ont été placés dans les microplaques à 96 puits Sarstedt (Nümbrecht, Allemagne), 10 μl de solution de MTT (5 mg/ml dans du PBS) ont été ajoutés à chaque puits et les plaques ont été incubées pendant 2 h supplémentaires à 37 °C. Le milieu de culture a ensuite été remplacé par 100 μl de DMSO; la formation de diformazan a été déterminée en mesurant l'absorption à 570 nm avec un lecteur de microplaques Tecan Infinite M200 Pro (Männedorf, Suisse).
Animaux
L'étude a été menée sur des rats mâles blancs de la lignée « Wistar » pesant 170 ± 5 g. Les animaux ont été maintenus dans des conditions standard dans le vivarium de l'ESC « Institut de biologie et de médecine », Université nationale Taras Shevchenko de Kiev. Les animaux avaient libre accès à la nourriture et à l'eau. Toutes les expériences ont été menées conformément aux principes internationaux de la Convention européenne pour la protection des animaux vertébrés sous le contrôle du Comité de bioéthique de l'institution susmentionnée.
Estimation de l'hémolyse des érythrocytes
Des érythrocytes ont été obtenus à partir de sang hépariné de rat de la lignée « Wistar » et dilués dans une solution de NaCl à 0,85% à 0,700 o.u. à 630 nm sur le spectrophotomètre Scinco (Allemagne). L'hémolyse des érythrocytes a été causée par 0,001 N de HCl. La cinétique d'hémolyse a été mesurée par spectrophotométrie (λ = 630 nm) toutes les 10 s pendant 2 min. Le pourcentage d'érythrocytes hémolysés a été calculé comme présenté dans [20]. Les érythrocytes ont été incubés dans une solution de NaCl à 0,85% avec C60 fullerène (16 μM) ou HL (2,5 et 10 μM) séparément et ensemble pendant 1 h. Erythrocytes sans ajout de HL ou C60 fullerène ont été reçus à 100 % (l'échantillon de contrôle contenait 0,05 M de DMSO).
Étude In Silico
La molécule d'ADN en double hélice a été utilisée comme matrice à partir de la base PDB (Protein Data Bank). L'interaction de la molécule d'ADN avec HL séparément et en combinaison avec C60 le fullerène a été étudié. Nous avons pris en considération les structures suivantes de la molécule d'ADN :2MIW (CCATCGCTACC - intercalation du composé dans un petit sillon d'hélice d'ADN), 1XRW (CCTCGTCC - intercalation de composé dans un petit sillon d'hélice d'ADN) et 2M2C (GCGCATGCTACGCG - liaison de composé avec de grandes et petites rainures d'hélice d'ADN). Nous avons appliqué l'algorithme d'amarrage systématique (SDOCK+), intégré au package QXP (cette méthode démontre toutes les conformations possibles des structures étudiées avec la valeur minimale de l'écart quadratique moyen (RMSD)) [21]. Nous avons généré 300 complexes potentiellement possibles avec l'ADN, dont les dix meilleurs ont été sélectionnés pour l'étape suivante, à l'aide d'une fonction de notation, intégrée au package QXP [22].
Les interactions de la molécule d'ADN avec HL séparément et en combinaison avec le C60 fullerène ont été caractérisés par les paramètres suivants :(1) le nombre de liaisons hydrogène, (2) la surface de contact de l'ADN et la structure correspondante, (3) la distance entre l'ADN et la structure amarrée, et (4) l'énergie totale de la structure de liaison.
Évaluer la stabilité des complexes de composé chimique avec C60 fullerène, nous avons réalisé la dynamique moléculaire courte (DM, 100 ps) à l'aide du logiciel Gromacs [23] selon un algorithme Nosé-Poincaré-Anderson (NPA) [24, 25] basé sur le champ de force OPLS-AA [26, 27] .
Les calculs ont été effectués sur les paramètres suivants :température (en Kelvin) - 300; pression (en kilopascal) - 100; la liaison impliquant l'atome d'hydrogène ou le ligand était limitée par l'algorithme [25].
Analyse statistique
Les données ont été représentées par la moyenne ± SD de plus de quatre expériences indépendantes. La moyenne (M) et l'écart type (SD) ont été calculés pour chaque groupe. L'analyse statistique a été réalisée en utilisant une ANOVA à deux facteurs suivie de tests post Bonferroni. Une valeur de p <0,05 a été considéré comme statistiquement significatif. Le traitement et le traçage des données ont été effectués par IBM PC à l'aide d'applications spécialisées GraphPad Prism 7 (GraphPad Software Inc., États-Unis).
Résultats et discussions
Etude In Silico
Interaction du LH avec l'ADN
Il a été montré que la HL pouvait s'intercaler dans l'ADN et former un complexe stable lorsqu'elle était liée dans un petit sillon d'ADN via les nucléotides AGC-GCTA (Fig. 3a). Dans ce cas, l'interaction d'empilement entre la base azotée du nucléotide A et le groupe phényle HL ainsi que l'interaction électrostatique entre CCl3 groupe et le nucléotide C a été formé. Après simulation MD, les valeurs RMSD pour la double hélice d'ADN et HL se sont avérées être respectivement de 3,3 et 1,62 Å. L'environnement nucléotidique de HL (GCA-CTA) a été partiellement modifié et l'interaction d'empilement a été perdue, tandis qu'une liaison hydrogène s'est formée entre le nucléotide G et le groupe CO de HL.
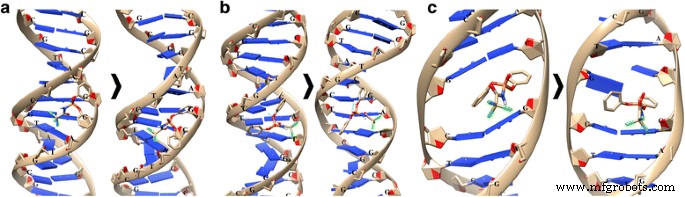
Interaction du diphényl-N-(trichloroacétyl)-amidophosphate (HL) avec la molécule d'ADN :a , b reliure avec rainures mineures et majeures; c intercalation dans un petit sillon. La structure d'ADN utilisée de la base de données PDB :a , b —2M2C et c -1XRW
La liaison de HL avec un sillon d'ADN majeur s'est produite via les nucléotides TCG-AT (Fig. 3b). Dans ce cas, une liaison hydrogène entre le groupe CO de HL et la base azotée du nucléotide A s'est formée et une interaction d'empilement entre les phényles HL et les bases azotées des nucléotides C et G s'est produite. De plus, une probabilité de liaison électrostatique entre HL CCl3 le groupe et les bases azotées des nucléotides AT sont apparus.
Après simulation MD, aucun changement dans l'environnement nucléotidique de HL n'a été détecté. Les valeurs RMSD pour l'ADN et le HL étaient respectivement de 2,77 et 1,58 Å. En raison de cela, l'interaction d'empilement entre le nucléotide C et le groupe phényle a disparu.
Dans le cas de l'intercalation de HL dans l'ADN, son environnement était constitué de nucléotides CG-CG (Fig. 3c). L'interaction d'empilement avec les nucléotides CG est apparue :un groupe phényle était coincé entre les bases azotées et l'autre formait une interaction d'empilement avec le nucléotide C.
Après simulation MD, les valeurs RMSD pour l'ADN double hélice et HL étaient de 1,71 et 1,89 Å, respectivement. L'environnement nucléotidique de HL n'a pas été modifié. L'un des groupes phényle a formé une interaction ion-π avec la base azotée du nucléotide G, qui a semblé être décalée de 1,12 Å.
Les paramètres énergétiques obtenus ont témoigné que l'énergie des affrontements stériques entre l'ADN et le LH ainsi qu'au sein du LH lui-même était insignifiante (Tableau 1).
Nous avons effectué l'analyse comparative des paramètres énergétiques de la liaison de HL avec des sillons d'ADN mineurs et majeurs ou son intercalation dans un sillon d'ADN mineur. Les valeurs de bosse se sont avérées être de 6,2 kJ/mol dans le cas de l'intercalation de HL dans l'ADN et de 2,5 kJ/mol dans le cas de sa liaison avec des sillons d'ADN mineurs et majeurs (tableau 1). Les valeurs Int étaient de 8,7 kJ/mol dans le cas de l'intercalation de HL dans l'ADN, de 6,3 kJ/mol dans le cas de sa liaison avec un sillon majeur d'ADN et de 3,6 kJ/mol dans le cas de sa liaison avec un sillon mineur d'ADN. Ces données ont montré que la liaison de HL avec un petit sillon d'ADN était la plus stable.
Interaction combinée de HL et C60 Fullerène avec ADN
Auparavant, avec l'utilisation de la simulation informatique, nous avons démontré que C60 la molécule pourrait interagir avec l'ADN et former un C60 stable + Complexe ADN lors de la liaison avec le petit sillon de l'ADN [15]. Comme le montre la figure 4, C60 le fullerène pourrait également former des liaisons ion-π avec CCl3 groupes de molécule HL.
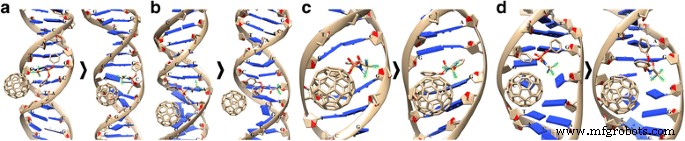
Interaction combinée du diphényl-N-(trichloroacétyl)-amidophosphate (HL) et du C60 fullerène avec ADN (HL+C60 ou C60 + versions HL) :a , b reliure avec rainures mineures et majeures, c , d intercalation dans les rainures mineures et majeures. Les structures d'ADN utilisées de la base de données PDB :a , b —2M2C, c -1XRW, et d —2MIW
Nous avons utilisé deux versions de modélisation moléculaire de HL, C60 fullerène et interaction ADN, qui ont été proposés dans [16] et se sont avérés utiles pour l'interprétation des résultats de simulation MD. Nous avons utilisé la structure 1XRW PDB de la molécule d'ADN dans la version, initialement HL puis C60 molécule intercalée dans l'ADN (HL+C60 ) et structure 2MIW PDB de la molécule d'ADN - dans la version, lorsqu'initialement C60 molécule, puis HL s'intercalent dans l'ADN (C60 +HL).
La liaison avec un petit sillon d'ADN dans le cas de HL+C60 version s'est produite via les nucléotides GCTA-GCAT (Fig. 4a). Les groupes phényle ont rempli un petit sillon et sont entrés dans des interactions d'empilement :un groupe avec C60 fullerène et l'autre avec la base azotée du nucléotide G. Les interactions électrostatiques sont apparues entre CCl3 groupe de HL et à la fois la base azotée du nucléotide G et C60 fullerène.
Selon les résultats de la simulation MD, une double hélice d'ADN dans ce cas était caractérisée par une mobilité considérable (la valeur RMSD est de 3,08 Å), la valeur RMSD pour HL était de 2,04 Å, tandis que C60 le fullerène est resté pratiquement immobile. En conséquence, l'environnement nucléotidique de HL+C60 structure a été modifiée par TGC-GCATG. En outre, une liaison hydrogène entre le groupe amino de HL et l'ADN et des interactions d'empilement entre les nucléotides des bases GC azotées et C60 fullerène est apparu.
La liaison de HL+C60 avec un sillon d'ADN majeur s'est produit via les nucléotides C-ATCC (Fig. 4b). Des liaisons hydrogène se sont formées entre le groupe HL CO et la base azotée du nucléotide A. Les groupes phényle ont rempli un sillon majeur de l'ADN et sont entrés en interaction d'empilement avec C60 fullerène.
Selon les résultats de la simulation MD, l'environnement nucléotidique de HL+C60 la structure n'a pas été modifiée :les valeurs de RMSD pour l'ADN et le HL étaient respectivement de 3,14 et 2,24 Å, C60 le fullerène est resté pratiquement immobile. Dans ce cas, toutes les interactions entre HL et C60 le fullerène a disparu et HL n'a interagi stériquement qu'avec l'ADN. On suppose qu'en résultat C60 le fullerène ainsi que le HL seraient expulsés du sillon principal de l'ADN.
Lorsque HL+C60 ont été intercalés dans un petit sillon d'ADN (Fig. 4c), la liaison avec les nucléotides CGT-GAG s'est produite. C60 le fullerène s'est avéré être intégré dans un sillon d'ADN mineur et interagir avec lui de manière stérique. Les groupes phényle HL ont formé des interactions d'empilement avec les bases azotées des nucléotides CG-CG. Selon la simulation MD, les valeurs de RMSD pour l'ADN et le LH étaient respectivement de 2,29 et 2,13 Å, C60 fullerène est resté pratiquement immobile, et CC13 groupe de HL est entré en interaction électrostatique avec la base azotée du nucléotide G.
Dans le cas de C60 Version +HL, la liaison avec un sillon d'ADN mineur (Fig. 4d) s'est produite via les nucléotides CGC-GCC. L'un des groupes phényle HL a formé un empilement avec C60 fullerène et l'autre avec le nucléotide G. Le CC13 groupe de HL semblait former une liaison électrostatique avec la base azotée du nucléotide C. Selon l'analyse MD, les valeurs de RMSD pour l'ADN et le HL dans ce cas étaient respectivement de 2,35 et 2,75 Å, C60 le fullerène est resté immobile, et l'environnement nucléotidique de C60 La structure +HL a été modifiée par CGCT-GC. De plus, le C60 molécule a pénétré plus profondément dans l'ADN et a formé une interaction d'empilement avec la base azotée du nucléotide C.
D'après les paramètres énergétiques calculés, le complexe formé dans le cas de C60 L'intercalation +HL dans un sillon d'ADN mineur était la plus rigide (la valeur de Bump 20,0 kJ/mol) (tableau 1). En revanche dans le cas de HL+C60 interaction avec l'ADN, ce paramètre n'était que de 6,2 kJ/mol lorsque HL+C60 était intercalé dans un sillon d'ADN mineur, 7,8 kJ/mol lorsqu'il était lié à un sillon d'ADN mineur et 8,8 kJ/mol lorsqu'il était lié à un sillon d'ADN majeur. En outre, les paramètres énergétiques ont montré que la formation de fortes liaisons hydrogène à l'intérieur de HL+C60 Le complexe + ADN n'était possible que dans le cas de la liaison avec un sillon majeur de l'ADN, lorsque la valeur de Hbnd était de - 2,3 kJ/mol, dans d'autres types d'interaction, elle était égale à zéro ou à - 1,0 kJ/mol (tableau 1). De plus, selon les résultats de MD dans ce cas à la fois C60 fullerène et HL semblaient être déplacés d'un sillon majeur de l'ADN.
Par conséquent, C60 La liaison +HL avec un sillon d'ADN mineur est suggérée comme étant la version la plus probable de C60 interaction combinée fullerène, HL et ADN.
Étude in vitro des effets biologiques du LH
Viabilité des cellules CCRF-CЕM
Dans des expériences in vitro, l'influence à long terme du diphényl-N(trichloroacétyl)-amidophosphate (HL) dans la plage de 2,5 à 10 μM sur la viabilité des cellules leucémiques humaines CCRF-CЕM a été estimée par le test MTT. Les cellules ont été incubées pendant 24, 48 et 72 h dans un milieu RPMI 1640 avec soit 16 μM C60 fullerène ou HL seuls ou leur combinaison. Viabilité des cellules incubées sans C60 ou HL a été considéré comme égal à 100 %.
À 24 h d'incubation, aucun effet de la HL sur la viabilité des cellules CCRF-CЕM n'a été observé (Fig. 5). Toujours à une incubation plus prolongée, l'activité cytotoxique de la HL à des concentrations de 5 et 10 μM est devenue évidente, la viabilité cellulaire à 48 h a été inhibée de 25 et 33 %, respectivement, et a continué à baisser à 72 h.
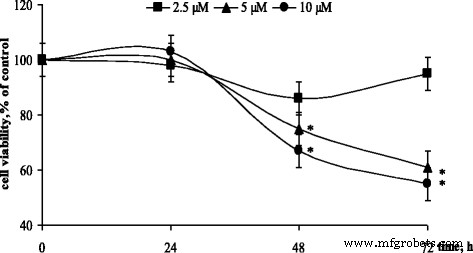
Viabilité des cellules CCRF-CEM incubées avec du diphényl-N-(trichloroacétyl)-amidophosphate (HL) à différentes concentrations. (M ± m, n = 8) ; *p < 0,05 par rapport aux cellules témoins
Il est à noter que 50% de diminution de la viabilité des cellules CCRF-CЕM (IC50 ) a été détecté à 72 h sous l'action de HL en concentration de 10 μM (Fig. 5). Récemment, nous avons montré qu'un autre dimorfolido-N-trichloracétylphosphorylamid représentatif du CAPh provoquait une diminution de 50 % de la viabilité des cellules CCRF-CЕM à 72 h à une concentration de 1 mM [16]. L'analyse comparative de ces données démontre que l'introduction de groupes phénoxy au lieu de groupes morfolido dans la structure du dérivé de CAPh a permis de diminuer de deux ordres sa concentration toxique efficace contre les cellules leucémiques. Nous supposons que la flexibilité conformationnelle de –P(O)(OC6 H5 ) core a assuré une interaction plus efficace de ce composé avec l'ADN.
Aucune influence de C60 le fullerène utilisé seul sur la viabilité cellulaire pendant la période d'incubation a été détecté (données non présentées). Dans le même temps, les résultats présentés sur la figure 6 démontrent que C60 le fullerène a intensifié l'activité cytotoxique de HL contre les cellules CCRF-CЕM. Sous action combinée de C60 fullerène et HL, une diminution de 50% de la viabilité cellulaire a été observée à une concentration de HL plus faible (5 μM) et à une période d'incubation plus précoce (48 h) que sous l'action de HL seul. De plus à 72 h d'action combinée de C60 fullerène et HL, l'effet cytotoxique du HL a été détecté à une faible concentration de 2,5 μM à laquelle le HL en lui-même n'avait aucune influence sur la viabilité cellulaire (Fig. 6).
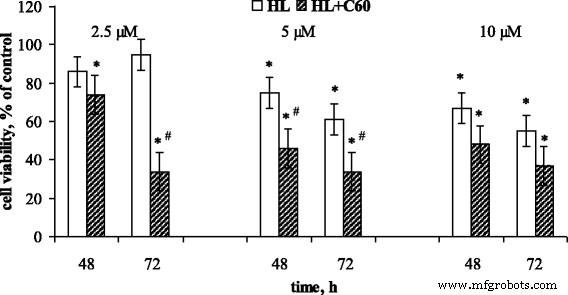
Viabilité des cellules CCRF-CEM incubées avec du diphényl-N-(trichloroacétyl)-amidophosphate (HL) seul ou en association avec 16 μM C60 fullerène. (M ± m, n = 8) ; *p <0,05 par rapport aux cellules témoins ; # p < 0,05 par rapport à HL
Ainsi, C60 Le fullerène potentialise les effets cytotoxiques du LH et augmente significativement la sensibilité des cellules leucémiques à son action à faible concentration. Tenant compte du fait que C60 le fullerène est capable de s'accumuler à l'intérieur des cellules leucémiques sur 24 h [28] et de se localiser dans les compartiments intracellulaires [29, 30, 31], en particulier dans le noyau [32, 33], son interaction avec l'ADN nucléaire des cellules cancéreuses proliférées activement ne devrait pas être exclu.
Ainsi les données obtenues in vitro sont en accord avec les résultats de l'étude in silico et démontrent que la liaison initiale de C60 molécule puis de HL avec un petit sillon d'ADN avec formation d'un complexe stable pourrait être l'une des raisons possibles de leur inhibition synergique de la prolifération des cellules CCRF-CЕM.
Résistance des érythrocytes à l'hémolyse
Sur l'estimation du potentiel anticancéreux de HL et C60 combinaison de fullerènes, il est important de prendre en compte ses effets possibles sur les cellules non malignes, en particulier sur les cellules sanguines.
L'étude de la résistance des érythrocytes à l'hémolyse acide permet d'élucider l'influence de l'agent pharmacologique au niveau membranaire. La dynamique de l'hémolyse reflète la dynamique de la rupture de la membrane plasmique des érythrocytes et donc la stabilité de son organisation structurelle. Dans la Fig. 7, la dépendance du pourcentage d'érythrocytes d'hémolyse ont été incubés pendant 1 h dans une solution de NaCl sans ajouts (contrôle) et avec soit HL soit C60 fullerène seul ou en combinaison. Aucune influence de 16 μM C60 fullerène sur les érythrocytes, une hémolyse a été détectée (non montré). HL en concentration de 2,5 μM seul ou en combinaison avec C60 érythrocytes affectés résistance à l'hémolyse (Fig. 7). Pendant ce temps, sous l'action de HL à une concentration de 10 μM, une accélération de l'hémolyse avec un maximum à 20 s a été détectée. Action combinée de 10 μM HL et C60 le fullerène a été suivi d'une intensification supplémentaire de l'hémolyse avec 60 % des érythrocytes hémolysés à 20 s.
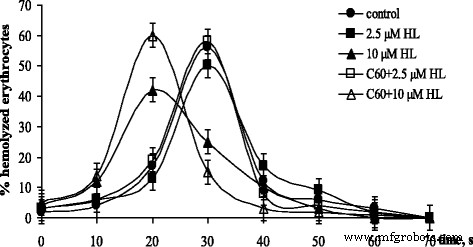
Résistance des érythrocytes à l'hémolyse en présence de diphényl-N-(trichloroacétyl)-amidophosphate (HL) séparément et en combinaison avec 16 μM C60 fullerène. (M ± m, n = 8)
Les données obtenues ont montré que l'application de C60 fullerène en combinaison avec 2,5 μM de HL n'a eu aucun effet nocif sur la stabilité structurelle de la membrane des érythrocytes sanguins et permet en même temps d'augmenter de manière significative l'activité cytotoxique de HL à cette faible concentration contre les cellules leucémiques. Malgré l'effet cytotoxique synergique du C60 fullerène et HL en concentration de 10 μM contre les cellules leucémiques, l'application de leur combinaison semble être limitée par l'intensification de l'effet hémolytique.
Enfin, dans le contexte de l'étude in vitro ci-dessus, il est important de souligner qu'une interface eau/solide contient de l'eau confinée qui peut également affecter à la fois le transport, les propriétés thermodynamiques des nanostructures [34, 35], et leur interaction avec les membranes cellulaires. [36].
Il existe des données de la littérature sur la localisation intracellulaire des dérivés des carbacylamidophosphates, en particulier la pénétration des phosphoramidates dans les cellules. Ainsi, les dérivés de phosphoramidate peuvent pénétrer à travers la membrane des lignées cellulaires MDA-231 du cancer du sein et du cancer du poumon (H460, H383 et H2009) [37]. Il a été démontré que les moutardes au nitrobenzyl phosphoramide traversent les membranes cellulaires et sont localisées dans les mitochondries de NTR + cellules de mammifères [10]. Il n'est pas exclu que C60 le fullerène, capable de pénétrer la membrane de la cellule cancéreuse par diffusion passive ou endocytose [28, 30, 32] avec accumulation dans le noyau et les mitochondries [30, 32, 33], pourrait être un transporteur de petites molécules antitumorales [ 38,39,40].
Conclusions
Un nouveau représentant des dérivés de carbacylamidophosphates qui ont deux substituants phénoxy près du groupe phosphoryle diphényl-N-(trichloroacétyl)-amidophosphate (HL) a été synthétisé et testé en tant qu'agent cytotoxique lui-même et en combinaison avec C60 fullerène. Selon les résultats de la simulation moléculaire, lorsque C60 fullerène puis HL ont été liés avec un sillon d'ADN mineur, un complexe rigide s'est formé stabilisé par empilement des interactions des groupes phényle HL avec C60 fullerène et nucléotide ADN G, ainsi que par les interactions de HL CCl3 grouper par liaisons ion-π avec C60 molécule et par liaisons électrostatiques avec le nucléotide G de l'ADN.
Avec l'utilisation du test MTT, nous avons montré une activité cytotoxique de HL contre des cellules leucémiques humaines CCRF-CM avec IC50 valeur détectée à une concentration de 10 μM à 72 h de traitement des cellules. The cytotoxic effect of HL was facilitated by C60 fullerene. Under combined action of 16 μM C60 fullerene and HL, the value of IC50 was detected at lower 5 μM HL concentration and at earlier 48 h period of incubation and besides the cytotoxic effect of HL was observed at a low 2.5 μM concentration at which HL by itself had no influence on cell viability.
Previously, we have shown a significant toxic effect of dimorfolido-N-trichloroacetylphosphoramide against human leukemic cells of different origin, but its effective concentration was high and no enhancement of toxicity after combined action with C60 fullerene was observed [16]. We assume that introduction of flexible of –P(O)(OC6 H5 ) groups instead of morfolido groups into CAPh derivative contributed to lowering of its toxic concentration against human leukemic cells ensuring its effective interaction with C60 molecule and DNA. Binding of C60 fullerene and HL with minor DNA groove with formation of a stable complex is assumed to be one of the possible reasons of their synergistic inhibition of CCRF-CЕM cells proliferation.
We have revealed that application of C60 fullerene in combination with 2.5 μM HL had no harmful effect on structural stability of blood erythrocytes membrane, while combination of C60 fullerene with 10 μM HL appeared to be limited by intensification of hemolytic effect.
Thus, C60 fullerene was shown to potentiate cytotoxic effect of HL and to increase significantly human leukemic cells sensitivity to its action in a low concentration. A combination of C60 fullerene with HL in a low concentration 2.5 μM may be promising for further biomedical studies.
Abréviations
- DMSO:
-
Dimethyl sulfoxide
- DNA:
-
Deoxyribonucleic acid
- FBS:
-
Fetal bovine serum
- HL:
-
Diphenyl-N-(trichloroacetyl)-amidophosphate
- IR :
-
Infrared spectroscopy
- MD:
-
Molecular dynamics
- MTT:
-
3-(4,5-Dimethyl-2-thiazolyl)-2,5-diphenyl-2-H-tetrazolium bromide
- NMR:
-
Nuclear magnetic resonance
- RPMI - 1640 medium:
-
Roswell Park Memorial Institute medium
Nanomatériaux
- L'interaction rotation-orbite de Coin Paradox améliore l'effet magnéto-optique et son application dans l'isolateur optique intégré sur puce
- Étude in vitro de l'influence des nanoparticules Au sur les lignées cellulaires HT29 et SPEV
- Effets d'interaction lors de l'assemblage de nanoparticules magnétiques
- Effets synergiques des nanoparticules d'Ag/BiV1-xMoxO4 avec une activité photocatalytique améliorée
- Fabrication, caractérisation et activité biologique de systèmes de nano-administration d'avermectine avec différentes tailles de particules
- Promotion de la croissance cellulaire SH-SY5Y par des nanoparticules d'or modifiées avec de la 6-mercaptopurine et un peptide pénétrant dans les neurones
- Propriétés des nanoparticules d'oxyde de zinc et leur activité contre les microbes
- Influence des nanotubes de carbone et de leurs dérivés sur les cellules tumorales in vitro et paramètres biochimiques, composition cellulaire du sang in vivo
- Évaluation de l'activité du cytochrome P450 3A4 inhibée par les nanoparticules d'or et des mécanismes moléculaires sous-jacents à sa toxicité cellulaire dans la lignée cellulaire de carcinome …



