Nanoparticules d'or de forme ronde :effet de la taille et de la concentration des particules sur la croissance des racines d'Arabidopsis thaliana
Résumé
De nos jours, en raison d'un large éventail d'applications de nanoparticules (NP) dans de nombreux domaines industriels, les accumulations de ces entités dans l'environnement posent un grand risque. En raison de leur inertie, les NP de métaux nobles peuvent rester longtemps inchangées dans les sols contaminés. Dans ce contexte, l'absorption de particules dépendante de la taille, de la forme et de la concentration par les plantes appartient à un domaine inexploré. Dans ce travail, nous présentons des solutions aqueuses d'AuNPs sphériques synthétisés biologiquement avec une distribution de taille assez étroite dans une plage de tailles allant de 10 à 18 nm. Leur caractérisation approfondie par spectroscopie d'absorption atomique, plasma à couplage inductif équipé d'une spectroscopie de masse, diffusion dynamique de la lumière (DLS) et méthodes MET a été suivie par l'étude de leur effet sur la croissance d'Arabidopsis thaliana (racines primaires et latérales), de manière dépendante de la taille des particules et de la concentration. En raison de la forme strictement ronde des AuNP et de l'absence d'agglomération des particules, la taille et la distribution de taille dérivées du DLS étaient en bonne concordance avec celles obtenues à partir de MET. La longueur et le nombre de A. thaliana les racines latérales étaient significativement affectées par tous les types d'AuNPs. Les AuNP les plus petites à la concentration la plus élevée ont inhibé la longueur des racines primaires et, en revanche, ont amélioré la croissance des racines des cheveux.
Contexte
De nos jours, la chimie et l'ingénierie modernes produisent d'énormes quantités de nano-objets afin d'améliorer les propriétés d'utilité de la matière non seulement dans des applications spéciales mais de plus en plus dans des produits de consommation quotidienne. Les matériaux nanostructurés, c'est-à-dire les nanoparticules [1, 2], les nanotiges [3], les nanotubes [4], les nanotextiles non tissés [5], tels qu'ils sont debout ou attachés à différents types de supports, augmentent considérablement les rendements dans presque tous les domaines d'applications industrielles allant des cosmétiques [6] et des soins de santé [7], en passant par la bio-ingénierie [8, 9], jusqu'aux applications de conversion d'énergie [10] et aux catalyseurs [3]. Alors que l'inclusion de nanomatériaux dans ces produits peut améliorer leurs performances, leur dégradation à la fin de leur durée de vie utile fournit plusieurs points d'entrée clés pour les NP synthétiques dans l'environnement. Les NP spécialement conçues, qui ont été largement utilisées dans les catalyseurs, les stabilisateurs de colorants protecteurs contre les UV, les agents antimicrobiens dans l'industrie textile ou les produits de santé et les cosmétiques (en particulier ceux à haute inertie chimique tels que Au, Ag, Pt et Pd) doivent faire l'objet d'une attention particulière, car ils peuvent s'accumuler dans l'environnement presque sans changement pendant de nombreuses années, déclenchant des processus jusqu'à présent inconnus lors de leur absorption par les plantes. Concernant les nanoparticules de métaux nobles (NMNPs), des travaux pionniers ont été publiés sur l'effet des nanoparticules d'argent (AgNPs) sur les semis de cresson de thale (Arabidopsis thaliana ), indiquant que de très faibles concentrations d'AgNPs (< 1 ppm) pourraient être toxiques pour les plantules [11]. Des AgNP de 20 à 80 nm ont clairement retardé la croissance et leur phytotoxicité dépend de la concentration et de la taille des particules. On a observé que l'extrémité de la racine (coiffe et columelle) virait au brun clair lorsque les racines primaires étaient exposées aux AgNPs. La pointe brune a été attribuée à l'adsorption d'AgNPs soit elle-même, soit en conjonction avec des matériaux de paroi cellulaire ou des métabolites secondaires produits par les pointes des racines. Cependant, le mécanisme exact n'a pas encore été élucidé.
Même s'il existe des études portant sur le rôle des NP dans l'environnement [12], celles ciblant les nanoparticules d'or (AuNP) sont encore rares [13]. Si elles sont disponibles, la majorité des données publiées sur la nanotoxicologie se sont concentrées sur la cytotoxicité chez les mammifères [14,15,16] ou les impacts sur les animaux et les bactéries [17,18,19,20], et seules quelques études ont considéré la toxicité des NP aux plantes. De plus, l'interaction des NMNP avec les plantes et d'autres organismes partageant des similitudes avec les cellules végétales, telles que les algues, a été peu étudiée jusqu'à présent, ce qui implique que les conséquences générales de l'exposition aux NMNP pour les cellules végétales restent encore incertaines [11]. L'absence de ces données conduit à une mauvaise compréhension de la façon dont les NMNP sont transférés et accumulés dans les différents niveaux de la chaîne alimentaire.
Dans ce travail, nous rapportons l'effet des nanoparticules d'or sur la croissance des plantes, en particulier sur le développement des racines primaires et latérales de A. thaliana en présence de particules de tailles différentes. Les AuNPs ont été synthétisés par voie humide dans le cadre d'un protocole biologiquement convivial n'utilisant aucun stabilisant, produisant des nanoparticules sphériques avec un contrôle précis de leur taille et de leur distribution de taille. Avant le traitement des plantes, les AuNP ont été soigneusement caractérisées par un large éventail de méthodes analytiques (AAS, ICP-MS, DLS et TEM).
Expérimental
Matériaux, appareils et procédures
Des nanoparticules d'or ont été synthétisées par une procédure légèrement adaptée publiée par Batús et al. [20]. Brièvement, 149 ml d'eau ont été chauffés dans un ballon à fond rond à deux cols de 250 ml jusqu'à ce qu'il commence à refluer. Ensuite, 1 mL de citrate de sodium 0,33 M et 0,945 mL de 10 mg/mL de tétrachloroaurate (III) de potassium dans de l'eau ont ensuite été ajoutés. Après 30 min, le chauffage a été arrêté et le mélange réactionnel a été laissé refroidir. Dans toutes les expériences de préparation, de l'eau Milli-Q (18,2 MΩ à 25 °C) a été utilisée.
Pour les dosages racinaires de A. thaliana , des AuNPs synthétisés de trois tailles différentes (10, 14 et 18 nm) ont été centrifugés à 5 000g pendant 1 h pour augmenter la concentration de particules jusqu'à la valeur limite de 2000 mg/L.
A. thaliana Les graines de Columbia (Col-0) (obtenues à partir de graines de Lehle, USA) ont été stérilisées en surface avec 30% (v /v ) solution d'eau de Javel pendant 10 min et rincée cinq fois avec de l'eau stérile. Des graines stériles ont été semées sur des plaques de gélose contenant ½ de milieu Murashige-Skoog (MS) et 1 % de gélose végétale (pH 5,8). Pour synchroniser la germination des graines, les plaques de gélose ont été maintenues à 4 °C pendant 2 jours. A. thaliana les plantes ont été cultivées pendant 5 jours dans des plaques orientées verticalement dans une chambre de croissance à 22 °C avec 100 μmol m − 2 s − 1 intensité lumineuse dans des conditions de journée longue (16 h/8 h cycle lumière/obscurité).
Des semis de cinq jours de taille similaire ont été transférés dans des plaques de gélose (20 plantes par plaque) contenant du milieu MS 1/16, différentes concentrations d'AuNP (0, 1, 10 et 100 mg/L) et de la gélose végétale à 1 % ( pH 5,8). AuNPs ont été ajoutés au milieu après autoclavage. En tant que contrôle, l'effet du tampon citrate de sodium a également été étudié. La longueur de la racine a été marquée et les semis ont été cultivés pendant les 5 jours suivants. L'incrément de la racine primaire et la longueur des racines latérales ont tous deux été mesurés à l'aide du logiciel JMicroVision 1.2.7.
Méthodes analytiques
Les solutions préparées d'AuNPs ont été caractérisées par spectroscopie d'absorption atomique (AAS), plasma à couplage inductif équipé d'une spectroscopie de masse (ICP-MS), diffusion dynamique de la lumière (DLS) et microscopie électronique à transmission (TEM).
Les concentrations de NP préparées ont été déterminées au moyen de l'AAS par un appareil VarianAA880 (Varian Inc., USA) en utilisant un atomiseur à flamme à une longueur d'onde de 242,8 nm. L'incertitude typique de concentration déterminée par cette méthode est inférieure à 3%.
Un plasma à couplage inductif avec détecteur de spectroscopie de masse (ICP-MS) a été utilisé pour déterminer la concentration d'ions Au provenant de la source chimique d'Au n'ayant pas réagi, à l'aide du spectromètre triple quadripôle Agilent 8800 (Agilent Technologies, Japon) connecté à un échantillonneur automatique. La solution colloïdale AuNPs a été pipetée dans des microtubes hydrophobes de 1,5 ml et centrifugée à 30 000g sur centrifugeuse Eppendorf 5430 pendant 1 h. Après la centrifugation, 0,3 mL de surnageant a été soigneusement retiré à l'aide d'une pipette et analysé par ICP-MS. La nébulisation de l'échantillon a été réalisée à l'aide d'un appareil MicroMist équipé d'une pompe péristaltique. Une solution tampon pure (2,2 mM de citrate de sodium) a été utilisée comme échantillon à blanc. L'incertitude de la mesure était inférieure à 3 %.
Les images MET ont été mesurées à l'aide de JEOL JEM-1010 (JEOL Ltd., Japon) fonctionnant à 400 kV. Une goutte de solution colloïdale a été placée sur une grille de cuivre recouverte d'un mince film de carbone amorphe sur un papier filtre. L'excès de solvant a été éliminé. Les échantillons ont été séchés à l'air et conservés sous vide dans un dessiccateur avant de les placer sur un porte-échantillon. La taille des particules a été mesurée à partir des micrographies MET et calculée en prenant en compte au moins 500 particules.
La distribution granulométrique a été déterminée par Zetasizer ZS90 (Malvern Instruments Ltd., Angleterre) dans le régime DLS pour la distribution granulométrique, équipé d'une photodiode à avalanche pour la détection du signal. Un laser à solide pompé par diode (50 mW, 532 nm) a été utilisé comme source lumineuse. Les mesures ont été effectuées dans des cuvettes en polystyrène à température ambiante.
Résultats et discussion
Caractérisation de nanoparticules
La taille et la distribution des tailles des AuNPs ont été déterminées par des analyses MET et DLS. Les résultats sont résumés dans le tableau 1, ainsi que les concentrations d'AuNP déterminées par AAS immédiatement après la synthèse des NP et les concentrations d'ions Au résiduels déterminées par ICP-MS. À partir de ces données, il est évident que notre protocole de synthèse fournit des nanoparticules d'Au bien contrôlées en taille avec une distribution de taille assez étroite. Ici, nous avons utilisé la méthode modifiée publiée par Batús et al. [20] pour la synthèse d'AuNPs stabilisées au citrate à taille et à forme contrôlées. Le protocole développé permet une extension de taille ciblée basée sur l'agrandissement d'AuNPs pré-synthétisés au moyen d'une réduction catalysée par la surface d'Au 3+ avec une inhibition simultanée efficace de la nucléation secondaire.
Wang et al. [21] ont trouvé qu'au cours d'une exposition hydroponique de 3 jours à A. thaliana soit à Ag + et AgNPs (5 nm) à la même concentration, la concentration d'Ag a diminué plus rapidement dans l'Ag + -solution traitée que dans celle d'AgNP, indiquant une absorption plus rapide d'Ag + ions. Par conséquent, nous avons porté une attention particulière à minimiser l'effet possible des ions Au sur la distorsion du résultat. Les AuNPs telles que synthétisées ont été centrifugées jusqu'à une concentration limite de 2000 mg/L et diluées avec du milieu MS aux concentrations requises (1, 10 et 100 mg/L). Après cette procédure, la concentration d'ions Au résiduels dans des solutions contenant 100 mg/L d'AuNPs a été déterminée par ICP-MS (voir Tableau 1). Apparemment, la centrifugation a eu un effet positif à la fois sur la présence d'ions Au résiduels dont les concentrations ont été réduites de deux ordres de grandeur par rapport aux solutions telles que synthétisées (tableau 1, AAS) et sur le contenu du tampon citrate lui-même.
Pour quantifier la polydispersité des NP, nous avons effectué une mesure DLS, qui est très sensible à la présence de conglomérats de particules éventuellement formés (Fig. 1). Dans cette mesure, même une petite quantité de NP agglomérées provoque la dominance du pic correspondant à des diamètres considérablement plus élevés, en particulier dans la distribution de taille pondérée en intensité (voir l'encadré sur la Fig. 1). Heureusement, aucune agglomération de particules n'a été détectée, et ainsi, la crédibilité de l'évaluation de la taille ne peut être affectée que par une approximation sphérique [22]. Malgré cet inconvénient, la mesure DLS fournit une image globale statistiquement plus significative de la distribution de la taille des particules par rapport à la MET, car elle évalue tout le volume de l'échantillon à la fois. En raison de la nature principalement ronde des NP préparées (voir Fig. 2), les tailles dérivées du DLS étaient en bon accord avec celles obtenues par MET (tableau 1). Les agglomérats de particules apparents, visibles sur l'image MET (Fig. 2, 10 nm), étaient plus probablement causés par la nécessité d'éliminer le solvant dans les mesures MET, plutôt que par l'interconnexion de particules individuelles dans la solution colloïdale elle-même.
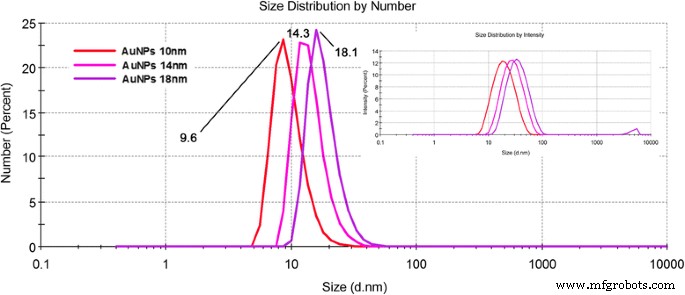
Analyse dynamique de diffusion de la lumière (distribution de taille pondérée en nombre) de solutions aqueuses d'AuNPs de différentes tailles. L'encart montre des données pondérées en intensité « brutes ». Les chiffres se réfèrent au diamètre moyen des particules en nm
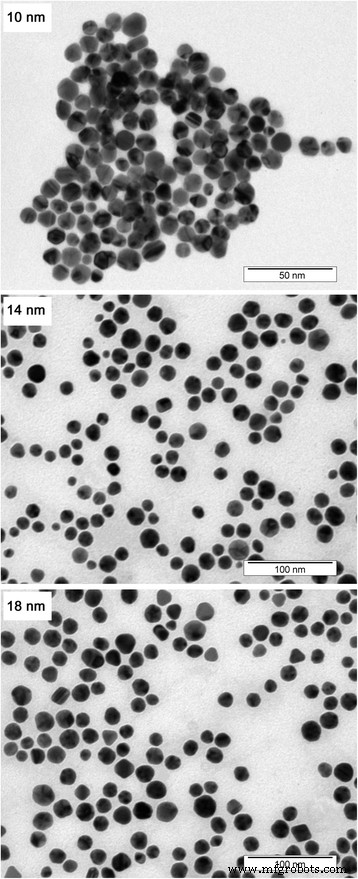
Images MET d'un ensemble préparé d'AuNPs. Veuillez noter que le grossissement de l'image diffère pour des tailles de NP particulières
Adaptation de solutions de nanoparticules pour répondre aux conditions de biologie végétale
En raison de la forte tendance à l'agrégation des AuNPs dans les milieux de croissance des plantes (milieu MS), couramment utilisés pour la croissance des plantes in vitro [23], nous avons dû optimiser le rapport mutuel de ces deux composants pour éviter l'agrégation des NPs tout en préservant des conditions acceptables pour la croissance des plantes. Différentes dilutions de MS ont été testées. L'agrégation des AuNPs était facilement visible par le changement de couleur (passage du rouge au violet). En raison de la faible concentration initiale d'AuNPs tels que synthétisés (environ 30 mg/L, voir le tableau 1), insuffisante pour les expériences biologiques, il a été nécessaire d'augmenter la concentration de NP par centrifugation. Par cette procédure, nous avons augmenté la concentration de particules jusqu'à la valeur limite de 2000 mg/L. Ces solutions de NPs ont ensuite été diluées aux concentrations finales, ce qui a également diminué la concentration du tampon citrate dans nos expériences. Pour les expériences de culture de A. thaliana , nous avons dilué les AuNPs dans un milieu 1/16 MS. Une agrégation minimale de NP était détectable dans ce milieu et les NP étaient beaucoup plus stables par rapport à 1/2 MS, 1/4 MS et 1/8 MS avec une croissance des plantes presque inchangée. La concentration des AuNPs dans les solutions finales a été déterminée par AAS. Étant donné que les expériences de croissance des plantes ont été réalisées in vitro (dans des conditions stériles), l'effet de la procédure de stérilisation sur les NP a également été étudié. L'autoclavage couramment utilisé (121 °C, 20 min) des milieux de croissance préparés a provoqué une agrégation complète des NP étudiées. Par conséquent, cette procédure n'était pas adaptée à nos expériences. L'ajout de NP dans un milieu gélosé autoclavé à environ 60 °C a finalement été utilisé comme procédure alternative dans laquelle aucune agrégation de NP n'a été détectée et le processus de stérilisation était toujours efficace.
Effet des NP sur la croissance des racines d'Arabidopsis thaliana in vitro
Des plantes modèles telles que la dicotylédone A. thaliana ont le potentiel d'aider à comprendre les facteurs de stress qui réduisent les rendements mondiaux des cultures dans le but d'identifier les gènes qui peuvent améliorer la viabilité dans des conditions de stress [24]. Toutes les formes testées d'AuNPs ont eu un effet significatif sur les racines latérales (LR). La longueur (Fig. 3a) et le nombre (Fig. 3b) des LR ont été réduits dans les plantes traitées au NP. Les concentrations les plus élevées d'AuNPs (100 mg/L) de toutes les tailles de particules étudiées ont induit une diminution de la longueur des LR à environ 50 %. Le nombre de LR diminue jusqu'à environ 70 % dans le cas des AuNPs de 18 nm et de la concentration la plus élevée (100 mg/L). Une réduction légèrement plus faible du nombre de LR a été observée lorsque la concentration la plus élevée de AuNPs plus petits (14 et 10 nm) a été utilisée (Fig. 3b). La longueur des racines primaires a également diminué après le traitement AuNP (Fig. 3c). L'effet négatif de l'AuNP à 10 nm était considérable, en particulier à des concentrations de particules plus élevées. L'effet des particules plus grosses (14, 18 nm) était beaucoup plus petit et similaire à l'effet du tampon citrate de sodium utilisé comme contrôle. La plupart des études publiées avec des NP modifiées ont indiqué un certain degré de phytotoxicité, en particulier à des concentrations élevées de NP. Par exemple, les AgNPs recouverts de citrate ont inhibé A. thaliana allongement des racines des plantules avec une dose-réponse linéaire de 67 à 535 μg/L après 2 semaines [25]. Plusieurs autres études utilisant les tests d'élongation des racines et de germination des graines ont démontré que la phytotoxicité était affectée par la taille des NP. De nombreuses études ont conclu que plus les NPs sont petites, plus elles sont phytotoxiques. Cependant, cette généralisation sur la toxicité dépendante de la taille des nanomatériaux manufacturés n'est pas toujours vraie pour toutes les combinaisons de plantes et de types de NP [21, 25]. Contrairement à cela, les nanotubes de carbone à paroi unique ont affecté positivement l'allongement des racines de la tomate, du chou, de la carotte et de la laitue en 24 à 48 h [26]. L'effet positif des AuNPs 24 nm sur le taux de germination des graines et la croissance végétative a été rapporté par Kumar et al. [13].
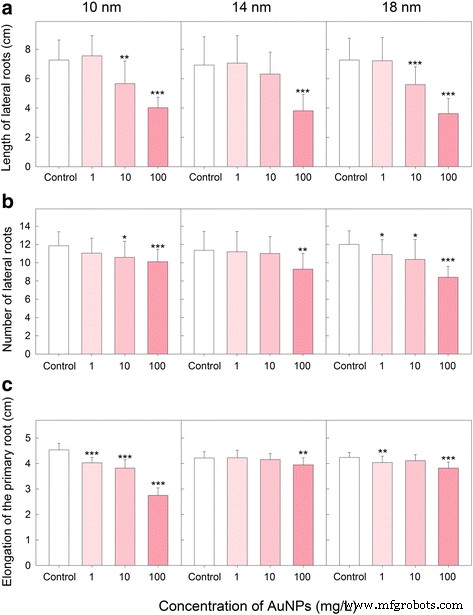
Effet des AuNP sur a longueur et b nombre de racines latérales et c allongement de la racine primaire de A. thaliana semis. Les plantes ont été exposées à différentes concentrations (0,1, 10 et 100 mg/L) de AuNPs de 10, 14 et 18 nm. Les données sont des moyennes + SD de 19–20 usines. *P < 0,05, ***i>P < 0,01, ****P < 0,001 ; t tester
Un effet positif substantiel des AuNPs de 10 nm sur la croissance des poils absorbants a été observé au cours des expériences de croissance des racines (Fig. 4). Cet effet présentait une forte dépendance à la concentration. L'augmentation de la concentration de NP a induit une croissance plus prononcée des poils absorbants (Fig. 4e). Ce comportement a souvent été observé chez des racines cultivées dans des sols pauvres en phosphore [27]. Un effet similaire n'a pas été observé dans le cas des AuNPs de 14 et 18 nm. Contrairement à cela, García-Sánchez et al. [28] ont observé, au cours de A. thaliana traitement avec des AgNPs disponibles dans le commerce, inhibition d'un certain nombre de poils absorbants liés à 1 cm de racine de plante. Une diminution des racines des cheveux a été observée dans le cas de toutes les particules testées, quelle que soit leur taille spécifique (10, 20, 40 et 80 nm), en utilisant une concentration uniforme de solutions de traitement de 200 mg/L. Les poils absorbants augmentent considérablement la surface des racines en contact avec le sol, et la plupart de l'eau et des nutriments qui pénètrent dans la plante sont absorbés par eux. Ainsi, leur développement est significativement affecté par les stimuli de l'environnement et les signaux de stress [29].
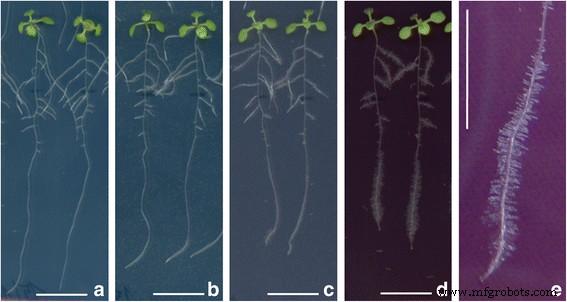
Effet de différentes concentrations d'AuNPs de 10 nm sur la croissance des poils absorbants dans A. thaliana semis. un Contrôle, b –d plantules traitées avec 1, 10 et 100 mg/L d'AuNPs, respectivement, et e détail de la croissance induite des poils absorbants chez une plante exposée à 100 mg/L d'AuNPs. Les barres d'échelle correspondent à 1 cm
Conclusions
Nous avons préparé avec succès des nanoparticules d'or par réduction douce à deux composants (citrate de sodium-tétrachloroaurate de potassium) dans l'environnement de l'eau, fournissant des particules de forme ronde et à distribution étroite avec un excellent contrôle sur leur taille résultante. La centrifugation post-synthèse a permis d'atteindre les concentrations de NP souhaitées et d'éliminer l'influence des ions et du tampon citrate sur la distorsion des résultats dans les expériences sur les plantes. L'effet des AuNPs de différentes tailles (10, 14 et 18 nm de diamètre) et de concentrations (1, 10 et 100 mg/L) sur la croissance des racines de A. thaliana a été étudiée. Le nombre et la longueur des racines latérales ont été significativement diminués après le traitement avec des solutions de NPs de concentrations de particules plus élevées, quelle que soit leur taille spécifique. Un effet négatif sur la croissance des racines primaires a été observé dans le cas des AuNPs de 10 nm. Étonnamment, les plus petits AuNP (10 nm) ont clairement induit la croissance des poils absorbants. Dans l'ensemble, cette étude a montré que l'exposition directe des plantes aux AuNPs contribuait de manière significative à la phytotoxicité et souligne la nécessité d'une élimination éco-responsable des déchets et des boues contenant des nanoparticules d'Au.
Abréviations
- AAS :
-
Spectroscopie d'absorption atomique
- AgNP :
-
Nanoparticules d'argent
- AuNP :
-
Nanoparticules d'or
- DLS :
-
Diffusion dynamique de la lumière
- ICP-MS :
-
Spectroscopie de masse équipée d'un plasma couplé par induction
- LR :
-
Racines latérales
- MS :
-
Murashige et Skoog
- NMNP :
-
Nanoparticules de métaux nobles
- NP :
-
Nanoparticules
- TEM :
-
Microscopie électronique à transmission
Nanomatériaux
- Nanoparticules plasmoniques
- À propos des nanoparticules semi-conductrices
- Nanoparticules d'or multifonctionnelles pour des applications diagnostiques et thérapeutiques améliorées :une revue
- Préparation de nanoparticules mPEG-ICA chargées en ICA et leur application dans le traitement des dommages cellulaires H9c2 induits par le LPS
- Des nanoparticules comme pompe à efflux et inhibiteur de biofilm pour rajeunir l'effet bactéricide des antibiotiques conventionnels
- Propriétés paramagnétiques des nanomatériaux dérivés du fullerène et de leurs composites polymères :effet de pompage drastique
- Polyglycérol hyperramifié modifié comme dispersant pour le contrôle de la taille et la stabilisation des nanoparticules d'or dans les hydrocarbures
- Effet de la méthode de synthèse des nanoparticules de manganite La1 − xSr x MnO3 sur leurs propriétés
- Promotion de la croissance cellulaire SH-SY5Y par des nanoparticules d'or modifiées avec de la 6-mercaptopurine et un peptide pénétrant dans les neurones



