Faible décroissance tunnel des jonctions monomoléculaires alcanes à terminaison iode
Résumé
Un problème clé pour le développement de dispositifs électroniques moléculaires est de comprendre le transport d'électrons des jonctions monomoléculaires. Dans ce travail, nous explorons le transport d'électrons de jonctions moléculaires uniques d'alcanes à terminaison iode en utilisant l'approche de jonction de rupture basée sur un microscope à effet tunnel. Le résultat montre que la conductance diminue de façon exponentielle avec l'augmentation de la longueur moléculaire avec une constante de désintégration β N = 0,5 par –CH2 (ou 4 nm −1 ). Il est important de noter que la décroissance tunnel de ces jonctions moléculaires est beaucoup plus faible que celle des molécules d'alcane avec des groupes thiol, amine et acide carboxylique comme groupes d'ancrage et même comparable à celle des molécules oligophényles conjuguées. La faible décroissance tunnel est attribuée à la faible hauteur de barrière entre la molécule d'alcane à terminaison iode et Au, ce qui est bien étayé par les calculs DFT. Le travail suggère que la décroissance tunnel peut être efficacement réglée par le groupe d'ancrage, ce qui peut guider la fabrication de fils moléculaires.
Contexte
La compréhension du transport électronique des jonctions monomoléculaires est cruciale pour le développement de dispositifs électroniques moléculaires [1,2,3,4,5,6,7,8,9,10,11,12,13,14,15,16 ]. Le modèle d'effet tunnel non résonnant a souvent été utilisé pour décrire le processus de transport d'électrons à travers une petite molécule, où la conductance de contact, la longueur moléculaire et la constante de décroissance tunnel sont les principaux paramètres [17, 18]. Dans la plupart des systèmes moléculaires, la constante de désintégration est fortement liée aux propriétés électroniques du squelette organique. Par exemple, les systèmes moléculaires conjugués ont une faible décroissance tunnel, contrairement aux systèmes non conjugués [17, 19]. Étant donné que la décroissance tunnel est déterminée par la hauteur de la barrière entre le niveau de Fermi de l'électrode et l'orbitale moléculaire inoccupée la plus basse (LUMO) ou l'orbitale moléculaire occupée la plus élevée (HOMO) des jonctions moléculaires [17, 20], il est possible de régler le niveau d'énergie moléculaire. vers le niveau de Fermi pour obtenir la faible décroissance [21,22,23,24].
Dans les jonctions monomoléculaires, le groupe d'ancrage joue un rôle important dans le contrôle du couplage électronique entre les squelettes organiques avec les électrodes [21, 23, 24, 25]. Une série de mesures de conductance pour les molécules à base d'alcanes a montré un effet significatif de différents groupes d'ancrage sur la géométrie de liaison, les probabilités de formation de jonctions, la conductance de contact et même le canal de conductance (via LUMO ou HOMO) des jonctions moléculaires [21,22, 23,24,25]. Étant donné que le groupe d'ancrage peut réguler les orbitales frontières dans la jonction moléculaire, la décroissance tunnel de la molécule peut également être réglée par le groupe d'ancrage [24]. Cependant, une étude limitée a été axée sur ce domaine.
Ici, nous rapportons le transport d'électrons de molécules d'alcanes terminées par un groupe iode en utilisant la jonction de rupture de microscopie à effet tunnel (STM-BJ) (Fig. 1) [26, 27]. Les mesures de conductance moléculaire unique montrent que la conductance diminue de façon exponentielle avec l'augmentation des longueurs moléculaires et que la constante de décroissance des molécules d'alcane avec le groupe iode est beaucoup plus faible que celle des analogues avec d'autres groupes d'ancrage. Les différentes constantes de décroissance tunnel pour les molécules d'alcane avec des groupes d'ancrage variés s'expliquent par la hauteur de la barrière entre la molécule et l'électrode.
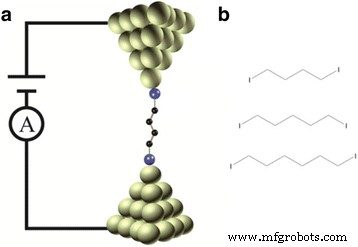
Schéma de principe de la jonction de rupture de microscopie à effet tunnel (STM-BJ) et des structures moléculaires. un Schéma du STM-BJ avec jonction moléculaire. b Structures moléculaires des molécules d'alcane iodé
Méthodes
Le 1,4-butanediiodo, le 1,5-pentanediiodo et le 1,6-hexanediiodo ont été achetés auprès d'Alfa Aesar. Toutes les solutions ont été préparées avec de l'éthanol. Au (111) a été utilisé comme substrat, tandis que des pointes d'Au coupées mécaniquement ont été utilisées comme pointes. Avant chaque expérience, l'Au (111) a été poli électrochimiquement et soigneusement recuit dans une flamme au butane, puis séché à l'azote.
Le substrat Au (111) a été immergé dans une solution d'éthanol fraîchement préparée contenant des molécules cibles 0,1 mM pendant 10 min. La mesure de la conductance a été réalisée sur le Nanoscope IIIa STM modifié (Veeco, USA.) en utilisant la méthode STM-BJ à température ambiante [28,29,30], qui a simplement mesuré la conductance des jonctions monomoléculaires formées en déplaçant à plusieurs reprises la pointe dans et hors du substrat à une vitesse constante. Au cours du processus, les molécules pourraient s'ancrer entre les deux électrodes métalliques et former des jonctions moléculaires uniques. Des milliers de ces courbes ont été collectées pour une analyse statistique. Toutes les expériences ont été réalisées avec une tension de polarisation fixe de 100 mV. Étant donné que les molécules avec de l'iode comme groupe d'ancrage sont un matériau photosensible, l'expérience a été réalisée sous ombrage.
Résultats et discussion
Mesure de la conductance des jonctions moléculaires simples alcanes à terminaison iode
Les mesures de conductance ont d'abord été réalisées sur Au(111) avec monocouche de 1,4-butanediiodo par STM-BJ. La figure 2a donne les traces de conductance typiques présentant la caractéristique pas à pas. Les traces de conductance montrent un plateau à 1 G 0 , indiquant la formation d'un contact atomique Au stable. Plateau à une valeur de conductance de 10 −3,6 G 0 (19,47 ns) se trouve également à côté du 1 G 0 , en raison de la formation de jonction moléculaire. Un histogramme de conductance pourrait également être obtenu en traitant avec le logarithme et le binning de la valeur de conductance de plus de 3000 traces de conductance, puis, l'intensité de l'histogramme de conductance a été normalisée par le nombre de traces utilisées et montre un pic de conductance à 10 − 3.6 G 0 (19,44 ns) (Fig. 2b). Ceux-ci montrent que le groupe iode peut servir de groupe d'ancrage efficace formant une jonction moléculaire. Cependant, cette valeur est inférieure à la valeur de conductance moléculaire unique de la 1,4-butanediamine avec une amine comme groupe d'ancrage, ce qui peut provenir d'une faible interaction entre l'iode et l'électrode Au [31].
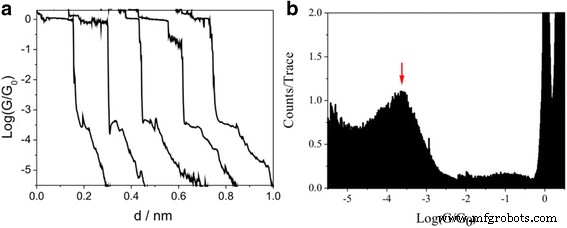
Conductance moléculaire unique des jonctions Au–1,4-butanediiodo–Au. un Courbes de conductance typiques des jonctions Au–1,4-butanediiodo–Au mesurées à un biais de 100 mV. b Histogramme de conductance à l'échelle logarithmique des jonctions 1,4-butanediiodo avec contacts Au
En comparaison avec le 1,4-diiodobutane, pics prononcés à 10 −3,8 G 0 (12,28 ns) et 10 −4,0 G 0 (7,75 ns) sont trouvés pour le 1,5-pentanediiodo et le 1,6-hexanediiodo, respectivement (Fig. 3). Les valeurs de conductance diminuent avec l'augmentation de la longueur de la molécule. Pendant ce temps, les valeurs de conductance du 1,5-pentanediiodo et du 1,6-hexanediiodo sont respectivement inférieures à celles de la 1,5-pentanediamine et de la 1,6-hexanediamine [31], ce qui peut être causé par l'interaction différente dans l'alcane- à base de jonctions moléculaires entre les groupes d'ancrage d'iode et d'amine se liant aux électrodes d'Au [32].
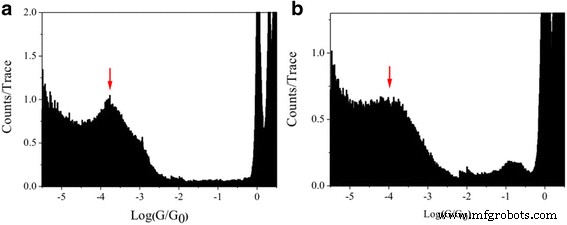
Conductance moléculaire unique de 1,5-pentanediiodo et 1,6-hexanediiodo avec électrode Au. Histogramme de conductance à l'échelle logarithmique de jonctions moléculaires uniques avec a 1,5-pentanediiodo et b 1,6-hexanediiodo
Les histogrammes de conductance bidimensionnels ont également été construits pour ces jonctions moléculaires (Fichier supplémentaire 1 :Figure S1) et donnent des valeurs de conductance similaires des histogrammes unidimensionnels. Typiquement, la distance de rupture des jonctions moléculaires augmente avec l'augmentation de la longueur moléculaire. Nous analysons également la distance par rapport à la valeur de conductance de 10 −5,0 G 0 à 10 −0,3 G 0 comme le montre la figure 4, et des distances de rupture de 0,1, 0,2 et 0,3 nm sont trouvées pour le 1,4-butanediiodo, le 1,5-pentanediiodo et le 1,6-hexanediiodo, respectivement. Ici, les distances de rupture sont obtenues à partir du pic maximum de l'histogramme des distances de rupture [33]. Il a été rapporté qu'il existe une distance de retour de 0,5 nm pour Au après la rupture du contact Au-Au [34, 35] ; ainsi, les distances absolues pour ces jonctions moléculaires entre les électrodes pourraient être de 0,6, 0,7 et 0,8 nm, qui se trouvent respectivement pour le 1,4-butanediiodo, le 1,5-pentanediiodo et le 1,6-hexanediiodo. Ces distances sont comparables à la longueur des molécules. Eder et al. ont rapporté que l'adsorption de monocouche de 1,3,5-tri (4-iodophényl)-benzène sur Au (111) peut provoquer une déshalogénation partielle [36]; cependant, une valeur de conductance très supérieure pour ces jonctions moléculaires de contact covalentes Au-C peut être trouvée pour les molécules avec quatre (environ 10 −1 G0 ) et six (plus grand que 10 −2 G0 ) –CH2 – unités [37]. Ainsi, nous proposons que les molécules actuellement étudiées entrent en contact avec l'Au via le contact Au-I.
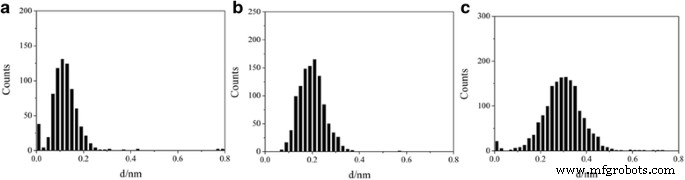
Distances de rupture pour les alcanes à terminaison iode. Distances de rupture de a 1,4-butanediodo, b 1,5-pentanediiodo, et c 1,6-hexanediiodo obtenu à partir de courbes de conductance entre 10 −5,0 G 0 et 10 −0,3 G 0
Constante de décroissance tunnel des jonctions moléculaires simples alcanes terminées par l'iode
Sous le biais actuel, la conductance de ces molécules peut être exprimée sous la forme G = G c exp(–β N N ). Ici, G est la conductance de la molécule et G c est la conductance de contact et est déterminée par l'interaction entre le groupe d'ancrage et l'électrode. N est le nombre de méthylène dans la molécule, et β N est la constante de décroissance tunnel, qui reflète l'efficacité de couplage du transport d'électrons entre la molécule et l'électrode. Comme le montre la figure 5, nous traçons une échelle de conductance en logarithme naturel en fonction du nombre de méthylène ; constante de décroissance tunnel β N de 0,5 par –CH2 est déterminé à partir de la pente de l'ajustement linéaire. Cette décroissance tunnel est très faible dans les molécules à base d'alcanes. Pour les molécules à base d'alcanes, β N se trouve généralement autour de 1,0 par –CH2 pour le thiol (SH) [23, 38], tandis qu'environ 0,9 et 0,8 par –CH2 sont déterminés pour l'amine (NH2 ) [23, 31] et l'acide carboxylique (COOH), respectivement [39]. Ainsi, la décroissance tunnel avec l'iode montre la valeur la plus faible parmi les groupes d'ancrage avec une tendance β N (thiol)> β N (amine)> β N (acide carboxylique)> β N (iode), ce qui peut être dû à la différence dans l'alignement des niveaux d'énergie moléculaire au niveau de Fermi de l'électrode Au [23, 31]. La décroissance tunnel de 0,5 par –CH2 peut également être converti en 4 nm −1 , qui est comparable aux oligophényles avec 3,5 à 5 nm −1 [40, 41].
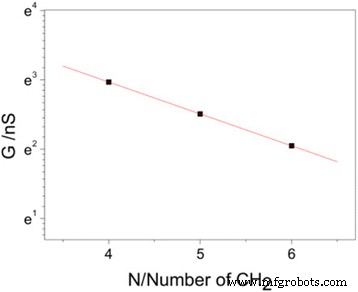
Conductance d'une molécule en fonction de la longueur moléculaire pour les alcanes à terminaison iode. Tracés logarithmiques de la conductance d'une molécule en fonction de la longueur moléculaire pour les alcanes à terminaison iode
Le β N pour les jonctions métal-molécule-métal peut être simplement décrit par l'équation ci-dessous [17, 20, 38],
$$ {\beta}_N\ \alpha\ \sqrt[2]{\frac{2 m\varPhi}{h^2}} $$
où m est la masse effective des électrons et 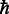 est la constante de Planck réduite. Φ représente la hauteur de la barrière, qui est déterminée par l'écart énergétique entre le niveau de Fermi et les niveaux d'énergie moléculaire dans la jonction. De toute évidence, le β N La valeur est proportionnelle à la racine carrée de la hauteur de la barrière. Ainsi, nous pouvons proposer que les molécules d'alcanes à terminaison iode ont de petits Φ avec l'électrode Au.
est la constante de Planck réduite. Φ représente la hauteur de la barrière, qui est déterminée par l'écart énergétique entre le niveau de Fermi et les niveaux d'énergie moléculaire dans la jonction. De toute évidence, le β N La valeur est proportionnelle à la racine carrée de la hauteur de la barrière. Ainsi, nous pouvons proposer que les molécules d'alcanes à terminaison iode ont de petits Φ avec l'électrode Au.
Hauteur de barrière de jonctions moléculaires uniques avec différents groupes d'ancrage
Prendre le –(CH2 )6 - en tant qu'épine dorsale, nous avons effectué les calculs approximatifs (voir les détails de calcul dans le fichier supplémentaire 1) pour étudier les orbitales moléculaires frontières des complexes avec quatre atomes d'Au aux deux extrémités, y compris le 1,6-hexanedithiol (C6DT), 1,6- l'hexanediamineb (C6DA), l'acide 1,6-hexanedicarboxylique (C6DC) et le 1,6-hexanediiodo (C6DI). Comme le montre le tableau 1, les valeurs HOMO et LUMO sont respectivement de − 6.18 et − 1.99 eV pour C6DT, tandis que HOMO (6.02 eV) et LUMO (− 1.85 eV) sont trouvées pour C6DA. Pendant ce temps, les niveaux d'énergie HOMO et LUMO sont calculés pour C6DC (-6,33 et -2,58 eV) et C6DI (-6,22 et -2,61 eV).
Pour le niveau de Fermi de l'électrode Au, nous devons considérer l'influence de l'adsorption des molécules. Dans la condition de vide, l'Au propre donne une fonction de travail de 5,1 eV [42] ; en attendant, cette valeur peut être évidemment modifiée par l'adsorption de molécules. Kim et al. [43] et Yuan et al. [44] ont trouvé que le travail de sortie d'Au est d'environ 4,2 eV (4,0 à 4,4 eV) sur les monocouches auto-assemblées adsorbées (SAM) mesurées par le spectromètre photoélectronique ultraviolet (UPS). Low et al. a également étudié le transport d'électrons des molécules à base de thiophène de TOTOT (LUMO -3,3 eV, HOMO - 5,2 eV) et TTOp TT (LUMO − 3,6 eV, HOMO − 5,1 eV) avec Au comme électrode (T, O et Op désignent respectivement le thiophène, le thiophène-1,1-dioxyde et la thiénopyrrolodione oxydée) [45]. Les résultats montrent que le niveau Fermi d'Au est au milieu de LUMO et HOMO. Ainsi, nous pouvons en déduire que le niveau de Fermi de Au peut être autour du niveau d'énergie moyen de LUMO et HOMO, qui sont de − 4.25 et − 4.35 eV établis à partir de TOTOT et TTOP TT, respectivement. Le niveau de Fermi de Au − 4,25 et − 4,35 eV est similaire à celui mesuré par UPS avec − 4,2 eV [43]. D'après ce qui précède, nous utiliserons le − 4,2 eV comme niveau de Fermi de l'électrode Au avec l'adsorption de la molécule.
En supposant le niveau de Fermi de − 4,2 eV pour Au avec SAM, C6DT et C6DA sont le transport d'électrons dominé par HOMO, tandis que le transport d'électrons dominé par LUMO est proposé pour le C6DC et le C6DI. Ainsi, la hauteur de barrière Φ peut être établi à 1,98 eV (C6DT), 1,82 eV (C6DA), 1,62 eV (C6DC) et 1,59 eV (C6DI) (Tableau 1). La tendance de la hauteur de barrière entre la molécule et Au est Φ C6DT (thiol)> Φ C6DA (amine)> Φ C6DC (acide carboxylique)> Φ C6DI (iode), ce qui est cohérent avec la tendance de la décroissance tunnel (β ). Ainsi, la faible décroissance tunnel inhabituelle peut être due à la faible hauteur de barrière entre les molécules d'alcanes à terminaison iode et Au.
Conclusions
En conclusion, nous avons mesuré la conductance de molécules à base d'alcanes avec un groupe iode en contact avec des électrodes Au par STM-BJ à température ambiante. Une désintégration tunnel β N de 0,5 par –CH2 a été trouvé pour les molécules avec des électrodes Au, ce qui est beaucoup plus faible que celui des molécules à base d'alcanes avec d'autres groupes d'ancrage. Cela peut être causé par la faible hauteur de barrière entre la molécule d'alcane à terminaison iode et Au. Le travail actuel montre le rôle important du groupe d'ancrage dans les caractéristiques électriques des jonctions moléculaires uniques, qui peuvent régler la décroissance tunnel de la jonction moléculaire et guider le fil moléculaire de fabrication.
Abréviations
- HOMO :
-
Orbitale moléculaire la plus occupée
- LUMO :
-
Orbitale moléculaire inoccupée la plus basse
- SAM :
-
Monocouches auto-assemblées
- STM-BJ :
-
Jonction de rupture de microscopie à effet tunnel
- UPS :
-
Spectroscopie de photoélectrons ultraviolets
Nanomatériaux
- Le Conseil européen de la recherche finance la recherche sur les dispositifs à molécule unique par manipulation d'atomes
- Effet de surface sur le transport du pétrole dans les nanocanaux :une étude de dynamique moléculaire
- Propriétés de photoluminescence des modifications polymorphes du poly(3-hexylthiophène) de bas poids moléculaire
- Modélisation et simulation de dynamique moléculaire de la coupe de diamant de cérium
- Dépendance de la température de la bande interdite dans le MoSe2 cultivé par épitaxie par faisceau moléculaire
- Électrode porte d'argent imprimée par jet d'encre et durcie aux UV avec une faible résistivité électrique
- Lasers DFB Quantum Cascade à substrat à faible consommation d'énergie
- Étude de l'effet de la direction d'impact sur le processus de coupe nanométrique abrasif avec la dynamique moléculaire
- Causes du faible facteur de puissance



