CdS Nanoparticle-Modified Nanoparticle α-Fe2O3/TiO2 Nanorod Array Photoanode pour une oxydation photoélectrochimique efficace de l'eau
Résumé
Dans ce travail, nous démontrons un processus d'adsorption et de réaction de couche ionique successif facile accompagné d'une méthode hydrothermale pour synthétiser du α-Fe2 modifié par des nanoparticules de CdS O3 /TiO2 réseau de nanotiges pour une oxydation photoélectrochimique (PEC) efficace de l'eau. En intégrant CdS/α-Fe2 O3 /TiO2 système ternaire, la capacité d'absorption de la lumière de la photoanode peut être efficacement améliorée avec une réponse optique évidemment élargie à la région de la lumière visible, facilite grandement la séparation des porteurs photogénérés, donnant lieu à l'amélioration des performances d'oxydation de l'eau PEC. Surtout, pour l'hétérostructure anormale de type II conçue entre Fe2 O3 /TiO2 , la position de la bande de conduction de Fe2 O3 est supérieur à celui de TiO2 , les électrons photogénérés à partir de Fe2 O3 se recombinera rapidement avec les trous photogénérés de TiO2 , conduit ainsi à une séparation efficace des électrons photogénérés de Fe2 O3 /trous de TiO2 au Fe2 O3 /TiO2 interface, améliorant considérablement l'efficacité de séparation des trous photogénérés dans Fe2 O3 et améliore l'efficacité d'injection d'électrons photogénérés dans TiO2 . Fonctionnant comme photoanodes de l'oxydation de l'eau PEC, CdS/α-Fe2 O3 /TiO2 l'électrode hétérostructure présente une densité de photocourant améliorée de 0,62 mA cm − 2 à 1,23 V par rapport à une électrode à hydrogène réversible (RHE) dans un électrolyte alcalin, avec un potentiel de début manifestement décalé de 80 mV. Ce travail fournit des méthodes prometteuses pour améliorer les performances d'oxydation de l'eau PEC du TiO2 -à base de photoanodes à hétérostructure.
Contexte
Pour résoudre le grave problème de la pollution et des ressources limitées en ressources fossiles, la séparation photoélectrochimique (PEC) de l'eau pour produire de l'hydrogène a été considérée comme l'une des stratégies les plus prometteuses pour la conversion de l'énergie solaire. Depuis le premier rapport sur l'oxydation de l'eau PEC à base de TiO2 [1], TiO2 a attiré beaucoup d'attention en tant que matériaux de photoanode pour l'oxydation de l'eau PEC, en raison de ses propriétés PEC stables, de sa forte réponse optique et de sa position de bande d'énergie appropriée [2, 3]. Cependant, les performances PEC du TiO2 vierge la photoanode est fortement confinée par la lente cinétique d'oxydation de l'eau due à la faible capacité de séparation des supports photogénérés et à une capacité d'absorption de lumière insuffisante [4, 5].
Par conséquent, diverses stratégies ont été adoptées pour améliorer les performances d'oxydation de l'eau PEC du TiO2, vierge. telles que la modification de surface [6], la sensibilisation aux points quantiques et la construction d'hétérojonctions [7, 8]. Une méthode efficace pour améliorer les performances de séparation des supports photogénérés consiste à construire une photoanode hétérostructurée. Par exemple, construire une hétérojonction entre TiO2 et d'autres semi-conducteurs à oxyde métallique avec des structures de bandes d'énergie adaptées (comme Co3 O4 /TiO2 [9] et ZnIn2 S4 /TiO2 [10, 11]) peut faciliter efficacement la séparation des électrons et des trous photogénérés ; par conséquent, les performances de séparation de l'eau PEC du TiO2 vierge peut évidemment être amélioré. Parmi divers semi-conducteurs à oxyde métallique, l'hématite (α-Fe2 O3 ) est considéré comme un matériau de photoanode prometteur en raison de la bande interdite appropriée (~ 2,0 eV) pour la récolte de la lumière solaire, une excellente stabilité et un faible coût [12]. De plus, l'efficacité de conversion de puissance théorique (PCE) de α-Fe2 O3 peut atteindre 15,3 %, avec une densité de photocourant de 12,6 mA cm − 2 à 1,23 V par rapport à une électrode à hydrogène réversible (RHE) sous l'irradiation solaire standard [13]. Par conséquent, en construisant α-Fe2 O3 /TiO2 photoanode hétérostructurée ne peut pas seulement améliorer les performances de séparation des porteurs dans TiO2 mais aussi étendre efficacement la plage d'absorption lumineuse du TiO2 . Pendant ce temps, selon les dernières recherches, α-Fe2 O3 Les photoanodes souffrent d'une courte durée de vie des paires électron-trou et d'une longueur de diffusion des trous (2 à 4 nm), ce qui entraîne un taux de recombinaison élevé des porteurs photogénérés, ce qui entrave l'amélioration des performances du PEC [12]. Dans ce cas, pour améliorer encore les performances de séparation de l'eau PEC de Fe2 O3 /TiO2 les photoanodes, certains semi-conducteurs à bande interdite étroite, comme le CdS [14, 15] et le PbS [16], peuvent être couplés pour faciliter la séparation des porteurs photogénérés. Parmi eux, CdS/Fe2 O3 /TiO2 La photoanode hétérostructurée est considérée comme un choix prometteur avec une bande interdite adaptée et une plage d'absorption de la lumière étendue. En outre, le processus de transport des porteurs peut être efficacement amélioré car les porteurs photogénérés peuvent être rapidement séparés à l'interface de CdS/Fe2 O3 /TiO2 , diminuant ainsi considérablement les taux de recombinaison des porteuses.
De plus, afin de construire une électrode avancée pour le système de séparation d'eau PEC, les matériaux d'électrode doivent posséder des caractéristiques telles qu'une capacité de capture de lumière incidente suffisante et des tunnels pour le transport de charge. Par rapport aux photoanodes planaires générales, les photoanodes à matrice de nanotiges (NR) unidimensionnelles (1D) présentent de bonnes performances de récupération de la lumière incidente en raison des processus de multidiffusion améliorés [17], ce qui conduirait à une performance améliorée d'oxydation de l'eau PEC. En outre, il est rapporté que le réseau 1D NR présente également d'excellentes performances de transport de porteurs puisque les porteurs photogénérés peuvent être directement transportés le long du NR, ainsi la recombinaison directe des porteurs à la frontière cristalline peut être efficacement évitée [18]. De plus, afin d'élargir davantage la surface de ces réseaux 1D NR, qui peuvent apporter plus de sites de réaction PEC et améliorer les performances PEC, 1D NR avec des nanostructures ramifiées est attendu [19]. Une telle architecture intégrée offre un long chemin optique pour une collecte efficace de la lumière, une courte distance de diffusion pour un excellent transport de charge et une grande surface pour une collecte rapide de charge interfaciale, ce qui est très avantageux pour l'amélioration des performances PEC. Par conséquent, il serait particulièrement intéressant de concevoir un Fe2 modifié par CdS O3 /TiO2 réseau d'hétérostructure NR pour l'oxydation de l'eau PEC.
Ici, nous avons rapporté une méthode hydrothermale d'adsorption et de réaction de couche ionique successive facile (SILAR) pour synthétiser Fe2 modifié par CdS O3 /TiO2 Réseau NR pour une oxydation efficace de l'eau PEC. L'étude UV-vis confirme le CdS/Fe2 O3 /TiO2 La matrice NR affiche d'excellentes performances de réponse optique avec une plage d'absorption de lumière élargie évidente. Un processus de transfert de charge amélioré et un taux de recombinaison de charge diminué peuvent être mis en évidence au moyen du spectre PL et des tracés EIS. Appliqué comme photoanode pour l'oxydation de l'eau PEC, CdS/Fe2 O3 /TiO2 La matrice NR présente une densité de photocourant considérablement améliorée de 0,62 mA cm − 2 (1,23 V contre RHE) dans l'électrolyte alcalin par rapport au TiO2 vierge (0,32 mA cm − 2 à 1,23 V contre RHE). On pense que la voie de synthèse et l'application de CdS/Fe2 O3 /TiO2 La matrice NR actuellement signalée est d'une grande importance et peut être appliquée dans d'autres dispositifs photovoltaïques et photoélectroniques.
Méthodes
Préparation de CdS/Fe2 O3 /TiO2 Photoanode hétérostructurée NR
Synthèse de TiO2 Tableau NR
Pour synthétiser TiO2 Réseau NR sur le verre FTO, le FTO a été découpé en rectangle et nettoyé par ultrasons avec de l'eau déminéralisée, de l'acétone et de l'éthanol, successivement. Ensuite, le FTO a été placé dans l'autoclave contenant une solution mélangée d'eau déminéralisée (20 ml), d'acide chlorhydrique (20 ml) et d'isopropoxyde de titane (1,1 ml) et cuit à 160 °C pendant 6 h. Après la réaction, le FTO a été lavé plusieurs fois avec de l'eau déminéralisée et de l'éthanol, puis a été recuit à l'air à 450 °C pendant 0,5 h.
Synthèse de Fe2 O3 /TiO2 Tableau NR
Pour faire pousser α-Fe2 O3 sur TiO2 NR, tel qu'obtenu TiO2 La matrice NR a été placée dans une solution mélangée de FeCl3 (15 ml, 0,1 M) et NaNO3 (15 ml, 0,5 M) puis transféré à l'autoclave. En chauffant à 100 °C pendant 2 h, l'autoclave a été refroidi à température ambiante et le substrat FTO a été lavé plusieurs fois avec de l'eau déminéralisée et de l'éthanol. Enfin, le substrat FTO a été recuit sous air à 450 °C pendant 1 h.
Synthèse de CdS/Fe2 O3 /TiO2 NR
Le -Fe2 obtenu O3 /TiO2 La matrice NR a été prétraitée avec une solution d'éthanol d'acide mercaptopropinioc (MPA, 0,3 M) pendant une nuit à 50 °C, puis lavée avec de l'éthanol pour éliminer l'excès de MPA. Afin de déposer la couche de CdS, une méthode d'adsorption et de réaction de couche ionique successive facile (SILAR) est appliquée. La matrice NR prétraitée a été successivement immergée dans quatre solutions différentes pendant 30 s, y compris Cd(NO3 )2 ·4H2 O (éthanol, 0,1 M), éthanol pur, Na2 S·9H2 O (méthanol, 0,2 M) et méthanol pur, respectivement. Le processus SILAR a été répété cinq fois, puis le substrat a été lavé avec du méthanol pour éliminer le CdS supplémentaire.
Caractérisation des matériaux
Les structures de phase ont été caractérisées par diffractomètre à rayons X sur poudre (XRD) dans une plage 2θ de 20 à 80°. La morphologie des produits a été étudiée avec une microscopie électronique à balayage à émission de champ (FE-SEM) associée à une spectroscopie de rayons X à dispersion d'énergie (EDS). Les images de microscopie électronique à transmission (MET) ont été collectées via un équipement Tecnai 20 U-Twin. Les spectres d'absorption et de photoluminescence (PL) ont été testés avec TU-1900 et Hitachi U-4100, respectivement.
Caractérisation des performances photoélectrochimiques
Les performances d'oxydation de l'eau PEC ont été caractérisées avec la station électrochimique CHI660E avec un mode à trois électrodes. L'électrolyte appliqué était constitué de NaOH 1M. Avant le test, le système a été barboté avec de l'argon pendant 30 minutes pour éliminer le gaz dissous dans l'électrolyte. Les voltamogrammes linéaires (LSV) et chronoampérométriques I-t les courbes ont été enregistrées sous des éclairages solaires standard (100 mW cm − 2 ). Les tracés de Mott-Schottky ont été mesurés dans l'obscurité à une fréquence alternative de 1,0 kHz.
Par la suite, le potentiel d'électrode a été converti en potentiel RHE avec l'équation de Nernst :
$$ {E}_{\mathrm{RHE}}={E}_{\mathrm{Ag}/\mathrm{AgCl}}+0.059\ \mathrm{pH}+{E^o}_{\mathrm{ Ag}/\mathrm{AgCl}} $$ (1)où E RHE était le potentiel converti par rapport à RHE, E Ag/AgCl était le potentiel mesuré par rapport à l'électrode Ag/AgCl, et E o Ag/AgCl = 0,1976 V à 25 °C.
Résultat et discussion
Caractérisation de la structure et de la morphologie
Les structures de phase des produits synthétisés sont caractérisées par les motifs XRD de la figure 1. Comme le montre la figure 1a, le rutile TiO2 les réseaux de nanotiges (NR) sont synthétisés avec succès. Les pics de diffraction à 36,0°, 44,1°, 54,3°, 62,7°, 64,0°, 65,4° et 69,8° correspondent bien à (101), (210), (211), (002), (310), (221 ), et (112) plans de rutile TiO2 (JCPDS. 21-1276). Après dépôt de Fe2 O3 , les pics de diffraction XRD supplémentaires à 32,9° et 45,2° peuvent être indexés sur les plans (222) et (332) de Fe2 O3 (JCPDS. 39-0238). Le procédé SILAR est appliqué pour faire croître des nanoparticules de CdS, les pics de diffraction à 26,4°, 28,2° correspondant bien aux plans (002) et (101) de CdS (JCPDS. 65-3414) confirment le succès de croissance des nanoparticules de CdS sur Fe 2 O3 /TiO2 . L'image SEM de la figure 1b montre que TiO2 Les NR sont cultivés uniformément sur le substrat FTO d'un diamètre de 50 nm. La surface NR est relativement lisse. Après croissance de Fe2 O3 en surface de TiO2 , le diamètre de Fe2 O3 /TiO2 s'agrandit et augmente jusqu'à 60 nm. De plus, la surface des NR devient beaucoup plus rugueuse. Un dépôt supplémentaire de nanoparticules de CdS peut entraîner une augmentation du diamètre du Fe2 O3 /TiO2 NR composite. Pour confirmer davantage la distribution des éléments du CdS/Fe2 obtenu O3 /TiO2 NR, les images de cartographie EDS croisées sont enregistrées et affichées dans le fichier supplémentaire 1 :figure S1, fichier supplémentaire 2 :figure S2. On peut voir que les éléments Ti, Fe, Cd et S sont uniformément répartis entre les échantillons.
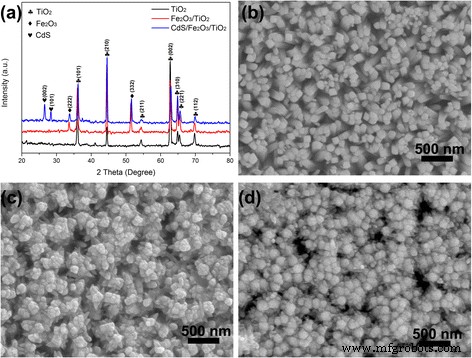
un Les modèles XRD et b Images SEM de TiO2 NR, Fe2 O3 /TiO2 NR et CdS/Fe2 O3
L'image HRTEM et le modèle de diffraction électronique à zone sélectionnée (SAED) de CdS/Fe2 O3 /TiO2 NR sont montrés dans la Fig. 2. On peut voir que les deux TiO2 et Fe2 O3 sont bien cristallisés et les nanoparticules de CdS sont cultivées à la surface de Fe2 O3 . L'espacement des réseaux de 0,31, 0,27 et 0,21 nm peut être bien mis en correspondance avec les plans (101), (222) et (210) de CdS, Fe2 O3 , et TiO2 , respectivement (Fig. 2a). Les anneaux de diffraction du modèle SAED enregistré sur la figure 2b peuvent être vus, qui peuvent être bien indexés sur (101), (210) plans de rutile TiO2 , (222), (332) plans de Fe2 O3 , et (002), (101) plans de CdS, respectivement. Les résultats MET sont en bon accord avec les résultats de la caractérisation XRD.

un Image HRTEM de CdS/Fe2 O3 /TiO2 NR. L'espacement d marqué de 0,31 nm correspond bien au plan (101) de CdS, l'espacement d de 0,27 nm correspond bien au plan (222) de Fe2 O3 et l'espacement d de 0,21 nm correspond bien au plan (210) de TiO2 . b Diagramme de diffraction électronique à zone sélectionnée de CdS/Fe2 O3 /TiO2 NR, les anneaux de diffraction correspondent aux (002), (101) plans de CdS, (222), (332) plans de Fe2 O3 et (101), (210) plans de TiO2
La composition chimique et les états de valence du CdS/Fe2 O3 /TiO2 les NR hybrides sont étudiés par des spectres XPS. La figure 3a montre les spectres d'étude, l'existence des éléments Ti, Fe, O, Cd et S est démontrée. L'apparition de l'élément C est attribuée au confinement à base de carbone. Pour le spectre Ti 2p XPS de la figure 3b, ces deux pics distincts séparés à 458,2 et 464,2 eV peuvent être attribués à Ti 2 p3/2 et 2 p1/2 de TiO2 [20]. Le spectre XPS de Fe 2p est représenté sur la figure 3c. On observe deux pics distincts à 710,6 et 724,10 eV, qui correspondent bien à Fe 2 p3/2 et 2 p1/2 pics de α-Fe2 O3 [21]. Le spectre XPS au niveau du noyau de O 1s est illustré à la Fig. 3d, où le pic à 531,2 eV est attribué à la liaison Ti-O entre le titane et l'oxygène, et le pic à 531,9 eV peut être attribué à la liaison Fe-O entre fer et oxygène [20, 21]. La figure 3e montre le spectre XPS du Cd, qui est attribué au Cd 3d5/2 à 405,2 eV. Le spectre XPS de S 2P est représenté sur la figure 3f [22]. Le pic central est divisé en deux pics de S 2p1/2 et 2p3/2 à 161,5 et 162,6 eV [22].
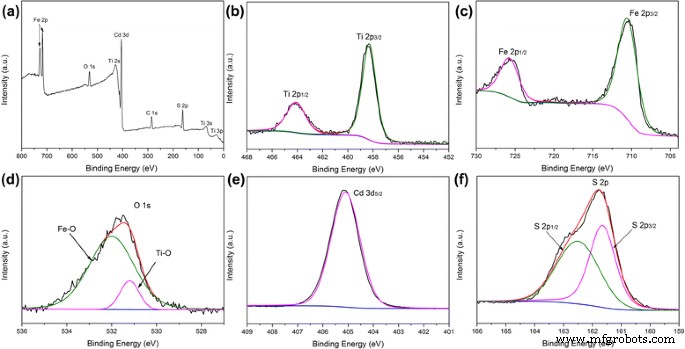
un Spectres XPS de CdS/Fe2 O3 /TiO2 Échantillon NR, b Spectres XPS de Ti 2p dont Ti 2p1/2 et Ti 2p3/2 , c Spectres XPS de Fe 2p incluant Fe 2p1/2 et Fe 2p3/2 , d Spectres XPS d'O 1 comprenant la liaison Fe-O et la liaison Ti-O, e Spectres XPS de Cd 3d5/2 , et f Spectres XPS de S 2p dont S 2p1/2 et S 2p3/2
La figure 4a montre les spectres d'absorption de différentes photoélectrodes. TiO2 montre un bord de bande d'absorption typique à 400 nm, qui peut être attribué à l'absorption intrinsèque de la bande interdite du TiO2 (3,2 eV). Après couplage avec Fe2 O3 , Fe2 O3 /TiO2 montre une absorption accrue dans la région de la lumière visible à environ 540 nm. L'extension du bord de la bande d'absorption est due à la composante sensible au visible de Fe2 O3 (2,0-2,2 eV). Après une nouvelle modification des nanoparticules de CdS, le bord d'absorption de la lumière peut être encore étendu à 580 nm. Il confirme que le couplage TiO2 avec Fe2 O3 et CdS peut ajuster efficacement la propriété d'absorption de la lumière à la région de la lumière visible. Le spectre de photoluminescence (PL) est appliqué pour étudier l'influence de l'incorporation de CdS et Fe2 O3 dans le CdS/Fe2 O3 /TiO2 hybride sur le comportement de transport et de recombinaison des porteurs photogénérés. Plus l'intensité du pic PL est faible, plus l'efficacité de séparation des paires de porteurs photogénérés dans les échantillons est élevée. La figure 4b montre les spectres PL de TiO2 , Fe2 O3 /TiO2 , et CdS/Fe2 O3 /TiO2 échantillons. Il est évident que Fe2 O3 /TiO2 NR atteint un taux de recombinaison de porteuses inférieur à celui du TiO2 vierge , et CdS/Fe2 O3 /TiO2 NR atteint les meilleures performances de transport par transporteur.
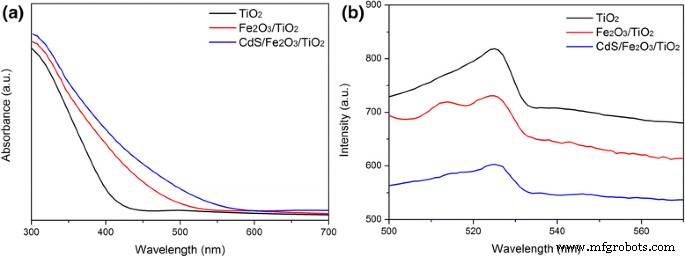
un Spectres d'absorption UV-vis et b Spectres PL de TiO2 NR, Fe2 O3 /TiO2 NR et CdS/Fe2 O3 /TiO2 NR échantillons
Afin de confirmer davantage cette conclusion, les tracés transitoires de fluorescence résolus en picosecondes sont testés et affichés en tant que fichier supplémentaire 3 :Figure S3. La durée de vie moyenne τ est calculé selon τ = (B1 τ1 [2] + B 2 τ 2 [2])/(B1 τ1 + B2 τ2 ) et la constante de temps des transitoires de fluorescence à 511 nm est répertoriée dans le fichier supplémentaire 4 :tableau S1 [23]. On peut voir qu'après avoir modifié le TiO2 vierge avec Fe2 O3 , la durée de vie du porteur photogénéré est prolongée. Couplé au CdS, la durée de vie du support peut être encore améliorée. Ce résultat démontre évidemment que les performances de séparation des charges peuvent être efficacement améliorées en formant du CdS/Fe2 O3 /TiO2 multijonction.
Le processus de transport de support possible est illustré à la Fig. 5. Dans le CdS/Fe2 O3 /TiO2 système ternaire, car la position de la bande de conduction et la position de la bande de valence de CdS sont plus élevées que celles de Fe2 O3 , les électrons photoinduits dans le CdS seront transportés vers la bande de conduction de Fe2 O3 , tandis que les trous photoinduits dans la bande de valence dans Fe2 O3 seront transportés vers le CdS. Pour l'hétérostructure anormale de type II conçue entre Fe2 O3 /TiO2 , la position de la bande de conduction de Fe2 O3 est supérieur à celui de TiO2 . Sous un éclairage solaire, des paires électron-trou photoexcitées généreront à la fois du TiO2 et Fe2 O3 . Électrons photogénérés dans la bande de conduction de Fe2 O3 passera immédiatement à la bande de valence de TiO2 se recombiner avec les trous photogénérés, améliorant ainsi considérablement l'efficacité de séparation des trous photogénérés dans Fe2 O3 et améliore l'efficacité d'injection d'électrons photogénérés dans TiO2 [24, 25]. Cela implique que le couplage de TiO2 avec Fe2 O3 et CdS peut réduire efficacement le taux de recombinaison des paires de porteurs photogénérées. Pendant ce temps, les électrons photogénérés dans TiO2 passer à la contre-électrode où se produit la réaction de réduction. Ainsi, l'hétérostructure anormale de type II entre Fe2 O3 /TiO2 joue un rôle important dans l'amélioration des performances d'oxydation de l'eau PEC.
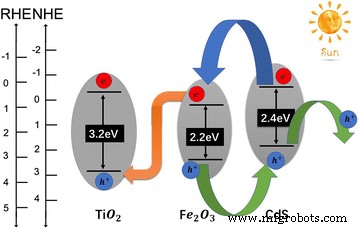
Les positions de bande relatives de CdS/Fe2 O3 /TiO2 système ternaire
La figure 6 illustre des voltamogrammes à balayage linéaire (LSV) et des I-t chronoampérométriques courbes de CdS/Fe2 O3 /TiO2 , Fe2 O3 /TiO2 , et TiO2 échantillons. Comme le montre la figure 6a, la densité de photocourant des photoanodes sous éclairage augmente progressivement après couplage avec α-Fe2 O3 et les nanoparticules de CdS, et le CdS/Fe2 O3 /TiO2 L'échantillon NR présente la plus grande densité de photocourant de 0,61 mA cm − 2 à 1,2 V par rapport à RHE, ce qui correspond presque au double du TiO2 nu goûter. Je-t des courbes à un potentiel de polarisation de 1,2 V par rapport à RHE sous un éclairage haché sont présentées sur la figure 6b, on peut voir que les échantillons restent une excellente stabilité et une bonne propriété de réponse optique sous un éclairage haché. CdS/Fe2 O3 /TiO2 L'échantillon NR maintient une densité de photocourant d'environ 0,6 mA cm − 2 , ce qui est conforme aux courbes LSV.
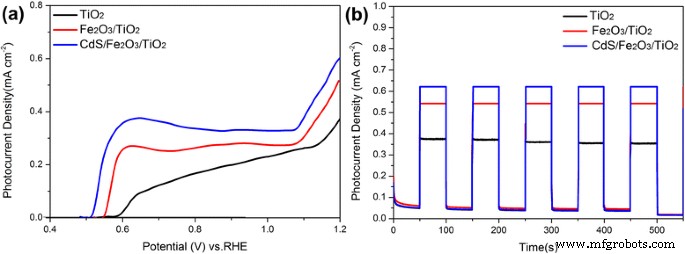
un Courbes LSV de TiO2 NR, Fe2 O3 /TiO2 NR et CdS/Fe2 O3 /TiO2 NR échantillons d'éclairage dans 1M NaOH, b I-t chronoampérométrique courbes à un potentiel de polarisation de 1,2 V sous éclairage haché
La mesure EIS est effectuée sous éclairage et les tracés de Nyquist sont illustrés à la figure 7a et au fichier supplémentaire 5 :figure S4. Ils démontrent que les tracés de Nyquist ont deux demi-cercles avec une résistance série de contact (R s ) sur le substrat FTO. Le petit demi-cercle dans les tracés de Nyquist est attribué à la résistance de transport de charge à l'interface électrode/électrolyte, et le grand demi-cercle représente la résistance de transfert de charge liée au transport/recombinaison d'électrons dans les matériaux de photoanode. La résistance feuille (R s ) du substrat, la résistance de transfert de charge de la contre-électrode (R ct1 ), et la résistance de transfert de charge (R ct2 ) ont été simulés par le logiciel Zview et les données correspondantes sont présentées dans le fichier supplémentaire 6 :tableau S2. Le R équipé s et R ct1 les valeurs pour tous les échantillons sont similaires en raison de la même configuration et des substrats de croissance sont appliqués, tandis que le R ct2 les valeurs montrent évidemment une variation de 1079,5, 880,6 et 679,5 Ω pour TiO2 , Fe2 O3 /TiO2 , et CdS/Fe2 O3 /TiO2 , respectivement. On voit qu'après avoir modifié TiO2 avec Fe2 O3 et CdS, la cinétique de transfert de charge interfaciale est grandement améliorée.
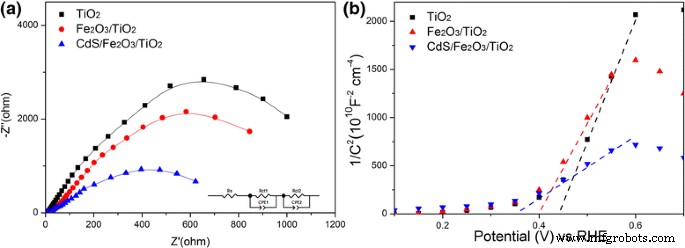
un Spectres EIS mesurés à un potentiel de polarisation de 1,2 V sous éclairage et b Tracés de Mott-Schottky collectés à une fréquence de 1 KHz dans l'obscurité pour le TiO2 NR, Fe2 O3 /TiO2 NR et CdS/Fe2 O3 /TiO2 NR échantillons
Les tracés de Mott-Schottky des échantillons tels qu'ils ont été obtenus sont indiqués sur la figure 7b. Les pentes déterminées à partir des tracés de Mott-Schottky sont utilisées pour estimer la densité de porteurs selon l'équation suivante [26] :
Nd = \( \frac{2}{e_0{\varepsilon \varepsilon}_0}\times \left[\frac{dV}{d\left(1,/,{C}^2\right)}\right] \)
où e 0 est la charge électronique, ε est la constante diélectrique de l'échantillon, ε 0 est la permittivité du vide, Nd est la densité du donneur, et V est la tension appliquée. En général, une pente relativement plus petite représente une densité de porteurs plus élevée.
Le potentiel de bande plate peut être estimé par l'équation suivante :
$$ \frac{1}{C^2}=\frac{2}{e_0{\varepsilon \varepsilon}_0\mathrm{Nd}}\times \left[E-{E}_{\mathrm{fb} }-\frac{kT}{e}\right] $$Le potentiel de bande plate (E fb ) est déterminé en prenant le x intercept d'un ajustement linéaire au diagramme de Mott-Schottky, 1/C 2 , en fonction du potentiel appliqué (E ). De plus, un décalage cathodique remarquable du potentiel plat de 0,44 V pour TiO2 échantillon à 0,36 V pour le CdS/Fe2 O3 /TiO2 Un échantillon NR a été observé. Cela suggère une plus grande accumulation d'électrons dans l'hétérojonction et reflète une diminution de la recombinaison des charges.
Il convient de noter que les performances d'oxydation de l'eau PEC de l'échantillon de CdS/Fe2O3/TiO2 tel que synthétisé sont comparables à certains travaux connexes. Par exemple, Sharma et al. signalé Fe-TiO2 /Zn-Fe2 O3 films minces avec une performance de 0,262 mA cm − 2 à 0,95 V (vs. SCE) [27], tandis que le FTO/Fe2 O3 /ZnFe2 O4 la photoanode atteint une densité de photocourant de 0,4 mA cm − 2 [28]. De plus, pour le Fe2 signalé O3 /TiO2 photoanodes nanotubes, une densité de photocourant de 0,5 mA cm − 2 est atteint [29, 30]. En comparant avec les travaux connexes, on peut voir que l'on obtient CdS/Fe2 O3 /TiO2 La photoanode obtient ici des performances de séparation de l'eau PEC exceptionnelles et fiables.
Conclusions
En conclusion, une méthode hydrothermale facile d'adsorption et de réaction de couches ioniques successives (SILAR) est développée pour fabriquer du Fe2 modifié par CdS. O3 /TiO2 Réseau NR pour une oxydation efficace de l'eau PEC. L'étude UV-vis confirme le CdS/Fe2 O3 /TiO2 La matrice NR affiche d'excellentes performances de réponse optique avec une plage d'absorption de lumière élargie évidente. Appliqué comme photoanode pour l'oxydation de l'eau PEC, CdS/Fe2 O3 /TiO2 La photoanode à matrice NR présente une densité de photocourant considérablement améliorée de 0,62 mA cm − 2 (1,23 V contre RHE) dans l'électrolyte alcalin par rapport au TiO2 vierge (0,32 mA cm − 2 à 1,23 V contre RHE).
Nanomatériaux
- Composites de graphène quantique/TiO2 co-dopé S, N pour une génération d'hydrogène photocatalytique efficace
- Dopage de substitution pour les minéraux d'aluminosilicate et performances supérieures de fractionnement de l'eau
- Exploration du cadre organique Zr-Metal-Organic comme photocatalyseur efficace pour la production d'hydrogène
- Hétérostructure hiérarchique des sphères creuses ZnO@TiO2 pour une évolution photocatalytique hautement efficace de l'hydrogène
- Nanocristal Sb2O3 dopé S :un catalyseur efficace à lumière visible pour la dégradation organique
- Synthèse simple en un seul pot de points de carbone de polydopamine pour la thérapie photothermique
- Matrices de nanotubes TiO2 bien alignées avec des nanoparticules d'Ag pour une détection très efficace de l'ion Fe3+
- Traitement de surface TiO2 efficace à l'aide de Cs2CO3 pour les cellules solaires Sb2S3 de type planaire traitées en solution
- Utilisation d'un système de surveillance du niveau de la rivière alimenté par l'IdO pour une gestion efficace de l'eau



