Le laitier de haut fourneau et son rôle dans le fonctionnement du four
Le laitier de haut fourneau et son rôle dans le fonctionnement du four
L'importance du laitier de haut fourneau (BF) dans le bon fonctionnement du BF est illustrée par le vieil adage « si vous prenez soin du laitier, le four se chargera du reste ». Il y a eu une énorme quantité de travail a été fait sur le laitier BF étudiant les propriétés, les mécanismes de formation et les impacts sur les opérations du four. Un laitier de bonne qualité est nécessaire pour produire une bonne qualité de métal chaud dans le BF.
La pratique du laitier BF est nécessaire pour répondre à certaines exigences pour un fonctionnement BF efficace. Ces exigences comprennent (i) qu'il doit absorber tous les composants non volatils non réduits de la charge et les éliminer du BF, (ii) qu'il doit être liquide de faible viscosité, (iii) qu'il doit être capable d'absorber le soufre principalement contenu dans les combustibles, (iv) il doit contenir la plus petite quantité possible d'oxyde de fer afin d'augmenter le rendement de la fonte, (v) son volume doit être le plus faible possible sans affecter la désulfuration, ( vi) la plage de températures où les composants de la charge deviennent cohésifs doit être étroite pour assurer une meilleure perméabilité de la colonne de charge, et (vii) sa qualité doit être telle qu'elle puisse être transformée en matériau commercialisable. Ces exigences sont en partie complémentaires et en partie mutuellement exclusives. Il est donc nécessaire d'énoncer des priorités.
Heureusement, il existe des relations générales qui donnent une vision plus pratique de la nature des scories utilisables au quotidien. Il est important, cependant, d'avoir une compréhension de base de la nature fondamentale du laitier BF pour comprendre les relations générales.
Fondamental du laitier BF
Les fondamentaux du laitier BF sont complexes. À environ 40 %, l'oxygène est l'élément le plus important du laitier. Le laitier est donc un système d'oxyde et de nature ionique. En raison de la nature du procédé BF, la formation de scories est un processus en plusieurs étapes impliquant des changements considérables de composition et de température. Les quatre principaux composants du laitier BF sont SiO2 (silice), CaO (chaux), MgO (magnésie) et Al2O3 (alumine). Ces quatre composants du laitier BF forment de nombreux composés qui se traduisent par une large gamme de propriétés chimiques et physiques. Les composants moins importants du laitier présentent un intérêt particulier en ce qui concerne la chimie des métaux chauds et le contrôle du four ajoutent à la complexité des propriétés physico-chimiques du laitier.
Les fondamentaux du laitier BF comprennent les problèmes liés au processus BF. Ces problèmes incluent la formation de laitier, l'écoulement dans le foyer, la structure moléculaire du laitier et la relation entre la structure et les indices chimiques connus sous le nom de basicité, la solidification du laitier et l'impact des changements d'état thermique du four sur la composition du laitier.
Formation de scories – Le BF est un réacteur à lit à garnissage sous pression, à contre-courant, à reflux, gaz-solide-liquide. Il a trois fonctions principales, à savoir (i) la réduction des oxydes de fer en fer métallique (ii) la fusion du fer métallique et des oxydes, qui permet la (iii) séparation des impuretés de la charge et du combustible du fer liquide. Ces caractéristiques du procédé conduisent à diviser le four en trois zones verticales par rapport aux scories (i) à savoir (i) zone granulaire, (ii) zone de formation de laitier et (iii) zones de sole. Ces trois zones et certaines réactions spécifiques pour chaque zone sont données dans la figure 1.
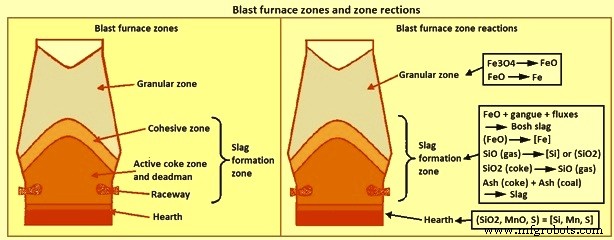
Fig 1 Zones de haut fourneau et réactions de zone
La zone granulaire est située dans la partie supérieure du four où tous les composants chargés sont en phase solide. La zone granulaire est délimitée par la ligne de souche en haut et par le début de formation des phases liquides, la zone cohésive, en bas. Au fur et à mesure que la charge descend à travers la zone granulaire, elle est chauffée par les gaz de la partie inférieure du four et une partie de la réduction des oxydes de fer est effectuée. La quantité de réduction qui se produit dans la zone granulaire est fonction de la nature des matériaux contenant du fer, de la répartition de la charge, de la composition du gaz et des schémas d'écoulement.
La zone de formation de laitier commence au niveau de la zone cohésive, où le ramollissement de la charge commence, et continue jusqu'en dessous de l'élévation de la tuyère. La zone de formation de scories comprend donc la zone cohésive, la zone de coke actif, l'homme mort et le chemin de roulement. Le laitier formé dans la partie supérieure de la zone de formation du laitier est appelé laitier "bosh" ou "primaire", et le laitier quittant la zone inférieure est le laitier "foyer". Le laitier primaire est normalement supposé être constitué de tous les composants du laitier de charge, y compris les oxydes de fer non réduits dans la zone granulaire, mais n'inclut pas les cendres du coke ou du charbon injecté. La composition du laitier change au fur et à mesure qu'il descend dans le four en raison de l'absorption des cendres de coke et de charbon, du soufre et du silicium du gaz et de la réduction de l'oxyde de fer. La température du laitier augmente de l'ordre de 500°C à mesure qu'il descend vers l'élévation de la tuyère. Ces changements de composition et de température peuvent avoir un impact considérable sur les propriétés physiques du laitier, notamment la température de liquidus et la viscosité.
La troisième zone est la couche de laitier dans la sole du four. Le laitier produit dans la zone de formation du laitier s'accumule dans la couche de laitier, remplissant les vides dans le coke de foyer et «flottant» sur la couche de métal chaud. Le métal chaud traverse la couche de laitier pour atteindre la couche de métal chaud. La surface élevée entre le métal chaud et le laitier lorsque le métal chaud traverse la couche de laitier améliore la cinétique des réactions chimiques. Ces réactions entraînent des changements considérables dans la chimie du métal chaud. En particulier, les teneurs en [Si] et [S] avant d'entrer dans la couche de laitier sont beaucoup plus élevées que celles dans la couche de métal chaud. La formation de scories dans la zone de formation de scories est très spécifique au four en raison de l'impact des propriétés de la charge et du fonctionnement du four.
Structure du laitier – La conceptualisation de la structure du laitier (Fig 2) est basée sur la structure formée par la silice. Au niveau moléculaire, l'atome de silicium est situé au centre d'un tétraèdre entouré de quatre atomes d'oxygène, un atome d'oxygène à chaque coin du tétraèdre comme le montre la figure 2a. Chaque atome d'oxygène est lié à deux atomes de silicium et donc chaque atome d'oxygène est un coin de deux tétraèdres. Le partage des atomes d'oxygène se traduit par un polymère ou un réseau en trois dimensions à l'état cristallin où tous les coins sont partagés (Fig 2b). Au fur et à mesure que la silice est chauffée, certaines des liaisons d'angle sont rompues, mais la nature polymère de la structure est conservée même lorsqu'elle est fondue, comme le montre la figure 2c.
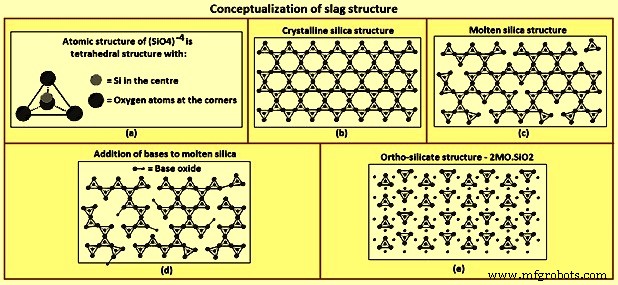
Fig 2 Conceptualisation de la structure du laitier
L'ajout d'oxydes métalliques, tels que CaO et MgO décompose la structure du polymère. Ces oxydes agissent comme des donneurs d'oxygène, remplaçant un atome d'oxygène dans un coin d'un tétraèdre et rompant la liaison tétraèdre à tétraèdre (Fig 2d). La décomposition de la structure du polymère se poursuit avec l'ajout de plus d'oxydes métalliques jusqu'à ce que le rapport molaire des oxydes métalliques à la silice soit égal à deux, moment auquel toutes les liaisons d'angle tétraèdre à tétraèdre sont rompues (Fig 2e). Le rapport molaire de deux est la composition d'ortho-silicate, 2CaO-SiO2, 2MgO-SiO2 et CaO-MgO-SiO2. Al2O3 agit de la même manière que SiO2 en formant des polymères et en acceptant des atomes d'oxygène à partir d'oxydes basiques. Les oxydes qui acceptent l'oxygène, SiO2 et Al2O3, sont appelés oxydes acides. Les oxydes qui donnent de l'oxygène, CaO et MgO sont appelés s oxydes basiques.
Basicité du laitier – Il est très utile, lorsqu'il s'agit de relier les propriétés d'un système à plusieurs composants à sa composition, de développer un indice basé sur la composition. Le problème dans l'élaboration d'un indice est de savoir comment refléter l'importance de chaque composante du système dans l'indice. La nature différente des oxydes acides (A) et des oxydes basiques (B) a été utilisée dans le développement d'indices de composition de laitier, normalement appelés basicités. Des exemples d'indices de basicité qui ont été développés sont (i) bases en excès ={(CaO) + (MgO)} – {(SiO2) + (Al2O3)}, (ii) basicité (B/A) ={(CaO) + (MgO)} / {(SiO2) + (Al2O3)}, (iii) rapport de cloche ={(CaO) + 0,7(MgO)} / {0,94(SiO2)+ 0,18(Al2O3)}, et (iv) basicité optique ={(CaO) + 1,11(MgO) + 0,915(SiO2) + 1,03 (Al2O3)} / {(CaO) + 1,42(MgO) + 1,91(SiO2) + 1,69(Al2O3)}.
Les indices de basicité peuvent être regroupés en catégories générales, à savoir (i) les différences entre la quantité de bases et d'acides, comme indiqué dans l'équation (i) ci-dessus, (ii) les rapports bases/acides basés sur les pourcentages en poids, comme indiqué dans l'équation (ii) ci-dessus, (iii) les rapports bases/acides basés sur les concentrations molaires, comme indiqué dans l'équation (iii) ci-dessus, et (iv) la somme de la basicité de chaque composant et de sa concentration molaire, comme indiqué dans l'équation (iv) ci-dessus. Comme on pouvait s'y attendre sur la base de la description précédente de la structure du laitier, les indices qui reflètent la nature moléculaire de la composition du laitier, les équations (iii) et l'équation (iv) tendent à être de meilleurs prédicteurs des propriétés du laitier. Cependant, comme l'indice défini par l'équation (ii) est probablement la définition la plus couramment utilisée.
Impact de la température - [Si], basicité et volume de laitier – Il y a augmentation de la quantité de [Si] avec l'augmentation de la température du métal chaud dans le BF, comme indiqué sur la figure 3. La quantité d'augmentation de [Si] pour une augmentation de température donnée varie d'un four à l'autre, mais la tendance est la identique pour tous les fours. Lorsque le [Si] augmente, le (SiO2) diminue et donc la basicité augmente et le volume de laitier diminue. La quantité d'augmentation de la basicité pour une augmentation spécifique de [Si] est fonction du volume de laitier. La figure 3a montre la variation de B/A pour des volumes de laitier initiaux de 200 kg/tML (kilogrammes par tonne de métal chaud) et 300 kg/tML et pour la relation [Si] et température du métal chaud donnée sur la figure. La tendance normale démontrée ici est que plus le volume de laitier est grand, plus le changement de B/A est petit pour le même changement de [Si] ou de température du métal chaud.
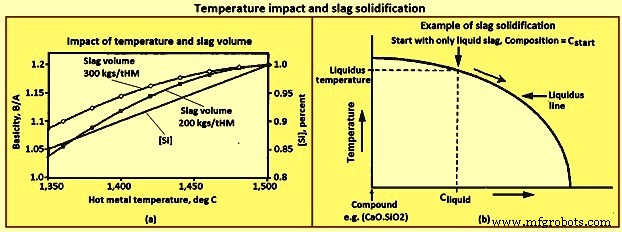
Fig 3 Impact de la température et solidification du laitier
Solidification du laitier - La définition commune de la température de fusion ne s'applique qu'à un système à un seul composant tel que l'eau, où seule l'eau liquide existe au-dessus de la température de fusion et seule l'eau solide existe en dessous de la température de fusion. Le laitier est un système à plusieurs composants et, par conséquent, n'a pas la définition commune de la température de fusion, sauf à des compositions spécifiques. La majorité des compositions de scories ont des phases solides et liquides présentes sur une plage de températures. La température la plus basse à laquelle seule la phase liquide existe pour une composition spécifique est appelée température de liquidus.
La figure 3b montre que le chemin de solidification d'un laitier est illustré sur le diagramme de phase simplifié. Commencer avec du laitier de composition Cstart à des températures où seul le laitier liquide existe. Au fur et à mesure que le laitier se refroidit, en descendant verticalement sur le diagramme, la composition du laitier liquide ne change pas jusqu'à l'intersection avec la « ligne de liquidus ». L'intersection avec la "ligne de liquidus" est la température de liquidus pour la composition Cstart. Une très petite quantité du composé solide se forme à la température de liquidus à gauche. Trois changements se poursuivent au fur et à mesure que la température est encore réduite en dessous de la température du liquidus, à savoir (i) plus de composé solide se forme, (ii) la quantité de laitier liquide diminue et (iii) la composition du laitier liquide change, se déplaçant vers le tout le long de la "ligne de liquidus". Dans l'exemple où le composé formé est 2CaO.SiO2, la basicité du laitier liquide diminue au fur et à mesure du refroidissement du laitier puisque 2CaO.SiO2 contient environ deux fois plus de CaO que de SiO2.
Le chemin de solidification montre comment un composé peut être formé même lorsque la composition du laitier liquide est considérablement différente de la composition du composé. Le rapport pondéral de CaO à SiO2 =1,86 pour le composé silicate dicalcique, 2CaO.SiO2. Alors qu'aucun BF n'a jamais été exploité avec succès en utilisant des scories avec un CaO à SiO2 approchant 1,86, des quantités considérables de silicate dicalcique peuvent être formées dans les scories des BF en fonctionnement. La formation d'une quantité suffisante de silicate dicalcique donne un laitier solide qui se décompose en poussière lors du refroidissement, appelé laitier « tombant » ou « saupoudré ». La panne est causée par l'expansion volumique de 10 % du silicate dicalcique lorsqu'il subit un changement de phase à 675 deg C. A2O3) + 1,75(S).
Il est important de se rappeler que les diagrammes de phase sont basés sur des conditions d'équilibre. Les conditions d'équilibre impliquent que la vitesse de refroidissement est lente par rapport à la vitesse des réactions, comme la formation de silicate dicalcique. Le chemin de solidification décrit ci-dessus est "contourné" si la vitesse de refroidissement est très élevée comme dans la granulation du laitier et, dans une moindre mesure, la pelletisation du laitier. Le refroidissement rapide enferme la composition dans une phase vitreuse solide, où la cinétique des réactions est trop lente pour que les composés se forment.
Coulée de scories Dans le foyer – Le contrôle du niveau de laitier dans la sole est important pour maintenir un fonctionnement stable du four, d'autant plus que les cadences de production de fonte ont été augmentées. Des niveaux élevés de laitier entraînent une augmentation de la pression de souffle et du travail des parois en bosh, et perturbent la descente uniforme de la charge. L'un des problèmes de contrôle du niveau de laitier est l'écoulement du laitier dans le foyer lors de la saignée. Dans le foyer, l'écoulement des scories vers le trou de coulée est plus difficile que l'écoulement du métal chaud vers le trou de coulée. Le flux de métal chaud a une force motrice plus importante en raison de la densité plus élevée du métal chaud par rapport au laitier. On pense que le chemin d'écoulement du métal chaud passe principalement par des régions «sans coke» en dessous et / ou autour du coke homme mort. Le chemin d'écoulement des scories vers le trou de coulée passe par le coke homme mort.
La figure 4 montre la configuration du foyer et une séquence possible d'étapes du foyer pendant le coulage qui conduisent à un faux état de foyer sec à la fin du coulage. On pense que la surface du métal chaud reste relativement plate sur toute la zone du foyer tout au long du taraudage en raison de la densité élevée du métal chaud et du chemin «sans coke» vers le trou de coulée. La surface de laitier peut être considérablement plus faible dans la région autour du trou de coulée que dans d'autres régions du foyer. Lorsque le débit de coulée de laitier est supérieur au débit de laitier à travers le foyer vers la région du trou de coulée, un épuisement du laitier se produit dans la région du trou de coulée et la surface du laitier commence à se courber vers le trou de coulée, comme indiqué à l'étape 4 de Fig 4. L'épuisement du laitier se poursuit jusqu'à ce qu'il n'y ait plus de laitier au trou de coulée et que le four semble être sec alors qu'il reste encore beaucoup de laitier dans le foyer, comme indiqué à l'étape 5 de la Fig 4. Minimisation de la résistance à l'écoulement du laitier dans le foyer minimise le laitier restant dans le foyer à l'issue d'une saignée. La résistance à l'écoulement du laitier dans le foyer est réduite à mesure que la porosité du lit de coke du foyer augmente et que la viscosité du laitier est réduite.
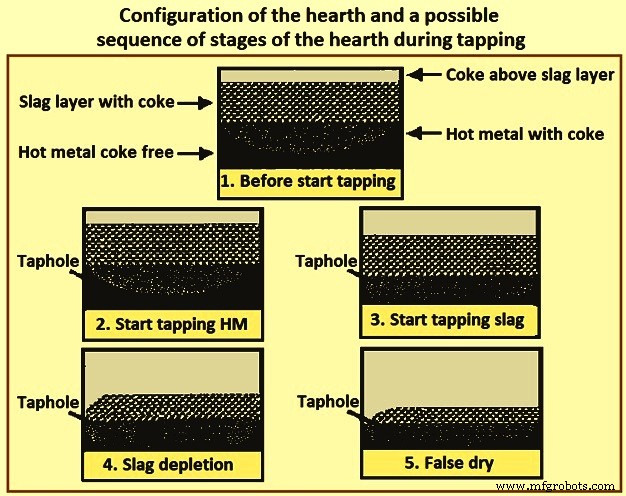
Fig 4 Configuration du foyer et enchaînement possible des étapes du foyer lors du tapotement
Système d'oxyde
Environ 95 % des scories sont constituées de SiO2, CaO, MgO et Al2O3. L'exigence de faible viscosité peut être satisfaite par une variété de composants dans ce système quaternaire. Ignorant la présence de MgO, le diagramme de phase du système d'oxyde ternaire CaO-Al2O3-SiO2 (Fig 5) montre une région à basse température de fusion qui est parallèle au binaire CaO-SiO2 avec une faible teneur en Al2O3. Cette région s'étend d'une teneur élevée en SiO2 à l'isotherme de saturation pour 2CaO.SiO2 puis pour une teneur en CaO essentiellement constante vers une teneur élevée en Al2O3. La teneur en MgO du laitier n'affecte pas sensiblement la position relative de la région à basse température de fusion et n'affecte que les valeurs absolues des températures de fusion.
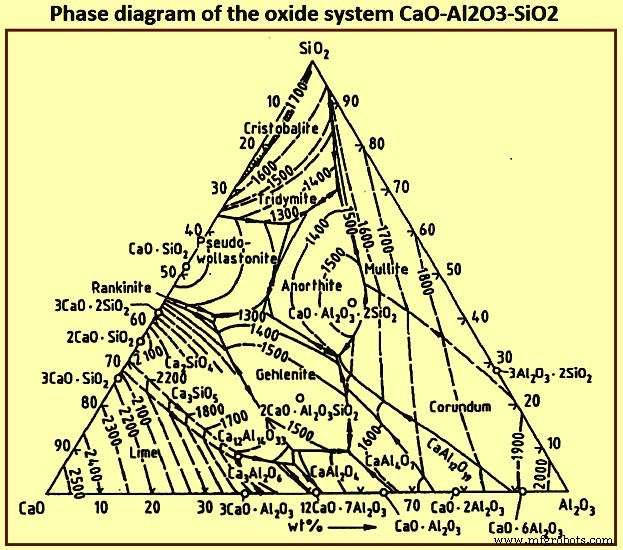
Fig 5 Diagramme de phase du système d'oxyde CaO-Al2O3- SiO2
Le système oxyde à la base des scories BF est le système chaux-silice-alumine (CaO-SiO2-Al2O3) modifié en raison de la présence d'un certain pourcentage de MgO dans les scories. La figure 6 montre le diagramme de phase du système CaO-Al2O3-SiO2-10 % MgO.
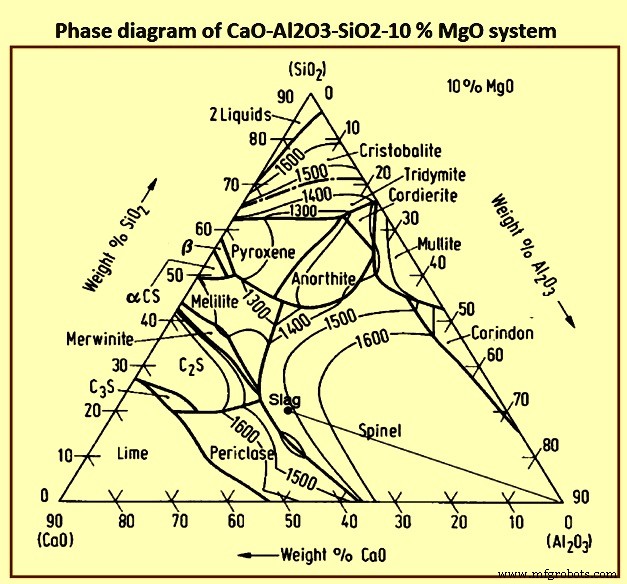
Fig 6 Diagramme de phase du système CaO-Al2O3-SiO2-10 % MgO
The compositions of BF slags as encountered under various operating conditions are shown in Fig 7. The desulphurization of hot metal increases with slag basicity, i.e. with increasing CaO and / or MgO content, region 1 in Fig 7 can, hence, be used only for processing low sulphur burden. Since the gangue constituents normally form a low basicity slag, region 1 largely represents the slag composition without addition of fluxes. The furnace can be operated at a relatively low temperature because of the low melting points. Region 2 is reached for low iron content burden with acid gangue constituents. This mode of operation prevails, and needs extensive desulphurization of the hot metal outside of the BF. The attainment of a basicity which results in adequate desulphurization within the furnace needs a large lime (CaO) addition which leads to a high slag volume and hence a higher coke rate. Region 3 represents the world wide preferred slag compositions for large blast furnaces. In this case, depending on the alumina content, dolomite is to be added to satisfy the needed MgO contents.
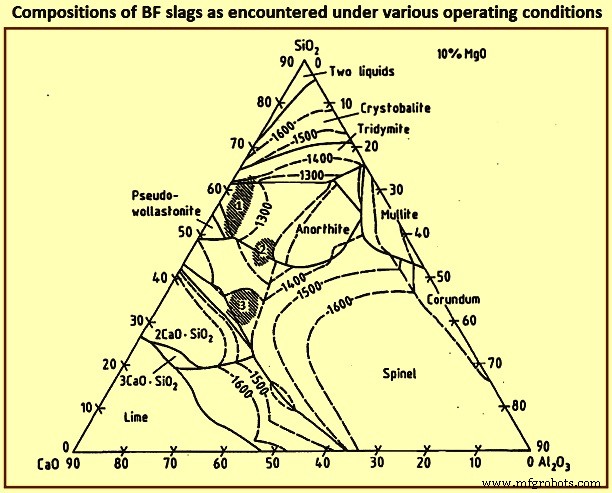
Fig 7 Compositions of BF slags as encountered under various operating conditions
Tab 1 shows the optimum components of the BF slag. Slags with higher basicities (B) as shown in Tab 1 do favour optimum softening conditions. The softening and the melting range of the gangue constituents is around 80 deg C to 130 deg C for B=0.5, and around 20 deg C to 50 deg C for B =2. Because of the higher melting temperature of the highly basic slag and of extra energy needed due to the larger quantity of the flux addition, the slag basicity is hence maintained at around 1.2.
| Tab 1 Optimum composition of BF slag | |||
| Al2O3 | CaO | MgO | SiO2 |
| % | % | % | % |
| 5 | 43 | 16 | 36 |
| 10 | 44 | 14 | 32 |
| 15 | 44 | 12.5 | 28.5 |
| 20 | 45 | 11 | 24 |
| 25 | 48 | 8 | 19 |
| 30 | 56 | 5 | 9 |
| 35 | 54 | 4 | 7 |
Slag properties
The physical and chemical properties of slags are primarily a function of the slag composition and temperature. The following describes these relationships for the purpose of developing general trends.
Liquidus temperatures – The relationships of liquidus temperature and composition for the four primary components of slag are represented on a quaternary phase diagram. Fig 8 has been generated from ternary planes of the quaternary phase diagram. Figures 8a and 8b are not phase diagrams. There are two general trends derived from these figures. The first is that the liquidus temperatures increase with increases in (Al2O3) and B/A, and the second is that the (MgO) in the range of 8 % to 14 % tends to minimize the increase in liquidus temperature caused by the increase in either (Al2O3) or B/A.
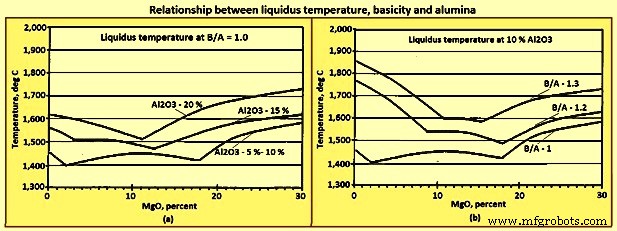
Fig 8 Relationship liquidus temperature, basicity, and alumina
Viscosity – Viscosity is a measure of the quantity of force needed to change the form of a material and is reported in unit called ‘poise’. The higher the viscosity, the more force is needed to cause a liquid to flow. For comparison purposes considering that at 20 deg C the viscosity of water is 0.01002 poise, a typical acceptable slag viscosity is around 2 to 5 poise, and the viscosity of the liquid SiO2 is of the order of 100,000 poise. The high viscosity of liquid SiO2 is caused by the polymer structure. The breakdown of the polymer structure by the basic oxides lowers the viscosity. The decrease in the viscosity of all liquid slags with increasing the B/A is shown Fig 9a. In general, the viscosity of any liquid / solid mixture increases as the quantity of suspended solids increases. The impact of temperature on slag viscosity is considerably higher at temperatures below the liquidus temperature than above the liquidus temperature as shown in Fig 9b.
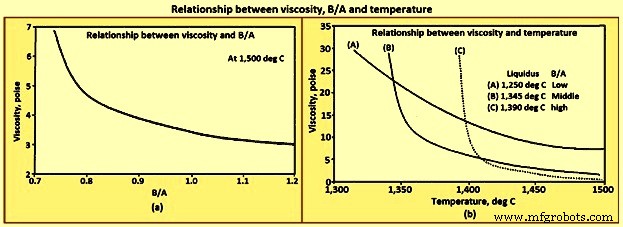
Fig 9 Relationship between viscosity, B/A and temperature
There are two general trends which are seen for the viscosity. Above the liquidus temperature, the viscosity of liquid slags decreases with increasing temperature and B/A. At temperatures below the liquidus temperature, the viscosity decreases with increasing temperature, and decreasing B/A.
Sulphur partition ratio – The BF ironmaking is a very good desulphurizing process compared to the steelmaking process because of the difference in the oxygen potential of the slags of the processes. The effect of the oxygen potential on desulphurization can be shown using equation (CaO) + [S] =(CaS) + (FeO), where the oxygen potential is indicated by the (FeO). The higher the (FeO) the more the reaction is driven to the left and the higher the [S]. Steelmaking slags with (FeO) of 15 % to 25 % are, hence, weaker desulphurizing slags than the BF hearth slags with (FeO) of less than 1 %.
Essentially all the sulphur into the BF leaves the furnace in the hot metal and slag. A relationship for the prediction of [S] can be developed based upon a mass balance of sulphur for one ton of hot metal, as per the equation (i) below, and the defined term sulphur partition as per the equation (ii) below. The prediction of [S], by equation (iii) below, is derived by the substitution of [S] from the equation (i) into equation (ii) and then solving for [S].
Equation(i) is St =[S] /100 x 1,010 + (S) /100 x Svol where 1,010 is the kgs of hot metal in a ton of hot metal including a 1 % yield loss, St is the sulphur loading which is the total weight of sulphur in kgs/tHM. Svol is the slag volume which is the weight of slag in kgs/tHM. Equation (ii) Sp =(S) /[S] where Sp is the sulphur partition ratio. Equation (iii) is [S] =St x 100 / (Sp x Svol + 1,010).
The slag Sp can be predicted based upon equation (iv) Sp =147.7 x BB + 37.7 x [Si] – 190 and equation (v) BB ={(CaO) + 0.7(MgO)} / {0.94(SiO2) + 0.18(Al2O3)}. Here BB is the basicity as defined by the bell’s ratio. It is to be noted that the coefficients in equation (iv) have been developed from regression analysis of a specific furnace. Equation (iv) and equation (v) have been used to construct Fig 10(a), and equation (iii), equation (iv), and equation (v) have been used in the construction of Fig 10 (b).
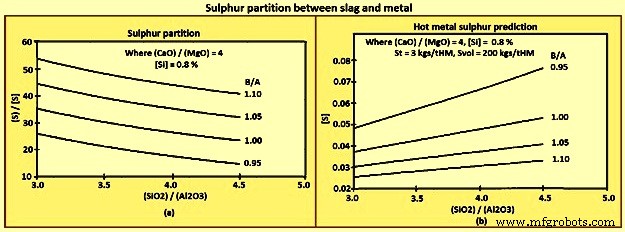
Fig 10 Sulphur partition between slag and metal
The general trends which can be derived from the above equations and figures are (i) [S] decreases with decreasing St and increasing Sp and Svol, (ii) however, Sp normally increases with B/A, (iii) CaO is a better desulphurizer than MgO, and (iv) Al2O3 has a smaller effect on Sp than SiO2.
Alkali capacity – A ‘refluxing’ or ‘recycling’ phenomena occurs in the BF due to the counter-current flow of gases versus solids / liquids, particularly for sulphur, zinc, and alkalis. The recycling of the alkali potassium (K) is shown in Fig 11a. The recycling phenomena is when an element travels down the furnace in a solid or liquid phase, reacts to form gas species in the higher temperature regions of the furnace, then travels back up the furnace as gases, where it reacts and is absorbed by the solid / liquid phases in the lower temperature region of the furnace. The recycling results in much higher internal concentrations of the recycled element than the concentration going in or out of the furnace. For example the internal loading of K can be 10 kgs/tHM, when the materials being charged contain only 2 kgs/tHM.
Alkalis have no beneficial, but many deleterious effects on the BF. Alkalis are absorbed by refractories, coke, and ore causing degradation of the refractories and coke, and ore swelling. Alkalis can also form scabs which can peel off upsetting the thermal condition of the furnace, or build up and constrict burden and gas flow. Alkalis cannot be avoided as they are contained in all coals, cokes, and to a lesser extent ores. The alkali loading is to be minimized wherever possible.
A portion of the alkalis leave the furnace in the top gas, the quantity being a function of the top temperature profile. The remaining alkalis are to be removed in the slag. The ability of slag to remove alkalis from the furnace is referred to as the alkali capacity of the slag. The relationships of alkali capacity to slag composition and temperature are shown in Fig 11b. In general the alkali capacity increases with lower B/A, and with lower temperature.
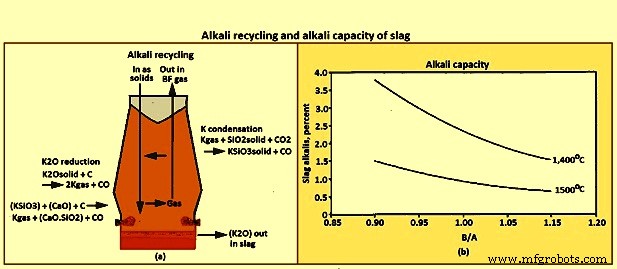
Fig 11 Alkali recycling and alkali capacity of slag
Silica activity – The [Si] produced is dependent upon the burden materials, furnace operation, and slag chemistry. The impact of the slag chemistry is shown in the equation [Si] =(SiO2) x GSiO2 / GSi x Keq / (P to the power 2)co. Here CO is carbon mono-oxide. This equation is developed from the equilibrium constant, equation Keq ={ASi x (P to the power 2)co} / { ASiO2 x Ac}, for the reaction given in equation (SiO2) + 2C =[Si] + 2COgas, the definitions of the activities of (SiO2) and [Si], equation ASiO2 =(SiO2) x GSiO2 and equation ASi =[Si] x GSi, and assuming that the activity of the carbon in the hearth is equal to one. The trend implied by Equation [Si] =(SiO2) x GSiO2 / GSi x Keq / (P to the power 2)co is that the [Si] decreases as the (SiO2) decreases.
Slag design factors
In some of the BFs, a typical slag composition which is formed from the gangue in the ore and ash of the coke is 9 % CaO, 5 % MgO, 75 % SiO2, and 10 % Al2O3. A slag of this composition has a liquidus temperature of the order of 1,600 deg C and does not flow well even above its liquidus temperature. Hence, CaO and MgO are added to the burden to ‘flux’ the gangue and ash resulting in acceptable liquidus temperatures and flow characteristics.
Basic slag design is the selection of the types and quantities of fluxes to be used with a burden and coke to produce a slag of acceptable properties. Burden and coke selections are largely driven by economic issues such as local versus imported sources and degree of beneficiation. These economic driving forces have resulted in a wide range of slag compositions throughout the world.
The general factors to be considered in designing a slag for normal operation are (i) liquidus temperature, that is, the slag is to be completely liquid in the hearth and cast house, (ii) viscosity, that is, the slag is to have a low viscosity, high fluidity, so as to drain from the hearth and down the cast house runners, (iii) sulphur capacity that is the Sp is to be sufficient to produce hot metal with sulphur contents within specifications, (iv) alkali capacity, that is, the slag alkali capacity is to be sufficient to prevent alkali build up in the furnace, (v) hot metal silicon control, that is, the effect of the slag chemistry on the [Si] is to be considered, (vi) slag volume, that is, the slag volume is to be high enough to contribute to the stability of the slag properties and hot metal quality, but not so high as to require excessive fuel or contribute to furnace instability, (vii) robust properties, that is, the slag properties are to be as insensitive to variations in normal variations in furnace operation as possible, specifically hot metal temperature, and (viii) end use, that is, the requirements of the end use of the slag is to be considered.
Slag design is to recognize that the above factors are not independent and that the design always involves a balancing of the above factors to resolve the conflicting trends (Tab 2).
| Tab 2 Normal conflicting trends | ||
| Desired parameter | Basicity | Al2O3 |
| Lower liquidus temperature | Lower | Lower |
| Lower viscosity | Higher | |
| Higher K removal | Lower | Lower |
| Lower [S] | Higher | Higher |
| Lower [Si] | Higher | Higher |
Two examples of the slag design are described below. In the first example (Tab 3) , the issue is to increase the alkali removal without increasing the [S]. The resolution of the issue is to increase the slag volume through the use of additional SiO2 in the burden, while decreasing the slag basicity.
| Tab 3 Example of designing slag for increased K2O removal | |||||
| Basicity | Slag volume | K2O | K2O removed | (S) | S removed |
| B/A | kgs/tHM | % | kgs/tHM | % | kgs/tHM |
| 1.10 | 225 | 0.47 | 1.30 | 1.82 | 5.00 |
| 1.05 | 282 | 0.55 | 1.55 | 1.77 | 5.00 |
| 1.00 | 290 | 0.63 | 1.85 | 1.72 | 5.00 |
| 0.95 | 298 | 0.71 | 2.10 | 1.68 | 5.00 |
The issue in the second example (Tab 4) is to lower the [Si] without negatively impacting the other properties of slag and furnace operation. The resolution of the issue is to decrease the (SiO2) by increasing the (Al2O3) using quartzite, a high (Al2O3) burden material, while holding the (CaO) and (MgO) constant. The change in slag chemistry results into a decrease of both [Si] and [S].
| Tab 4 Example of designing slags with lower [Si] | |||||
| Period | Unit | Base | Number 1 | Number 2 | Number 3 |
| Basicity | 1.12 | 1.13 | 1.13 | 1.12 | |
| (MgO) | % | 11.8 | 11.5 | 11.7 | 11.5 |
| (Al2O3) | % | 7.8 | 10.2 | 10.3 | 11.7 |
| [Si] | % | 0.76 | 0.53 | 0.54 | 0.49 |
| [S] | % | 0.043 | 0.031 | 0.029 | 0.026 |
Slag after the BF
The use of BF slag is driven by the economics of processing and market demand. In the place, where the processing and marketing is performed by the organization producing the slag, the markets tend to be local in nature with minimal processing. As per the present trend, independent organizations take ownership of the liquid slag at the end of the slag runner which has led to wider markets with more extensive processing. The product slag can be classified by the rate of cooling.
Air-cooled slags are those produced with low cooling rates. These are slags which are solidified in pits and frequently cooled with water sprays. The largest uses for air cooled slag are in road construction, railroad ballast, and aggregate. Air-cooled slag has also been used in the production of cement, mineral wool insulation, roofing, and glass.
Pelletized and granulated slags are those produced with high cooling rates. Pelletized slag is produced by pouring liquid slag onto a rotating drum, sometimes with water. Granulated slags are produced by either pouring the liquid slag directly into a large slag pit of water or through the use of high pressure water sprays which breaks the slag up into droplets. Rapidly cooled slags have been used for the same applications as air-cooled slags. The high glass content of rapidly cooled slags makes it particularly suitable for Portland cement production.
Processus de fabrication
- Système d'automatisation, de mesure et de contrôle du processus de haut fourneau
- Génération et utilisation de gaz de haut fourneau
- Granulation de laitier de haut fourneau à la fonderie
- Productivité des hauts fourneaux et paramètres d'influence
- Exploitation du laitier à haute teneur en alumine et du haut fourneau
- Irrégularités du haut fourneau pendant le fonctionnement
- Le répartiteur et son rôle dans la coulée continue de l'acier
- Fabrication du fer par haut fourneau et émissions d'oxyde de carbone
- Ingénierie de précision et son rôle dans la fabrication



