Vaccin
Contexte
Le développement de vaccins pour protéger contre les maladies virales est l'une des caractéristiques de la médecine moderne. Le premier vaccin a été produit par Edward Jenner en 1796 dans le but d'offrir une protection contre la variole. Jenner a remarqué que les laitières qui avaient contracté la variole, une infection relativement inoffensive, semblaient résistantes à la variole, une maladie humaine qui atteignait régulièrement des niveaux épidémiques avec des taux de mortalité extrêmement élevés.
Jenner a théorisé (à juste titre) que la variole, une maladie des animaux, était similaire à la variole. Il a conclu que la réaction humaine à une injection de virus cowpox apprendrait d'une manière ou d'une autre au corps humain à réagir aux deux virus, sans causer de maladie grave ni de décès. Aujourd'hui, la variole est totalement éradiquée. Il n'existe que deux échantillons congelés de ce virus virulent (l'un aux États-Unis, l'autre en Russie) et, à la mi-1995, il existe un sérieux débat scientifique sur l'opportunité de détruire les échantillons ou de les conserver pour une étude plus approfondie en laboratoire.
Un virus est un petit morceau d'ARN (acide ribonucléique) et/ou d'ADN (acide désoxyribonucléique), le matériel contenu dans toutes les cellules vivantes qui indique à la cellule comment se développer et se reproduire. Les virus ne peuvent pas se reproduire par eux-mêmes, mais seulement en prenant le contrôle du noyau d'une cellule hôte et en ordonnant à la cellule de fabriquer des virus supplémentaires. Lorsqu'un virus envahit avec succès un organisme, il prend en charge le processus de croissance cellulaire chez l'hôte.
Dans des circonstances ordinaires, le corps humain réagit à l'invasion virale de plusieurs manières différentes. Une immunité généralisée contre un virus peut être développée par les cellules du corps qui sont les cibles d'une invasion virale. Dans cette situation, les virus sont empêchés d'accéder aux cellules hôtes. Une protection plus courante est la capacité du corps à développer des cellules sanguines et lymphatiques qui détruisent ou limitent l'efficacité du virus envahissant. Souvent, un corps humain infecté "apprendra" comment réagir à un virus spécifique à l'avenir, de sorte qu'une seule infection, en particulier à partir d'un virus relativement bénin, apprend généralement au corps comment réagir à des invasions supplémentaires du même virus. Le rhume, par exemple, est causé par l'un des centaines de virus. Après avoir récupéré d'un rhume, la plupart des gens sont résistants au virus particulier qui a causé le rhume, bien que des virus du rhume similaires provoquent toujours des symptômes similaires ou identiques. Pour certains virus inoffensifs, une personne peut même développer une immunité sans devenir visiblement malade.
Familles de virus
Il existe généralement plusieurs variantes ou souches d'un virus particulier. Selon le nombre de variétés, un biologiste peut regrouper les virus en types ou en souches. Les vaccins sont souvent fabriqués à partir de plus d'un groupe de virus apparentés; une réaction préventive à la vaccination multivalente entraînera probablement une immunité contre presque toutes les variantes du groupe, ou au moins contre les variantes qu'une personne est susceptible de rencontrer. Le choix des membres spécifiques du groupe à utiliser dans un vaccin est fait avec un soin et une délibération minutieux.
Le processus de fabrication
La fabrication d'un vaccin anti-virus aujourd'hui est un processus compliqué, même après la période ardue 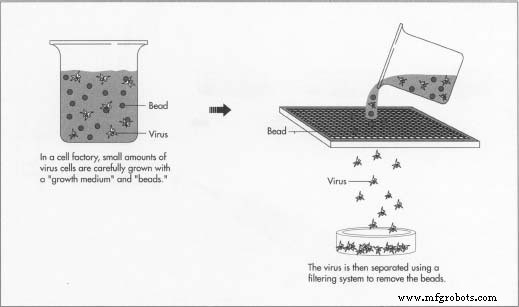 tâche de créer un vaccin potentiel en laboratoire. Le passage de la fabrication d'un vaccin potentiel en petites quantités à la fabrication de gallons de vaccin sûr dans une situation de production est dramatique, et une simple procédure de laboratoire peut ne pas se prêter à une situation de « mise à l'échelle ».
tâche de créer un vaccin potentiel en laboratoire. Le passage de la fabrication d'un vaccin potentiel en petites quantités à la fabrication de gallons de vaccin sûr dans une situation de production est dramatique, et une simple procédure de laboratoire peut ne pas se prêter à une situation de « mise à l'échelle ».
La graine
- 1 La fabrication commence avec de petites quantités d'un virus (ou d'une graine) spécifique. Le virus doit être exempt d'impuretés, y compris d'autres virus similaires et même des variantes du même type de virus. De plus, la graine doit être conservée dans des conditions "idéales", généralement congelées, qui empêchent le virus de devenir plus fort ou plus faible que souhaité. Stockés dans de petits récipients en verre ou en plastique, des quantités aussi petites que 5 ou 10 centimètres cubes, mais contenant des milliers, voire des millions de virus, conduiront à terme à plusieurs centaines de litres de vaccin. Les congélateurs sont maintenus à des températures spécifiées ; des graphiques et/ou des cadrans à l'extérieur du congélateur conservent un enregistrement continu de la température. Les capteurs déclencheront des signaux d'alarme sonores et/ou des alarmes informatiques si la température du congélateur sort des limites.
Cultiver le virus
- 2 Après décongélation et réchauffement du virus de la semence dans des conditions soigneusement spécifiées (c'est-à-dire à température ambiante ou dans un bain-marie), la petite quantité de cellules virales est placée dans une l'ajout d'un milieu approprié, permet aux cellules virales de se multiplier. Chaque type de virus se développe mieux dans un milieu qui lui est spécifique, établi dans des procédures de laboratoire de pré-fabrication, mais tous contiennent des protéines de mammifères sous une forme ou une autre, telles que des protéines purifiées de sang de vache. Le milieu contient également d'autres protéines et composés organiques qui favorisent la reproduction des cellules virales. En ce qui concerne le virus, le milieu d'une usine cellulaire est un hôte pour la reproduction. Mélangés avec le milieu approprié, à la température appropriée et avec une durée prédéterminée, les virus se multiplieront.
- 3 En plus de la température, d'autres facteurs doivent être surveillés, notamment le pH du mélange. Le pH est une mesure de l'acidité ou de la basicité, mesurée sur une échelle de 0 à 14, et les virus doivent être maintenus à un pH défini au sein de l'usine cellulaire. L'eau plate, qui est
 ni acide ni basique (neutre) n'a un pH de 7. Bien que le récipient dans lequel les cellules se développent soit pas très grand (peut-être la taille d'un pot de 4 à 8 pintes), il y a un nombre impressionnant de valves, de tubes et de capteurs qui y sont connectés. Des capteurs surveillent le pH et la température, et il existe diverses connexions pour ajouter des milieux ou des produits chimiques tels que l'oxygène pour maintenir le pH, des endroits pour prélever des échantillons pour analyse microscopique et des dispositions stériles pour ajouter les composants de l'usine de cellules et retirer le produit intermédiaire lorsqu'il est prêt.
ni acide ni basique (neutre) n'a un pH de 7. Bien que le récipient dans lequel les cellules se développent soit pas très grand (peut-être la taille d'un pot de 4 à 8 pintes), il y a un nombre impressionnant de valves, de tubes et de capteurs qui y sont connectés. Des capteurs surveillent le pH et la température, et il existe diverses connexions pour ajouter des milieux ou des produits chimiques tels que l'oxygène pour maintenir le pH, des endroits pour prélever des échantillons pour analyse microscopique et des dispositions stériles pour ajouter les composants de l'usine de cellules et retirer le produit intermédiaire lorsqu'il est prêt. - 4 Le virus de l'usine cellulaire est ensuite séparé du milieu, et placé dans un second milieu pour une croissance supplémentaire. Les premières méthodes d'il y a 40 ou 50 ans utilisaient une bouteille pour contenir le mélange, et la croissance résultante était une seule couche de virus flottant sur le milieu. On a vite découvert que si la bouteille était tournée pendant que les virus se développaient, encore plus de virus pouvaient être produits car une couche de virus se développait sur toutes les surfaces intérieures de la bouteille. Une découverte importante dans les années 1940 était que la croissance cellulaire est fortement stimulée par l'ajout d'enzymes à un milieu, dont le plus couramment utilisé est la trypsine. Une enzyme est une protéine qui fonctionne également comme un catalyseur dans l'alimentation et la croissance des cellules.
Dans la pratique actuelle, les bouteilles ne sont pas du tout utilisées. Le virus en croissance est conservé dans un récipient plus grand mais similaire à l'usine cellulaire, et mélangé à des « billes », proches de particules microscopiques auxquelles les virus peuvent se fixer. L'utilisation des billes fournit au virus une zone beaucoup plus grande pour se fixer et, par conséquent, une croissance beaucoup plus importante du virus. Comme dans l'usine cellulaire, la température et le pH sont strictement contrôlés. Le temps passé à cultiver le virus varie selon le type de virus produit et est, dans chaque cas, un secret bien gardé du fabricant.
Séparation
- 5 Lorsqu'il y a un nombre suffisant de virus, ils sont séparés des billes d'une ou plusieurs manières. Le bouillon peut être forcé à travers un filtre avec des ouvertures suffisamment grandes pour permettre aux virus de passer, mais suffisamment petites pour empêcher les billes de passer. Le mélange peut être centrifugé plusieurs fois pour séparer le virus des billes dans un récipient d'où ils peuvent ensuite être retirés. Encore une autre alternative pourrait être d'inonder le mélange de billes avec un autre milieu qui lave le virus des billes.
Sélection de la souche
Le vaccin éventuel sera soit composé d'un virus atténué (affaibli), soit d'un virus tué. Le choix de l'un ou de l'autre dépend d'un certain nombre de facteurs, dont l'efficacité du vaccin obtenu et ses effets secondaires. Le vaccin Ru, qui est développé presque chaque année en réponse à de nouvelles variantes du virus responsable, est toujours un vaccin atténué. La virulence d'un virus peut dicter le choix; le vaccin contre la rage, par exemple, est toujours un vaccin tué.
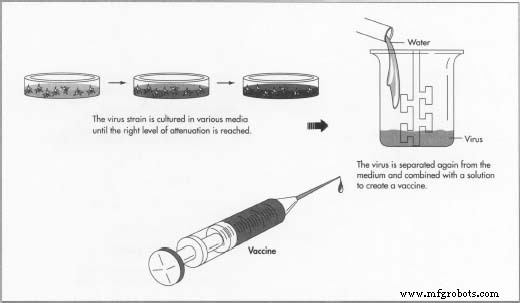
- 6 Si le vaccin est atténué, le virus est généralement atténué avant de passer par le processus de production. Des souches soigneusement sélectionnées sont cultivées (cultivées) à plusieurs reprises dans divers milieux. Il existe des souches de virus qui deviennent en fait plus fortes au fur et à mesure de leur croissance. Ces souches sont clairement inutilisables pour un vaccin atténué. D'autres souches deviennent trop faibles au fur et à mesure qu'elles sont cultivées à plusieurs reprises, et celles-ci sont également inacceptables pour une utilisation vaccinale. Comme la bouillie, la chaise et le lit que Goldilocks aimait, seuls certains virus sont « corrects », atteignant un niveau d'atténuation qui les rend acceptables pour une utilisation vaccinale, et ne change pas de force. La technologie moléculaire récente a rendu possible l'atténuation des virus vivants par manipulation moléculaire, mais cette méthode est encore rare.
- 7 Le virus est ensuite séparé du milieu dans lequel il a été cultivé. Les vaccins qui sont de plusieurs types (comme la plupart le sont) sont combinés avant conditionnement. La quantité réelle de vaccin administrée à un patient sera relativement faible par rapport au milieu dans lequel elle est administrée. Les décisions d'utiliser de l'eau, de l'alcool ou une autre solution pour un vaccin injectable, par exemple, sont prises après des tests répétés de sécurité, de stérilité et de stabilité.
Contrôle qualité
Pour protéger à la fois la pureté du vaccin et la sécurité des travailleurs qui fabriquent et emballent le vaccin, des conditions de propreté du laboratoire sont respectées tout au long de la procédure. Tous les transferts de virus et de milieux sont effectués dans des conditions stériles, et tous les instruments utilisés sont stérilisés dans un autoclave (une machine qui tue les organismes par la chaleur, et qui peut être aussi petite qu'une boîte à bijoux ou aussi grande qu'un ascenseur) avant et après utilisation. Les travailleurs effectuant les procédures portent des vêtements de protection comprenant des blouses jetables en tyvek, des gants, des chaussons, des filets à cheveux et des masques faciaux. Les salles de fabrication elles-mêmes sont spécialement climatisées afin qu'il y ait un nombre minimal de particules dans l'air.
Le processus d'approbation
Pour que des médicaments délivrés sur ordonnance soient vendus aux États-Unis, un fabricant de médicaments doit satisfaire à des exigences strictes en matière de licence établies par la loi et appliquées par la Food and Drug Administration (FDA).
Tous les médicaments d'ordonnance doivent subir trois phases de test, bien que les données de la deuxième phase puissent parfois être utilisées pour répondre aux exigences de la troisième phase. Les tests de phase 1 doivent prouver qu'un médicament est sûr, ou au moins qu'aucun effet indésirable ou inattendu ne se produira de son administration. Si un médicament réussit les tests de phase I, il doit ensuite être testé pour son efficacité - il doit faire ce qu'il est censé faire; on ne peut pas vendre un médicament qui est inutile ou qui revendique un effet qu'il n'a pas. Enfin, les tests de phase III sont conçus pour quantifier l'efficacité d'un médicament ou d'un médicament. Bien que l'on s'attende à ce que les vaccins aient une efficacité proche de 100 %, certains médicaments pourraient bien être acceptables même s'ils ont une efficacité limitée, à condition que le médecin prescripteur en connaisse les chances.
L'ensemble du processus de fabrication est soigneusement examiné par la FDA qui examine les enregistrements des procédures ainsi que la visite du site de fabrication lui-même. Chaque étape du processus de fabrication doit être documentée et le fabricant doit démontrer un « état de contrôle » pour le processus de fabrication. Cela signifie que des enregistrements scrupuleux doivent être conservés pour chaque étape du processus, et qu'il doit y avoir des instructions écrites pour chaque étape du processus. Sauf en cas d'erreur grave, la FDA ne détermine pas si chaque étape d'un processus est correcte, mais seulement si elle est sûre et suffisamment documentée pour être exécutée comme le stipule le fabricant.
Le futur
La production d'un vaccin antiviral utilisable et sûr implique un grand nombre d'étapes qui, malheureusement, ne peuvent pas toujours être réalisées pour chaque virus. Il y a encore beaucoup à faire et à apprendre. Les nouvelles méthodes de manipulation moléculaire ont amené plus d'un scientifique à croire que la technologie des vaccins n'entre que maintenant dans un "âge d'or". Des améliorations des vaccins existants sont possibles à l'avenir. Le vaccin antirabique, par exemple, produit des effets secondaires qui le rendent insatisfaisant pour la vaccination de masse; aux États-Unis, le vaccin antirabique n'est désormais utilisé que sur des patients qui ont contracté le virus à partir d'un animal infecté et sont susceptibles, sans vaccination, de développer la maladie mortelle.
Le virus VIH, dont les biologistes pensent qu'il cause le SIDA, ne se prête pas actuellement aux méthodes traditionnelles de production de vaccins. Le virus du SIDA mute rapidement d'une souche à l'autre et aucune souche donnée ne semble conférer d'immunité contre les autres souches. De plus, un effet immunisant limité du virus atténué ou tué ne peut être démontré ni en laboratoire ni chez les animaux d'essai. Aucun vaccin contre le VIH n'a encore été développé.
Processus de fabrication
- 14 types de virus informatiques différents [à partir de 2021]
- 15 pires virus informatiques de tous les temps | Expliqué
- Cinq raisons pour lesquelles la vague de virus dans le commerce électronique est là pour rester
- Comment préparer la chaîne du froid pour les demandes de vaccins COVID-19
- Rôle des technologies dans la distribution d'un vaccin dans le monde
- Comment donner un coup de fouet au déploiement du vaccin
- Cinq problèmes d'expédition qui mettent la livraison de vaccins en danger
- Sept leçons du dernier kilomètre qui pourraient améliorer la distribution des vaccins
- Quatre façons dont la blockchain pourrait faire progresser le déploiement du vaccin COVID-19



