Croissance in situ de nanocristaux de sulfure métallique dans du poly(3-hexylthiophène) :[6,6]-Phenyl C61-Butyric Acid Methyl Ester Films for Cellules solaires hybrides inversées avec photocourant amélioré
Résumé
Il a été rapporté que les performances des cellules solaires organiques à hétérojonction en vrac peuvent être améliorées par l'incorporation de nano-hétérostructures de métaux, de semi-conducteurs et de matériaux diélectriques dans la couche active. Dans ce manuscrit, CdS ou Sb2 S3 des nanocristaux ont été générés in situ à l'intérieur du poly(3-hexylthiophène) :acide [6,6]-phényl C61-butyrique (P3HT:PC61 BM) en mélangeant aléatoirement P3HT et PC61 BM en présence de précurseur de xanthate de cadmium ou d'antimoine. Cellules solaires hybrides (HSC) avec les configurations de substrat d'oxyde d'indium dopé à l'étain (ITO)/Couche d'interface CdS/P3HT:PC61 BM : x % en poids CdS/MoO3 /Ag et couche d'interface ITO/CdS /P3HT:PC61 BM : x % en poids Sb2 S3 /MoO3 /Ag ont été fabriqués. Couches actives hybrides (P3HT:PC61 BM : x % en poids CdS ou P3HT:PC61 BM : x % en poids Sb2 S3 ) ont été complètement formés par recuit thermique du film, entraînant la décomposition du précurseur du xanthate de cadmium ou d'antimoine en CdS ou Sb2 S3 nanocristaux, respectivement. Les effets de x wt.% CdS (ou Sb2 S3 ) des nanocristaux sur les performances des CSH ont été étudiés. D'après l'absorption UV-Vis, la mobilité des trous et les caractérisations morphologiques de surface, il a été prouvé que l'incorporation de 3 % en poids de CdS (ou Sb2 S3 ) nanocristaux dans la couche active de P3HT:PC61 Les cellules solaires à base de BM ont amélioré l'absorption optique, la mobilité des trous et la rugosité de surface par rapport à P3HT:PC61 Cellules solaires à base de BM, permettant ainsi d'améliorer l'efficacité de conversion d'énergie (PCE) des appareils.
Contexte
Les dispositifs photovoltaïques à base de semi-conducteurs organiques sont complétés par diverses caractéristiques avantageuses, telles que la légèreté, le faible coût, la facilité de fabrication à grande échelle basée sur des solutions et la compatibilité avec les matériaux flexibles [1, 2]. En outre, les semi-conducteurs inorganiques sont idéaux pour les cellules solaires hautement efficaces pour leur mobilité de charge supérieure, leur stabilité chimique, ainsi que l'absorption de la lumière améliorée (potentiel d'ajuster leur bande interdite optique dans la région du proche infrarouge) [3, 4]. Par conséquent, les cellules solaires hybrides (HSC), composées à la fois de semi-conducteurs organiques et de semi-conducteurs inorganiques, ont suscité une attention considérable, principalement en raison de la promesse d'intégrer les qualités attrayantes des deux classes de matériaux [5,6,7]. Un HSC typique est basé sur le concept d'hétérojonction en vrac dans lequel un mélange de matériaux organiques et de nanoparticules inorganiques couche active pris en sandwich entre deux électrodes collectrices de charges [5,6,7]. À ce jour, une large gamme de matériaux organiques, tels que les polymères conjugués à faible bande interdite [7], ainsi que de nombreux matériaux inorganiques, y compris les nanomatériaux métalliques (Ag, Au) [8, 9], le silicium [10, 11], l'oxyde métallique nanoparticules (ZnO, TiO2 ) [12,13,14], nanoparticules de dioxyde de silicium (SiO2 ) [15], composés de cadmium (CdS, CdSe, CdTe) [16,17,18], nanoparticules à faible bande interdite (PbS, PbSe, Sb2 S3 ,Cu2 S, SnS2 , CuInS2 , FeS2 ) [19,20,21,22,23,24,25], et ainsi de suite, ont été appliqués comme couche active dans les HSC.
Les performances des CSH dépendent de manière critique de la capacité à contrôler les matériaux et la structure de l'interface à l'échelle nanométrique [26]. Le procédé conventionnel de préparation de la couche active composite organique et inorganique consiste à mélanger directement un polymère organique donné avec le nanocristal inorganique coiffé d'un ligand tel que préparé en utilisant un cosolvant [16,17,18,19,20,21,22,23, 24,25]. Bien que l'incorporation des ligands de surface dans le composite organique/inorganique puisse améliorer la distribution des nanocristaux dans un polymère conjugué, les ligands à longue chaîne formeraient une interface isolante entre la matrice polymère et les nanocristaux. En conséquence, l'interface isolante inhibera le transfert de charge entre le polymère et les nanocristaux, et le cosolvant affectera négativement l'orientation de la chaîne du polymère ainsi que la solubilité des nanocristaux inorganiques, affectant ainsi les rendements de conversion de puissance (PCE) des dispositifs [ 5, 27]. Ces inconvénients peuvent être largement contournés par plusieurs stratégies alternatives, notamment l'échange de ligands [27, 28], l'utilisation de thiols, de poly- et d'oligothiophènes et de tensioactifs copolymères fonctionnalisés par une amine [29, 30, 31], en utilisant des ligands thermiquement clivables [ 32] et la synthèse de nanocristaux dans une solution de polymère conducteur [33]. Une autre stratégie alternative est la génération in situ du semi-conducteur inorganique à l'intérieur du matériau organique sans tensioactifs ni ligands [26, 34, 35]. Dans le processus, une solution de polymère contenant un précurseur organométallique bien soluble des nanoparticules inorganiques est déposée. Parce que le précurseur organométallique est facilement soluble dans les milieux organiques, il peut être coulé en un film mince avec le polymère de la solution. Lors de la décomposition thermique du film, le précurseur organométallique est converti en matériau inorganique avec la couche de polymère, assurant un mélange intime et un transport de charge photo-induit efficace en même temps. De cette manière, les couches actives hybrides peuvent être formées dans des conditions d'absence de ligands de surface et de cosolvant. Le groupe de Haque a rapporté une méthode générale basée sur la décomposition thermique contrôlée in situ d'un précurseur de xanthate métallique à source unique à l'intérieur d'un film polymère [26, 36, 37, 38, 39, 40]. Dispositifs photovoltaïques basés sur de telles couches hybrides avec la configuration d'un substrat d'oxyde d'indium dopé à l'étain (ITO)/TiO2 /Couche d'interface CdS/P3HT :CdS/poly(3,4-éthylènedioxythiophène) dopé acide polystyrène sulfonique (PEDOT:PSS)/Ag et ITO/TiO2 /Couche interface CdS/P3HT :Sb2 S3 /PEDOT:PSS/Ag ont montré des PCE de 2,17 et 1,29 %, respectivement [36, 38].
Dans cet article, pour les considérations d'utilisation des effets synergiques entre P3HT:PC61 Cellules solaires à base de BM et nanocristaux de sulfure métallique (CdS et Sb2 S3 ) en tant que matériau dopé pour offrir une mobilité de charge supérieure et améliorer l'absorption de la lumière, nous rapportons les HSC avec la configuration de la couche d'interface ITO/CdS/P3HT :PC61 BM : x % en poids CdS/MoO3 /Ag et couche d'interface ITO/CdS/P3HT:PC61 BM : x % en poids Sb2 S3 /MoO3 /Ag. Ici, ITO et Ag ont été fabriqués comme cathode et l'anode supérieure, tandis que la couche d'interface CdS et MoO3 ont été utilisés pour les couches de transport d'électrons et de trous, respectivement. CdS ou Sb2 S3 des nanocristaux ont été générés in situ à l'intérieur du P3HT:PC61 Système BM en mélangeant aléatoirement P3HT et PC61 BM en présence ou en absence de précurseur de xanthate de cadmium ou d'antimoine. Couches actives hybrides (P3HT:PC61 BM : x % en poids CdS ou P3HT:PC61 BM : x % en poids Sb2 S3 ) ont été complètement formés par recuit thermique du film, entraînant la décomposition du précurseur du xanthate de cadmium ou d'antimoine en CdS ou Sb2 S3 nanocristaux, respectivement. Les effets de x wt.% CdS (ou Sb2 S3 ) nanocristaux sur les performances de P3HT:PC61 Les CSH à base de BM ont été étudiées. Et les PCE les plus élevés de 2,91 et 2,92 % ont été obtenus pour les CSH avec 3 % en poids de nanocristaux de CdS et 3 % en poids de Sb2 S3 nanocristaux, respectivement. L'absorption UV-Vis, les mobilités des trous et les caractérisations morphologiques de surface des couches actives ont été réalisées afin de comprendre les raisons probables de l'amélioration des performances de l'appareil.
Méthodes/Expérimental
Fabrication et caractérisation des HSC
Les HSC organiques/inorganiques, avec configuration de périphérique de la couche d'interface ITO/CdS /P3HT:PC61 BM : x % en poids CdS ou Sb2 S3 /MoO3 /Ag ont été fabriqués comme suit :d'une part, le précurseur de xanthate de cadmium (Di(ethylxanthato-κ 2 S ,S ′)bis(pyridine-κ N )cadmium(II), Cd(S2 COEt)2 (C5 H4 N)2 , Et = ethy) et précurseur de xanthate d'antimoine (Tri(ethylxanthato-κ 2 S ,S ′)antimoine(III), Sb(S2 COEt)3 ) ont été préparés respectivement selon la procédure précédemment publiée [26, 38, 39]. Deuxièmement, un verre à revêtement ITO à motifs avec une résistance de feuille de 10~15 Ω carré −1 a été nettoyé à tour de rôle dans de l'eau désionisée, de l'acétone et de l'isopropanol. Après cela, la couche d'interface CdS (10 nm) a été déposée en tant que couche de transport d'électrons à la suite des travaux publiés précédemment [41], à partir d'une solution de chlorobenzène à 100 mg/mL de Cd(S2 COEt)2 (C5 H4 N)2 par centrifugation à 6000 tr/min pendant 40 s suivi d'un recuit à 160 °C pendant 15 min dans une boîte à gants d'azote. La couche active a été déposée au-dessus de la couche d'interface CdS. Le parfait P3HT:PC61 BM à une solution de rapport pondéral 1:1 dans du chlorobenzène avec une concentration de 17 mg mL −1 de P3HT a été préparé. Pour former la solution hybride, le précurseur de xanthate de cadmium (Cd(S2 COEt)2 (C5 H4 N)2 ) ou précurseur de xanthate d'antimoine (Sb(S2 COEt)3 ) ont été ajoutés à la solution vierge (x % en poids CdS ou Sb2 S3 rapport au poids de P3HT). La couche active a été coulée par centrifugation à partir de ces solutions de mélange à 600 tr/min pendant 40 s, suivie d'un recuit sur une plaque chauffante à 160 °C pendant 30 min dans une boîte à gants. Dans une expérience de contrôle, P3HT:PC61 Couche uniquement BM (à une solution de rapport pondéral 1:1 dans du chlorobenzène avec une concentration de 17 mg mL −1 de P3HT) sans Cd(S2 COEt)2 (C5 H4 N)2 ou Sb(S2 COEt)3 a également été revêtu par centrifugation et recuit dans les mêmes conditions expérimentales. Ensuite, les échantillons ont été transférés dans une chambre à vide poussé (sous vide de 3 × 10 −5 Pa) pour compléter les HSC, où un MoO3 de 8 nm d'épaisseur une couche collectrice de trous et une anode en Ag de 100 nm d'épaisseur ont été évaporées thermiquement à travers des masques d'ombre. L'épaisseur de la cathode évaporée a été contrôlée par un moniteur d'épaisseur/rapport de cristal de quartz (SI-TM206, Shenyang Science Co.). De plus, chaque appareil avait une surface active de 0,10 cm 2 . Tous les processus de fabrication ont été effectués à l'intérieur d'une atmosphère contrôlée dans une boîte sèche à l'azote (Etelux Co.) contenant moins de 1 ppm d'oxygène et d'humidité.
Caractérisation des couches minces et des appareils
Les données de diffraction des rayons X (XRD) ont été mesurées sur un diffractomètre à rayons X PAN alytical X'Pert Pro équipé d'un rayonnement Cu Kα monochromatisé en graphite (λ = 1,541874 Å). La tension d'accélération a été fixée à 40 kV avec un flux de 40 mA dans la plage 2θ de 10 à 70 °. Les mesures d'analyse thermogravimétrique (TGA) du complexe précurseur de xanthate métallique ont été effectuées sur un système d'analyse thermique (pyris diamond 6300, PerkinElmer) sous un chauffage taux de 10 °C min −1 et un débit d'azote de 20 mL min −1 . Les mesures d'absorption UV-Vis des échantillons ont été enregistrées à température ambiante avec un spectrophotomètre U-3900H (Shanghai Tianmei). Les PCE des HSC résultants ont été mesurés sous 1 soleil, condition AM 1.5G (Air mass 1.5 global) à l'aide d'un simulateur solaire (XES-70S1, San-EI Electric Co.) (100 mW cm −2 ). Les caractéristiques de densité de courant-tension (J-V) ont été enregistrées avec une unité de mesure de source Keithley 2410 dans la boîte sèche d'azote (Etelux Co.). Les réponses spectrales des dispositifs ont été mesurées avec une configuration commerciale EQE/photon incident à efficacité de conversion de courant (IPCE) (7-SCSpecIII, Beijing 7-star Optical Instruments Co., Ltd.). Un détecteur au silicium calibré a été utilisé pour déterminer la photosensibilité absolue. Les images de microscopie à force atomique (AFM) en mode tapotement ont été obtenues à l'aide d'un système MFP-3D-SA (Asylum Research).
Résultats et discussion
Stabilités thermiques de Cd(S2 COEt)2 (C5 H4 N)2 et Sb(S2 COEt)3 ont d'abord été étudiés par TGA, comme le montre la figure 1. Cd(S2 COEt)2 (C5 H4 N)2 commence à se décomposer à environ 50 °C et est complète à 150 °C, la masse résiduelle finale (environ 25,0%) est proche de celle de CdS (28,1%), ce qui a également été prouvé dans les travaux précédents [41]. Sb(S2 COEt)3 commence à se décomposer à environ 120 °C et se termine à 160 °C, et le poids restant (35,8 %) correspond à Sb2 S3 (35,0 %), ce qui est cohérent avec les travaux antérieurs [42].
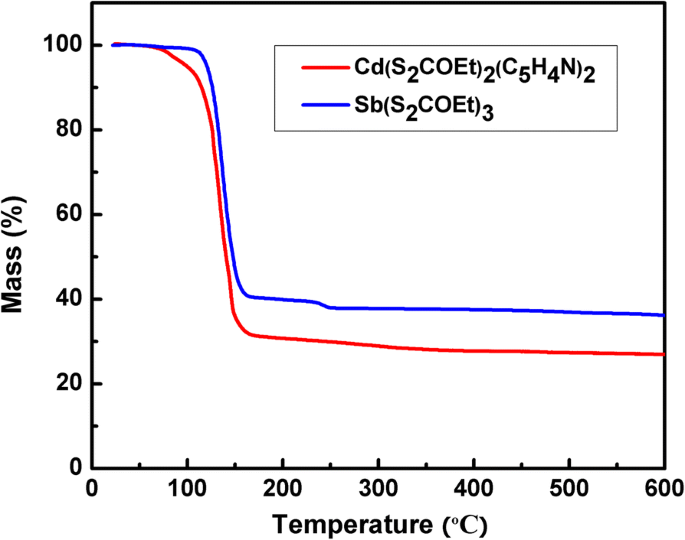
Tracés TGA de Cd(S2 COEt)2 (C5 H4 N)2 et Sb(S2 COEt)3
Des films minces ont été enduits par centrifugation à partir d'une solution de chlorobenzène de Cd(S2 COEt)2 (C5 H4 N)2 ou Sb(S2 COEt)3 tout d'abord, puis ont été recuits à 160 °C pendant 30 min. En conséquence, les films minces jaunes ou oranges ont été obtenus, respectivement. Afin de caractériser les propriétés de structure des films minces, des études XRD des films recuits ont été réalisées. Les diagrammes XRD du produit sont présentés sur la figure 2. Selon les diagrammes de référence pour le CdS hexagonal (PDF 41-1049) et le CdS cubique (PDF 01-080-0019), il est évident que les pics de diffraction sur la figure 2a peut être indexé sur un mélange de structures cristalline hexagonale et cubique, qui ont été montrées au-dessus des pics (h et c indiquent respectivement la phase hexagonale et cubique), comme décrit dans l'article précédent [37]. Les pics de diffraction de la figure 2b peuvent être entièrement indexés sur la phase orthorhombique de Sb2 S3 (constantes de cellule a = 11,23 Å, b = 11,31 Å, c = 3,841 Å ; Fichier de carte JCPDS 42–1393) [43, 44], ce qui est en bon accord avec les résultats TG de la figure 1.
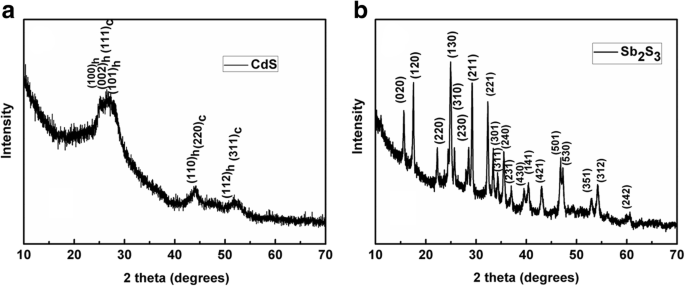
Diagrammes XRD des films minces obtenus par décomposition thermique de a (Cd(S2 COEt)2 (C5 H4 N)2 ) et b Sb(S2 COEt)3 , respectivement
Les morphologies de surface de CdS et Sb2 S3 des couches minces ont également été exploitées. Fichier supplémentaire 1 : La figure S1 présente l'évolution de la morphologie de l'ITO avant (Fichier supplémentaire 1 : Figure S1a) et après décomposition thermique (160 °C, 15 min) de la solution de chlorobenzène de Cd(S2 COEt)2 (C5 H4 N)2 (Fichier supplémentaire 1 :Figure S1b) et Sb(S2 COEt)3 (Fichier supplémentaire 1 :Figure S1c). Comme décrit dans nos travaux précédents [41], on peut voir que la surface de l'ITO nu montre un rassemblement densément compacté de cristaux fins avec une taille de grain d'environ 10 nm. Après décomposition thermique de la solution de chlorobenzène de précurseur de xanthate de cadmium ou d'antimoine, il est évident que le film de nanocristaux de CdS (environ 60~100 nm) ou Sb2 S3 un film de nanocristal (agrégats de 100 à 200 nm) est formé sur un substrat d'ITO.
Afin d'étudier l'effet de CdS (ou Sb2 S3 ) nanocristaux sur les performances de P3HT:PC61 HSC basés sur BM, les dispositifs ont été fabriqués en utilisant la structure ITO/CdS interface layer/P3HT:PC61 BM : x % en poids CdS (ou Sb2 S3 )/MoO3 /Ag comme le montre la figure 3a. CdS ou Sb2 S3 des nanocristaux ont été générés in situ à l'intérieur du P3HT:PC61 Système BM en mélangeant aléatoirement P3HT et PC61 BM en présence ou en absence de précurseur de xanthate de cadmium ou d'antimoine. Couches actives hybrides (P3HT:PC61 BM : x % en poids CdS ou P3HT:PC61 BM : x % en poids Sb2 S3 ) ont été complètement formés par recuit thermique du film provoquant la décomposition du précurseur de xanthate de cadmium ou d'antimoine en CdS ou Sb2 S3 nanocristaux, respectivement (images SEM de P3HT:PC61 BM, P3HT : PC61 BM :3 % en poids de CdS et P3HT :PC61 BM :3 % en poids Sb2 S3 les films sur substrats ITO ont été présentés dans le fichier supplémentaire 1 :Figure S2). Une température de recuit de 160 °C et un temps de recuit de 30 min ont été choisis dans notre expérience afin de faire décomposer complètement le précurseur du xanthate de cadmium ou d'antimoine (voir les tracés TGA de Cd(S2 COEt)2 (C5 H4 N)2 et Sb(S2 COEt)3 dans la figure 1).
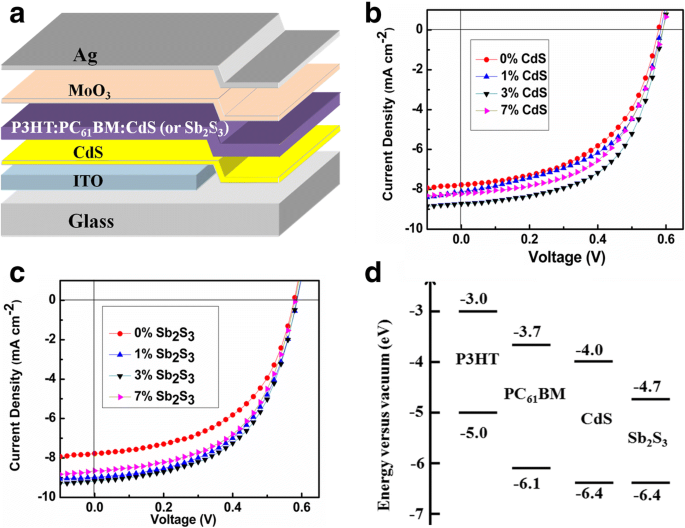
un Schéma de principe des HSC. b Courbes J–V des HSC basées sur P3HT:PC61 BM :CdS avec différents % en poids de nanocristaux de CdS. c Courbes J–V des HSC basées sur P3HT:PC61 BM :Sb2 S3 avec différents % en poids de Sb2 S3 nanocristaux. d Diagramme de bandes d'énergie des matériaux utilisés dans la couche active des CSH
Caractéristiques J–V des HSC avec différents % en poids de CdS (ou Sb2 S3 ) les nanocristaux incorporés dans les couches organiques sont représentés sur la Fig. 3b (ou Fig. 3c), et les paramètres photovoltaïques, dont le courant de court-circuit (J sc ), tension en circuit ouvert (V oc ), le facteur de remplissage (FF), la résistance série (R S ) et PCE, sont répertoriés dans le tableau 1. Toutes les données fournies sont des valeurs moyennes calculées à partir de plus de 20 appareils. L'appareil sans CdS (ou Sb2 S3 ) nanocristaux (couche interface ITO/CdS/P3HT:PC61 BM :/MoO3 /Ag) a montré un J sc de 7,77 mAcm −2 , un V oc de 0,58 V, un FF de 0,52 et un PCE de 2,34 %. Avec ajout de CdS ou Sb2 S3 nanocristaux, il a été observé que V oc , qui est limité par la différence d'énergie entre le niveau d'orbitale moléculaire occupé le plus élevé (HOMO) du donneur de polymère et le niveau d'orbitale moléculaire inoccupé (LUMO) le plus bas de l'accepteur dans les cellules solaires en polymère [45, 46], reste autour de 0,58 à 0,59 V dans tous les HSC. Cela peut être compris du fait que PC61 BM agit en tant qu'accepteur et CdS ou Sb2 S3 pourrait agir comme une cascade d'électrons (le diagramme de bande d'énergie des matériaux utilisés dans la couche active dans les HSC est montré sur la figure 3d), comme mentionné dans les travaux précédents [47]. Pour les HSC avec ajout de CdS, J sc augmente tout d'abord de 7,77 à 8,72 mA cm −2 avec l'augmentation de CdS de 0 à 3 % en poids, puis diminue à 8,23 mA cm −2 lorsque la masse de CdS augmente encore de 3 à 7 % en poids. Simultanément, R S réduit évidemment de 22,15 Ω cm 2 (0 % en poids de CdS) à 16,70 Ω cm 2 (3 % en poids de CdS), contribuant à une augmentation remarquable de FF de 0,52 à 0,56. En conséquence, le HSC avec 3 % en poids de nanocristaux de CdS offre les meilleures performances de l'appareil, offrant un PCE de 2,91 %. Il est à noter ici que cette valeur est bien supérieure au meilleur PCE de 0,95% que le groupe de Chand a obtenu dans les HSC (ITO/PEDOT:PSS/P3HT:PC61 BM:CdS/Al) en utilisant des nanocristaux de CdS fabriqués par chimie en solution comme l'un des composants de la couche active [48]. Les règles de changement de J sc et FF dans les HSC avec ajout de Sb2 S3 étaient similaires à ceux des HSC avec ajout de CdS, à l'exception de l'augmentation plus évidente de J sc (de 7,77 à 9,15 mA cm −2 ) avec l'augmentation de Sb2 S3 de 0 à 3 % en poids. Par coïncidence, l'appareil avec 3 % en poids de Sb2 S3 les nanocristaux fournissent également le PCE le plus élevé de 2,92% avec J sc de 9,15 mAcm −2 , V oc de 0,58 V, FF de 0,54.
Un autre paramètre utile pour déterminer le PCE des HSC est l'IPCE, qui atteint 100 % lorsque tous les photons incidents génèrent des paires électron-trou. Cependant, dans des situations pratiques, en raison des pertes causées par la réflexion des photons incidents, l'absorption imparfaite des photons par le semi-conducteur et la recombinaison des porteurs de charge dans le semi-conducteur, l'IPCE est généralement inférieur à 100 % [8]. Spectres IPCE pour les dispositifs photovoltaïques basés sur P3HT:PC61 BM, P3HT : PC61 BM : 3 % en poids de CdS et P3HT :PC61 BM :3 % en poids Sb2 S3 sont affichés sur la Fig. 4a à des fins de comparaison. Bien que tous les spectres IPCE soient de forme similaire, la valeur IPCE pour les HSC contenant P3HT:PC61 BM : 3 % en poids de CdS (ou P3HT :PC61 BM :3 % en poids Sb2 S3 ) est supérieur à celui du P3HT:PC61 BM dans toutes les longueurs d'onde (300-650 nm). Par exemple, le dispositif photovoltaïque de P3HT:PC61 BM s'est avéré avoir un IPCE maximum proche de 55% à 540 nm et les IPCE des HSC avec P3HT:PC61 BM :3 % en poids de CdS et P3HT :PC61 BM :3 % en poids Sb2 S3 sont respectivement à 60 et 65 % à la même longueur d'onde.
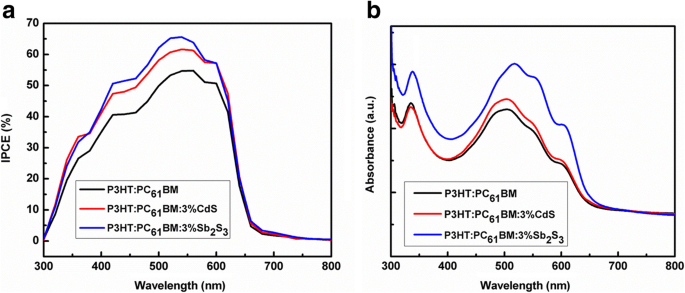
un Courbes IPCE des CSH basées sur P3HT:PC61 BM, P3HT : PC61 BM :3 % en poids de CdS et P3HT :PC61 BM :3 % en poids Sb2 S3 . b Spectres d'absorbance UV-Vis des films de P3HT:PC61 BM, P3HT : PC61 BM :3 % en poids de CdS et P3HT :PC61 BM :3 % en poids Sb2 S3
Afin de comprendre les raisons probables de l'amélioration des performances de l'appareil par l'ajout de CdS ou Sb2 S3 nanocristaux, des études d'absorption UV-Vis ont d'abord été menées sur les films de P3HT:PC61 BM, P3HT : PC61 BM :3 % en poids de CdS et P3HT :PC61 BM :3 % en poids Sb2 S3 avec la même épaisseur. Les spectres d'absorption UV-Visible de la Fig. 4b montrent que l'absorption de l'addition des films de CdS ou Sb2 S3 nanocristaux dans P3HT:PC61 BM étaient presque similaires à celui de P3HT:PC61 BM, tandis que l'absorption de P3HT:PC61 BM : 3 % en poids de CdS était légèrement supérieur à celui de P3HT:PC61 BM. De plus, l'absorption de P3HT:PC61 BM :3 % en poids Sb2 S3 était évidemment supérieur à celui de P3HT:PC61 BM. C'est-à-dire l'enrobage de 3 % en poids de CdS ou Sb2 S3 dans P3HT:PC61 La matrice BM a bien amélioré l'absorption optique par rapport à P3HT:PC61 BM, améliorant ainsi le J SC des appareils.
Après cela, les mobilités de trous des appareils basés sur P3HT:PC61 BM, P3HT : PC61 BM :3 % en poids de CdS et P3HT :PC61 BM :3 % en poids Sb2 S3 ont été déterminés en appliquant le modèle de courant limité à charge d'espace (SCLC) [49]. La figure 5 montre J 1/2 –Courbes V des appareils à trous seuls (ITO/PEDOT:PSS/P3HT:PC61 BM(ou P3HT:PC61 BM :3 % en poids de CdS ou P3HT :PC61 BM :3 % en poids Sb2 S3 )/MoO3 /Ag). Les mobilités apparentes des trous calculées à partir du modèle SCLC se sont avérées être de 4,09 × 10 −5 cm 2 V −1 s −1 , 1,53 × 10 −4 cm 2 V −1 s −1 , et 1,69 × 10 −4 cm 2 V −1 s −1 pour les appareils avec P3HT:PC61 BM, P3HT : PC61 BM :3 % en poids de CdS et P3HT :PC61 BM :3 % en poids Sb2 S3 comme couche active, respectivement. De toute évidence, la mobilité du trou augmente lorsque 3 % en poids de CdS ou Sb2 S3 intégré dans P3HT:PC61 Matrice BM. Des études ont montré que dans P3HT:PC61 BM, la mobilité des électrons est supérieure à la mobilité des trous et ce déséquilibre des porteurs comme cela est préjudiciable aux performances photovoltaïques [9, 50]. L'augmentation de la mobilité des trous de l'appareil basé sur P3HT:PC61 BM :3 % en poids de CdS ou P3HT :PC61 BM :3 % en poids Sb2 S3 permet un transport de charge plus équilibré dans la couche active, améliorant ainsi le J SC et FF, améliorant en outre le PCE de l'appareil, comme mentionné dans le travail précédent [9].
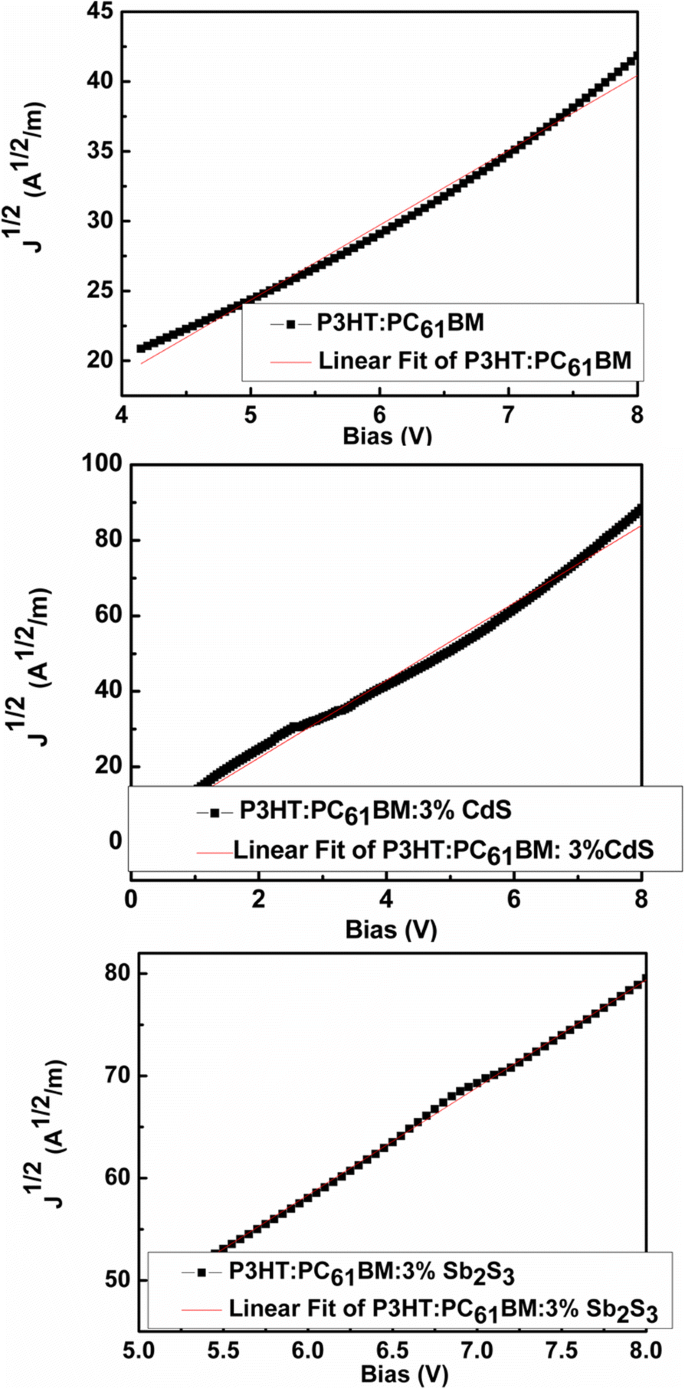
J 1/2 – Courbes en V des appareils à trous seuls pour les appareils avec P3HT:PC61 BM, P3HT : PC61 BM :3 % en poids de CdS et P3HT :PC61 BM :3 % en poids Sb2 S3 comme couche active, respectivement
Les micromorphologies des couches actives ont été étudiées plus avant avec l'AFM en mode taraudage pour révéler les effets de l'ajout de CdS ou Sb2 S3 . Les images de hauteur d'un P3HT:PC61 vierge Film BM et deux films ternaires avec 3 % en poids de CdS et 3 % en poids de Sb2 S3 sont illustrés à la Fig. 6. La morphologie de la surface du P3HT:PC61 BM :3 % en poids de CdS et P3HT :PC61 BM :3 % en poids Sb2 S3 couche montrent une augmentation évidente de la rugosité de surface avec la rugosité quadratique moyenne passant de 2,82 à 8,89 nm et 7,13 nm, respectivement. La plus grande rugosité observée pour le P3HT:PC61 BM :3 % en poids de CdS et P3HT :PC61 BM :3 % en poids Sb2 S3 le film pourrait être une conséquence de la présence du CdS et du Sb2 S3 nanocristaux dans le P3HT:PC61 Couche active BM. Le CdS ou Sb2 S3 on pense que les nanocristaux servent de support pour améliorer l'interpénétration des molécules P3HT et PC61 BM dans le film composite, conduisant à une dissociation supérieure des excitons. En raison de cette dissociation supérieure des excitons, le J SC des HSC basés sur P3HT:PC61 BM :3 % en poids de CdS et P3HT :PC61 BM :3 % en poids Sb2 S3 ont été augmentés [51]. En revanche, l'incorporation de CdS ou Sb2 S3 nanocristaux dans P3HT:PC61 BM augmente la rugosité de surface du film, augmente ainsi la zone de contact interfacial entre la couche active (P3HT:PC61 BM :3 % en poids de CdS ou P3HT :PC61 BM :3 % en poids Sb2 S3 ) et la couche de transport de trous (MoO3 ). De cette façon, une collection de trous plus efficace à l'anode est apparue, ce qui pourrait entraîner une amélioration du J SC et FF des appareils [52].
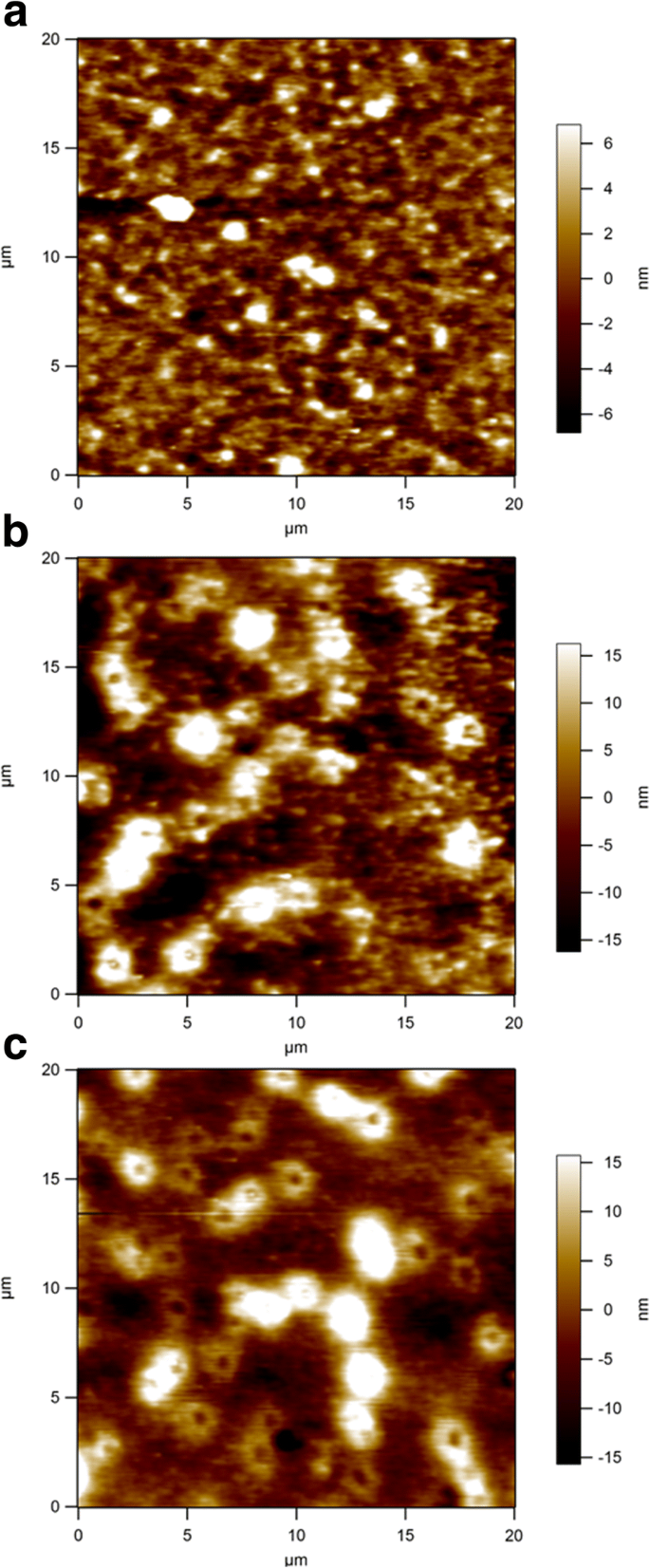
Images de hauteur AFM de a P3HT : PC61 BM, b P3HT : PC61 BM :3 % en poids de CdS et c P3HT : PC61 BM :3 % en poids Sb2 S3 films sur substrats ITO
Conclusions
En conclusion, en tant que matériau dopé pour offrir une mobilité de charge supérieure et améliorer l'absorption de la lumière, CdS ou Sb2 S3 des nanocristaux ont été générés in situ à l'intérieur du P3HT:PC61 Système BM en mélangeant aléatoirement P3HT et PC61 BM en présence de précurseur de xanthate de cadmium ou d'antimoine. La stabilité thermique du précurseur du xanthate de cadmium ou d'antimoine et la structure du CdS ou Sb2 S3 les films ont été caractérisés. Les HSC avec la configuration de la couche d'interface ITO/CdS/P3HT:PC61 BM : x % en poids CdS/MoO3 /Ag et couche d'interface ITO/CdS /P3HT:PC61 BM : x % en poids Sb2 S3 /MoO3 /Ag ont été fabriqués. Les effets de x wt.% CdS (ou Sb2 S3 ) nanocristaux sur les performances de P3HT:PC61 Les CSH à base de BM ont été étudiées. Il a été prouvé que l'incorporation de CdS (ou Sb2 S3 ) nanocristaux dans la couche active de P3HT:PC61 Les cellules solaires à base de BM aident à améliorer les PCE. Et les PCE les plus élevés de 2,91 et 2,92 % ont été obtenus pour les CSH avec 3 % en poids de nanocristaux de CdS et 3 % en poids de Sb2 S3 nanocristaux, respectivement. D'après l'absorption UV-Vis, la mobilité des trous et les caractérisations morphologiques de surface, nos études ont suggéré que 3 % en poids de CdS ou Sb2 S3 intégré dans P3HT:PC61 La matrice BM a amélioré l'absorption optique, la mobilité des trous et la rugosité de surface par rapport à P3HT:PC61 BM, entraînant ainsi l'amélioration des PCE des appareils. La méthode de génération in situ de nanocristaux semi-conducteurs inorganiques à l'intérieur des matériaux organiques peut être appliquée pour concevoir des HSC à haute efficacité.
Nanomatériaux
- Nano arbres pour cellules solaires à colorant
- Nano-hétérojonctions pour cellules solaires
- Nanofibres polymères électrofilées décorées de nanoparticules de métaux nobles pour la détection chimique
- Effet optique non linéaire amélioré dans les cellules hybrides à cristaux liquides basées sur des cristaux photoniques
- PEDOT:Couche de transport de trous transparents PSS hautement conducteur avec traitement au solvant pour cellules solaires hybrides silicium/organique hautes performances
- Stabilité améliorée des nanoparticules magnétiques d'or avec du poly(acide 4-styrènesulfonique-co-acide maléique) :propriétés optiques adaptées pour la détection des protéines
- Synthèse de nanocristaux de ZnO et application dans des cellules solaires polymères inversées
- Cellules solaires à pérovskite inversée hautement efficaces avec couche de transport d'électrons CdSe QD/LiF
- Pérovskite hybride cultivée en vapeur séquentielle pour cellules solaires à hétérojonction planaire



