Combustion de combustible et transfert de chaleur dans un four
Combustion de combustible et transfert de chaleur dans un four
La chaleur est nécessaire dans un four pour chauffer la charge du four (matériau à chauffer dans le four) et parfois pour les réactions chimiques. Les trois sources d'énergie thermique sont (i) la combustion de combustibles, (ii) l'énergie électrique et (iii) l'énergie chimique disponible par les réactions exothermiques. Hormis les fours électrothermiques, ce besoin de chaleur (hors énergie chimique) est satisfait par la combustion d'un combustible. Le combustible peut être un combustible gazeux (par exemple, des sous-produits gazeux tels que le gaz de cokerie, le gaz de haut fourneau et le gaz de convertisseur, le gaz naturel et le gaz de pétrole liquéfié, etc.), un combustible liquide (par exemple, le mazout et le goudron, etc.) , ou un combustible solide (par exemple, charbon, coke, etc.).
Tous les combustibles contiennent de l'énergie potentielle. Lors de la combustion, cette énergie potentielle est libérée dans les produits de combustion (POC). La combustion est normalement considérée comme la libération contrôlée de chaleur et d'énergie provenant de la réaction chimique entre un combustible et un comburant. La quasi-totalité de la combustion dans les procédés industriels utilise un combustible hydrocarboné. Une réaction de combustion généralisée pour un combustible hydrocarboné typique est donnée par l'équation combustible + comburant =dioxyde de carbone (CO2) + vapeur d'eau (H2O) + autres espèces. Les « autres espèces » dépendent du type de comburant utilisé et du rapport entre le combustible et le comburant. Le comburant le plus couramment utilisé est l'air, qui se compose de près de 79 % d'azote (N2) en volume et qui est généralement utilisé dans le processus de combustion. Si la combustion est riche en carburant, ce qui signifie qu'il n'y a pas assez d'oxygène (O2) pour brûler complètement le carburant, il existe alors des hydrocarbures non brûlés dans les produits d'échappement et peu ou pas d'excès d'O2. Si la combustion est pauvre en carburant, ce qui signifie qu'il y a plus d'O2 que nécessaire pour brûler complètement le carburant, puis il y a un excès d'O2 dans les produits d'échappement.
Le combustible a une influence significative sur le transfert de chaleur dans le système de combustion du four. L'une des propriétés les plus importantes est le pouvoir calorifique du combustible. Ceci est utilisé pour déterminer la quantité de combustible à brûler pour traiter le taux de production souhaité du matériau qui est chauffé. Le pouvoir calorifique est spécifié comme le pouvoir calorifique supérieur (PCS) ou le pouvoir calorifique inférieur (PCI).
Le LHV exclut la chaleur de vaporisation, qui est l'énergie nécessaire pour convertir l'eau liquide en vapeur. Cela signifie que le LHV suppose que tous les POC sont gazeux, ce qui est généralement le cas pour presque toutes les applications de combustion industrielle. Si les produits de combustion doivent quitter le processus à une température suffisamment basse pour que toute l'eau soit convertie d'un gaz à un liquide, alors la chaleur de condensation doit être libérée dans le processus en tant que source d'énergie supplémentaire. Le PCS d'un combustible inclut cette énergie supplémentaire.
La composition du carburant est importante pour déterminer la composition du POC et la quantité d'oxydant nécessaire pour brûler le carburant. La densité du combustible est nécessaire pour déterminer les débits à travers le système d'alimentation en combustible de la fournaise et les tailles de tuyaux associées.
La composition des gaz d'échappement est très importante pour déterminer le transfert de chaleur dans le four. Les hydrocarbures non brûlés dans les gaz d'échappement indiquent que le carburant n'a pas été entièrement brûlé et que, par conséquent, toute la chaleur disponible n'a pas été libérée. Des niveaux élevés d'excès d'O2 dans les gaz d'échappement indiquent généralement qu'une trop grande quantité d'oxydant a été fournie. L'excès d'oxydant transporte l'énergie sensible à travers les gaz d'échappement. Cela signifie à nouveau qu'une partie de la chaleur disponible du combustible n'a pas été entièrement utilisée pour chauffer la charge du four. Si le comburant est de l'air, alors une grande partie de l'énergie disponible dans le combustible s'effectue dans la cheminée avec les produits d'échappement.
Le POC transfère l'énergie calorifique à la charge du four pour élever sa température à la valeur requise puis quitte le four. La chaleur sensible dans le POC à la température de procédé critique n'est pas disponible pour le four. Plus la température critique du processus est élevée, plus la chaleur sensible dans le POC est élevée. Cette chaleur sensible dans POC est très importante du point de vue de l'utilisation du carburant.
Il existe deux types courants d'oxydants utilisés dans les procédés de combustion industriels. La majorité des procédés utilisent l'air comme oxydant. Cependant, de nombreux procédés à haute température utilisent un oxydant contenant une concentration d'O2 plus élevée que celle disponible dans l'air (environ 21 % en volume). Ce type de combustion est appelé combustion assistée par O2. Dans de nombreux cas, le taux de production dans un processus de chauffage peut être considérablement augmenté avec seulement des quantités relativement faibles d'enrichissement en O2.
Dans plusieurs cas, les brûleurs air/combustible peuvent fonctionner avec succès avec un comburant contenant jusqu'à environ 30 % d'O2 avec peu ou pas de modifications. À des concentrations d'O2 plus élevées, la flamme peut devenir instable ou la température de la flamme peut devenir trop élevée pour un brûleur conçu pour fonctionner dans des conditions air/combustible. Dans les applications à température plus élevée, où les avantages d'un O2 de pureté plus élevée justifient les coûts supplémentaires, des oxydants de pureté plus élevée peuvent être utilisés (plus de 90 % d'O2). Le processus de chauffage est considérablement intensifié par l'O2 de haute pureté. La pureté du comburant a une influence significative sur le transfert de chaleur dans un système de combustion.
Un aspect important dans un système de combustion est le rapport du combustible au comburant. Il existe de nombreuses façons de le spécifier. Ceux-ci sont discutés ici en bref. Une réaction de combustion globale utilisant du CH4 (méthane) comme combustible peut s'écrire CH4 + (xO2 + yN2) =CO, CO2, H2, H2O, N2, NOx, O2, composants traces. La stoechiométrie d'une réaction indique le rapport O2/carburant pour un système de combustion donné. Une méthode de quantification de la stoechiométrie consiste à ne considérer que l'O2 dans l'oxydant, puisque les inertes dans l'oxydant ne sont pas nécessaires à la réaction. Ainsi, en considérant le CH4 comme un carburant, la réaction stoechiométrique globale simplifiée avec l'air peut s'écrire CH4 + (2O2 + 7,52N2) =CO2 + 2H2O + 7,52N2. Dans cette réaction, l'air est représenté par 2O2 + 7,52N2. Ici, le rapport stoechiométrique est de 2 puisque 2 molécules d'O2 sont nécessaires pour brûler une molécule de CH4.
Cette méthode de spécification du rapport stoechiométrique est généralement utilisée pour les systèmes de combustion incorporant un enrichissement en O2. En effet, la quantité d'O2 fournie au système de combustion est importante.
Les flammes réelles nécessitent généralement un excès d'O2 pour une combustion complète du carburant. Cela est dû à un mélange incomplet entre le carburant et le comburant. Pour la combustion riche en carburant de CH4, le rapport stoechiométrique est inférieur à 2. En cas de combustion pauvre en carburant de CH4, le rapport stoechiométrique est supérieur à 2. Par conséquent, la composition du comburant est importante. Une manière courante de spécifier la composition de l'oxydant consiste à calculer la fraction molaire d'O2 dans l'oxydant.
De nombreux processus de combustion industriels fonctionnent avec environ 3 % d'O2 en plus que ce qui est théoriquement nécessaire pour une combustion parfaite. Il s'agit souvent de la quantité d'O2 en excès nécessaire pour minimiser les émissions d'hydrocarbures imbrûlés et assurer la combustion complète du carburant. Cela peut être dû aux limitations de mélange entre le carburant et le comburant, en particulier dans les systèmes non prémélangés.
Trop d'excès d'O2 signifie que de l'énergie est gaspillée dans le chauffage de l'air de combustion en excès, au lieu de la charge du four. Par conséquent, il est souhaitable de n'utiliser que juste assez d'excès d'O2 pour obtenir de faibles émissions de CO (monoxyde de carbone). Un exemple de réaction globale simplifiée pour le CH4 avec 3 % d'excès d'O2 est la réaction CH4 + (2,06O2 + 7,75N2) =CO2 + 2H2O + 0,06O2 + 7,75N2.
La plupart des flammes industrielles sont turbulentes, ce qui est généralement déterminé par un nombre de Reynolds turbulent (Re). L'échelle de longueur caractéristique turbulente est normalement appelée longueur de Kolmogorov. La longueur de Kolmogorov est représentative de la dimension où se produit la dissipation. L'échelle de longueur de Taylor peut être définie comme le rapport du taux de déformation aux forces visqueuses. Les différentes longueurs peuvent être utilisées pour caractériser une flamme. Une flamme peut être (i) une flamme ridée, (ii) une flamme fortement ridée, (iii) des flammelettes dans les tourbillons et (iv) un front de réaction distribué. Un nombre de Damköhler adimensionnel (Da) indique le type de temps de réaction qui est significatif pour le type spécifique de réaction de combustion. Ce nombre est le rapport du temps de réaction au débit.
Propriétés de combustion
Les propriétés de combustion normales généralement utilisées dans les applications industrielles sont (i) la composition des produits de combustion, (ii) la température de la flamme, (iii) la chaleur disponible et (iv) le volume des gaz de combustion après combustion. Celles-ci sont importantes pour calculer le transfert de chaleur de la flamme. et les gaz d'échappement au four et à la charge du four.
Produits de combustion
Il existe un certain nombre de variables qui peuvent avoir un impact significatif sur les produits de combustion. Certaines des variables importantes comprennent la composition de l'oxydant, le rapport de mélange, les températures de préchauffage de l'air et du carburant et la composition du carburant. Ceux-ci sont brièvement discutés ci-dessous.
Composition de l'oxydant – En prenant l'exemple de la combustion du CH4, la combustion stoechiométrique du CH4 avec de l'air peut être représentée par l'équation globale CH4 + 2O2 + 7,52N2 =CO2, 2H2O, 7,52N2 et composants traces. On peut voir que plus de 70 % en volume des gaz d'échappement sont du N2. De même, un processus de combustion stoechiométrique O2/CH4 peut être représenté par l'équation CH4 + 2O2 =CO2, 2H2O et des espèces traces. Le volume des gaz d'échappement est considérablement réduit par l'élimination du N2. En général, un processus de combustion stoechiométrique de CH4 enrichi en O2 peut être représenté par l'équation CH4 + 2O2 + xN2 =CO2 + 2H2O + xN2 + composants traces.
La composition réelle des produits d'échappement de la réaction de combustion dépend de plusieurs facteurs, notamment la composition de l'oxydant, la température des gaz et le rapport d'équivalence. Le rapport d'équivalence est défini comme le rapport du rapport carburant/air réel sur le rapport carburant/air stœchiométrique. La combustion stoechiométrique se produit lorsque tout l'O2 est consommé dans la réaction et qu'il n'y a pas d'O2 moléculaire dans les produits.
Un processus adiabatique signifie qu'aucune chaleur n'est perdue pendant la réaction, ou que la réaction se produit dans une chambre parfaitement isolée. Ce n'est pas le cas dans un processus de combustion réel où la chaleur est perdue de la flamme par rayonnement. Le produit majeur prédit pour la combustion à l'équilibre adiabatique du CH4 est fonction de la composition de l'oxydant.
Un processus d'équilibre signifie qu'il y a un temps infini pour que les réactions chimiques aient lieu, ou que les produits de réaction ne soient pas limités par la cinétique chimique. Cependant, dans les conditions réelles, les réactions de combustion s'achèvent en quelques fractions de seconde. En outre, à mesure que N2 est éliminé de l'oxydant, la concentration de N2 dans les produits d'échappement diminue en conséquence. De même, il y a une augmentation des concentrations de CO, CO2 et H2O. Pour ce processus adiabatique, il y a une quantité importante de CO à des niveaux plus élevés d'O2 dans l'oxydant.
Les produits radicalaires H, O et OH augmentent tous avec l'O2 dans l'oxydant. Le NO (oxyde nitrique) augmente initialement puis diminue après environ 60 % d'O2 dans l'oxydant à mesure que davantage de N2 est retiré du système. Lorsque le comburant est de l'O2 pur, il n'y a pas de formation de NO puisqu'il n'y a pas de N2 disponible. Le combustible non brûlé sous forme de H2 et le comburant n'ayant pas réagi sous forme de O2 augmentent également avec la concentration en O2 dans le comburant. Cette augmentation des concentrations de radicaux, du carburant non brûlé sous forme de CO et de H2, et de l'O2 n'ayant pas réagi sont toutes dues à une dissociation chimique qui se produit à des températures élevées.
La température de flamme réelle est inférieure à la température de flamme d'équilibre adiabatique en raison de la combustion imparfaite et du rayonnement de la flamme. La température réelle de la flamme est déterminée par la façon dont la flamme rayonne sa chaleur et la façon dont le système de combustion, y compris la charge du four et les parois réfractaires, absorbe ce rayonnement.
Une flamme très lumineuse a généralement une température de flamme inférieure à celle d'une flamme très non lumineuse. La température réelle de la flamme est également plus faible lorsque la charge du four et les parois absorbent mieux le rayonnement. Cela se produit lorsque la charge et les parois du four sont à des températures plus basses et ont des absorptivités radiantes plus élevées.
Lorsque les produits de combustion gazeux quittent la flamme, ils perdent généralement plus de chaleur par convection et rayonnement lorsqu'ils traversent la chambre de combustion. L'objectif d'un procédé de combustion est de transférer l'énergie chimique contenue dans le combustible vers la charge du four, ou dans certains cas vers la chambre de combustion. Plus le processus de combustion est thermiquement efficace, plus la chaleur est transférée des produits de combustion à la charge du four et à la chambre de combustion. Par conséquent, la température du gaz dans la cheminée d'échappement est de manière souhaitable bien inférieure à celle dans la flamme dans un processus de chauffage thermiquement efficace. La composition des produits de combustion change alors avec la température des gaz.
Rapport de mélange – Les concentrations en O2 et N2 dans les gaz d'échappement décroissent strictement avec le rapport d'équivalence. Les concentrations de H2O et de CO2 culminent dans des conditions stoechiométriques. Ceci est important car ces deux gaz produisent un rayonnement gazeux non lumineux. Les combustibles imbrûlés sous forme de H2 et de CO augmentent tous deux avec le rapport d'équivalence. Cela se reflète dans la chaleur disponible car tout le carburant n'est pas entièrement brûlé.
Température de préchauffage de l'air et du carburant – Dans de nombreux procédés de combustion industriels, la chaleur est récupérée pour améliorer l'efficacité thermique globale du procédé afin de réduire les coûts d'exploitation. La chaleur récupérée est normalement utilisée pour préchauffer l'air de combustion entrant et est parfois utilisée pour préchauffer le combustible entrant. Le préchauffage de l'air ou du combustible affecte la composition des produits de combustion. CO2, H2O et N2, tous diminuant dans les gaz d'échappement avec le préchauffage de l'air, en raison de la dissociation chimique. En raison de considérations de sécurité et de la possibilité d'encrassement de la tuyauterie d'alimentation en carburant, des températures de préchauffage du carburant plus élevées ne sont pas pratiques ou recommandées dans la plupart des conditions. On constate généralement qu'il n'y a qu'une légère diminution des concentrations des composants majeurs et une légère augmentation des concentrations des composants mineurs des gaz d'échappement. Ceci est dû au fait que la masse de carburant est relativement faible par rapport à la masse d'air de combustion fournie au système de combustion. Cela signifie que le préchauffage de l'air de combustion a un impact beaucoup plus important que le préchauffage du combustible pour une température de préchauffage donnée.
Composition du carburant – Les produits de combustion dépendent de la composition du combustible. Les compositions de produits de combustion prédites pour différents combustibles dans diverses conditions de fonctionnement peuvent être calculées. Les combustibles gazeux les plus couramment utilisés sont H2 (hydrogène), CH4, C3H8 (propane) et des mélanges de H2 et CH4. Celles-ci sont destinées à être représentatives des carburants normalement utilisés dans les applications industrielles. En termes de luminosité, H2 produit des flammes non lumineuses, CH4 produit des flammes à faible luminosité et C3H8 produit des flammes à luminosité plus élevée.
Température de la flamme – La température de la flamme est une variable critique pour déterminer le transfert de chaleur de la flamme à la charge du four. La température de flamme adiabatique est affectée par les compositions de comburant et de combustible, le rapport de mélange et les températures de préchauffage de l'air et du combustible. Cependant, les températures de flamme réelles ne sont pas aussi élevées que la température de flamme adiabatique, mais les tendances sont comparables et représentatives des conditions réelles.
Comburant et composition du carburant – La température de la flamme augmente considérablement lorsque l'air est remplacé par de l'O2 car le N2 agit comme un diluant qui réduit la température de la flamme. La température de la flamme varie normalement pour l'air et l'O2 pur. Il y a une augmentation rapide de la température de la flamme depuis l'air jusqu'à environ 60 % d'O2 dans le comburant. La température de la flamme augmente à un rythme plus lent pour des concentrations d'O2 plus élevées. De plus, la composition du combustible a un fort impact sur la température de la flamme. Dans un mélange de carburant de H2 et CH4, la température augmente à mesure que la teneur en H2 dans le mélange augmente. Il est important de noter que l'augmentation n'est pas linéaire, avec une augmentation plus rapide à des niveaux plus élevés de H2. En raison du coût relativement élevé du H2 par rapport au CH4 et au C3H8, il n'est pas utilisé dans de nombreuses applications industrielles. Cependant, les carburants à haute teneur en H2 sont souvent utilisés dans de nombreuses applications d'hydrocarbures. Ces carburants sont des sous-produits du processus de fabrication chimique et donc beaucoup moins chers que l'achat de H2 auprès d'un fournisseur de gaz industriel et plus rentables que l'utilisation d'autres carburants achetés.
Rapport de mélange – Les températures maximales de la flamme se produisent dans des conditions stoechiométriques. Plus la concentration d'O2 dans le comburant est faible, plus la température de la flamme est réduite en fonctionnant dans des conditions non stœchiométriques (soit riche en carburant, soit pauvre en carburant). Cela est dû à la concentration plus élevée de N2, qui absorbe la chaleur et abaisse la température globale. Dans des conditions stoechiométriques, il y a juste assez d'oxydant pour brûler complètement tout le carburant. Tout oxydant supplémentaire absorbe l'énergie sensible de la flamme et réduit la température de la flamme. Dans la plupart des flammes réelles, la température maximale de la flamme se produit souvent dans des conditions légèrement pauvres en combustible. Cela est dû au mélange imparfait où un peu plus d'O2 est nécessaire pour brûler complètement tout le carburant. Presque toutes les applications de combustion industrielle fonctionnent dans des conditions pauvres en carburant pour garantir que les émissions de CO sont faibles. Par conséquent, selon la conception réelle du brûleur, la température de la flamme peut être proche de son maximum, ce qui est souvent souhaitable pour maximiser le transfert de chaleur. Un problème fréquemment rencontré lors de la maximisation de la température de la flamme est que les émissions de NOx (oxydes de N2) sont également maximisées puisque les NOx augmentent approximativement de façon exponentielle avec la température des gaz. Cela a conduit à de nombreux concepts de conception pour réduire la température de flamme maximale dans la flamme afin de minimiser les émissions de NOx. Cela affecte également le transfert de chaleur de la flamme.
Température de préchauffage du comburant et du carburant – La température de flamme adiabatique est variable et fonction de la température de préchauffage du comburant pour les flammes air/CH4 et O2/CH4. L'augmentation de la température de la flamme est relativement faible pour la flamme O2/CH4 car l'augmentation de la chaleur sensible de l'O2 ne représente qu'une fraction de l'énergie chimique contenue dans le combustible. Pour les flammes air/CH4, le préchauffage de l'air a un impact plus important car l'augmentation de la chaleur sensible est très importante du fait de la masse d'air importante dans la réaction de combustion. La température de la flamme adiabatique augmente rapidement pour les flammes air/combustible dans de nombreux combustibles.
Chaleur disponible – La chaleur disponible dans le système de combustion du four est importante dans la détermination de l'efficacité thermique globale et est donc un facteur lors du calcul du transfert de chaleur dans le processus. Il est moins efficace d'essayer de maximiser le transfert de chaleur dans le système qui a par nature une faible chaleur disponible. La chaleur disponible est définie comme la valeur calorifique brute du combustible, moins l'énergie dégagée du processus de combustion par les gaz d'échappement chauds.
La chaleur brute disponible (GAH) dans le four est donnée par l'équation GAH =pouvoir calorifique du combustible + chaleur sensible des réactifs - chaleur transportée par le POC sortant du four. GAH représente la chaleur disponible à la température critique du procédé. Il ne représente pas la chaleur disponible pour remplir une fonction donnée en raison des différents types de pertes. Il peut être utilisé comme critère pour comparer différents systèmes de combustion de carburant.
En outre, dans un four, il y a des pertes de chaleur qui sont régies par la température critique du procédé, l'épaisseur du revêtement réfractaire et la conductivité thermique du réfractaire. Par conséquent, la chaleur nette disponible (NAH) dans le four est donnée par l'équation NAH =GAH − pertes de chaleur. NAH peut être utilisé comme critère pour comparer l'efficacité de fusion/fusion/chauffage de différents fours.
La chaleur perdue du procédé par les ouvertures du four, à travers les parois du four ou par l'infiltration d'air n'est pas prise en compte dans le calcul de la chaleur disponible théorique car celle-ci dépend du procédé. La chaleur disponible théorique doit être proportionnelle à la quantité d'énergie réellement absorbée par la charge du four dans un processus réel, qui est directement liée à l'efficacité thermique du système. Par conséquent, la chaleur disponible théorique est généralement utilisée pour montrer les tendances de l'efficacité thermique en fonction de la température des gaz d'échappement, des compositions de comburant et de carburant, du rapport de mélange et des températures de préchauffage de l'air et du carburant.
La chaleur disponible varie en fonction de la température des gaz d'échappement et diminue rapidement avec la température des gaz d'échappement et est relativement indépendante de la composition du carburant. Par conséquent, pour maximiser l'efficacité thermique du procédé, il est souhaitable de minimiser la température des gaz d'échappement. Cela se fait généralement en maximisant le transfert de chaleur des gaz d'échappement vers la charge du four (et les parois du four) et en récupérant une partie de la chaleur dans les gaz d'échappement en préchauffant le comburant et/ou le combustible.
Lorsque la température des gaz d'échappement augmente, plus d'énergie est évacuée du système de combustion et il en reste moins dans le système. La chaleur disponible diminue jusqu'à zéro à la température de flamme d'équilibre adiabatique où aucune chaleur n'est perdue par les gaz. La chaleur disponible d'un système de combustion CH4/O2 même à la température des gaz d'échappement d'environ 2000 degrés C, la chaleur disponible est toujours de 57 %. De plus, il n'est généralement pas très économique d'utiliser des systèmes CH4/air pour les processus de chauffage et de fusion à haute température. À une température d'échappement d'environ 1300 °C, la chaleur disponible pour le système CH4/air n'est que d'un peu plus de 30 %. La récupération de chaleur sous forme d'air préchauffé est généralement utilisée pour les processus de chauffage à haute température afin d'augmenter l'efficacité thermique du four.
Lorsque la température des gaz d'échappement augmente, la chaleur disponible diminue car plus d'énergie est transportée avec les gaz d'échappement. Il y a une augmentation initiale rapide de la chaleur disponible lorsque la concentration d'O2 dans le comburant augmente par rapport aux 21 % trouvés dans l'air. C'est l'une des raisons pour lesquelles l'enrichissement en O2 est une technique populaire puisque l'augmentation progressive de l'efficacité est très importante. L'efficacité thermique du système CH4/air est deux fois supérieure lorsque l'air est préchauffé à environ 1 100 deg C.
Pour le système CH4/O2, l'augmentation de l'efficacité est beaucoup moins spectaculaire en préchauffant l'O2. En effet, le rendement initial sans préchauffage est déjà de 70 % et la masse d'O2 n'est pas aussi importante dans la réaction de combustion par rapport à la masse d'air dans un système air/carburant. Il existe également des craintes pour la sécurité lors de l'écoulement d'O2 chaud dans un pipeline, un équipement de récupération de chaleur et un brûleur. Les économies de carburant pour une technologie donnée peuvent être calculées à l'aide des courbes de chaleur disponibles.
Volume de gaz d'échappement – Le débit de gaz à travers une chambre de combustion de four est proportionnel au transfert de chaleur par convection vers la charge du four. Plusieurs facteurs influencent ce débit. L'un est la température du gaz, car les gaz à température plus élevée ont des débits réels plus élevés (mètres cubes par heure) en raison de la dilatation thermique des gaz. Cela signifie que le préchauffage du combustible ou du comburant, qui tous deux augmentent normalement la température de la flamme, produit des débits réels plus élevés. Cependant, le débit des gaz est le même lorsqu'il est corrigé aux conditions de température et de pression standard (STP).
Un autre facteur qui a une très forte influence sur le débit de gaz à travers le système de combustion est la composition du comburant. La combustion assistée par O2 consiste essentiellement à éliminer le N2 de l'oxydant. Un changement majeur par rapport à la combustion air/combustible est la réduction du volume des fumées. Cela signifie que pour chaque unité de volume de carburant, 3 volumes normalisés de gaz sont produits pour la combustion O2/carburant contre 10,5 volumes pour la combustion air/carburant. Cette réduction peut avoir des effets à la fois positifs et négatifs, mais l'effet sur le transfert de chaleur par convection est une réduction de la vitesse moyenne du gaz à travers une chambre de four et une réduction résultante du transfert de chaleur par convection vers la charge du four.
Propriétés de transport des gaz d'échappement
Les propriétés de transport des composants gazeux dans la chambre du four sont importantes pour déterminer le transfert de chaleur et la dynamique des fluides. Les propriétés dépendent fortement de la température et des composants du gaz. Les propriétés importantes des gaz pour le transfert de chaleur dans les chambres de fours industriels varient en fonction de la composition du combustible et de l'oxydant, du rapport de mélange et des températures de préchauffage de l'air. La variation de propriété en fonction de la température de préchauffage du combustible a un effet minime. La composition et la température du gaz sont nécessaires pour calculer le rayonnement gazeux non lumineux. Les propriétés de transport du gaz sont nécessaires pour calculer le coefficient de transfert de chaleur par convection, qui est souvent donné sous la forme nombre de Nusselt (Nu). Nu est calculé à partir du nombre de Prandtl (Pr) et du nombre de Reynolds (Re). Le coefficient de transfert de chaleur par convection ‘h’ est ensuite calculé à partir du nombre de Nusselt en utilisant Nu =hd/k où d est une dimension caractéristique pour le système d'écoulement et k est la conductivité thermique du fluide. Les propriétés du gaz sont nécessaires pour calculer les nombres Nu, Pr et Re sont données ci-dessous.
Densité – La densité du gaz peut être utilisée pour calculer le nombre Re, qui est généralement nécessaire pour calculer le coefficient de transfert de chaleur par convection. La densité est également utilisée pour calculer la vitesse moyenne du gaz à travers la chambre du four, qui est également normalement nécessaire pour calculer le coefficient de convection. La densité du gaz est inversement proportionnelle à la température du gaz de sorte que lorsque la température augmente, la densité diminue. La réduction de la densité du gaz est à peu près proportionnelle à l'inverse de la température absolue du gaz. De plus, la densité du gaz diminue rapidement à mesure que la teneur en O2 dans le comburant augmente. Cela est dû à l'augmentation des températures de flamme. Une densité de gaz inférieure signifie un nombre Re inférieur et donc un transfert de chaleur convectif réduit, si toutes les autres variables restent les mêmes. Cependant, le débit massique des gaz diminue également. Par conséquent, la vitesse moyenne du gaz n'est pas affectée de manière significative en raison de l'effet combiné d'une densité et d'un débit massique inférieurs, de sorte que l'impact sur la convection dû à la vitesse du gaz est minime.
La densité de gaz atteint un minimum à des rapports d'équivalence intermédiaires. Ceci peut à nouveau être attribué à la température de flamme à l'équilibre adiabatique. De plus, la densité de gaz diminue presque linéairement à mesure que la température de préchauffage de l'air augmente, ce qui est inversement corrélé aux courbes de température de flamme. Aussi, la densité de gaz ne décroît pas linéairement en fonction de la composition du mélange gazeux, comme on s'y attend généralement instinctivement. Encore une fois, la densité correspond à l'inverse des températures de flamme adiabatique.
Chaleur spécifique – La chaleur spécifique du gaz, parfois appelée capacité calorifique du gaz, est une autre propriété de transport qui a un impact sur le transfert de chaleur par convection dans le système de four. Il est utilisé pour calculer le nombre Pr, qui est souvent utilisé pour calculer le coefficient de transfert de chaleur par convection. Il y a une augmentation non linéaire de la chaleur spécifique du gaz par rapport à la température du produit d'échappement. La chaleur spécifique augmente plus rapidement à des températures plus élevées. De plus, la chaleur spécifique des gaz d'échappement augmente presque linéairement à mesure que le pourcentage d'O2 dans le comburant augmente. Toutes choses étant égales par ailleurs, cela améliore le transfert de chaleur par convection des gaz de combustion vers la charge du four.
Cependant, il existe une relation beaucoup plus compliquée entre la chaleur spécifique et le rapport d'équivalence, y compris une forte dépendance au carburant. Tous les combustibles montrent une augmentation initiale de la chaleur spécifique à mesure que le rapport d'équivalence augmente, atteignant un maximum local dans des conditions stoechiométriques. Au-delà des conditions stoechiométriques, la chaleur spécifique décroît alors, plafonne, puis augmente à nouveau. Dans le cas du CH4, la chaleur spécifique augmente très rapidement aux hautes valeurs d'équivalence. Bien que la relation entre la chaleur spécifique et le rapport d'équivalence soit assez compliquée, la réalité est que la plupart des processus de combustion industriels fonctionnent dans des conditions légèrement pauvres en combustible où il existe une relation forte mais plus linéaire entre le rapport d'équivalence et la chaleur spécifique. Dans le cas des mélanges de carburant H2/CH4, la chaleur spécifique augmente rapidement à des teneurs élevées en H2 dans le mélange de carburant. La température de la flamme montre une relation très similaire à la teneur en H2 dans le mélange.
Conduction thermique – Comme la chaleur spécifique, la conductivité thermique du gaz affecte le nombre Pr, qui à son tour affecte le coefficient de transfert de chaleur par convection. Dans ce cas, il existe une relation inverse entre la conductivité thermique et le nombre Pr. Lorsque la conductivité thermique augmente (diminue), le nombre Pr diminue (augmente) avec le coefficient de convection, en supposant que toutes les autres variables restent constantes. La conductivité thermique d'un gaz dépend approximativement de la racine carrée de la température absolue. Une augmentation non linéaire similaire de la conductivité thermique se produit avec la température du gaz comme pour la chaleur spécifique.
De plus, la conductivité thermique augmente rapidement à mesure que la teneur en 02 dans l'oxydant augmente. La relation est presque linéaire bien qu'il y ait une augmentation plus rapide à des teneurs en O2 plus faibles par rapport à celle à une teneur en O2 plus élevée dans l'oxydant. Cependant, il existe une relation compliquée entre une propriété de transport et le rapport d'équivalence. Il y a un maximum local aux conditions stoechiométriques. Pour H2, le maximum local est également le maximum global pour une large gamme de rapports d'équivalence. Pour le CH4, il y a une augmentation rapide de la conductivité thermique dans des conditions très riches en combustible (rapports d'équivalence élevés), la conductivité dépassant la valeur maximale locale dans des conditions stoechiométriques. Bien que moins dramatique, il existe un phénomène similaire pour le C3H8. Bien que la plupart des processus industriels soient exécutés dans des conditions légèrement pauvres en carburant, il existe toujours un changement rapide de la conductivité thermique du côté pauvre en carburant des conditions stoechiométriques.
Une relation beaucoup plus simple existe entre la conductivité et la température de préchauffage de l'air de combustion. La conductivité augmente légèrement plus vite que linéairement à mesure que la température de préchauffage augmente. De plus, la conductivité thermique augmente beaucoup plus rapidement à mesure que la teneur en H2 dans le mélange de carburant H2/CH4 augmente.
Viscosity – The absolute or dynamic viscosity is a measure of momentum diffusion. Gas viscosity is having a similar relationship to the thermal conductivity. The viscosity is important in calculating both the Pr and Re numbers, but in opposite ways. As the gas viscosity increases (decreases), the Pr number increases (decreases) and the Re number decreases (increases) assuming that all the other variables are constant. The kinematic viscosity is related to the dynamic viscosity.
There is a nearly linear increase in gas viscosity with the exhaust product temperature. The gas viscosity increases as the O2 content in the oxidizer increases, similar to the adiabatic flame temperature. The gas viscosity peaks at an equivalence ratio of 1.0 (stoichiometric conditions) and declines as the mixture becomes either more fuel rich or more fuel lean. The gas viscosity also increases with the air preheat temperature, comparable to the flame temperature. The viscosity increases as the H2 content increases in an H2/CH4 fuel blend. The increase in the viscosity is more rapid at higher H2 contents.
Pr number – The Pr number is frequently used to calculate the convection heat transfer coefficient. The components of Pr include the specific heat, viscosity, and thermal conductivity. The combination of these variables which forms the Pr number changes as functions of the fuel and oxidizer compositions, the mixing ratio, and the air preheat temperature. However, there is little change in Pr number as a function of the fuel preheat-temperature. The Pr number decreases as a function of temperature, but in a non-uniform way. Initially, it decreases moderately quickly, then decreases more slowly, and finally decreases rapidly at higher temperatures.
There is also a highly nonlinear relationship between the Pr number and the oxidizer composition. For CH4 and C3H8, the Pr number decreases rapidly at first and then levels off at higher O2 contents. For H2, the Pr number actually has a minimum at around 50 % O2 content. Also, a highly nonlinear relationship exists between the Pr number and the equivalence ratio. Most of the fuels show local maximum and minimum. The Pr number also declines almost linearly with the air preheat temperature. The Pr number declines as the H2 content in an H2/CH4 fuel blend decreases, and decreases rapidly at high H2 contents.
Lewis number – The Lewis number (Le) is the ratio of the thermal diffusivity to the molecular (mass) diffusivity. The Le number is important for the heat transfer in combustion systems. In general, for Le values greater than 1, there are some enhancements in convective heat transfer due to chemical recombination reactions. The Le number is 1 for temperatures below 1200 deg C, depending on the fuel, and then rises fairly rapidly at higher temperatures. The Le number is greater than one for all oxidizer compositions under adiabatic equilibrium conditions, which equates to the highest flame temperature possible for those conditions. The values of Le number peaks at intermediate oxidizer compositions and declines at higher O2 contents. There is a dramatic peak in the Le number at stoichiometric conditions, with the Le number going below 1.0 at higher equivalence ratios. The Le number increases almost linearly with the air preheat temperature for adiabatic equilibrium conditions. It increases more rapidly as the H2 content in a fuel blend of H2/CH4 increases.
Heat transfer in a furnace
Factors affecting the heat transfer in a furnace to the furnace charge are described below.
Flow of heat within the furnace charge – In case of an electrically heated furnace charge where the charge is used as a resistance in a circuit or by induction heating, the flux lines concentrate just inside the surface. In a fuel-fired heating process, heat enters the charge through its surface (by radiation or by convection) and diffuses throughout the charge by conduction. This heat flow requires a difference in temperature within the charge. Steady heat flows through a flat furnace charge. For other than flat charge, heat flux lines are seldom parallel and rarely steady. In transient heat flow, determination of the temperature at a given time and point within the charge necessitates use of the finite element method. Increasing the furnace temperature (a high ‘thermal head’) or ‘high-speed heating’ often results in non-uniform heating, which necessitates a longer soak time, sometimes defeating the purpose of high-speed heating.
Thermal conductivity and diffusion – There is normally wide variation in thermal conductivities of various metals, which has a direct bearing on the ability of heat to flow through or diffuse throughout them, and hence has a very strong effect on temperature distribution or uniformity in solids. The factor which affects temperature distribution is the thermal diffusivity. It is thermal conductivity divided by the volume specific heat of the solid material and is represented by the equation thermal diffusivity =thermal conductivity/ (specific heat x density). In this equation, the numerator is a measure of the rate of heat flow into a unit volume of the material while the denominator is a measure of the amount of heat absorbed by that unit volume. With a higher ratio of numerator to denominator, heat gets conducted into, distributed through, and absorbed.
Thermal conductivities and diffusivities of solids vary greatly with temperature. Specific heats and densities vary little, except for steels at their phase transition point. The thermal conductivities of solid pure metals drop with increasing temperature, but the conductivities of solid alloys generally rise with temperature.
Lag time – The effect of thermal conductivity on heat flow and internal temperature distribution is shown in Fig 1 for three same-size slabs of ferrous alloys heated from two sides. The surface temperatures in all the three cases generally rise very quickly, but the interior temperatures of rise differentially because of their poorer diffusivities. The slabs take different time to come to the equilibrium condition with the furnace temperature.
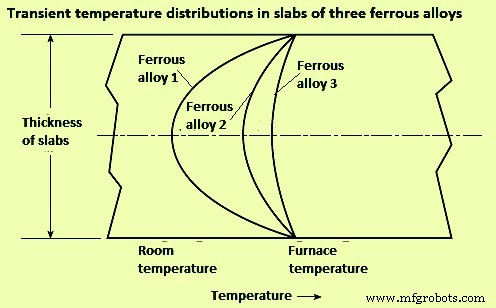
Fig 1 Effect of thermal conductivity on heat flow and internal temperature distribution
Solid materials which are heated in industrial furnaces are not necessarily continuous. Many times, the charge consists of coiled strip material or separate pieces piled to various depths or close side by side. In such cases, heat only can flow from one piece to the adjacent piece through small contact points on their surfaces, or through gas filled spaces, the thermal conductivity of which is very small. A stack of flat plates is an example of very low conductance. Even very small gaps constitute a big thermal resistance than solid metal. A stack cannot be treated as a solid, since thin air spaces are insulators. The differing air gaps in a stack result in bad non-uniformities in temperatures.
Rapid heat flow in each piece of a piled charge is obtained only by circulation of hot gases through the piled material by convection and gas radiation. These gas masses are to be constantly replaced with new hot gas since they have low mass, low specific heat, and thin gas beam thickness, so they cool quickly without delivering much heat to the loads. For uniform heating and precise reproducibility, piling of pieces of materials are to be avoided.
Heat transfer to the surface of the furnace charge – In furnace practice, heat is transferred by three modes namely (i) conduction, (ii) convection, and (iii) radiation. There are some essentials of heat transfer which are helpful to designers and operators of industrial furnaces. Most industrial furnaces, ovens, kilns, incinerators, boilers, and heaters use combustion of fuels as their heat source. Combustion, as used in industrial furnaces, comes from rapid and large chemical reaction kinetics and this result into conversion of chemical energy to sensible heat (thermal) energy. Increasing fuel and oxidizer (usually air) mixing surface area or increasing temperature of the reactants can cause faster combustion reactions, usually resulting in higher heat source temperatures. Fuel oxidation reactions are exothermic, so they can develop into a runaway condition (e.g. thermal energy being released faster than it can be carried away by heat transfer). This positive feedback can cause an explosion.
A flame is a thin region of rapid exothermic chemical reaction. An example is a Bunsen burner flame. In a Bunsen burner, a thoroughly premixed laminar stream of fuel gas and air is ignited by an external heat source, and a cone-shaped reaction zone (flame front) forms. Turbulence increases the thickness and surface area of the reaction zone, resulting in higher burning velocity. Laminar burning velocity for natural gas is around 18 metres per minute (mpm) while the turbulent burning velocity can be two to ten times faster. In a laminar flame, thermal expansion from chemical heat release can combine with increased reactivity caused by higher temperatures, resulting in acceleration to a turbulent flame. Except for long luminous flames, most industrial flames are turbulent.
Conduction heat transfer – Conduction heat transfer is molecule-to-molecule transfer of vibrating energy, usually within solids. Heat transfer solely by conduction to the charged load is rare in industrial furnaces. It occurs when cold metal is laid on a hot hearth. It also occurs, for a short time, when a piece of metal is submerged in a salt bath or a bath of liquid metal.
If two pieces of solid material are in thorough contact (not separated by a layer of scale, air, or other fluid), the contacting surfaces instantly assume an identical temperature somewhere between the temperatures of the contacting bodies. The temperature gradients within the contacting materials are inversely proportional to their conductivities (Fig 2).
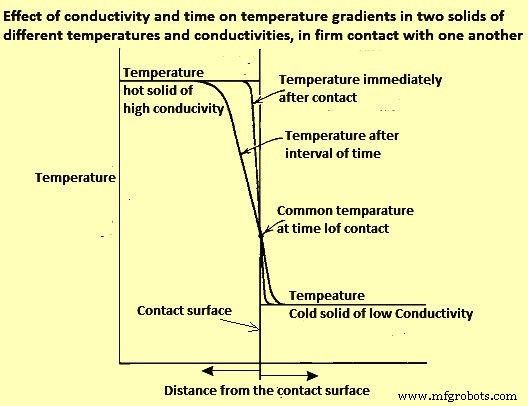
Fig 2 Effect of conductivity and time on temperature gradients in two solids of different temperatures and conductivities, in firm contact with one another
The heat flux (rate of heat flow per unit area) depends not only on the temperatures of the two solids but also on the diffusivities and configurations of the contacting solids. In practice, comparatively little heat is transferred to (or abstracted from) a charge by conduction, except in the flow of heat from a billet to water-cooled skids.
When a piece of cold metal is suddenly immersed in liquid salt, lead, zinc, or any other liquid metal, the liquid freezes on the surface of the cold metal, and heat is transferred by conduction only. After a very short time, the solid jacket, or frozen layer, remelts. From that time on, heat is transferred by conduction and convection.
Convection heat transfer
Convection heat transfer is a combination of conduction and fluid motion, physically carrying heated (or cooled) molecules to another surface. If a stream of gaseous fluid flows parallel to the surface of the solid, the vibrating molecules of the stream transfer some thermal energy to or from the solid surface.
A ‘boundary layer’ of stagnant, viscous, poorly conducting fluid tends to cling to the solid surface and acts as an insulating blanket, reducing heat flow. Heat is transferred through the stagnant layers by conduction. If the main stream fluid velocity is increased, it scrubs the insulating boundary layer thinner, increasing the convection heat transfer rate. The conductance of the boundary layer (film coefficient) is a function of mass velocity (momentum, Re number).
In furnaces which operate below 600 deg C, heat transfer by convection is of major importance since radiation is weak there. Modern high-velocity (high-momentum) burners give high convection heat transfer coefficients. High velocities often provide more uniform temperature distribution around a single piece charge, or among multiple piece charges, since more mass flow carries additional sensible heat at more moderate temperatures. At low furnace temperatures, high rates of total heat transfer can be obtained only by high gas velocities since heat transfer by radiation at around 550 deg C is less than one-tenth of what it is at around 1200 deg C. High-velocity (high momentum) burners are widely used to fill in where radiation cannot reach because of shadow problems.
Radiation heat transfer
Radiation between solids – Heat is radiated by solids even at low temperatures. The net radiant heat actually transferred to a receiver is the difference between radiant heat received from a source and the radiant heat re-emitted from the receiver to the source. The net radiant heat flux between a hot body (heat source) and a cooler body (heat receiver) can be calculated by Stefan-Boltzmann equations.
Emissivity and absorptivity of materials are important properties for radiation between solids. Emissivity is the radiant heat emitted (radiated) by a surface, expressed as a decimal of the highest possible (black body) heat emission in a unit time and from a unit area. Emittance is the apparent emissivity of the same material for a unit area of apparent surface which is actually much greater, due to roughness, grooving, and so on. Absorptivity is the radiant heat absorbed by a surface per unit time and unit area, expressed as a decimal of the most possible (black body) heat absorption.
Engineers use emissivity value of 0. 85 in conventional refractory lined furnaces. However, the temperature, surface condition, and alloy can make considerable difference. As an example, if stainless-steel strip is heated in less than three minutes in a catenary furnace, the emissivity may not change even though the temperature increases from ambient to 1100 deg C. By measuring both strip surface temperature and furnace temperature, it has been possible to revise heating curve calculations, assuming that oxidation has not changed the emissivity or absorptivity during the heating cycle.
Radiation from clear flames and gases – There are two origins of radiation from the products of combustion to solids. The two origins of radiation are (i) from clear flame and from gases, and (ii) from the micron-sized soot particles in luminous flame. Radiation from clear gas does not follow the Stefan-Boltzmann fourth-power law. The only clear gases which emit or absorb radiation appreciably are those having three or more atoms per molecule (triatomic gases) such as CO2, H2O, and SO2 (sulphur di-oxide). An exception is diatomic CO, which gives off less radiation. The other diatomic gases, such as O2, N2 (and their mixture, air), and H2 have only negligible radiating power.
Gaseous radiation does not follow the fourth-power law since gases do not radiate in all wavelengths, as do solids (gray bodies). Each gas radiates only in a few narrow bands. Radiation from clear gases depends on their temperature, on the partial pressure or percent volume of each triatomic gas present, and on the thickness of their gas layer.
The temperature of a radiating gas gets lower in the direction of gas travel. To maintain active gas radiation, the gas is to be continually replaced by new hot gas, which also improves convection. Higher gas feed velocities reduce the temperature drop along the gas path. This factor is very critical in maintaining good temperature uniformity in high temperature industrial furnaces.
The furnaces are often designed on the basis of refractory radiation heating the charge, with usually reasonable results, but some situations cannot be explained by refractory radiation alone. Direct radiation from furnace gases generally delivers 62 % (+/- 2 %) of the heat to the charge, and refractories transfer the remaining 38 % (+/- 2 %). Gas temperatures needed to transfer the heat to refractory and charge are generally much higher than generally assumed.
Radiation from luminous flames – If a fuel-rich portion of an air/fuel mixture is exposed to heat, as from a hotter part of the flame, the unburned fuel molecules polymerize or suffer thermal cracking, resulting in formation of some heavy, solid molecules. These soot particles glow when hot, providing luminosity, which boosts the flame’s total radiating ability.
If fuel and air are not thoroughly mixed promptly after they leave the burner nozzle, they can be heated to a temperature at which the hydrocarbons crack (polymerize). Further heating brings the resulting particles to a glowing temperature. As O2 mixes with them, they burn. As the flame proceeds, formation of new soot particles can equal the rate of combustion of previously formed particles. Farther along the flame length, soot production diminishes, and all remaining soot is incinerated. This series of delayed-mixing combustion processes are to be completed before the combustion gases pass into the flue. If the flame is still luminous at the flue entry, smoke can appear at the stack exit. Smoke is soot that has been cooled (chilled, quenched) below its minimum ignition temperature before being mixed with adequate air.
The added radiating capability of luminous flames causes them to naturally cool themselves faster than clear flames. This is performing their purpose—delivering heat. The cooling phenomenon can negate some of the gain from the higher luminosity (effective emissivity).
Luminous flames often have been chosen because the added length of the delayed mixing luminous flames can produce a more even temperature distribution throughout large combustion chambers. As industrial furnaces are supplied with very high combustion air preheat or more oxy-fuel firing, luminous flames can enable increases in heat release rates.
Fuels with high C/H2 ratios (most oils and solid fuels) are more likely to burn with luminous flames. Fuels with low C/H2 ratios (mostly gaseous fuels) can be made to burn with luminous flames namely (i) by delayed mixing, injecting equally low-velocity air and gas streams side-by-side, and (ii) by using high pressure to ‘shoot’ a high-velocity core of fuel through slower moving air so that the bulk of the air cannot ‘catch up’ with the fuel until after the fuel has been heated (and polymerized) by the thin ‘sleeve’ of flame annular interface between the two streams.
Flames from solid fuels can contain ash particles, which can glow, adding to the flame’s luminosity. With liquid and gaseous fuels, flame luminosity usually comes from glowing C and soot particles. The effective flame emissivity, as measured is usually between that of the POC gases and a maximum value of 0.95, depending on the total surface area of solid particles. Normally, heat transfer from a luminous flame is greater than that from a clear flame having the same temperature. The difference in the rate of heat transfer is quite noticeable in furnaces for reheating steel and metals. The difference becomes more pronounced at high temperature, where the radiating power of each triatomic gas molecule increases, but the gain is partially canceled by the decreasing density of radiating molecules per unit volume.
In another phenomenon, the bands of gaseous radiation hold their wavelengths regardless of temperature. At higher temperatures, however, the area of high intensity of solid radiation (glowing soot and C particles) moves toward shorter wavelengths (away from the gas bands). In higher temperature realms, radiation from clear gases does not increase as rapidly as radiation from luminous flames.
Flame radiation is a function of many variables such as C/H2 ratio of the fuel, air/fuel ratio, air and fuel temperatures, mixing and atomization of the fuel, and thickness of the flame. Some of these can change with distance from the burner. Fuels with higher C/H2 ratio, such as oils, tend to make more soot, so they usually create luminous flames, although blue flames are possible with light oils. Many gases have a low C/H2 ratio, and tend to burn clear or blue. It is difficult to burn tar without luminosity. It is equally difficult to produce a visible flame with blast furnace (BF) gas or with H2.
When comparing luminous and nonluminous flames, it is important to remember (i) soot radiation (luminous) usually ends where visible flame ends because soot is most often incinerated at the outer surface or skin of the flame, where it meets secondary or tertiary air, and (ii) gas radiation (nonluminous) occurs from both inside and outside the visible flame envelope, greatly increasing the uniformity and extent of its coverage, although gas radiation within the flame is somewhat shadowed by any surrounding soot particles or triatomic gases, and gas radiation outside the flame can be from cooler gases.
The effect of excess fuel on flame radiation is considerably greater than the effect of less excess air. The merits and demerits of clear flames versus long luminous flames have been debated for years. Modified burners and control schemes are helping to utilize the best of both. A problem common to several burner types is change of the flame characteristic as the burner input is turned down. Problems with some clear flame burners are (i) movement of the hump in the temperature profile closer to the burner wall as the firing rate is reduced, and (ii) at lower input rates, temperature falls off more steeply at greater distances from the burner wall (e.g., the temperature profile of a burner firing at 50 % of its rated capacity or below is at its peak temperature (maximum heat release at or near the burner wall, falling off further from the burner wall). At lower firing rates, the temperature drop off gets worse. At higher firing rates, the burner wall temperature decreases as the peak temperature moves away from it. In some steel reheating furnaces at maximum firing rate, the temperature difference between the burner wall and the peak can be 150 deg C.
The problem of a temperature peak at the far wall during high fire is aggravated by spur of furnace gases into the base of the flame, delaying mixing of fuel with O2. If the burner firing rate is increased, the spur of the products of complete combustion increases exponentially. Resulting problems are many. When side-firing a furnace at low firing rate, the peak temperature is at the burner wall, but at maximum firing rate, the peak temperature can be at the furnace centre or the opposite wall. Thus, the location of a single temperature control sensor is never correct. If the temperature sensor is in the burner wall, low firing rates have peak temperature hugging the furnace wall and driving the burner to low fire rate resulting into the rest of the furnace width receiving inadequate input. At high firing rates, a sensor in the burner wall is cool while the temperature away from the burner wall is very high, perhaps forming liquid scale on the surfaces of the charge pieces at the centre and/or far wall. To remedy this issue, inexperienced operators can lower the set point, reducing the furnace heating capacity.
Another example of the effect of the problem occurs with the bottom zone of a steel reheating furnace when fired longitudinally counter flow to the load movement, and with the control sensor installed 3 metre (m) to 6 m from the (end-fired) burner wall. At low-firing rates, with the zone temperature set at 1300 deg C, the burner wall can rise to higher than 1370 deg C. At that temperature, scale melts and drips to the floor of the bottom zone where it can later solidify as one big piece. At high firing rates, the peak temperature can move beyond the bottom zone T-sensor, possibly melting scale some distance toward the charge end of the furnace. Again, to avoid the problem, operators can lower temperature control settings, reducing the furnace capacity.
Control of the aforementioned problems requires an additional temperature sensor in each zone and a means for changing the mixing rate characteristic of the burner in response to the temperature measurements. Burners with adjustable spin (swirl) can be set to prevent much of the problem, especially if combined with a low-fire, forward-flow gas or air jet through the center of the burner. Such a jet is typically sized for 5 % of maximum gas or air flow.
Long, luminous flames, either laminar type or turbulent type, tend to have much less temperature hump and do not change length as rapidly when input is reduced. They can be great ‘levelers’, providing better temperature uniformity.
This information on in-flame soot radiation and triatomic gas radiation has been known for some time, but recent developments may be changing the picture. Use of oxy-fuel (100 % O2), both of which elevate flame turndown. The major gain from oxy-fuel firing is from more intense radiation heat transfer because of the higher concentration of triatomic gases, due to the elimination of N2 from the POC. This also decreases the mass of gas carrying heat out the flue (reducing stack loss). In another development, some lean premix gas flames (designed for low NOx emissions) make a ubiquitous flame field (seemingly transparent) through much of the chamber.
Processus de fabrication
- Four à induction et sidérurgie
- Génération et utilisation de gaz de haut fourneau
- Fours de réchauffage et leurs types
- Productivité des hauts fourneaux et paramètres d'influence
- Transfert de chaleur PCB
- Avantages et inconvénients d'une pompe à chaleur
- Traitement thermique de l'aluminium et des alliages d'aluminium
- Traitement thermique du cuivre et des alliages de cuivre
- Différence entre l'injection de carburant et le carburateur



