Nanofibres électrofilées de sulfate de chondroïtine/polycaprolactone/gélatine avec antithrombogénicité et affinité cellulaire endothéliale améliorée en tant qu'échafaudage potentiel pour l'ingénierie tissulaire des vaisseaux sanguins
Résumé
Les nanofibres polymères électrofilées ont attiré beaucoup d'attention dans l'ingénierie tissulaire des vaisseaux sanguins. Cependant, les matériaux conventionnels en nanofibres présentant les déficiences d'une endothélialisation lente et d'une thrombose ne sont pas efficaces pour favoriser la réparation et la régénération des tissus des vaisseaux sanguins. Ici, des nanofibres composites biomimétiques de gélatine (Gt)/polycaprolactone (PCL) incorporant une quantité différente de sulfate de chondroïtine (CS) ont été développées via la technologie d'électrofilage pour étudier leurs effets sur l'antithrombogénicité et l'affinité des cellules endothéliales. La variation des concentrations de CS dans les nanofibres de PG affecte la morphologie et le diamètre des fibres. Les nanofibres CS/Gt/PCL ont une porosité appropriée (~ 80%) et une absorption de solution PBS (jusqu'à 650%). L'introduction de CS dans les nanofibres Gt/PCL améliore considérablement leurs propriétés anticoagulantes, prolonge leur temps de coagulation et facilite les réponses cellulaires. En particulier, les nanofibres à 10 % CS/Gt/PCL présentent une fixation, un allongement et une prolifération cellulaires favorables. Ainsi, les nanofibres Gt/PCL contenant une certaine quantité de CS pourraient être d'excellents candidats en tant qu'échafaudage d'ingénierie tissulaire prometteur dans la réparation et la régénération des vaisseaux sanguins.
Introduction
Le développement de matériaux nanofibreux a suscité beaucoup d'attention en tant qu'échafaudages biomimétiques dans la réparation et la régénération des tissus en raison de leurs caractéristiques (bio)physicochimiques uniques, y compris leur structure de fibres ultrafines de type matrice extracellulaire (ECM), d'excellentes propriétés mécaniques, une grande surface spécifique et porosité élevée avec interconnectivité [1, 2]. Il a été démontré que les structures nanofibreuses jouent un rôle clé dans la médiation des réponses cellulaires, telles que l'adhésion cellulaire, la morphologie (p. ,4,5]. Alors que de nombreuses stratégies de nano-fabrication (p. , matériaux composites, etc.) à l'échelle industrielle [6,7,8].
En plus des signaux (bio)physiques, la sélection de biomatériaux appropriés peut affecter de manière significative les activités cellulaires ainsi que la réparation et la régénération des tissus [9]. Certaines caractéristiques clés, telles que la biocompatibilité, la biorésorbabilité, les propriétés mécaniques et la biofonction, doivent être prises en compte [9, 10]. Par rapport aux composites naturels/naturels et synthétiques/synthétiques, les matériaux composites en nanofibres constitués de polymères naturels et synthétiques ont reçu plus d'attention en raison de la combinaison des excellentes caractéristiques biologiques des polymères naturels et de la résistance mécanique des polymères synthétiques [9]. Parmi eux, la combinaison gélatine (Gt)/polycaprolactone (PCL) est l'un des systèmes hybrides naturels-synthétiques les plus représentatifs et est largement utilisé dans l'ingénierie des tissus vasculaires sanguins [11,12,13,14]. Cependant, les nanofibres composites Gt/PCL présentent encore certaines limites, telles qu'une endothélialisation lente et une thrombose. Récemment, le sulfate de chondroïtine (CS) est un polysaccharide sulfaté contenant du glycosaminoglycane et de la galactosamine, dont il a été démontré qu'il possède une forte adhérence aux cellules endothéliales (CE), une faible interaction avec les protéines et les plaquettes, ainsi qu'une répulsion électrostatique des composants sanguins chargés négativement [15 ,16,17]. De plus, le CS pourrait inhiber l'apoptose cellulaire et faciliter la cicatrisation des plaies vasculaires [18, 19]. Par conséquent, les nanofibres électrofilées Gt/PCL (PG) incorporant du CS seraient d'excellents candidats en tant qu'échafaudage d'ingénierie tissulaire bio-instructif pour la réparation et la régénération des vaisseaux sanguins.
Dans le présent travail, des nanofibres composites biomimétiques PG contenant différents ratios de CS ont été développées par électrofilage en une étape. La morphologie, la porosité des caractéristiques chimiques et la dégradation des nanofibres composites CS/PG ont été détectées par différentes techniques de caractérisation. L'anticoagulant des nanofibres composites PG/CS a été évalué. De plus, ces nanofibres composites avec différents ratios CS ont été ensemencées avec des cellules endothéliales aortiques humaines (HAEC) pour étudier leurs effets sur les réponses cellulaires.
Matériaux et méthodes
Matériaux
Le CS (trachée bovine, type A, pureté :95 %) a été fourni par Shanghai Macklin Biochemical Technology Co., Ltd. (Chine). Le PCL a été obtenu auprès d'Aladdin Biochemical Polytron Technologies Inc. (Chine). Le Gt (peau bovine, type B) a été obtenu auprès de Sigma-Aldrich Biochemical Technology Co., Ltd., (Chine). Le kit de temps de céphaline activée (APTT) a été acheté auprès de Leigen Biotechnology Co., Ltd (Chine). L'acide acétique (pureté :99,5 %) a été acheté auprès de Sinopharm Chemical Reagent Co., Ltd. (Chine). Les cellules endothéliales aortiques humaines (HAEC) ont été obtenues auprès de l'hôpital affilié de l'Université de Qingdao (Chine). Le milieu de culture Dulbecco's Modified Eagle Medium/Nutrient Mixture F-12 (DMEM/F-12), sérum bovin fœtal (FBS), 0,25% trypsine-EDTA ont été achetés auprès de Biological Industries (Israël). Tous les réactifs ont été achetés auprès de Sigma Aldrich (Chine) sauf indication contraire. L'eau utilisée dans toutes les expériences était désionisée.
Électrofilage de nanofibres
Le PCL (10 % p/v) a été dissous dans de l'acide acétique sous agitation mécanique à température ambiante pendant 4 h. Le Gt (10 % p/v) a été dissous dans de l'acide acétique à 90 % sous agitation constante pendant 2 h. Du CS à différentes concentrations a été ajouté à la solution de Gt et agité doucement à température ambiante pendant 1 h pour obtenir les solutions homogènes contenant 5, 10 et 15 % en poids de CS par rapport à la concentration totale en polymère. Ensuite, la solution de PG a été préparée en mélangeant les deux solutions ci-dessus dans un rapport pondéral de 50/50 (p/p) sous agitation pendant 2 h, nommées 5%CS@PG, 10%CS@PG et 15%CS@PG .
Les solutions homogènes préparées ont été soumises au processus d'électrofilage, équipées d'une seringue de 1 ml avec une aiguille de 21 G et d'un collecteur recouvert d'une feuille d'aluminium. Dans cette étude, la distance entre la plaque collectrice et la pointe de l'aiguille a été fixée à environ 18 cm, la tension a été fixée à 23 kV et les solutions polymériques ont été pompées à un débit de 1 mL/h. Toutes les solutions ont été électrofilées dans un instrument d'électrofilage (Technology, Tk602TH, Chine) à température ambiante et avec une humidité soigneusement contrôlée (< 40%). Avant toute autre expérience, les échantillons ont été placés dans une étuve de séchage sous vide pendant 72 h au moins pour éliminer tout solvant restant.
Microscopie électronique à balayage (MEB) et microscope électronique à transmission (MET)
La morphologie des échafaudages nanofibreux CS@PG a été étudiée par un SEM (VEGAS, TESCAN, tchèque) à une tension d'accélération de 20 kV à température ambiante. Le diamètre des nanofibres (n = 100) a en outre été mesurée à partir d'images SEM à l'aide d'un logiciel d'analyse d'images (Image J).
Les observations MET et les analyses par spectroscopie de rayons X à dispersion d'énergie (EDS) ont été réalisées à l'aide d'un JEOL JEM-2100 plus (Japon).
Spectroscopie infrarouge à transformée de Fourier (FTIR)
La FTIR a été réalisée par un spectromètre FTIR Nicolet iN10 (Thermo Fisher Scientific, Waltham, MA, USA) pour évaluer les groupes fonctionnels caractéristiques des nanofibres CS, PG et CS@PG. Les spectres d'échantillons ont été enregistrés avec le mode de transmission sur une plage de longueurs d'onde de 4000 à 500 cm −1 avec une résolution de 2 cm −1 .
Porosité et absorption de la solution saline tamponnée au phosphate (PBS)
La porosité des nanofibres a été réalisée par la méthode de déplacement de liquide. Premièrement, le poids sec des nanofibres a été pesé comme W1 . Ensuite, quatre groupes de nanofibres ont été immergés dans de l'éthanol pendant 2 h à 25 °C et pondérés en W2 . L'éthanol sur la surface de l'échantillon a été éliminé par du papier filtre, et les poids des échantillons ont ensuite été notés W3 . La porosité des nanofibres a été calculée par la formule suivante :
$${\text{Porosité}}\left( \% \right) =\left( {W_{3} - W_{1} } \right)/\left( {W_{3} - W_{2} } \droit) \fois 100$$Pour le test d'absorption en solution PBS, les nanofibres obtenues ont été pesées à l'état sec et enregistrées en Wd. Ensuite, les nanofibres ont été trempées dans du PBS pendant 24 h à 25 °C et le poids à l'état humide a été enregistré comme Ww après avoir éliminé l'excès de liquide sur la surface de l'échantillon. Le taux de gonflement peut être mesuré par l'équation suivante :
$${\text{PBS}}\;{\text{absorption}}\left( \% \right) =\left( {W_{{\text{W}}} - W_{{\text{d} }} } \right)/W_{{\text{d}}} \times 100$$Toutes les valeurs des expériences ci-dessus sont exprimées en moyenne ± SD (n = 3).
Comportement de dégradabilité in vitro
Pour déterminer la résistance des nanofibres obtenues au lysozyme, la dégradabilité des échantillons a été mesurée à un moment programmé (1, 4, 7, 10 et 14 jours). Le poids initial des nanofibres a été enregistré comme Wi . Ensuite, les échantillons ont été immergés dans une solution de PBS (pH 7,4) contenant du lysozyme (500 μg/mL) et incubés in vitro à 37 °C. Aux intervalles de dégradation prédéterminés, chaque groupe d'échantillons a été prélevé et lavé à l'eau déminéralisée, et lyophilisé pour obtenir le poids final (W f ). La solution de lysozyme a été changée trois fois par semaine. La masse restante (%) des échafaudages nanofibreux a été estimée telle que définie dans la formule suivante :
$${\text{Masse}}\;{\text{restant}}\left( \% \right) =\left( {1 - \frac{{w_{i} - w_{f} }}{{ w_{i} }}} \right) \times 100\%$$Pour évaluer le comportement de dégradation de l'échantillon après 7 jours, la morphologie des nanofibres a été observée par SEM.
Analyse de la compatibilité sanguine
Temps de coagulation
Le temps de thromboplastine partielle activée (APTT) a été utilisé pour évaluer l'activité des voies intrinsèques et communes de la coagulation en testant les temps de coagulation du plasma pauvre en plaquettes (PPP) après incubation avec des nanofibres électrofilées sur des lamelles. Pour cela, du sang anticoagulé (environ 10 mL) a été collecté et centrifugé à 3000 tr/min pendant 20 min pour obtenir un plasma pauvre en plaquettes (PPP). Chaque échantillon a été incubé avec 200 L de PPP pendant 10 min à 37 °C et analysé à l'aide du kit APTT en suivant les instructions du fabricant (n = 3).
Test d'hémolyse
Le taux d'hémolyse a été évalué en mesurant la concentration d'hémoglobine libérée dans la phase de solution par les érythrocytes dans le sang total dilué exposé aux nanofibres électrofilées. Les échantillons sur lamelles ont été placés individuellement dans des plaques à 24 puits et immergés dans 2 mL de PBS à 37 °C pendant 30 min. Les groupes témoins négatifs ne contenaient que 2 mL de PBS, tandis que les groupes témoins positifs étaient composés de 2 mL d'eau déminéralisée dans le but d'induire une lyse maximale des érythrocytes (n = 3 pour chaque groupe de test). Ensuite, 40 L de sang total frais anticoagulé susmentionné ont été ajoutés dans chaque puits et incubés pendant 60 min à 37 °C, après quoi les suspensions ont été prélevées dans des tubes à centrifuger et centrifugées à 100 × g pendant 5 minutes. Les surnageants ont été soumis à une mesure de l'absorbance à 570 nm à l'aide d'un lecteur de microplaques (SynergyH1/H1M, BioTek, Chine).
Thrombogénicité
Le potentiel thrombogène a été évalué in vitro après incubation d'échantillons électrofilés avec le plasma riche en plaquettes (PRP). Le PRP a été préparé par centrifugation (1 500 tr/min, 20 min) et la moitié supérieure du plasma a été jetée. Ensuite, les nanofibres sur les lamelles ont été incubées dans 100 L de PRP à 37 °C pendant 2 h et rincées doucement avec du PBS trois fois pour des expériences ultérieures. Pour évaluer l'activité plaquettaire après avoir été incubées avec du PRP, des nanofibres électrofilées ont été conservées dans le DMEM additionné de 10 % de FBS pendant 2 h et 24 h, puis un kit de dosage CCK-8 a été utilisé pour mesurer la viabilité des thrombocytes sur les nanofibres. La CCK-8 (20 L) a été ajoutée à 200 L de milieu DMEM sans sérum dans des plaques à 24 puits et incubée pendant 1 h. Enfin, les suspensions ont été mesurées par un lecteur de microplaques à une longueur d'onde de 450 nm.
Culture cellulaire et viabilité cellulaire
Des cellules endothéliales aortiques humaines (HAEC) ont été cultivées dans du DMEM supplémenté avec du FBS (10 %, v/v) et de la streptomycine/pénicilline (1 %, v/v) dans une atmosphère de 37 °C et 5 % de CO2 . Le milieu de culture a été remplacé trois fois par semaine. Les cellules ont généralement été isolées par 0,05 % de trypsine/EDTA pendant 3 min, centrifugées à 1 000 tr/min et mises en suspension dans le milieu frais pour effectuer le passage cellulaire ou l'ensemencement cellulaire.
Avant l'ensemencement cellulaire, tous les matériaux nanofibreux dans une plaque à 24 puits ont été stérilisés sous irradiation UV pendant 1 h et immergés dans 75 % d'éthanol (v/v, %) pendant 1 h. Ensuite, les nanofibres ont été rincées quatre fois avec une solution de PBS et trempées dans du DMEM pendant 12 h dans du CO2 incubateur. Les cellules ont été ensemencées à une densité de 1 × 10 4 cellules par puits sur des nanofibres et le milieu a été remplacé tous les jours. Après 24 h de co-culture, les cellules ont été lavées trois fois avec une solution de PBS, puis colorées avec un kit de coloration double Calcein-AM/PI (YEASEN Biochemical Technology Co., Ltd., Shanghai, Chine). L'IP a été utilisé pour colorer les cellules mortes et la Calcéine-AM pour les cellules vivantes.
Morphologie cellulaire sur les nanofibres
Pour observer l'adhésion cellulaire sur les nanofibres, la morphologie des cellules a été observée après 24 h de co-culture par Fluorescence Microscope (Nikon A1 MP, Japon). Dans un premier temps, les cellules ont été fixées avec du paraformaldéhyde à 4 % à température ambiante pendant 30 min. Ensuite, une solution à 0,5% de Triton X-100 a été utilisée pendant 5 minutes pour perméabiliser la membrane cellulaire. Enfin, le 4′6-diamidino-2-phénylindole (DAPI) a été utilisé pour colorer les noyaux cellulaires et la rhodamine-phalloidine a été utilisée pour colorer la F-actine. L'analyse quantitative (densité cellulaire, surface unicellulaire, élongation cellulaire) a été en outre réalisée avec Image J.
Prolifération cellulaire
L'activité de prolifération cellulaire sur les nanofibres composites a été réalisée avec un kit de dosage CCK-8. Les HAEC ont été ensemencées sur des nanofibres à une densité de 8 × 10 3 cellules/puits. Le milieu de culture a été changé tous les deux jours. Après 1, 4, 7 jours de co-culture, les cellules ont été lavées par une solution de PBS pour éliminer les cellules non adhérentes. Ensuite, 20 L de CCK-8 et le milieu complet à un rapport volumique de 1:10 ont été ajoutés dans la plaque à 24 puits pendant 1 h à l'incubateur. L'absorbance a été testée par Elisa Reader à 450 nm.
La coloration des cellules avec du DAPI et de la rhodamine-phalloidine a été réalisée avec un microscope à fluorescence pour observer directement les changements de nombre de cellules après co-culture avec différentes nanofibres pendant deux jours et six jours.
Analyse statistique
Tous les échantillons des expériences ont été traités en triple. Toutes les données sont représentées sous forme de moyennes ± déviations standard (SD). L'analyse statistique des échantillons a été déterminée par une analyse de variance à un facteur (ANOVA) pour comparer les différences avec la signification attribuée à p < 0,05.
Résultat et discussion
Préparation et caractérisation des nanofibres CS@PG
La figure 1 présente le diagramme schématique du processus d'électrofilage pour les échafaudages nanofibreux CS@PG et l'évaluation in vitro de l'anticoagulation et de la cytocompatibilité. Pour développer des échafaudages de tissus vasculaires conçus pour favoriser la prolifération des cellules endothéliales, différents ratios de CS (5, 10 et 15 % en poids) ont été incorporés dans des solutions de PG (10 %, v/v) pour fabriquer des nanofibres composites via un processus d'électrofilage.
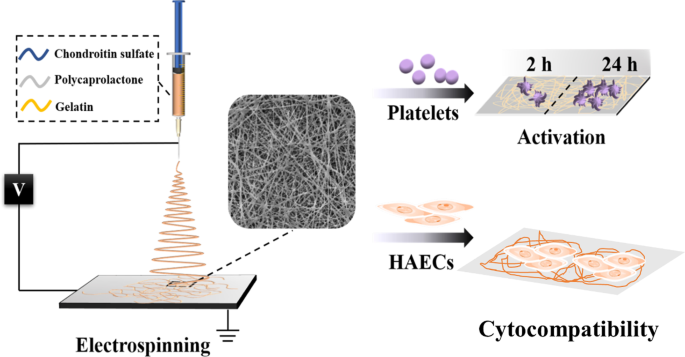
Illustration schématique de la fabrication de nanofibres et évaluation in vitro
Le SEM a été réalisé pour observer la structure des nanofibres électrofilées CS@PG. Comme le montre la Fig. 2, les images SEM des nanofibres PG, 5%CS@PG, 10%CS@PG, 15%CS@PG présentaient l'architecture fibreuse dense, contenant des fibres continues, lisses et nanométriques par technique d'électrofilage . Les nanofibres PG (Fig. 2a) présentaient de nombreuses billes irrégulières sur les nanofibres lors du processus d'électrofilage, ayant un diamètre moyen de 406,01 ± 146,28 nm. On pourrait expliquer que 10 % p/v de la solution électrofilée présentaient une faible viscosité, entraînant la formation de nanofibres non homogènes contenant des billes [20]. En augmentant la quantité de CS dans la solution polymère de 5 à 10 % en poids, des nanofibres homogènes sans billes ont pu être obtenues en raison de l'augmentation de la viscosité de la solution (Fig. 2b, c). De manière correspondante, 5%CS@PG et 10%CS@PG ont montré un diamètre moyen plus petit de 382,35 ± 152,99 nm et 300,29 ± 100,85 nm, respectivement. Ce résultat est principalement dû au fait que l'augmentation de la teneur en CS a augmenté en conséquence la conductivité de la solution d'électrofilage [20]. Cependant, lorsque la concentration en polymère atteignait 15 %, la viscosité de la solution de polymère est trop élevée pour être étirée dans le champ électrique. Au même débit de 1 mL/h que les groupes précédents, nous avons observé que sous la tension appliquée de 23 kV, le phénomène d'obstruction de la pointe de l'aiguille est apparu et le cône de Taylor n'a pas pu être observé. Par conséquent, le débit de la solution électrofilée et la tension appliquée ont été ajustés à 0,9 mL/h et 20 kV, respectivement. Les nanofibres 15%CS@PG ont été produites avec succès avec un diamètre moyen de 266,92 ± 105,43 nm.
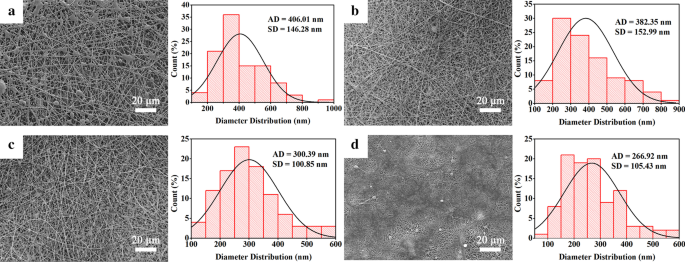
Images SEM et distribution de diamètre des échafaudages électrofilés CS@PG à différents rapports de CS. un PG, b 5%CS@PG, c 10%CS@PG, d 15%CS@PG
Comme le montre la figure 3a, il a été constaté que le CS était uniformément distribué dans les nanofibres 5%CS@PG et 10%CS@PG. Cependant, une agrégation CS a été détectée dans les fibres 15%CS@PG. Comme indiqué sur la figure 3b, une analyse élémentaire EDX a été effectuée pour détecter la teneur en soufre des fibres préparées. Comme prévu, la teneur en soufre a augmenté avec une concentration accrue de CS dans les fibres obtenues.

Images TEM (a ) et l'analyse élémentaire EDX des échafaudages électrofilés CS@PG à différents rapports de CS, c'est-à-dire PG, 5%CS@PG, 10%CS@PG et 15%CS@PG
Analyse des spectres FTIR
Une analyse des spectres FTIR a été réalisée pour déterminer les pics d'absorption caractéristiques du groupe chimique des échafaudages nanofibreux préparés. Le spectre FTIR de PG et CS a été considéré comme le groupe témoin à comparer avec les groupes de nanofibres CS@PG. Dans le spectre PG, de fortes bandes d'absorption apparaissant à 3 300 cm −1 et 2935 cm −1 peut être attribué au –NH2 et -OH vibration d'étirement, et CH2 étirement asymétrique, respectivement. Plusieurs pics d'absorption caractéristiques sont apparus à 1652 cm −1 (amide I) pour la vibration d'étirement C=O, 1542 cm −1 (amide II) pour les vibrations de flexion N–H, 1441 cm −1 pour CH2 étirement et 1267 cm −1 (amide III) pour les vibrations d'étirement C–N [21, 22]. Le spectre CS a réalisé une bande d'absorption caractéristique à 1245 cm −1 , représentant la vibration d'étirement S=O dans SO4 chargé négativement 2− [23, 24].
Comme le montre la figure 4, les spectres FTIR des nanofibres 5%CS@PG, 10%CS@PG et 15%CS@PG ont montré des pics caractéristiques de PCL, Gt et CS ensemble. Par rapport aux spectres du groupe PG, les groupes CS@PG ont montré la bande caractéristique du CS à 1245 cm −1 , et l'intensité de la bande CS augmentée par la présence de CS dans les nanofibres. Cette découverte a confirmé la présence de teneurs variables en CS dans les nanofibres électrofilées CS@PG.
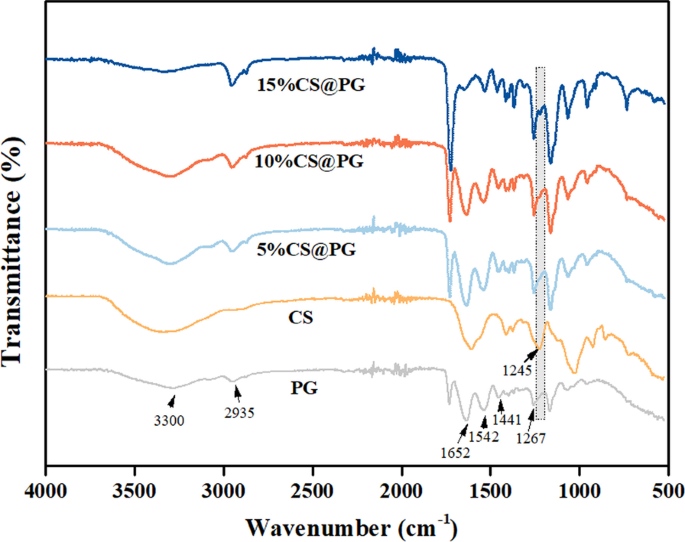
Spectre FT-IR des échafaudages électrofilés CS@PG
Porosité, taux de gonflement et dégradabilité des nanofibres
La porosité élevée de la fibre indique que le matériau a une excellente interconnectivité, ce qui favorise la diffusion de l'oxygène et des nutriments dans les pores et favorise l'infiltration cellulaire [25, 26]. La figure 5a montre la porosité des films nanofibreux. La porosité des nanofibres obtenues contenant différents rapports de CS était d'environ jusqu'à 80 %. L'architecture hautement poreuse obtenue par les nanofibres électrofilées peut imiter l'ECM naturel, fournissant ainsi un microenvironnement 3D favorable pour les cellules [27]. Il a été rapporté que les échafaudages en génie tissulaire avec une porosité allant jusqu'à 80% étaient bénéfiques pour le transport des nutriments et des métabolites.
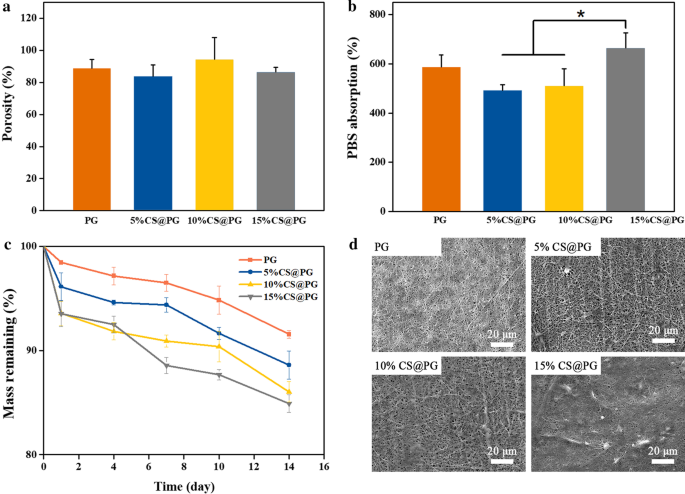
un La porosité des nanofibres préparées. b Absorption PBS de nanofibres préparées. c Masse restante des nanofibres CS@PG après dégradation dans une solution de PBS jusqu'à 14 jours. d Micrographies SEM de films nanofibreux dans une solution PBS à 37 °C pendant 7 jours
Le rapport d'absorption de PBS des échafaudages nanofibreux CS@PG a été comparé pour évaluer l'effet de CS sur l'absorption de PBS des films. Comme indiqué sur la figure 5b, le taux d'absorption PBS de l'échafaudage PG était de 586,34 ± 49,44 %, et les nanofibres 5%CS@PG et 10%CS@PG étaient de 492,86 ± 21,99% et 510,04 ± 69,55 %, respectivement. Le taux d'absorption PBS des groupes 15 % CS@PG (665,07 ± 59,81 %) était significativement plus élevé que celui de 5 % CS@PG et 10 %CS@PG. Ce résultat a indiqué que la teneur accrue en CS dans les nanofibres composites pourrait améliorer la propriété d'absorption du PBS des films, ce qui pourrait être dû à la haute hydrophilie des molécules CS contenant des groupes hydrophiles (carboxyle et hydroxyle) [28].
Les données de l'expérience de dégradabilité in vitro ont été représentées sur la figure 5c, et il a été constaté qu'avec l'augmentation du rapport CS, le taux de dégradation des échafaudages nanofibreux CS@PG était également augmenté. Cela pourrait être attribué à la présence de SO4 2− groupes [29]. Comme le montre la figure 5c, le taux de dégradation de la plupart des échafaudages a commencé à augmenter après 7 jours, et les résultats de dégradation au jour 14 étaient de 8,45 %, 11,39 %, 13,97 % et 15,10 % pour le PG, 5 % CS@PG, 10 Échafaudages nanofibreux %CS@PG et 15%CS@PG, respectivement. Les images SEM d'échafaudages nanofibreux (Fig. 5d) ont montré un léger gonflement après immersion dans une solution de PBS pendant 7 jours. Les images SEM indiquent que les nanofibres développées étaient suffisamment stables pour éviter une dégradation et une expansion graves jusqu'à 7 jours, affectant ainsi la réponse cellulaire in vivo ou in vitro.
Évaluation de l'hémocompatibilité
L'APTT est une méthode simple et fiable de détection du sang ou du plasma via le mécanisme de coagulation intrinsèque. L'APTT a été testé pour mesurer l'influence des nanofibres électrofilées sur le retard éventuel de la coagulation sanguine. Le temps de coagulation détecté par APTT a affiché une diminution statistiquement significative des temps de coagulation entre les nanofibres de contrôle PG et 5%CS@PG et 10%CS@PG. En revanche, un APTT prolongé a été trouvé après incubation de 15 % de nanofibres CS@PG avec PPP, indiquant sa fonction anticoagulante améliorée. Comme le montre la figure 6a, l'impact de la coagulation sanguine dépend du diamètre des échantillons de nanofibres. Le temps de coagulation APTT le plus bas a été trouvé après interaction avec 5%CS@PG nanofibrous et le APTT le plus élevé avec électrofilé 10%CS@PG, de manière similaire au degré d'hémolyse. Le temps de coagulation a été prolongé avec l'augmentation du rapport CS.
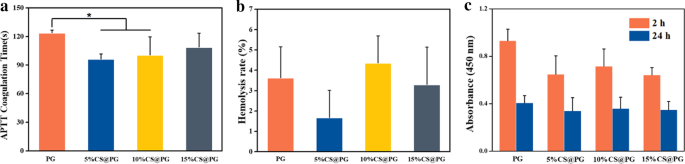
un APTT des nanofibres CS@PG. b Taux d'hémolyse des échantillons. c Activité métabolique des plaquettes sur les nanofibres. n = 3, *p < 0,05
Selon la norme ASTM F756-00 (2000), le taux d'hémolyse des biomatériaux doit être < 5% [30]. Le degré d'hémolyse dans cette étude a été réalisé à l'aide d'un dosage colorimétrique de l'hémoglobine libérée par les érythrocytes et peut être calculé par l'équation :Hémolyse (%) = (ODsam − ODnég )/(ODpos − ODnég ) × 100%. Comme indiqué sur la figure 6b, tous les échantillons étaient non hémolytiques et n'ont entraîné aucune hémolyse marquée (le taux d'hémolyse est inférieur à 5 %).
Les données de l'expérience de viabilité plaquettaire sont présentées sur la figure 6c. Après 2 h, l'activité métabolique des thrombocytes attachés était la plus élevée avec des valeurs maximales atteintes après interaction du PRP avec des nanofibres, en particulier des nanofibres de PG. Fait intéressant, après 24 h, l'activité plaquettaire a diminué dans tous les échantillons. Ce résultat pourrait être dû à l'activation rapide des thrombocytes par la structure des nanofibres, entraînant une consommation et une libération rapides de facteurs de croissance par rapport à une activation plaquettaire stable et à long terme au contact de la surface lisse [31]. La durée de vie normale des thrombocytes est d'environ 8 à 10 jours, et elle sera raccourcie à mesure que les plaquettes commenceront à s'activer.
Coloration des cellules vivantes/mortes
L'influence du CS sur la cytocompatibilité des nanofibres a été explorée par la viabilité cellulaire, la morphologie adhésive et la prolifération de l'évaluation des HAEC sur les nanofibres pendant 6 jours. Les cellules attachées ont été évaluées à l'aide du kit de double coloration Calcein-AM/PI, de la coloration DAPI et du kit de dosage CCK-8.
La figure 7a–e a montré les images de fluorescence des HAEC vivants et morts attachés aux différentes nanofibres. Calcein-AM (vert) et PI (rouge) ont été utilisés pour colorer les cellules vivantes et les cellules mortes, respectivement. Il a pu être observé que des cellules vivantes étaient collées sur les nanofibres composites CS@PG, indiquant que les nanofibres contenant différents ratios de CS n'avaient aucune toxicité pour les HAEC. Une analyse quantitative supplémentaire du nombre de cellules vivantes/mortes sur les nanofibres a été examinée par Image J (Fig. 7f). Par rapport à la proportion de cellules vivantes et mortes sur les nanofibres de PG, les trois autres groupes de PG contenant des ratios CS différents, en particulier les groupes 10%CS@PG et 15%CS@PG présentaient un pourcentage plus élevé de cellules vivantes, et le pourcentage était augmenté avec l'augmentation de la concentration de CS. Ce résultat a montré que la présence de CS dans les nanofibres était avantageuse pour maintenir la viabilité cellulaire [32].
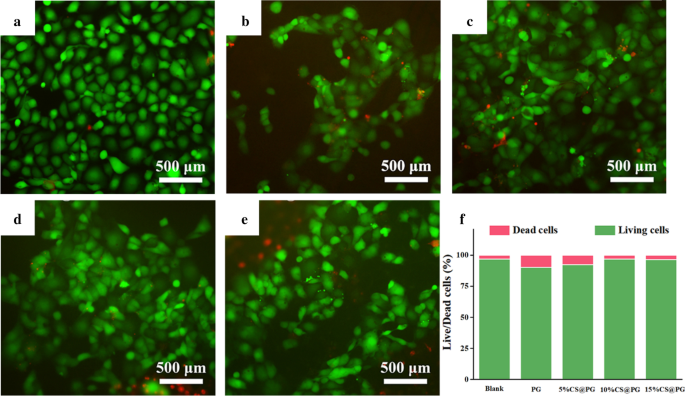
Viabilité cellulaire des HAEC sur les échafaudages CS@PG. un Plaque de culture tissulaire (TCP), b PG, c 5%CS@PG, d 10%CS@PG, e 15%CS@PG, f Le pourcentage de nombres de cellules vivantes/mortes de différents échafaudages nanofibreux, n = 3
Comportement d'adhésion cellulaire sur les nanofibres
Des échafaudages nanofibreux avec une bonne biocompatibilité sont considérés comme la principale exigence pour la génération de vaisseaux sanguins. Le PCL avec une bonne biodégradabilité et le Gt naturel avec une excellente biocompatibilité ont été largement utilisés en ingénierie tissulaire avec différentes structures, notamment des hydrogels, des nanofibres électrofilées et des échafaudages tridimensionnels [21, 33, 34]. La morphologie des HAEC sur l'interaction nanofibres composites et cellules-matériaux à 24 h a été observée au microscope à fluorescence. La densité cellulaire 10%CS@PG et 15%CS@PG était statistiquement significative que PG et 5%CS@PG, a indiqué que l'ajout de CS à un niveau plus élevé favorise l'adhésion cellulaire. Comme le montre la figure 8c, la zone unicellulaire de 5%CS@PG et 15%CS@PG était plus grande que les autres groupes de nanofibres. Cependant, l'allongement cellulaire de 10%CS@PG était significativement plus élevé que celui de PG, 5%CS@PG et 15%CS@PG (Fig. 8d). Ce résultat pourrait s'expliquer par le fait que l'ajout de CS à une concentration de 10 % peut faciliter la propagation des HAEC. Il a été constaté que les HAEC pouvaient adhérer, se propager et bien se développer sur les nanofibres composites, en particulier 10%CS@PG et 15%CS@PG. Ainsi, ces deux matériaux nanofibres peuvent être considérés comme un matériau vasculaire candidat sûr et prometteur en application clinique.
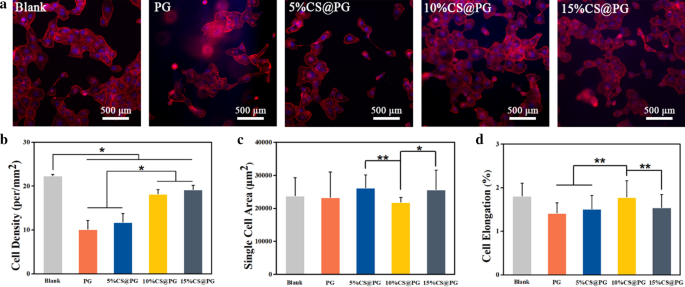
un Morphologie adhésive cellulaire des HAECs sur les scaffolds CS@PG (DAPI :noyaux cellulaires; Rhodamine-Phalloidin :cytosquelette). b Densité cellulaire. c Zone à cellule unique, d Allongement cellulaire dans différents groupes de nanofibres
Prolifération cellulaire
La croissance cellulaire et la viabilité sur les nanofibres CS@PG ont été étudiées in vitro par microscope à fluorescence et test CCK-8 (Fig. 9a–c). L'échafaudage électrofilé PG a été sélectionné comme contrôle positif. Les résultats du test CCK-8 pour différents films nanofibreux sont affichés sur la figure 9c. En 2, 4, 6 jours de culture cellulaire, le nombre de cellules a augmenté avec le temps de culture pour tous les groupes. Au jour 6, la valeur de DO des nanofibres 10%CS@PG était significativement plus élevée que celle de l'échafaudage PG. La comparaison de la prolifération cellulaire de 5%CS@PG, 10%CS@PG et 15%CS@PG a indiqué que le taux de prolifération cellulaire était augmenté en tant que présence de CS dans les nanofibres composites dans une certaine plage. Cependant, la capacité de prolifération cellulaire a également été influencée par la morphologie de surface des matériaux nanofibreux. Étant donné que la nanofibre 15 % CS@PG présentait une forte viscosité en raison du rapport CS plus élevé dans la solution polymère électrofilée, la prolifération cellulaire pourrait être affectée.
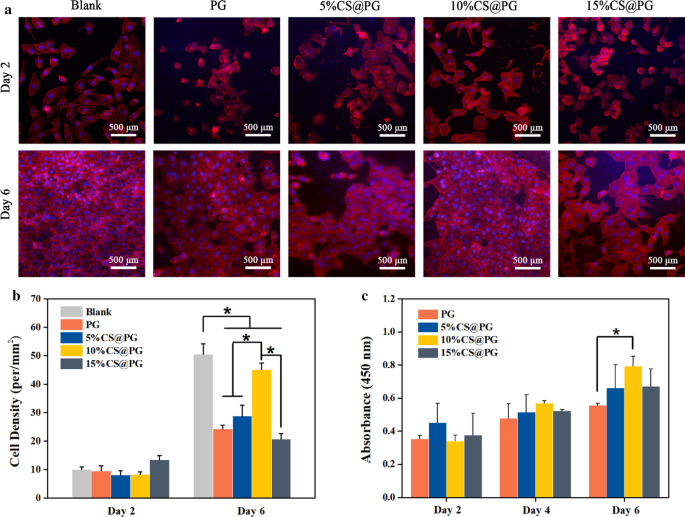
un Les HAEC ont proliféré sur les nanofibres détectées par coloration cellulaire pendant 2, 6 jours, b Densité cellulaire sur les échafaudages nanofibreux à 2, 6 jours, n = 3, *p < 0,05, c Dosage CCK-8 après HAEC cultivés sur PG, et nanofibres CS@PG à 2, 4, 6 jours
Conclusions
En résumé, des nanofibres composites biomimétiques CS@PG ont été fabriquées avec succès à l'aide de la technologie d'électrofilage. La morphologie et le diamètre des fibres modifiés ont été obtenus en faisant varier les concentrations de CS dans les nanofibres de PG. Les nanofibres CS@PG possédaient une porosité appropriée (~ 80%) et une absorption de solution PBS (jusqu'à 650%). L'incorporation de CS dans les nanofibres de PG a considérablement amélioré leurs propriétés anticoagulantes, prolongé leur temps de coagulation et amélioré les réponses cellulaires. En particulier, les nanofibres 10 % CS@PG ont présenté une adhérence, un allongement et une prolifération cellulaires favorables. Par conséquent, les nanofibres composites PG incorporées avec une certaine quantité de CS ont inhibé l'antithrombogénicité et amélioré les réponses des cellules endothéliales, qui pourraient être développées comme un échafaudage d'ingénierie tissulaire prometteur dans la réparation et la régénération des vaisseaux sanguins.
Disponibilité des données et des matériaux
Toutes les données générées ou analysées au cours de cette étude sont incluses dans cet article.
Nanomatériaux
- Nanofibres et filaments pour une administration améliorée des médicaments
- Ingénierie des procédés de revêtement par immersion et optimisation des performances pour les appareils électrochromes à trois états
- Nanofibres polymères électrofilées décorées de nanoparticules de métaux nobles pour la détection chimique
- Nanoparticules d'albumine chargées de resvératrol avec une circulation sanguine prolongée et une biocompatibilité améliorée pour une thérapie ciblée très efficace contre les tumeurs pancréat…
- Performances améliorées d'un nouveau catalyseur anodique PdAu/VGCNF pour l'électro-oxydation dans une pile à combustible au glycérol
- Promotion de la croissance cellulaire SH-SY5Y par des nanoparticules d'or modifiées avec de la 6-mercaptopurine et un peptide pénétrant dans les neurones
- Comparaison entre l'acide folique et la fonctionnalisation à base de peptide gH625 de nanoparticules magnétiques Fe3O4 pour une internalisation cellulaire améliorée
- Développement d'un biocomposite électrofilé de chitosan-oxyde de polyéthylène/fibrinogène pour des applications potentielles de cicatrisation
- Potentiel antiprolifératif et de déclenchement de l'apoptose des nanoparticules lipidiques ciblées à base de paclitaxel avec internalisation cellulaire améliorée par les récepteurs de la transf…



