Analyse photocatalytique, bactéricide et d'amarrage moléculaire de nanostructures d'oxyde d'étain recuit
Résumé
L'oxyde d'étain de taille nanométrique a été fabriqué avec une technique de précipitation simple et économique et a été analysé en effectuant une diffraction des rayons X sur poudre (XRD), une spectroscopie infrarouge à transformée de Fourier (FT-IR), une microscopie électronique à transmission haute résolution (HR-TEM) , rayons X à dispersion d'énergie (EDX) et spectroscopie UV-Vis. Les résultats XRD ont révélé que les particules d'oxyde d'étain possédaient une structure orthorhombique typique et présentaient une cristallinité améliorée avec le recuit. La calcination à 250 °C a produit principalement du SnO orthorhombique qui s'est transformé en SnO2 à des températures plus élevées de 500 et 750 °C. Les images HRTEM et FESEM ont montré l'existence d'agglomération au sein des particules d'oxyde d'étain. L'absorption s'est avérée augmenter jusqu'à une certaine température de recuit suivie d'une diminution, qui a été enregistrée par spectroscopie UV-Vis. L'effet de la température de recuit sur le comportement de décomposition du colorant des photocatalyseurs synthétisés a été étudié. Il a été noté que la température de recuit affecte la taille des particules synthétisées, la largeur de bande interdite et la photoactivité de l'oxyde d'étain. L'échantillon préparé à 500 °C a suivi une cinétique de premier ordre et a présenté une réactivité photocatalytique maximale vis-à-vis du bleu de méthylène. Les résultats expérimentaux obtenus à partir de la présente étude indiquent que SnO2 est un catalyseur prometteur et bénéfique pour éliminer les contaminants des eaux usées et de l'environnement. L'évaluation antimicrobienne du SnO recuit à 500 °C contre des cibles sélectionnées telles que E. coli et S. aureus ont représenté des zones d'inhibition significatives par rapport aux échantillons à 250 et 750 °C. De plus, les prédictions d'amarrage moléculaire de SnO2 des nanoparticules (NP) ont été réalisées contre une poche active de β -lactamase et enzyme ADN gyrase appartenant respectivement à la paroi cellulaire et à la voie de biosynthèse des acides nucléiques. Les NP fabriquées ont montré un bon score de liaison contre β -lactamase des deux E. coli (− 5.71 kcal/mol) et S. aureus (− 11,83 kcal/mol) aux côtés de l'ADN gyrase (− 9,57 kcal/mol ; E. coli et - 8.61 kcal/mol ; S. aureus ). Ces prédictions in silico suggéraient SnO2 Les NP en tant qu'inhibiteurs potentiels pour des cibles protéiques sélectionnées et faciliteront une compréhension claire de leur mécanisme d'action qui peut contribuer à la découverte de nouveaux antibiotiques.
Introduction
Des propriétés exceptionnelles et un large éventail d'applications technologiques associées aux oxydes métalliques conventionnels ont donné l'impulsion pour explorer ces matériaux sous leur forme nanostructurée. Parmi ceux-ci, l'oxyde d'étain (SnO2 ) est considéré comme un oxyde métallique important [1] qui présente une large bande interdite de 3,6 eV à température ambiante [2]. C'est un matériau semi-conducteur de type n qui présente des défauts intrinsèques sous forme de lacunes d'oxygène avec des atomes d'étain interstitiels qui interagissent avec des donneurs (porteurs de type n). Une augmentation du nombre d'électrons libres dans la bande de conduction entraîne une augmentation de la conductivité du matériau [3].
L'utilisation de SnO2 en tant que catalyseur d'oxydation, photocatalyseur, capteur de gaz et conducteur transparent présente la base pour étudier plus avant ce matériau [4,5,6,7,8,9]. Il a la capacité de détecter les gaz inflammables, explosifs et toxiques [10]. L'industrialisation a entraîné une augmentation des rejets de polluants nocifs pour l'air et l'eau tels que le CO et le SO2 dans l'atmosphère et les colorants azoïques nocifs dans les eaux usées. Il a été estimé qu'environ 500 tonnes de divers colorants sont déversées dans les eaux usées industrielles et une grande partie (~ 80 %) d'entre eux provient de l'industrie textile [11]. Les toxines chimiques et les combustibles organiques font partie de la pollution de l'air tandis que les colorants dangereux des plans d'eau affectent les écosystèmes terrestres, augmentant ainsi l'importance de la technologie utilisée pour détecter et empêcher ces polluants de nuire à l'environnement. En raison de ses propriétés physico-chimiques uniques, SnO2 a la capacité de fonctionner à basse température. En raison de sa non-stoechiométrie inhérente, il réduit les gaz nocifs en permettant une adsorption facile de l'oxygène à sa surface. De plus, il entraîne un coût inférieur par rapport à d'autres matériaux disponibles utilisés pour des applications similaires. Il possède également une transparence optique et une conductivité électrique substantielles, ce qui le rend approprié pour une utilisation dans les composants optoélectroniques [12]. Il est utilisé dans la fabrication d'électrodes transparentes et de cellules solaires destinées à être utilisées dans des panneaux et plusieurs dispositifs électrochromes [13,14,15,16,17].
Pour prévenir les maladies d'origine hydrique, l'élimination des bactéries des eaux usées est importante pour les systèmes d'abreuvement et d'assainissement. Entre 2003 et 2005 aux États-Unis, quatre maladies d'origine hydrique ont été signalées, qui se sont manifestées par des agents pathogènes présents dans l'eau potable, affectant environ 282 humains. Les techniques conventionnelles de désinfection des plans d'eau dépendent d'agents chimiques moins efficaces contre les protozoaires formant des kystes (Giardia et Cryptosporidium). De plus, ces techniques produisent parfois des sous-produits nocifs. La nanotechnologie est une technologie de nouvelle génération qui peut influencer l'économie mondiale via de nouveaux produits de consommation, l'utilisation des matériaux et les méthodes de fabrication [18]. Les nanostructures d'oxyde métallique présentent des propriétés antimicrobiennes améliorées attribuées à leur rapport surface/volume élevé, à leur stabilité et à leur biocompatibilité. Ils ont la capacité unique de pénétrer à travers la structure de la membrane cellulaire et de détruire les parties cellulaires des bactéries [19].
Deux oxydes d'étain basiques sont principalement étudiés tels que SnO et SnO2 , et l'existence de ces oxydes est attribuée au double degré de valence Sn (avec oxydation) + 2 et + 4. Ces deux oxydes sont également appelés matériaux semi-conducteurs à large bande interdite avec une structure PbO pour l'oxyde d'étain et un réseau tétragonal (structure rutile) pour SnO2 [20]. Il possède une large bande interdite d'énergie de 3,6 à 4,0 eV, un matériau semi-conducteur de type n et plus de 85 % de transparence [21]. Le SnO est un matériau de type p avec une bande interdite comprise entre 2,7 et 3,4 eV, mais la bande interdite expérimentalement atteinte peut atteindre 3,6 eV. De plus, les propriétés structurelles, optiques et électroniques de l'oxyde d'étain indiquent que l'augmentation de la pression conduit à la formation orthorhombique non structurelle de SnO et à la transmittance dans les régions UV-visible et proche infrarouge. L'augmentation de la température se traduit également par une structure orthorhombique SnO et tétragonale SnO2 formation. Ainsi, l'augmentation de la pression ou de la température déplace le bord d'absorption et augmente les énergies de bande interdite. Le SnO polycristallin fabriqué peut être converti en SnO2 phase en augmentant la température de 400 à 700 °C [22]. En raison du réglage de la bande interdite, des oxydes d'étain ont été utilisés dans l'industrie électronique.
SnO et SnO2 matériaux ont également été utilisés dans les batteries Li-ion [23,24,25]. La littérature rapportée démontre que les performances électrochimiques des nanomatériaux peuvent être améliorées en contrôlant leur taille [26]. Kida et al. ont signalé qu'une diminution de la taille des particules a provoqué une augmentation de la réponse du capteur pour H2 détection; cependant, la réponse à H2 S et CO augmentaient avec l'augmentation de la taille des particules [27]. Diverses méthodes pour produire SnO2 ont été rapportés dans la littérature. Merlin [28] a synthétisé ses nanoparticules d'une taille de 20 à 30 nm via une synthèse verte en utilisant un extrait de plante éthanolique-stevia rebaudiana qui a agi comme agent de coiffage et de réduction. Janardhan et al. [29] ont préparé des nanoparticules de SnO d'une taille moyenne de 50 nm en utilisant du HCl dilué et du SnCl2 ·2H2 O. Selvakumari et al. [30] fabriqué SnO2 particules avec une taille moyenne de cristal de 13 à 40 nm en utilisant une membrane de coquille d'œuf de poulet.
Généralement, les nanomatériaux peuvent être synthétisés en utilisant diverses méthodes, notamment la réduction électrochimique [31], sol-gel [32], hydrothermale [33] et la co-précipitation [34]. Dans le présent travail, la méthode de précipitation a été préférée car elle constitue une technique pratique et rentable pour synthétiser des nanostructures. Le but de cette étude était d'observer l'effet de différentes températures (250, 500 et 750 °C) utilisées lors de la synthèse sur la taille des cristallites, la morphologie et l'énergie de la bande interdite des matériaux non structuraux préparés. En outre, le comportement photocatalytique du produit synthétisé a été étudié en l'utilisant pour la dégradation du colorant bleu de méthylène qui est un polluant couramment rencontré dans l'industrie dans le monde entier. Des prédictions d'amarrage moléculaire in silico ont été effectuées pour dévoiler le mécanisme impliqué dans l'activité bactéricide de SnO2 contre β- lactamase appartenant à la voie de biosynthèse de la paroi cellulaire et ADN gyrase de la voie de biosynthèse des acides nucléiques de E. coli et S. aureus .
Méthodes
L'étude actuelle visait à synthétiser SnO2 nanoparticules par un processus de précipitation facile et simple et recuites à différentes températures. SnO recuit2 a été utilisé pour éliminer les polluants organiques des eaux usées et le potentiel antibactérien.
Produits chimiques
Chlorure d'étain(II) dihydraté (SnCl2 ·2H2 O) et l'éthanol de qualité analytique ont été acquis directement auprès de Sigma-Aldrich (Allemagne). L'hydroxyde de sodium (NaOH) et le bleu de méthylène (MB) ont été achetés respectivement auprès de Merk (Allemagne) et BDH (Royaume-Uni). L'eau distillée a été achetée sur le marché local pour fabriquer des nanostructures d'oxyde d'étain. La structure chimique du polluant (c'est-à-dire le colorant MB) utilisé dans cette étude est illustrée à la figure 1.
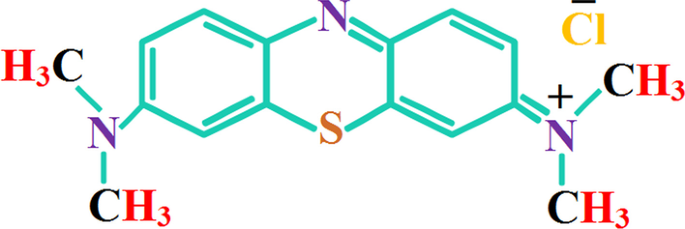
Structure chimique du contaminant MB
Préparation de nanostructures d'oxyde d'étain
Dans cette étude, des produits chimiques commerciaux de qualité analytique de haute pureté ont été utilisés pour préparer un nanomatériau d'oxyde d'étain en utilisant une procédure de précipitation (voir Fig. 2). Solutions aqueuses de SnCl2 ·2H2 O (19 g) et NaOH (8 g) ont été préparés séparément dans 50 mL d'eau distillée. Une solution aqueuse de NaOH a été versée goutte à goutte dans du SnCl2 .2H2 O solution (~ 10 gouttes/min) sous agitation constante à 70 °C en utilisant un ballon de 400 mL. Des précipités blancs sont apparus lors de l'addition goutte à goutte de la solution. Le produit obtenu a été lavé plusieurs fois en utilisant de l'eau distillée et de l'éthanol avec une centrifugeuse. Le matériau obtenu a ensuite été séché à température ambiante pendant 48 h pour éliminer la teneur en eau. Enfin, le produit solide séché a été broyé en une fine poudre à l'aide d'un mortier et d'un pilon. Trois échantillons ont été recuits dans un four à moufle à différentes températures (250, 500 et 750 °C) pendant trois heures avec une vitesse de chauffage de 0,5 °C/min [35].
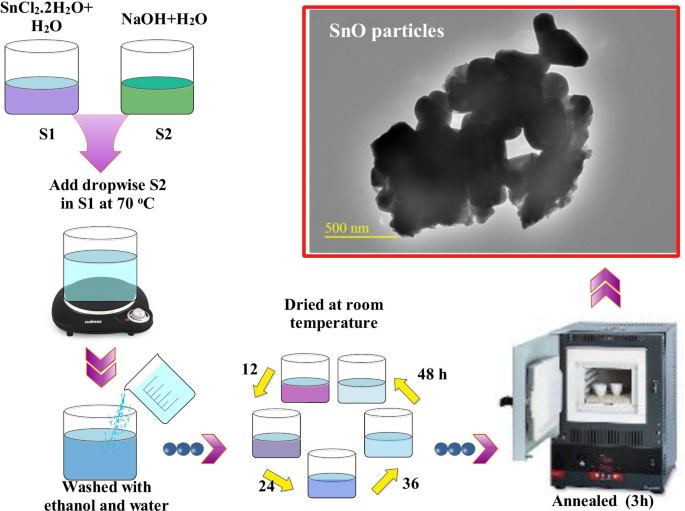
Représentation schématique de la synthèse d'échantillons d'oxyde d'étain
Processus d'activité photocatalytique
Le potentiel de photoactivité des échantillons d'oxyde d'étain recuit a été évalué en surveillant la photodégradation de la solution aqueuse de MB sous une source lumineuse ; mécanisme illustré à la Fig. 3 [36,37,38]. Pour chaque expérience de photoactivité, une masse connue de nanomatériau (10 mg) a été ajoutée dans 60 mL de solution aqueuse de colorant (10 mg/L). Avant l'exposition à la lumière, la suspension a été agitée magnétiquement dans l'obscurité pendant 5 min [38] pour obtenir un équilibre d'adsorption/désorption du colorant sur la surface du photocatalyseur. La solution de suspension a été irradiée pendant 80 min avec une lampe au mercure (400 W et λ = 400-700 nm) sous agitation (220 rpm). Des échantillons de MB de ~ 5 mL ont été prélevés de la solution d'essai pour surveiller la quantité résiduelle de MB à l'aide d'un spectrophotomètre UV-Vis allant de 300 à 750 nm. La variation de la longueur d'onde d'absorption maximale du MB (~ 665 nm) par rapport au temps de rayonnement a été enregistrée pour étudier la photodégradation du colorant MB. Les activités des produits synthétisés ont été évaluées en calculant le % de dégradation du colorant en utilisant la relation suivante :
$$\hbox{Dégradation}\, \% =[{({C}}_{0}-{C})/{{C}}_{0}]\times 100$$ (1)où C 0 désigne la concentration initiale de MB et C présente une concentration après irradiation. Sans photocatalyseur, l'expérience témoin a également été réalisée dans les mêmes conditions. Pour examiner la réutilisation des nanomatériaux, la solution de MB dégradée a été centrifugée (6000 tr/min/min) pendant 10 min pour récupérer le photocatalyseur. Plus tard, le produit récupéré a été séché à 80 °C (2 h) pour le réutiliser pour des expériences de dégradation du bromure de méthyle. Pour tester la durabilité du catalyseur, des expériences de photoactivité de recyclage ont été réalisées jusqu'à quatre cycles. Après chaque cycle, le produit a été centrifugé, séché et utilisé pour la prochaine photo-expérience.
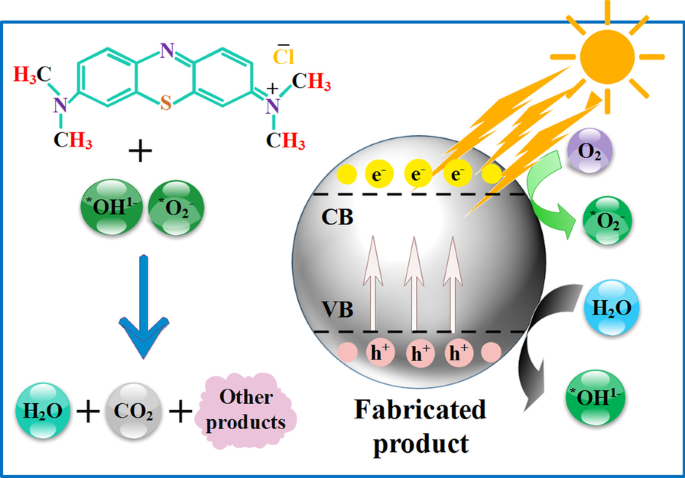
Illustration de la dégradation du bleu de méthylène MB par photocatalyseur
Activité antimicrobienne
L'action antibactérienne in vitro du SnO fabriqué à divers traitements de température a été évaluée contre les bactéries pathogènes les plus répandues E. coli et S. aureus isolé de la mammite caprine en utilisant un essai de diffusion en puits. Des boîtes de Pétri contenant des bactéries à croissance activée (standard de 0,5 Mc-Farland) sur de la gélose Macconkey solidifiée et de la gélose au sel de mannitol ont été incubées à 37 °C après avoir préparé un puits de 6 mm de diamètre en utilisant un foreur de liège stérile. Différentes concentrations de nanostructures synthétisées (500 et 1000 μg/50 μl) ont été appliquées à dose faible et élevée par rapport à la ciprofloxacine (5 μg/50 μl) et DIW (50 μl) comme contrôle positif et négatif, respectivement. Les boîtes de Pétri incubées pendant la nuit à 37 °C ont déclaré des zones d'inhibition (mm) qui ont été mesurées à l'aide d'un pied à coulisse. L'activité antibactérienne mesurée en termes de zones d'inhibition (mm) a été déclarée statistiquement significative en utilisant une analyse de variance à un facteur (ANOVA) avec SPSS 20.0.
Études d'amarrage moléculaire
La synthèse de la paroi cellulaire a été considérée comme une cible efficace pour la découverte de divers antibiotiques ayant différents modes d'action, comme les bêta-lactamines et les antibiotiques glycopeptidiques. Les bêta-lactamines ont été signalées comme les médicaments les plus commercialisés et représentent le traitement le plus courant des infections bactériennes [39, 40]. Ils inhibent la biosynthèse de la paroi cellulaire en se liant à la protéine de liaison à la pénicilline (PBP) et β -lactamases [41]. De même, les enzymes (c'est-à-dire l'ADN gyrase) appartenant à la synthèse des acides nucléiques ont également été considérées comme une cible efficace pour la découverte d'antibiotiques [42]. Ici, nous avons effectué des études d'amarrage moléculaire de SnO2 NP contre β -lactamase et enzyme ADN gyrase de E. coli et S. aureus pour avoir un aperçu de leur mode d'action possible.
Les structures cristallines 3D de cibles protéiques sélectionnées appartenant à E. coli et S. aureus ont été obtenus à partir de la banque de données de protéines avec le code d'accession :4KZ9; Rés :1,72 Å [43], 1 MWU ; Rés :2,6 Å [44] pour β -lactamase, tandis que 6KZX; Rés : 2.1 Å [45] et 5CTU ; Res :1,45 Å [46] pour l'ADN gyrase, comme indiqué sur la figure 4.
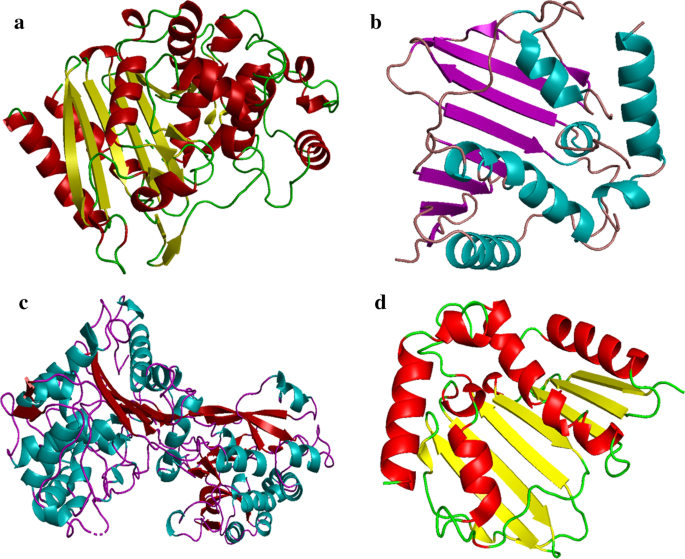
Structure 3D de a bêta-lactamase (PDB :4KZ9), b ADN gyrase (PDB :6KZX) de E. coli , c bêta-lactamase (PDB :1MWU) et d ADN gyrase (PDB :5CTU) de S. aureus
Des études d'amarrage moléculaire ont été réalisées à l'aide du logiciel ICM Molsoft (Molsoft L.L.C., La Jolla, CA) [47]. L'outil de préparation des récepteurs de l'ICM a été utilisé pour la structure des protéines impliquant l'ajout d'atomes d'hydrogène polaires, l'élimination des molécules d'eau et le ligand co-cristallisé. Les structures protéiques ont été optimisées à l'aide d'un outil de minimisation d'énergie avec des paramètres par défaut tandis que la grille a été utilisée pour identifier la poche active autour du ligand cristallisé. Plus tard, 10 meilleures conformations spécifiant l'orientation de SnO2 Des NP à l'intérieur de la poche active de l'enzyme ont été générées dans chaque cas. La conformation ayant obtenu le score de liaison le plus bas a été sélectionnée pour une analyse plus approfondie qui a dévoilé le modèle de liaison et la tendance à l'inhibition des NP fabriquées contre ces enzymes sélectionnées.
Le SnO2 La structure a été générée à l'aide de l'outil ligedit d'ICM tandis qu'une vue 3D de la conformation ancrée a été générée via ICM et le visualiseur de studio de découverte [48].
Caractérisation des matériaux
Diffraction des rayons X (XRD) Phaser BRUKER D2 dans une plage de 2θ = 10°–70° avec Cu Kα (λ = 1.540 Å) a été utilisé pour examiner la structure du réseau et récupérer des données sur la constitution des phases. Les groupes fonctionnels des produits synthétisés ont été évalués à l'aide d'un spectromètre infrarouge à transformée de Fourier (FTIR) de PerkinElmer. Le microscope électronique à balayage à émission de champ JEOL JSM-6610LV (FESEM) ainsi que le détecteur Oxford XMax EDS avec le logiciel INCA ont été utilisés pour analyser la morphologie et la composition élémentaire des échantillons préparés. Philips CM30 ainsi que le microscope électronique à transmission haute résolution JEOL JEM 2100F (HR-TEM) ont été utilisés pour enregistrer des images SAED, HRTEM et des motifs de franges de réseau. Les propriétés optiques des échantillons d'oxyde d'étain préparés ont été enregistrées de 300 à 800 nm via le spectromètre UV-vis GENESYS-10S.
Résultat et discussion
La figure 5 (a) présente les spectres XRD obtenus à partir d'échantillons d'oxyde d'étain synthétisés et recuits à différentes températures. Pour l'analyse compositionnelle de phase, le rayonnement CuKα a été utilisé tandis que la relation Debye-Scherer, \(D =K\lambda /\beta {\mathrm{Cos}}\theta\) où λ = 1,54 Å et k =0,9 a été utilisé pour calculer la taille des cristallites du matériau. À 250 °C, le modèle XRD montre des pics avec des valeurs 2θ de 29,12° (112), 31,60° (020), 33,57° (113), 40,15° (023), 45,54° (024), 51,35° (222) et 64,57 ° (225) qui sont tous attribués à la phase orthorhombique SnO (JCPDS :01-077-2296). Un seul pic enregistré à 26,66° (112) appartient à SnO2 structure orthorhombique (JCPDS :01-078-1063). Lorsque les échantillons ont été recuits à 500 et 750 °C, les pics de diffraction liés au SnO ont disparu et le produit résultant a été identifié comme étant du SnO2 orthorhombique. avec des plans cristallographiques 24,81° (110), 29,12° (113), 31,23° (020), 41,59° (211), 46,90° (117), 59,57° (135) qui correspond bien au dossier JCPDS n° 01-078- 1063 [49]. Les résultats XRD observés indiquent que le matériau préparé a d'abord été oxydé en SnO à 250 °C. Plus tard, à 500 °C et au-dessus, il s'est complètement transformé en SnO2 [50]. Les résultats montrent également que la cristallinité des échantillons s'améliore avec l'augmentation de la température. De plus, les modèles SAED obtenus à partir d'échantillons recuits à 250 et 750 °C ont représenté des anneaux de points lumineux comme illustré sur les Fig. 5b, c, respectivement. Les motifs analysés avec les plans de réseau (020), (023), (024) et (112) sont affectés aux plans de diffraction SnO orthorhombiques (Fig. 5b) et (020), (110), (117) et (135) sont attribué à SnO2 nanomatériau (Fig. 5c) pour les échantillons recuits à 250 et 750 °C, respectivement. La nature cristalline des produits a également été confirmée via des images SAED, ce qui est cohérent avec les observations de XRD.
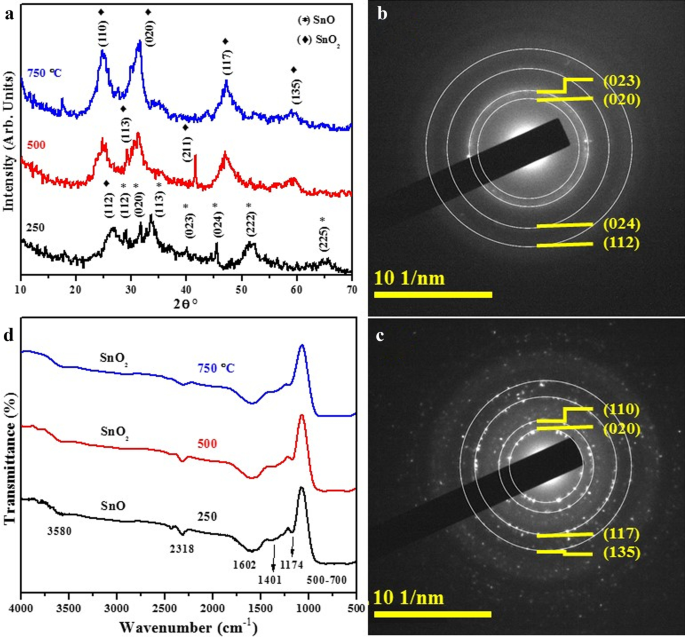
un Spectres XRD obtenus à partir de SnO recuit à 250, 500 et 750 °C b , c Anneaux SAED d'échantillons à 250 et 750 °C, respectivement, et d Modèles FTIR
Les spectres FTIR de nanomatériaux d'oxyde d'étain fabriqués et chauffés à 250, 500 et 750 °C sont présentés sur la figure 5d. Le pic d'absorption était centré à environ 3580 cm −1 couplé à près de 1602 cm −1 La bande a été attribuée à l'étirement/flexion du groupe O-H et de la liaison Sn-OH en raison du fait que l'oxyde d'étain absorbe une certaine quantité d'eau de l'atmosphère ambiante [51]. Le faible pic d'absorption allait de 2 300 à 2 400 cm −1 est attribué au dioxyde de carbone qui a été créé dans les produits lors de l'exposition à l'atmosphère [52]. Les liens apparaissant à 1174 cm −1 correspondent aux vibrations de divers types de groupes hydroxyle de surface tandis que le pic à 1401 cm −1 est due aux vibrations de flexion C–H [53, 54]. Les pics caractéristiques étaient compris entre 500 et 700 cm −1 sont attribuées aux vibrations de la couche superficielle Sn–O [55]. Une augmentation de la température de recuit provoque un décalage vers le bleu des pics tandis que les pics caractéristiques apparaissent forts et plus intenses. Cela peut être dû au processus de recuit où les atomes de nanomatériau acquièrent suffisamment d'énergie pour changer la position des atomes de nanoparticules, ce qui entraîne une recristallisation [56].
Des analyses FESEM et HRTEM ont été effectuées pour collecter des informations détaillées sur la morphologie et la nanostructure des produits fabriqués. Des images HRTEM d'oxyde d'étain recuit à 250, 500 et 750 °C ont été enregistrées, comme illustré sur la Fig. 6a–c. Les images fournissent des preuves de la formation d'agglomération au sein des nanoparticules avec une forme presque sphérique et une distribution aléatoire de la taille des particules (voir Fig. 6a, c). Sur la figure 6b, des particules de grande taille, légèrement transparentes et monodisperses avec peu d'agglomération ont pu être observées. Le même comportement de distribution des particules peut être observé à partir d'images incrustées à fort grossissement. Le changement brutal du comportement morphologique à 500 °C est perceptible. Cette température peut être une caractéristique au cours du processus d'oxydation [22]. De plus, la figure 6d–f affiche des micrographies HRTEM obtenues à partir d'échantillons recuits à 250, 500 et 750 °C, respectivement, pour détecter la distance interplanaire. Dans les cristallites, l'espacement des franges du réseau est de ~ 0,225 nm, comme illustré dans l'image de profil IFFT en médaillon de la figure 6d, qui correspond au plan de diffraction (023) de la phase orthorhombique de SnO (JCPDS :01-077-2296). L'espacement d calculé à partir des franges du réseau dans les échantillons traités à 500 et 750 °C est d'environ 0,364 et 0,367 nm, qui sont attribués au plan (110) de SnO2 structure orthorhombique selon JCPDS NO. 01-078-1063. Ces résultats sont en bon accord avec les résultats de la DRX [49, 57, 58]. À condition que les images IFFT montrent clairement une augmentation de l'espacement d avec l'augmentation de la température.
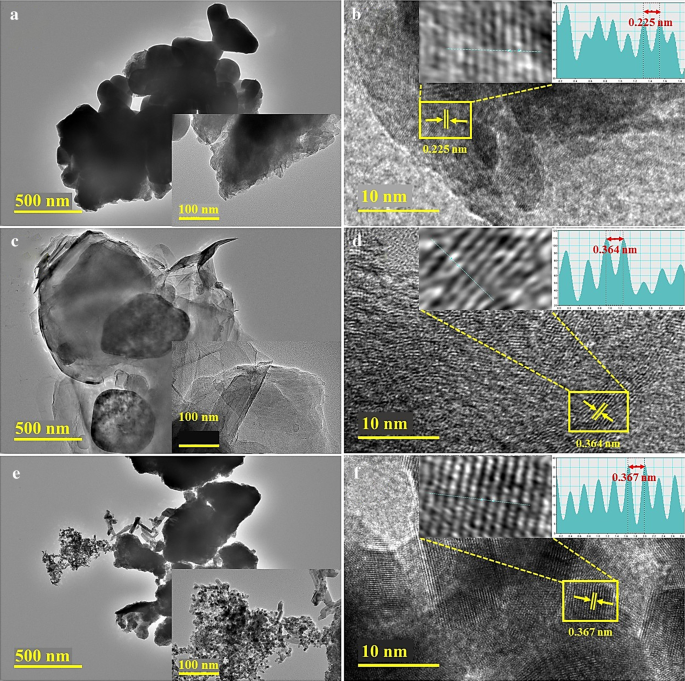
un –c RH-TEM et d –f franges réticulaires de nanostructures obtenues à des températures de recuit de 250, 500 et 750 °C, respectivement
Les images FESEM d'oxyde d'étain recuit à 250 (Fig. 7a) et 750 °C (Fig. 7b) illustrent la variation de la forme et de la taille des structures de réseau telles que la forme non uniforme ou aléatoire des particules avec des grains individuels grands et petits ainsi que l'agglomération . La figure 7b montre une micrographie FESEM de l'échantillon recuit à 750 °C, ce qui signifie de petites particules agglomérées et une structure bien développée par rapport à l'échantillon recuit à basse température avec une distribution aléatoire des particules. L'agglomération des particules entraîne une réduction de l'énergie libre de surface en raison d'une augmentation de leur taille entraînant une diminution de leur surface. L'agglomération des nanoparticules est due à l'adhérence des particules les unes aux autres par des forces faibles conduisant à des entités (sub)microniques. [59].
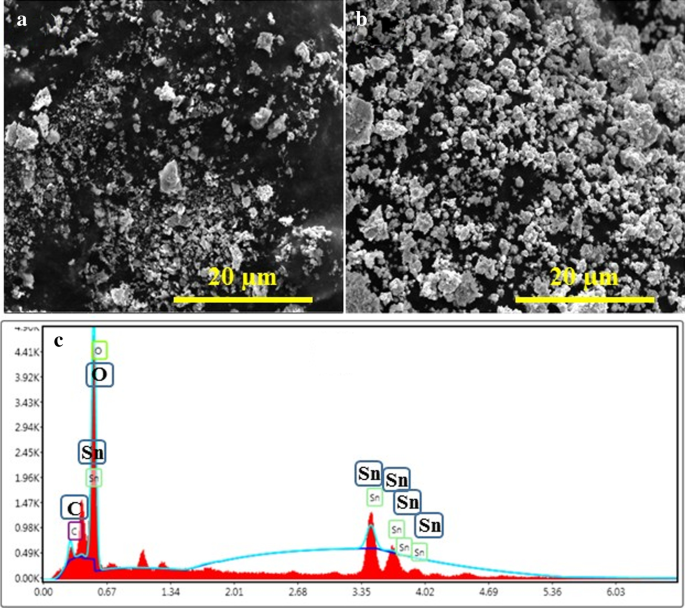
Micrographies FESEM à partir d'échantillons recuits à a 250 et b 750 °C et c Spectre EDX d'un échantillon recuit à 750 °C
La composition de l'oxyde d'étain fabriqué recuit à 750 °C a été analysée avec la technique EDX comme le montre la figure 7c. Les spectres des échantillons ont clairement montré la présence de Sn, O et C avec des % en poids de 53,7, 42,2 et 4,0 %, respectivement. Aucun constituant d'impureté n'était présent dans le produit, ce qui suggère une pureté élevée du SnO2 nanomatériau tandis que la teneur en C peut provenir des languettes de carbone utilisées pour contenir les échantillons.
Une technique de spectroscopie d'absorption non destructive a été utilisée pour étudier les propriétés optiques des nanomatériaux conducteurs et semi-conducteurs. Les spectres d'absorption obtenus à partir d'oxyde d'étain recuit à différentes températures sont illustrés sur la figure 8a. Plusieurs facteurs affectent l'absorbance attendue, tels que le manque d'oxygène, la bande interdite énergétique, la nature des impuretés et la rugosité de la surface. Les spectres obtenus à partir d'oxyde d'étain recuit présentaient une coupure ultraviolette à 300-365 nm [60], ce qui peut être dû à une photo-excitation des électrons de la cantonnière à la bande de conduction. Les spectres d'absorption ont légèrement diminué entre 300 et 365 nm avec l'augmentation de la température, comme le montre la figure 8a. Pour calculer la bande interdite, relation Tauc \(\alpha h\nu =A {(h\nu -{E}_{\mathrm{g}})}^{n}\) où α signifie coefficient d'absorption, A représente une constante tandis que n = 1/2 pour la bande interdite directe. Une extrapolation du tracé \({(\alpha h\nu )}^{2}\) par rapport à hν fournit une valeur de bande interdite optique E g (Fig. 8b). Les énergies de bande mesurées étaient de 3,51, 3,32 et 3,71 eV pour les échantillons recuits à 250, 500 et 750 °C, respectivement [61, 62]. La bande interdite des produits est cohérente avec les valeurs rapportées dans la littérature [61]. Globalement, à mesure que la température augmente, les atomes de nanoparticules atteignent plus d'énergie pour changer de position pour la recristallisation, ce qui modifie leur morphologie et réduit la taille des grains (peut être analysé à partir des données HRTEM). À mesure que la taille des particules diminue, la valeur de la bande interdite augmente, ce qui est attribué à l'effet de confinement quantique normal. Une tendance similaire a été observée par Malik et al. [63]. La bande interdite la plus faible présentée par un nanomatériau recuit à 500 °C a été attribuée à des nanostructures uniques ou à la synthèse amorphe d'oxyde d'étain polycristallin et à la génération de lacunes d'oxygène qui produisent un décalage vers le rouge. Le modèle Tauc indique que les semi-conducteurs de surface amorphes ou désordonnés ont des états de queue de bande localisés avec une énergie de bande inférieure [64].
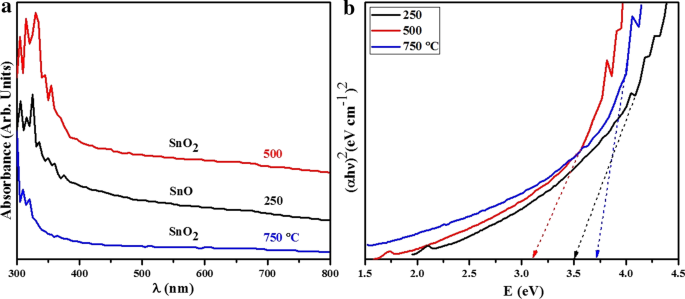
un Spectres d'absorbance UV-Vis et b valeurs d'écart énergétique obtenues à partir d'échantillons recuits à 250, 500 et 750 °C, respectivement
La photoactivité des produits d'oxyde d'étain recuits à différentes températures a été examinée en procédant à la photodégradation du colorant MB sous irradiation lumineuse (Fig. 9). Variation de l'absorption optique de la solution MB à λ max = 665 nm au cours de sa photo-décomposition est représenté sur la figure 9a. L'ajout d'échantillons fabriqués produit une diminution de la bande d'absorption MB avec le temps. La performance photocatalytique maximale a été présentée par l'échantillon recuit à 500 °C (E g = 3,32 eV) qui est attribué à une morphologie spécifique et à un faible taux de recombinaison électron-trou. Nous avons observé une dégradation de 86,0, 92,4 et 71,6% du MB par des photocatalyseurs à base d'oxyde d'étain préparés par recuit à 250, 500 et 750 °C en 80 min, respectivement (Fig. 9b). La photoactivité des matériaux semi-conducteurs est également liée à leur énergie de bande interdite qui influence le potentiel redox de la paire électron-trou photogénérée pendant le processus de dégradation du MB. Parmi les trois échantillons testés ici, le photocatalyseur recuit à 500 °C présentait l'énergie de bande interdite la plus faible (3,32 eV), tandis que le pourcentage de dégradation considérablement amélioré présenté par ce produit était attribué à sa structure unique et à son degré élevé d'agglomération, comme le montre la figure 9b. Une dégradation de colorant de pseudo-premier ordre est illustrée en utilisant ln (C o /C ) en fonction du temps d'irradiation :ln (C o /C ) = kt comme le montre la figure 9c où k désigne une constante de vitesse, C o et C représente respectivement la concentration initiale et finale du colorant (MB), [63, 65, 66, 67]. La valeur de k utilisant un nanomatériau préparé à 500 °C était de 0,59 min −1 et une diminution significative des échantillons synthétisés à 250 et 750 °C a été observée à environ 0,50 et 0,31 min −1 , respectivement (Fig. 9d).
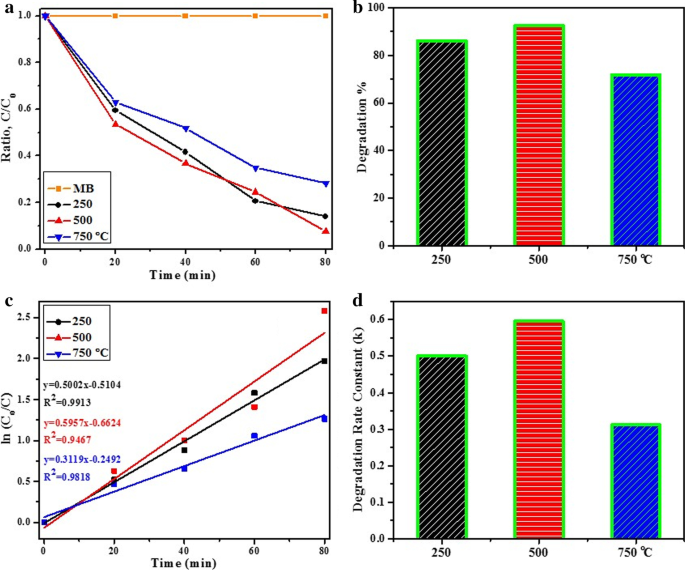
un Résultats de la dégradation du MB présentés par les photocatalyseurs fabriqués b graphique à barres % de dégradation c ln (Co /C) en fonction du temps d'irradiation et de d graphique de constante de taux de dégradation calculé
Pour le traitement de l'eau polluée, les photocatalyseurs doivent présenter une stabilité et une réutilisation pendant de longues périodes de temps pour rendre le processus économiquement réalisable. Dans la présente étude, quatre cycles de tests ont été effectués pour éliminer le MB à l'aide de photocatalyseurs fabriqués à base d'oxyde d'étain afin de déterminer leur stabilité. L'observation de quatre cycles consécutifs de dégradation du colorant est présentée dans la Fig. 10a, b. Le nanomatériau recuit à 500 °C a montré une légère diminution de la photo-décomposition du MB après quatre cycles (diminution de 6 %). Les résultats de l'élimination des contaminants de l'eau rapportés dans cette étude sont comparables à ceux rapportés par Prakash et al. [65].
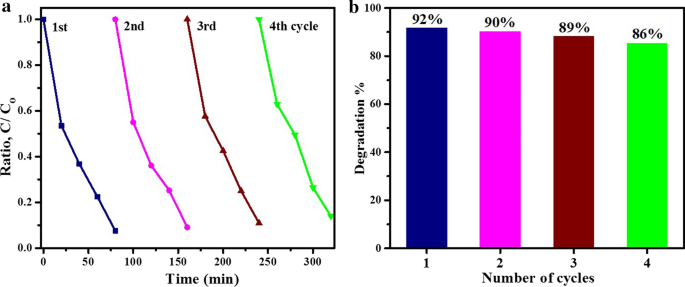
un Réutilisabilité du photocatalyseur à l'oxyde d'étain recuit à 500 °C et b graphique à barres % de dégradation
Les nanostructures de SnO fabriquées à divers traitements de température in vitro, l'activité antibactérienne mesurée en termes de zones d'inhibition (mm) ainsi que le pourcentage d'efficacité comparatif sont présentés dans la figure 11a–d et le tableau 1. Les graphiques présentent la proportion directe entre la concentration de nanostructures et les zones d'inhibition formé. Zones d'inhibition significatives enregistrées pour les échantillons de SnO (250, 500 et 750 °C) pour E. coli et S. aureus ranged between 2.85–3.5 mm, 3.35–3.75 mm and 3.25–4.75 mm and 4.55–5.35 mm at low and high concentrations, respectively, Fig. 11a, b and Table 1. The efficacy %age of synthesized nanomaterials increased from 67.0–82.3 to 78.8–88.2% for E. coli and similarly, 45.4–66.4% and 63.6–74.8% for S. aureus , respectively, Fig. 11c, d. All measured results were compared with DIW (0 mm). Positive control depicted 4.25 mm and 7.15 mm inhibition zones for E. coli et S. aureus , respectively, Fig. 11a, b. Overall SnO2 nanostructures optimized at 500 °C found more potent at both concentrations and more broadly, SnO2 found more potent against gram-negative (G –ve) E. coli compared with gram-positive (G +ve) S. aureus .
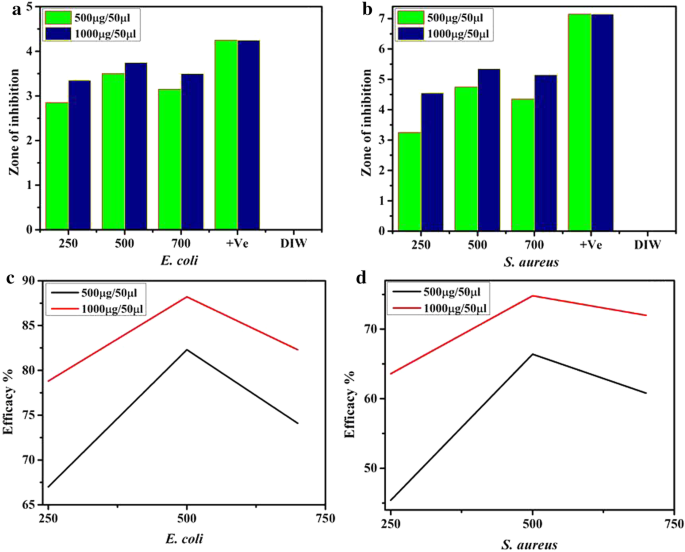
un In vitro bactericidal action of SnO annealed at different temperatures for E. coli b S. aureus c In vitro bactericidal efficacy %age of fabricated NPs for E. coli (d) et S. aureus , respectivement
Size, concentration and morphology of nanostructures directly affects oxidative stress produced. Antibacterial activity imperiling size and concentration portrays inverse relation to size [68,69,70]. Nanostructures more efficiently produce reactive oxygen species (ROS) which exist in bacterial membrane resulting cellular organelles extrusion and bacteria death [71]. SnO2 generate more efficiently ROS including hydrogen peroxide (H2 O2 ), OH groups and superoxide ions [72]. The increased antibacterial efficacy of fabricated SnO at various temperature treatments for E. coli compared to S. aureus could be attributed to difference in cell wall structures of bacteria. G –ve bacteria cell wall consists of peptidoglycan thin layer with an outer membrane containing proteins and phospholipids while G +ve cell wall contains thick layer of peptidoglycan with lipoteichoic and teichoic acids. This major difference in cell wall structure of both bacteria leads toward maximum efficacy of fabricated nanostructures toward G −ve compared to G +ve bacteria [18].
Resistance acquired by microbial pathogens against various antibiotic drugs especially multidrug resistance pose huge threat to public health around the globe and there is an urgent need of more antibiotic drugs with novel mode of action [73]. Antibiotics belonging to various classes follow different mechanisms for their activity and target pathways vital for bacterial survival. For instance, Beta-lactam antibiotics such as penicillin target enzymes involved in peptidoglycan synthesis (i.e., important precursor for cell wall synthesis) [74] while Rifampicin a well-known antibiotic target enzyme belongs to nucleic acid biosynthetic pathways [42] suggesting importance of both cell wall and nucleic acid biosynthetic pathways as target for new antibiotic discovery [75]. Although bactericidal activity of various nanoparticles has been reported previously in recent years still exact mechanism of their action is not known [76, 77]. Keeping in view good antibacterial activity of SnO2 against E. coli et S. aureus , we performed molecular docking studies to identify their possible mechanism of action against β -lactamase and DNA gyrase enzymes as potential target.
In case of β -lactamase from E. coli the best binding score observed was − 5.71 kcal/mol showing H-bonding interaction with Lys239 (1.80 Å) and Gly235 (1.66 Å) alongside metal contact interaction with Gln35 as shown in Fig. 12a, b. Similarly, the top binding score obtained for DNA gyrase from E. coli was − 9.57 kcal/mol having H-bonding interaction with Thr163 (1.46 Å), Gly77 (1.43 Å) and Glu50 (3.36 Å) along with metal contact interaction with Gly75 as depicted in Fig. 12c, d.
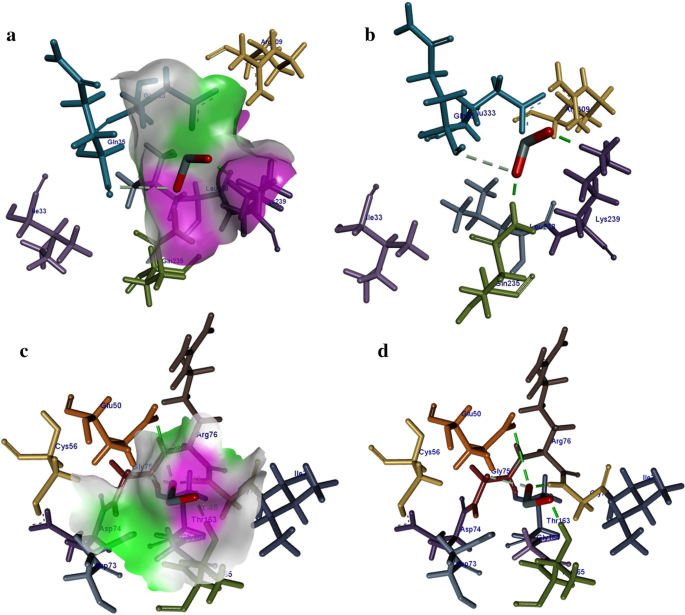
un , b Binding interaction pattern of SnO2 nanoparticle with active site residues of β -lactamase and c , d DNA gyrase from E. coli
The best binding score obtained for β -lactamase of S. aureus was − 11.83 kcal/mol. The binding patterns of SnO2 inside active pocket involved H-bonding interaction with Ser400 (2.16 Å), Gly522 (1.99 Å) and Ileu524 (1.90 Å). In addition, metal contact interaction was observed between SnO2 and Gln521 as depicted in Fig. 13a, b. For DNA gyrase from S. aureus the best conformation obtained showed H-bonding interaction with Gly85 (2.55 Å) and Thr173 (1.54 Å) having binding score − 8.61 kcal/mol (Fig. 13c, d).
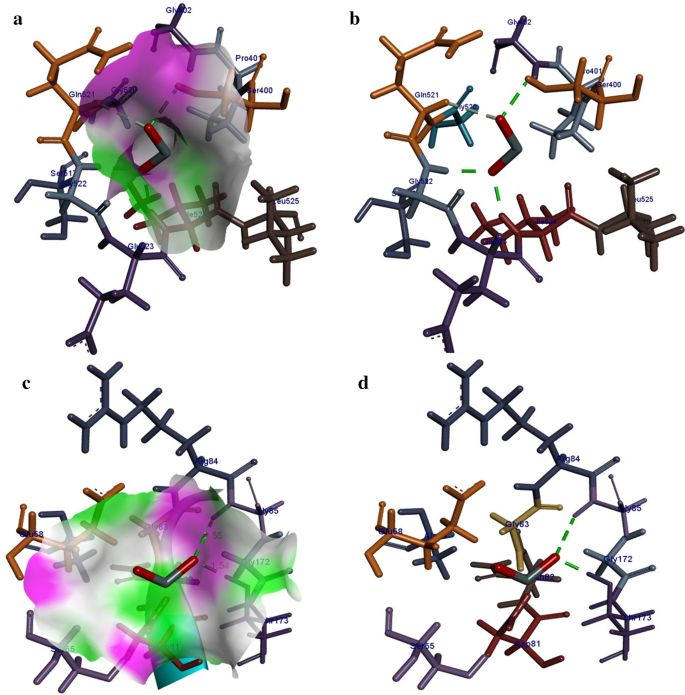
un , b Binding interaction pattern of SnO2 nanoparticle with active site residues of β -lactamase and c , d DNA gyrase from S. aureus
Conclusion
In summary, tin oxide nanoparticles annealed at various temperatures were synthesized by a facile and simple precipitation process. Annealing of samples at 250 °C during synthesis produced predominantly orthorhombic SnO which transformed to SnO2 at 500 and 750 °C. The XRD and HRTEM analyzes revealed that nanoparticles possessed orthorhombic structure while particle size increased initially with an increase in temperature to 500 °C followed by a decrease at 750 °C. Large particle size at 500 °C was attributed to unique structure exhibited by the sample annealed at that temperature. Fabricated nanostructures demonstrated well-crystallized behavior along with agglomeration. Photoactivity of annealed tin oxide nanomaterials was evaluated by decomposing MB dye that was used as a model organic contaminant and a comparison between annealed samples was realized. Product synthesized at 500 °C exhibited 6% higher activity compared to sample annealed at 250 °C during degradation of MB. Maximum MB degradation attained in this study was 92% after 80 min irradiation time by 500 °C sample. It is suggested that radical (*OH 1− and *O2 − ) and holes are major active entities in photocatalysis process. In silico predictions are in good agreement with in vitro bactericidal activity of SnO2 NPs. Molecular docking studies of SnO2 NPs against selected enzymes, i.e., beta lactamase and DNA gyrase, suggested their tendency to impede activity of these enzymes that need to be further explored and confirmed through enzyme inhibition assay studies.
Disponibilité des données et des matériaux
Toutes les données sont entièrement disponibles sans restriction.
Abréviations
- EDS :
-
Energy-dispersive x-ray spectroscopy
- FTIR :
-
Fourier-transform infrared spectroscopy
- G +ve:
-
Gram-positive
- G −ve:
-
Gram-negative
- HR-TEM :
-
Microscopie électronique à transmission haute résolution
- JCPDS :
-
Joint Committee on Powder Diffraction Standards
- NP :
-
Nanoparticules
- SnO:
-
Oxyde d'étain
- UV–Vis:
-
Ultra-violet visible spectroscopy
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- Exemples de circuits et de listes d'interconnexions
- Analyse de l'actine et de l'organisation de l'adhésion focale dans des cellules U2OS sur des nanostructures polymères
- Modélisation et simulation de dynamique moléculaire de la coupe de diamant de cérium
- Biosécurité et capacité antibactérienne du graphène et de l'oxyde de graphène in vitro et in vivo
- Préparation et performances photocatalytiques des photocatalyseurs à structure creuse LiNb3O8
- Synthèse facile d'oxyde d'étain mésoporeux semblable à un trou de ver via l'auto-assemblage induit par l'évaporation et les propriétés de détection de gaz améliorées
- Synthèse en un seul pot de nanoplaques Cu2ZnSnSe4 et leur activité photocatalytique induite par la lumière visible
- Progrès récents dans les méthodes de synthèse et les applications des nanostructures d'argent
- Cinétique de charge de direction des photocatalyseurs au niobate d'étain :rôles clés de la structure de phase et de la structure électronique



