Matrices verticales à l'échelle nanométrique de nanotiges d'or par auto-assemblage :mécanisme physique et application
Résumé
L'effet photonique unique des nanoparticules métalliques auto-assemblées est largement utilisé dans de nombreuses applications. Dans cet article, nous avons préparé un substrat de matrices verticales de nanotiges d'or (GNR) auto-assemblé par une méthode d'évaporation et avons constaté que la morphologie du substrat peut être régulée efficacement en modifiant le temps d'immersion dans la solution de molécules cibles pour obtenir différents effets d'amélioration Raman. Nous avons calculé séparément le champ électromagnétique local des réseaux verticaux GNR et du substrat de désordre par la méthode des éléments finis (FEM), ce qui était cohérent avec les résultats expérimentaux. Sur la base d'un temps de trempage optimal, la sensibilité, la reproductibilité et la stabilité des substrats ont été étudiées séparément. Les résultats expérimentaux montrent que les réseaux verticaux GNR peuvent détecter la Rhodamine 6G (Rh6G) à des concentrations aussi faibles que 10 −11 M et présentent une bonne reproductibilité et stabilité en raison de l'amélioration du champ électromagnétique (EM) local causée par le couplage de nanotiges adjacentes. Ainsi, notre travail peut démontrer que le substrat a une excellente activité de diffusion Raman améliorée en surface (SERS) et que les réseaux verticaux GNR obtenus ont un grand potentiel pour le biocapteur et la biodétection.
Introduction
Les nanostructures de métaux nobles (or, argent, cuivre, etc.) peuvent générer des champs EM localisés sur leurs surfaces en utilisant le rayonnement visible, ce qui fournit des conditions favorables pour améliorer les signaux spectraux des molécules sondes [1, 2]. Les conditions d'excitation spécifiques peuvent générer une résonance plasmonique de surface (SPR) à la surface des nanostructures métalliques, qui ont une importance importante pour la recherche et de nouveaux effets optiques en plasmonique, notamment la fluorescence améliorée en surface (SEF) et le SERS. Possédant une sensibilité élevée, une réponse rapide et un effet d'empreinte digitale, le SERS a un grand potentiel pour les applications, telles que la détection de matériaux, la biomédecine et les capteurs, etc. [3,4,5,6,7]. En général, le SERS est regroupé en deux catégories « amélioration du champ électromagnétique local » et « mécanismes d'amélioration chimique » [8]. Il est bien admis que « l'amélioration du champ EM » joue un rôle majeur dans le SERS et il montre des améliorations de 4 à 11 ordres de grandeur. Les « points chauds » produits entre des nanoparticules métalliques adjacentes peuvent entraîner un énorme champ électromagnétique local près de la surface métallique ; par conséquent, la diffusion Raman des molécules situées dans le champ EM peut être améliorée. Afin d'obtenir un bon effet SERS, un substrat métallique bien formé, des molécules sondes appropriées et la sélection des conditions d'excitation sont tous cruciaux [9]. Ces dernières années, de nombreux rapports ont été publiés sur le SERS. Sun et al. préparé des nanoarrays d'argent par la méthode de modèle qui possédait un excellent effet SERS sur le substrat [10]. Lu et al. ont découvert que les nanofils d'argent peuvent produire des changements morphologiques de surface au foyer du laser et ont de forts effets SERS sur les molécules cibles environnantes [11]. Cho et al. ont détecté des signaux Raman de 4-NTP avec de faibles concentrations sur un substrat de nanocristal de dendrite d'argent [12]. Bien qu'il y ait eu de nombreux rapports sur le SERS, la promotion du SERS fait encore face à de nombreux défis. Par exemple, préparer un substrat uniforme de grande surface à faible coût et réaliser une détection ultra-sensible, etc.
Les nanostructures métalliques auto-assemblées en tant que substrats prometteurs ont attiré de plus en plus d'attention dans les aspects expérimentaux et théoriques [13,14,15,16,17,18]. Comparé aux nanoparticules simples, le champ EM local des nanoparticules métalliques auto-assemblées montre une propriété optique extrêmement unique. De plus, le substrat à auto-assemblage présente les avantages d'un faible coût, d'une manipulation facile et d'une distribution uniforme sur une grande surface. En combinant ces avantages, on peut considérer que le substrat auto-assemblé a un grand potentiel pour promouvoir le SERS. Récemment, certains groupes de recherche ont signalé des substrats auto-assemblés en nanotiges d'or (GNR) pour le SERS [19,20,21]. Cependant, à notre connaissance, l'influence d'un changement de morphologie du substrat des réseaux verticaux GNR sur les signaux Raman des molécules cibles a été rarement étudiée. Ici, nous avons d'abord préparé un substrat de réseaux verticaux GNR auto-assemblés par la méthode d'évaporation [22]. Et puis, le substrat a été immergé dans une solution de molécule sonde; la morphologie des réseaux verticaux de GNR a été régulée en modifiant le temps de trempage. Enfin, les spectres Raman de la rhodamine 6G (Rh6G) et du cristal violet (CV) sur le substrat ont été obtenus dans des conditions d'excitation spécifiques. Afin de vérifier les résultats de l'expérience, nous avons utilisé des images SEM des réseaux verticaux GNR et des substrats de désordre pour simuler la distribution de champ local des substrats par FEM. Le résultat montre que le calcul de simulation est presque cohérent avec les données expérimentales. En outre, nous étudions également la sensibilité de détection, la reproductibilité et la stabilité du substrat SERS sur la base du temps de trempage optimal ci-dessus et avons discuté des résultats expérimentaux. Une sensibilité, une reproductibilité et une stabilité excellentes peuvent indiquer que le substrat des réseaux verticaux GNR peut être un bon candidat pour l'application de la zone de capteur optique.
Méthodes et expérience
Matériel
Rh6G (qualité laser) a été acheté chez Exciton (Amérique), CV a été acheté chez Sigma-Aldrich, chlorure d'or tétrahydraté, éthanol, nitrate d'argent et acide chlorhydrique ont été achetés chez Sinopharm Chemical Reagent Co., Ltd. (Chine). Le bromure de cétyltriméthylammonium (CTAB), le borohydrure de sodium et l'acide ascorbique sont achetés auprès de Shanghai Aladdin Bio-Chem Technology Co., Ltd. (Chine). Les plaquettes de silicium (Si) ont été achetées auprès de Li Jing Photoelectric Technology Co. Ltd. (Zhejiang, Chine). Tous les réactifs sont utilisés sans autre purification. De l'eau déminéralisée a été utilisée tout au long de l'expérience.
Préparation des tableaux verticaux GNR
Les GNR ont été réalisées via une méthode de croissance modifiée à médiation par les semences [23, 24]. La solution de GNR obtenue a été centrifugée trois fois à 10 000 rpm pendant 5 min pour éliminer l'excès de CTAB. Sur la base des méthodes précédentes [22], nous avons utilisé la méthode d'évaporation de solvant pour obtenir des réseaux verticaux GNR. Ensuite, le substrat a été trempé dans la solution des molécules sondes. Le processus de préparation de l'échantillon est illustré à la figure 1. À la fin du processus, le substrat a été doucement retiré, rincé à l'alcool, puis séché.
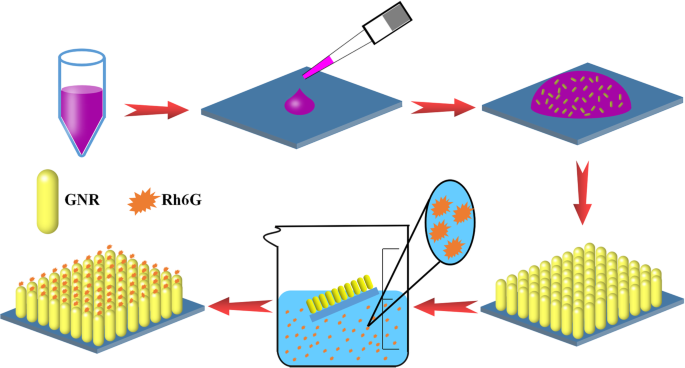
Le schéma du processus de préparation des tableaux verticaux GNR
Caractérisation
La taille et la morphologie du réseau vertical GNR ont été mesurées au microscope électronique à balayage (SEM, Nova Nano 450). Les signaux Raman ont été collectés par microscopie confocale Raman (LabRAM HR Evolution, HORIBA Jobin Yvon SAS). Le laser CW de 532 nm a été utilisé comme source d'excitation et la puissance du laser est de 0,5 mW. Les échantillons ont été exposés au microscope (× 50) et le temps d'intégration a été fixé à 1 s.
Résultats et discussion
Mécanisme d'auto-assemblage de nanotiges d'or
En général, un écoulement capillaire vers le bord est généré à l'intérieur des gouttelettes pour transporter les GNR en suspension jusqu'au bord des gouttelettes, provoquant le dépôt d'un grand nombre de GNR au bord pour former une distribution désordonnée du GNR, connue sous le nom d'effet « anneau de café ». [25, 26]. Néanmoins, les GNR en solution aqueuse sont disposés côte à côte pour former une structure initiale à six déformations par des forces d'attraction et des forces électrostatiques dans des conditions appropriées. Le flux de Marangoni et le recul de la ligne de contact des gouttelettes provoquent l'accumulation des GNR libres en solution autour du modèle initial, ce qui entraîne une augmentation continue de la surface des réseaux verticaux GNR. Enfin, les réseaux verticaux sont fixés sur le substrat en raison de la gravité et des interactions de van der Waals. Dans le processus de formation des réseaux verticaux GNR, il existe trois principaux facteurs d'influence :la force de van der Waals, la force d'épuisement et la force électrostatique [27]. La force de van der Waals et la force d'épuisement induite appartiennent à une force attractive, et la force électrostatique appartient à une force répulsive. Les forces de van der Waals et les forces d'épuisement rapprochent étroitement les GNR adjacents. La force électrostatique répulsive stabilise les GNR à une certaine distance et les empêche de se rassembler au hasard. La synergie entre la force attractive et la force répulsive induit des GNR dans des réseaux d'ordre élevé.
La température et l'humidité sont des facteurs d'influence importants dans l'auto-assemblage. Les gouttelettes de GNR forment un « anneau de café » dans un environnement à haute température ou à faible humidité. Dans le processus d'évaporation, la ligne de contact de la gouttelette est épinglée. En raison du taux d'évaporation plus élevé au bord de la gouttelette, les GNR sont transportés vers la ligne de contact d'épinglage par le flux capillaire et déposés pour former un motif annulaire. En revanche, la solution GNR produit un flux de Marangoni, et les GNR sont compacts et hautement ordonnés dans les circonstances appropriées. De plus, la concentration en tensioactif joue également un rôle clé dans le processus d'auto-assemblage. De nombreuses recherches ont montré que l'augmentation de la concentration de tensioactif CTAB est bénéfique pour la formation de substrats de réseaux verticaux GNR [28, 29]. La raison principale est que les GNR sont entraînés par le flux capillaire et se déplacent autour de la ligne de contact de la gouttelette. Si la concentration en tensioactif est trop faible pour former un écoulement de Marangoni, un grand nombre de particules se déposeront autour de la ligne de contact pour provoquer une distribution désordonnée. À l'inverse, l'augmentation de la concentration en tensioactif peut entraîner la poussée de nombreuses molécules de tensioactif sur la ligne de contact et produire plus facilement un écoulement de Marangoni. Une partie des GNR est déposée près de la ligne de contact pendant le processus d'évaporation, et les nanoparticules en excès sont renvoyées au centre de la goutte sous le tourbillon de Marangoni pour compléter l'assemblage ultérieur. On peut conclure que les nanotiges sont contrôlées par le flux de Marangoni pour compléter les réseaux ordonnés GNR. Le contrôle de ces facteurs d'influence peut aider à former des réseaux verticaux GNR ordonnés et à grande surface, qui peuvent fournir un support fiable pour le spectre suivant.
Morphologique des nanotiges d'or et réseau vertical
Le processus de préparation et le fonctionnement ultérieur des réseaux verticaux GNR sont présentés sur la figure 1. Par souci de simplicité, la procédure expérimentale n'est représentée que schématiquement. En bref, 5 μl de gouttes d'une solution de GNR centrifugée ont été versés goutte à goutte sur une plaquette de silicium lavée avec de l'acétone, de l'éthanol et de l'eau déminéralisée (6 × 6 mm 2 en taille). Ensuite, la plaquette de silicium avec des gouttelettes de GNR a été placée à 21°C et une humidité de 85 % pour s'évaporer lentement. Après 72 h, des réseaux verticaux GNR côte à côte ont été obtenus. D'après des rapports précédents, nous avons utilisé la « croissance induite par les semences » pour synthétiser les GNR [23, 24].
La figure 2a montre le spectre d'absorption ultraviolet-visible normalisé du GNR. On observe les deux pics d'absorption du GNR, qui sont attribués au pic longitudinal à 690 nm et au pic transversal à 520 nm. De manière générale, le pic d'absorption longitudinal correspondant aux GNR longs est décalé vers le rouge. Dans une certaine plage, le rapport hauteur/largeur des GNR peut être ajusté en modifiant la quantité de nitrate d'argent [23]. Le « SEM en médaillon » dans le coin supérieur droit de la figure 2a montre que les GNR ont une bonne apparence. Nous utilisons CTAB comme tensioactif pour préparer des GNR d'une longueur d'environ 69 ± 5 nm, d'une largeur d'environ 24 ± 2 nm et d'un rapport d'aspect d'environ 3. De nombreuses recherches antérieures ont rapporté que les GNR avec un rapport d'aspect relativement petit peuvent favoriser la formation de réseaux verticaux [28]. La figure 2b montre une image SEM d'une monocouche de GNR auto-assemblés verticalement formée sur une plaquette de silicium, et la figure 2c révèle que les GNR sont auto-assemblés avec succès sur la surface de la plaquette de silicium et ont une bonne reproductibilité sur une grande surface. Le substrat de réseau à grande surface offre des conditions favorables pour le développement spectral ultérieur. L'anisotropie des GNR peut être clairement observée à partir de la figure 2d, indiquant que les GNR sont perpendiculaires à la surface de la plaquette de silicium, et la structure compacte hexagonale est obtenue (marquée par des lignes rouges). La distance d'espacement interne entre deux nanotiges adjacentes dans des réseaux verticaux est d'environ 3 nm, ce qui est attribué à la longueur du tensioactif cationique à double couche CTAB, et est suffisante pour générer des « points chauds » [30, 31]. En raison de l'épinglage de la ligne de contact, les GNR sont poussés vers le bord de la gouttelette pour former un motif d'anneau de café sous un écoulement capillaire vers le bord, comme le montre la figure 2e. Cependant, une grande surface de matrices verticales GNR peut être obtenue dans l'échantillon de « tache de café » en raison du recul de la ligne de contact, comme le montre la figure 2f, ce qui est cohérent avec les rapports précédents [14, 28].

un Le spectre d'absorption ultraviolet-visible du GNR. b –d Les images SEM typiques des réseaux verticaux GNR. e , f Correspond aux images SEM des anneaux de café et des échantillons de taches de café
Amélioration du spectre avec la matrice verticale GNR
Fait intéressant, nous découvrons initialement que les intensités Raman des molécules de Rh6G ont de grands changements à mesure que le temps de trempage augmente. Nous avons effectué les tests plusieurs fois et sélectionné le pic Raman de Rh6G à 1650 cm −1 comme norme de référence. Ces résultats obtenus sont présentés sur les figures 3a et b, ce qui indique que l'effet d'amélioration Raman est optimal avec un temps de trempage de 30 min. Nous avons remplacé les molécules Rh6G par CV et répété l'expérience. Les signaux Raman de CV sont également donnés sur les figures 3c et d, qui révèlent que la tendance des signaux Raman des molécules CV est similaire à celle des molécules Rh6G pour un trempage de 30 min. Sur la base de ce phénomène expérimental, nous soupçonnons que le réseau GNR s'est effondré lorsque le substrat est trempé pendant 60 min et cela peut être causé par l'affaiblissement de la force de répulsion électrostatique et l'interaction d'épuisement entre les nanotiges et les substrats après la dissolution du CTAB. Nous avons utilisé le SEM pour caractériser des substrats avec différents temps de trempage.
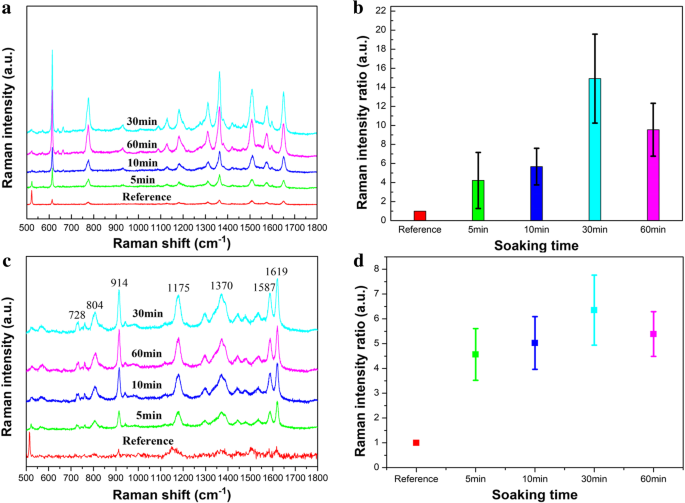
un Spectres Raman de 10 -7 M Rh6G sur le substrat de réseau vertical GNR avec différents temps de trempage. b Rapport d'intensité Raman du pic à 1650 cm −1 sur le substrat du réseau vertical GNR avec des temps de trempage différents. c Spectres Raman de 10 −6 M CV sur le substrat du réseau vertical GNR avec différents temps de trempage. d Rapport d'intensité Raman du pic à 1619 cm −1 sur le substrat du réseau vertical GNR avec différents temps de trempage
On peut voir à partir de la figure 4 que la morphologie du réseau vertical GNR change à peine de manière significative à mesure que le temps de trempage augmente ; cependant, les réseaux GNR se sont effondrés et sont devenus désordonnés lorsque le temps de trempage du substrat est de 60 min. Sur la base de la figure 4, le spectre Raman est expliqué comme suit :Pendant la période de pré-trempage, les réseaux sont relativement stables. Les molécules de Rh6G adsorbées à la surface des réseaux verticaux GNR augmentent également avec l'augmentation du temps de trempage. Sous l'irradiation laser, les « points chauds » à la surface des réseaux ou dans les lacunes des nanotiges d'or peuvent améliorer les signaux Raman des molécules cibles. Néanmoins, les intensités des signaux Raman des molécules sondes sur le substrat désordonné sont faibles en raison du nombre de « points chauds » entre les nanotiges adjacentes diminue, afin de mieux comprendre l'influence de la distribution du champ électromagnétique local de la verticale GNR. puces sur le SERS de la molécule cible.

un –d Images SEM de matrices GNR avec différents temps de trempage. Le temps de trempage des matrices GNR est de 5 min, 10 min, 30 min et 60 min, respectivement
Comme le montre la figure 5, nous avons utilisé la FEM pour simuler le champ électromagnétique local du substrat sous une irradiation laser de 532 nm. La lumière incidente est polarisée circulairement et est transmise le long du z -axe perpendiculaire au xy avion. On peut clairement voir à partir de la figure 5b que le réseau GNR présente un excellent effet d'amélioration du champ électromagnétique local par rapport au substrat désordonné. Sur la base du mécanisme de champ électromagnétique, la formule SERS d'amélioration du champ électromagnétique est donnée comme suit [32] :
$$ {\left|{M}_{\mathrm{EM}}\left({\lambda}_{\mathrm{L}},\lambda, {d}_{\mathrm{av}}\right) \right|}^2={\left|\frac{E_{\mathrm{loc}}\left({\lambda}_{\mathrm{L}},{d}_{\mathrm{av}}\ right)}{E_{\mathrm{in}}\left({\lambda}_{\mathrm{L}}\right)}\right|}^2\ast {\left|\frac{E_{\mathrm {loc}}\left(\lambda, {d}_{\mathrm{av}}\right)}{E_{\mathrm{in}}\left(\lambda \right)}\right|}^2={\left|{M}_1\left({\lambda}_{\mathrm{L}},{d}_{\mathrm{av}}\right)\right|}^2{\left|{M }_2\left(\lambda, {d}_{\mathrm{av}}\right)\right|}^2 $$ (1)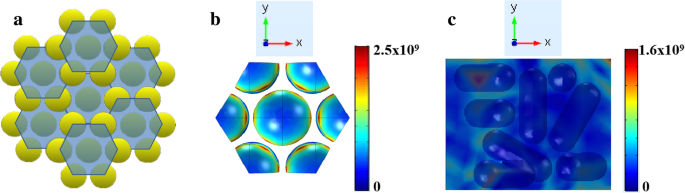
un Modèle de simulation de réseau hexagonal GNR. b Résultats de simulation de champ électromagnétique local de réseaux verticaux GNR. c Distribution locale du champ électromagnétique des GNR désordonnés
où, |M EM | 2 est le facteur d'amélioration du champ électromagnétique total, et |M 1 | 2 et |M 2 | 2 sont les facteurs d'amélioration du champ électromagnétique induits par le couplage par résonance plasmon et le couplage lumière-plasmon de diffusion Raman de la lumière incidente, respectivement. λ L et λ sont respectivement les longueurs d'onde de la lumière incidente et de la lumière émise. De plus, d av est la distance moyenne des molécules à la surface du métal. E dans et E loc sont l'intensité du champ lumineux incident et le champ local. |M EM | 2 est à peu près proportionnel à la quatrième puissance du renforcement du champ électrique sans la propriété vectorielle du champ et la propriété tensorielle de la polarisation Raman. Par conséquent, par rapport au substrat désordonné, le champ électromagnétique local autour des réseaux GNR est relativement fort et les « points chauds » denses peuvent améliorer l'activité SERS du substrat. Le résultat est presque cohérent avec l'expérience de notre inférence. Ainsi, dans des expériences ultérieures, tous les substrats de la matrice GNR ont été trempés dans la solution de molécule sonde pendant 30 min.
Afin d'évaluer efficacement les performances du Raman amélioré par le substrat, nous avons utilisé la molécule Rh6G comme cible détectée dans les tests spectraux Raman. Sur la base du temps de trempage optimal ci-dessus, la plaquette de silicium avec les réseaux verticaux GNR a été immergée dans la solution moléculaire de la sonde pendant 30 min. Après le trempage, la plaquette de silicium a été rincée à l'éthanol et séchée. Nous mesurons les spectres Raman des molécules sondes avec une longueur d'onde d'excitation de 532 nm. Premièrement, les spectres de Rh6G sont donnés sur la figure 6a, ce qui indique que les signaux Raman de Rh6G déposés sur les réseaux verticaux sont efficacement améliorés. De la plage de 500 à 1800 cm −1 , le Raman culmine à 613 cm −1 , 774 cm −1 , 1185 cm −1 , 1311 cm −1 , 1360 cm −1 , 1508 cm −1 , et 1650 cm −1 peut être clairement vu, ce qui est cohérent avec les rapports précédents [33]. Les signaux Raman de Rh6G diminuent à mesure que la concentration diminue. La sensibilité de détection du substrat se détériore lorsque la concentration de Rh6G est ajustée à 10 −11 M. Maintenant, seuls ces pics Raman à 613 cm −1 , 1360 cm −1 , 1508 cm −1 , et 1650 cm −1 peut être observé, ce qui indique que le substrat du réseau vertical GNR présente une sensibilité élevée. Les signaux de diffusion Raman des molécules cibles Rh6G sont renforcés par le champ électromagnétique localisé entre les espaces des nanotiges adjacentes. Le spectre Raman de 10 −3 M Rh6G est également représenté sur la figure 6b. Ici, nous évaluons le facteur d'amélioration (EF) du substrat SERS [34] :
$$ \mathrm{EF}=\frac{{\mathrm{I}}_{\mathrm{SERS}}/{\mathrm{I}}_{\mathrm{Ref}}}{{\mathrm{C} }_{\mathrm{SERS}}/{\mathrm{C}}_{\mathrm{Ref}}} $$ (2)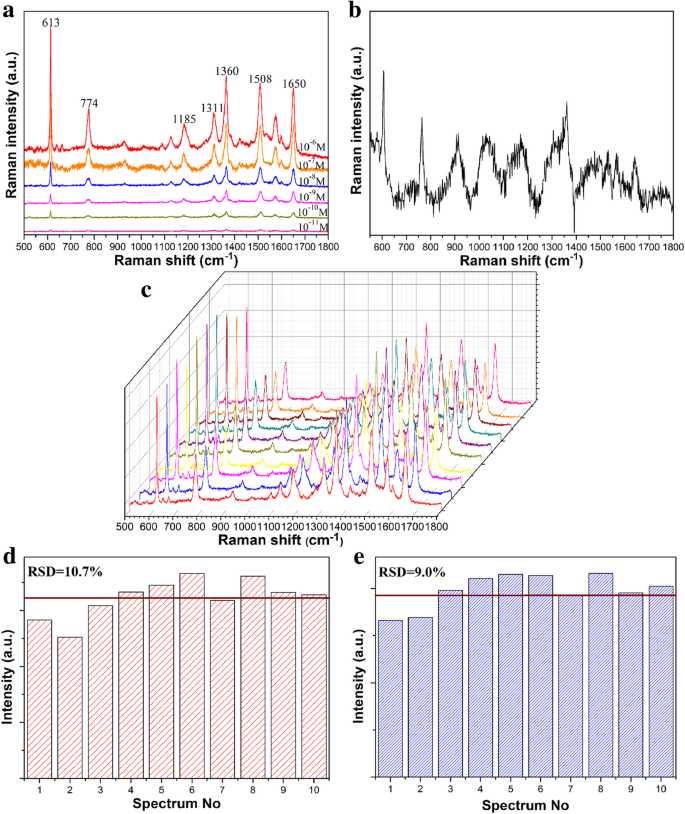
un Spectres Raman de Rh6G sur le substrat du réseau vertical GNR de 10 −6 à 10 −11 M, respectivement. b Le spectre Raman de 10 −3 M Rh6G sur substrat silicium. c Spectres Raman de Rh6G avec une concentration de 10 −7 M. d , e Distribution d'intensité des pics à 1360 cm −1 et 774 cm −1 pour le Rh6G avec une concentration de 10 −7 M à partir de 10 lots différents de substrats à matrice verticale GNR
C SERS et C Réf sont la concentration de Rh6G dans le substrat SERS (10 −10 M) et la référence (10 −3 M), respectivement. Je SERS et Je Réf sont les intensités SERS des réseaux GNR après trempage des signaux Rh6G et Raman de référence, respectivement. Les intensités du pic Raman à 613 cm −1 des Rh6G sont calculés que I SERS /Je Réf , C SERS /C Réf , et les EF sont d'environ 0,0965, 10 −7 , et 9,65 × 10 5 , séparément. L'EF calculé dans nos expériences est cohérent avec l'amplitude rapportée dans la littérature pour le substrat auto-assemblé [17, 35, 36].
En général, le substrat a non seulement une bonne sensibilité mais également une excellente reproductibilité pour les applications SERS. Afin de présenter la bonne reproductibilité, nous sélectionnons au hasard 10 points du substrat déposé sur les molécules de Rh6G. Comme le montre la figure 6c, les pics Raman de Rh6G sont cohérents avec ceux de la figure 6a. Les pics Raman de Rh6G à différentes positions ne sont pas déplacés. De plus, l'écart type relatif (RSD) du pic Raman, en tant que paramètre important, est utilisé pour évaluer la qualité de la reproductibilité du substrat. Ici, la formule d'écart relatif peut être exprimée sous la forme RSD =SD/I m [37], où SD est l'intensité de l'écart type du pic et I m est l'intensité Raman moyenne du pic principal. Nous calculons les valeurs RSD des pics Raman à 1362 cm −1 et 774 cm −1 des 10 points statistiques, respectivement. Les valeurs RSD sont d'environ 10,7 % et 9,0 % sur les figures 6d et e, respectivement, ce qui indique que la propriété SERS des réseaux verticaux GNR a une excellente reproductibilité.
La stabilité est utilisée comme un autre facteur important pour évaluer la qualité des substrats SERS. Afin de vérifier le substrat avec une stabilité élevée, comme le montre la Fig. 7a, spectres Raman de Rh6G avec la concentration de 10 −7 M sur substrat vertical GNR sont donnés après 30 jours et 60 jours. Avec le temps, les intensités du signal SERS des molécules Rh6G diminuent dans une certaine mesure après 30 et 60 jours en raison de la perte d'activité SERS. Cependant, les signaux Raman des molécules Rh6G sur le substrat ne sont évidemment pas atténués. Les intensités et le décalage Raman des pics caractéristiques à 774 cm −1 et 1360 cm −1 sont comptés sur la figure 6b pour les différentes périodes, respectivement. Même si le substrat imbibé de Rh6G est exposé à l'air pendant 60 jours, Rh6G sur le substrat maintient toujours un bon signal SERS. Pour le pic à 774 cm −1 , la perte des signaux Raman de Rh6G est d'environ 5,4% et 9,3% après 30 jours et 60 jours. Pour le pic à 1360 cm −1 , la perte de signaux Raman de Rh6G est d'environ 5,3 % et 11 %, respectivement. Combiné avec les rapports précédents [38, 39], on peut considérer que les réseaux verticaux GNR actuels ont une bonne stabilité. Combinez ces avantages mentionnés ci-dessus, ce substrat possède un grand potentiel de détection et de détection.
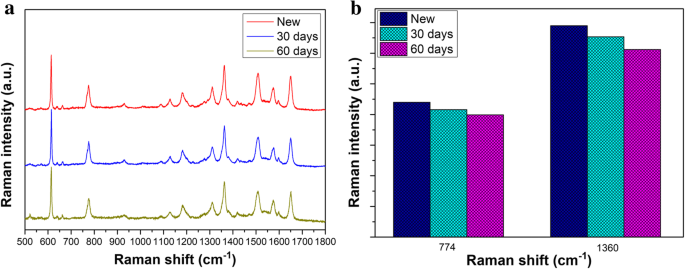
un Spectres Raman de 10 -7 M Rh6G sur le substrat du réseau vertical GNR avec des jours différents. b Comparaison avec les intensités des signaux SERS à des pics de 774 cm −1 et 1360 cm −1
Conclusion
En résumé, nous avons préparé avec succès des réseaux verticaux GNR auto-assemblés par une méthode d'évaporation. Plus important encore, nous avons constaté que la morphologie des réseaux verticaux GNR peut être régulée en modifiant le temps de trempage pour un bon effet d'amélioration Raman. Sur la base de la théorie du champ EM, nous avons utilisé le logiciel COMSOL pour analyser et discuter de la distribution du champ EM local du réseau vertical GNR et du substrat de désordre. Les résultats sont presque en accord avec les données expérimentales. En outre, nous avons étudié l'activité SERS du réseau vertical de GNR en fonction du temps de trempage optimal du substrat. Le substrat tel que fabriqué peut détecter la Rh6G à des concentrations aussi faibles que 10 −11 M en raison de l'amélioration du champ électromagnétique local et montre une grande reproductibilité et stabilité. Par conséquent, les réseaux verticaux GNR avec une sensibilité et une stabilité excellentes peuvent être utilisés pour la détection d'espèces, la détection et d'autres domaines.
Abréviations
- CTAB :
-
Bromure de cétyltriméthylammonium
- CV :
-
Violet cristal
- FEM :
-
Méthode des éléments finis
- GNR :
-
Nanotiges d'or
- Rh6G :
-
Rhodamine 6G
- RSD :
-
Écart type relatif
- SEF :
-
Fluorescence augmentée en surface
- SEM :
-
Microscope électronique à balayage
- SERS :
-
Diffusion Raman améliorée en surface
- Si :
-
Plaquettes de silicium
- SPR :
-
Résonance plasmonique de surface
Nanomatériaux
- Application du tungstène et des alliages de tungstène
- Nanotiges en or revêtues de BSA pour la thérapie photothermique NIR-II
- Revue sur l'application des biocapteurs et des nanocapteurs dans les agroécosystèmes
- Modulation des propriétés d'anisotropie électronique et optique du ML-GaS par champ électrique vertical
- Synthèse facile et propriétés optiques de petits nanocristaux et nanotiges de sélénium
- Fabrication par lots de microlentilles planes métalliques à large bande et de leurs réseaux associant l'auto-assemblage de nanosphères à la photolithographie conventionnelle
- Réglage de la chimie de surface du polyétheréthercétone par revêtement d'or et traitement au plasma
- Nanohélices d'or déposées obliquement sur des surfaces préparées sans lithographie nanoensemencées
- Synthèse de nanocristaux de ZnO et application dans des cellules solaires polymères inversées



