Formation de sphères de carbone monodispersées avec une taille ajustable via la synthèse assistée par copolymère tribloc et leurs propriétés de condensateur
Résumé
Une méthode de polymérisation hydrothermale facile a été développée pour la préparation de sphères de carbone monodispersées (MCS) en utilisant le copolymère tribloc F108 comme tensioactif. La synthèse est basée sur la réaction de polymérisation catalysée par l'ammoniac entre le phénol et le formaldéhyde (PF). Les MCS résultants ont une morphologie sphérique parfaite, une surface lisse et une grande dispersité. Les tailles de particules peuvent être réglées dans une large gamme de 500 à 2400 nm en ajustant le dosage du précurseur PF. Les MCS activés avec des hétéroatomes appropriés (N et O) dopés et une grande surface spécifique (960 m 2 g− 1 ) ont été obtenus. Une électrode haute performance de condensateurs électriques à double couche fabriqués par ces matériaux actifs ont une excellente capacité spécifique (310 F g −1 à 0,5 A g −1 ) et une stabilité de cycle exceptionnelle (rétention de capacité de 92 % après 10 000 cycles). Ce travail offre une nouvelle opportunité pour la fabrication de MCS avec des applications potentielles.
Introduction
Au cours des dernières décennies, les matériaux carbonés poreux ont été largement utilisés dans les domaines du stockage de gaz [1], des supports de catalyseurs [2], des supercondensateurs [3], des batteries lithium-ion [4], des cellules solaires [5] et de l'électronique. dispositifs [6] en raison de leurs avantages tels que la surface spécifique élevée, la bonne conductivité électrique et la stabilité chimique élevée. Du point de vue de la chimie des matériaux, des matériaux carbonés poreux de morphologie et de structure différentes tels que les aérogels de carbone [7], les fibres [8], les nanotubes [9], les nanosphères [10] et le charbon actif [11] ont été synthétisés avec succès. Récemment, les sphères de carbone monodispersées (MCS) ont fait l'objet d'études considérables sur les matériaux d'électrode fonctionnels pour les dispositifs de stockage et de conversion d'énergie en raison de leurs propriétés uniques telles qu'une densité d'empilement élevée, un chemin de diffusion ionique court inhérent et une bonne stabilité structurelle [12, 13]. Le contrôle précis de la morphologie, de la dispersion, de la surface lisse et de la taille des particules des MCS a été la clé pour répondre aux exigences de certaines applications pratiques spéciales [14].
La carbonisation de sphères polymères de résine phénolique pré-synthétisées avec une excellente stabilité thermique s'est avérée être une approche privilégiée pour la préparation de MCS. Le groupe Zhao a signalé une voie hydrothermale à faible concentration pour synthétiser des sphères de carbone mésoporeuses ordonnées hautement uniformes avec une taille ajustable de 20 à 140 nm en utilisant du résol phénolique comme précurseur de carbone [15]. En associant intelligemment le mécanisme de réaction de polymérisation par hydrolyse des résines résorcinol-formaldéhyde aux sphères de silice classiques de Stöber, Liu et ses co-chercheurs ont développé avec succès une extension de la méthode Stöber pour la synthèse de MCS avec une taille uniforme et contrôlable à l'échelle submicrométrique [16 ]. Sur la base de la chimie de la benzoxazine, Lu et ses collègues ont établi une nouvelle façon de synthétiser des MCS à haute dispersité avec des tailles adaptées dans la plage de 95 à 225 nm sous des températures de réaction programmées avec précision [17]. Après ces travaux révolutionnaires, une attention considérable a été accordée à la conception et à la synthèse des MCS [18,19,20,21]. Cependant, la plupart de ces approches nécessitent des processus de traitement hydrothermique fastidieux ou ne peuvent pas préparer une large granulométrie réglable avec une surface lisse et une distribution granulométrique étroite. Par conséquent, la synthèse de MCS de grande taille réglable, hautement uniformes et morphologiques clairement définis reste un grand défi.
Dans ce travail, nous proposons une méthode hydrothermale facile pour la préparation de MCS en utilisant le copolymère tribloc Pluronic F108 comme tensioactif basé sur la réaction de polymérisation catalysée par l'ammoniac du phénol et du formaldéhyde (PF). Le mécanisme de formation détaillé des MCS a été discuté. Les MCS tels que préparés ont une morphologie sphérique parfaite et une surface lisse et sont très uniformes. Les tailles de particules des MCS peuvent être réglées dans une large plage de 500 à 2400 nm en fonction de la concentration du précurseur PF. Lorsqu'ils sont utilisés comme matériaux d'électrode pour les supercondensateurs, les MCS activés présentent d'excellentes performances électrochimiques en raison du codopage à l'azote et à l'oxygène et de la surface spécifique élevée.
Méthodes
Synthèse des MCS
Dans une synthèse typique, 0,5 ml d'ammoniac aqueux (25 % en poids) a été mélangé avec 30 ml d'éthanol et 50 ml d'eau déminéralisée (H2 O). Ensuite, 10 mg de copolymère tribloc Pluronic F108 (Mw =14 600, PEO132 -PPO50 -PEO132 ) a été dissous dans la solution de mélange. Ensuite, 0,2 ml de phénol et 0,2 ml de formaldéhyde (37% en poids) ont été ajoutés respectivement, sous agitation douce pendant 30 min. Enfin, la solution résultante a été transférée dans un autoclave revêtu de téflon de 100 ml et la réaction hydrothermique a été régulée à 160 °C pendant 3 h. Les sphères de polymère de résine PF résultantes ont été obtenues par lavage avec H2 O et de l'éthanol plusieurs fois. Ensuite, les MCS-x ont été obtenus en recuit les sphères de résine PF sous N2 atmosphère à 600 °C pendant 3 h, « x » désigne le dosage de phénol et de formaldéhyde utilisé (par exemple 0,2, 0,4, 0,6 et 0,8 font référence à 0,2, 0,4, 0,6 et 0,8 ml de phénol et de formaldéhyde, respectivement). Les MCS-x ont ensuite été activés chimiquement par KOH (dans un rapport massique de 1:2) à 700 °C pendant 1 h dans un N2 ambiance pour préparer les aMCS-x.
Caractérisation
La microscopie électronique à balayage (MEB) a été réalisée sur un instrument NovaNanoSEM230. La microscopie électronique à transmission (MET) a été réalisée sur un instrument Tecnai G2 F20 S-TWIX. Les diagrammes de diffraction des rayons X (XRD) ont été réalisés avec un diffractomètre SIEMENS D500 avec un rayonnement Cu Kα (λ =0,15056 nm). La spectroscopie Raman a été réalisée sur un système LabRAMHR-800. L'analyse par spectroscopie photoélectronique à rayons X (XPS) a été réalisée sur un instrument ESCALAB 250Xi. Les isothermes d'adsorption-désorption d'azote ont été mesurées à 77 K sur un instrument ASAP 2020.
Mesure électrochimique
Le test électrochimique de voltamétrie cyclique (CV), de charge/décharge galvanostatique (GCD) et de spectroscopie d'impédance électrochimique (EIS) a été réalisé sur le poste de travail électrochimique CHI660E avec un système à trois électrodes dans une solution d'électrolyte KOH 6 M. La feuille de platine et Hg/HgO ont été utilisés comme contre-électrode et électrode de référence, respectivement. Les électrodes de travail ont été fabriquées par le mélange d'aMCS-x, de polytétrafluoroéthylène (60 % en poids) et de noir d'acétylène avec une proportion en masse de 8:1:1. La capacité spécifique à la gravimétrie a été calculée par l'équation suivante :
$$ Cg=\frac{I\Delta t}{m\Delta V} $$ (1)où je (A), t (s), V (V), et m (g) sont respectivement le courant appliqué, le temps de décharge, la fenêtre de potentiel et la masse de matière active des électrodes.
Résultats et discussion
Dans cette étude, nous présentons un mécanisme de synthèse possible des MCS dans le schéma 1. L'étape I est le processus sol-gel. Dans le chemin a, les gouttelettes d'émulsion se sont formées par l'interaction de liaison hydrogène entre le phénol, le formaldéhyde, la molécule d'ammoniac, l'éthanol et l'eau [16]. Les molécules d'ammoniac catalysent la polymérisation du PF qui a lieu depuis l'intérieur des gouttelettes d'émulsion [22]. De plus, un grand nombre d'unités PF à substitution hydroxyméthyle sont produites par réaction rapide du phénol et du formaldéhyde, qui sont positionnés à la surface externe des gouttelettes d'émulsion en raison de l'interaction électrostatique avec les ions ammoniac. Simultanément, le chemin b montre le processus d'autoformation des micelles F108 formées par des monomères F108 de copolymère tribloc, qui sont les blocs PPO hydrophobes pour former le noyau à l'intérieur et les segments PEO hydrophiles à l'extérieur [23]. Ensuite, dans le chemin c, d'abondantes gouttelettes d'émulsion/espèces PF hydroxyméthyl-substituées peuvent interagir avec les segments PEO hydrophiles des micelles F108 via une interaction de liaison hydrogène pour former l'émulsion colloïdale [24]. Dans l'étape II, dans des conditions de traitement hydrothermal douces, les espèces sont destinées à une polymérisation réticulée supplémentaire et donnent des sphères uniformes de résine PF/copolymère F108. Enfin, à l'étape III, les sphères résine PF/copolymère F108 sont suivies d'une carbonisation à haute température pour obtenir les MCS.
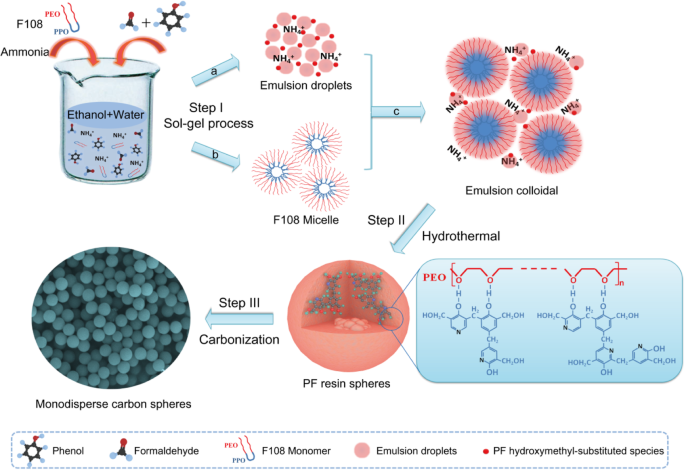
Le processus de synthèse des MCS
Les images SEM de MCS préparées à différentes doses de PF montrées sur la figure 1a–d démontrent que les MCS ont une morphologie sphérique parfaite avec une taille uniforme. Les images MET présentes sur la figure 1e–h confirment en outre que les MCS ont des particules sphériques, une surface lisse et une forte dispersité. Le diamètre moyen des particules a augmenté de 500 à 2400 nm avec l'augmentation du dosage du précurseur PF de 0,2 à 0,8 ml, comme le montre la figure 1i–l. En effet, la concentration croissante du précurseur PF a conduit à des gouttelettes d'émulsion et colloïdales de plus grande taille et a entraîné un diamètre final de MCS plus important. L'utilisation d'ammoniac dans ce système est essentielle à la synthèse réussie de ces MCS hautement dispersifs, qui peuvent fournir le NH4 + pour adhérer à la surface des sphères PF et inhiber l'agrégation. Il est à noter que les MCS étaient sans aucun défaut de surface évident et effondrement de la structure après carbonisation à haute température. C'est le principal avantage de la réaction de réticulation élevée entre le phénol et le formaldéhyde. De plus, nous avons également étudié le rôle du copolymère tribloc F108 dans ce système. Fichier complémentaire 1 :La figure S1a présente l'image MEB des sphères de carbone obtenues en l'absence de F108. Les produits ont une granulométrie non uniforme et rencontrent une agglomération. De plus, la taille des particules diminue systématiquement avec l'augmentation du dosage de F108 de 20 à 80 mg, et de petites particules et substances floconneuses apparaissent à la surface des sphères de carbone et rencontrent finalement une grande conglutination (Fichier supplémentaire 1 :Figure S1b~d). La raison en est que lorsque le copolymère tribloc F108 est suffisant dans le système, la tension superficielle diminue, une interaction de réticulation plus forte se produit et des gouttelettes d'émulsion et des sphères de carbone de plus petite taille se forment. Cependant, une concentration appropriée en F108 peut équilibrer la tension superficielle et les forces d'interaction de réticulation et obtenir une surface lisse et des sphères de carbone de taille uniforme. De plus, l'effet de la concentration de F108 sur les propriétés des électrodes des MCS a également été étudié, comme le montre le fichier supplémentaire 1 :Figure S2. Le résultat révèle que le copolymère tribloc F108 a joué le rôle d'agent tensioactif pour la formation de MCS.
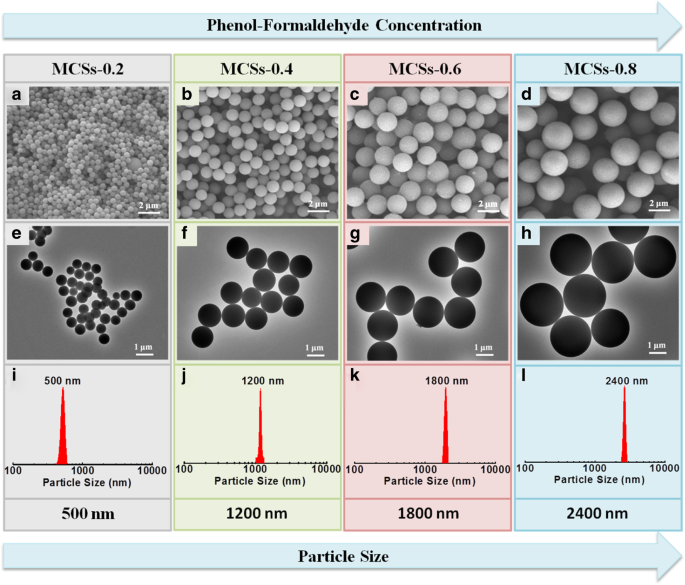
Images SEM et MET de MCS préparées à différentes doses de phénol et de formaldéhyde de a , e 0,2 ml, b , f 0,4 ml, c , g 0,6 ml, et d , h 0,8 ml, respectivement. je –l La distribution granulométrique des MCS correspondant aux images SEM (a –d )
Ces MCS synthétisés peuvent avoir des applications potentielles telles que la catalyse, l'adsorption et les matériaux d'électrode pour les supercondensateurs et les batteries lithium-ion. Afin de comprendre la propriété de structure du matériau tel que préparé, l'aMCS-0.4 a été sélectionné comme échantillon utilisé pour l'analyse de caractérisation. Comme le montre la figure 2a, le motif XRD de aMCS-0.4 affiche deux larges pics de diffraction évidents à 25° et 43°, correspondant aux plans de réseau (002) et (100) du matériau de carbone amorphe, respectivement. Il indique également la conversion complète de la résine PF en matériau carboné et la quasi-élimination du copolymère tribloc F108 après carbonisation. Le spectre Raman de l'aMCS-0.4 (Fig. 2b) présente deux pics typiques à 1337 cm −1 (bande D) et 1590 cm −1 (bande G), qui correspondent respectivement aux défauts cristallins et à la propriété graphitique hexagonale des matériaux carbonés. Le rapport d'intensité (I D /Je G ) des matériaux carbonés reflète le degré de graphitisation [25]. Le Je D /Je G la valeur de l'aMCSs-0,4 est d'environ 0,88, ce qui corrobore également les structures amorphes.
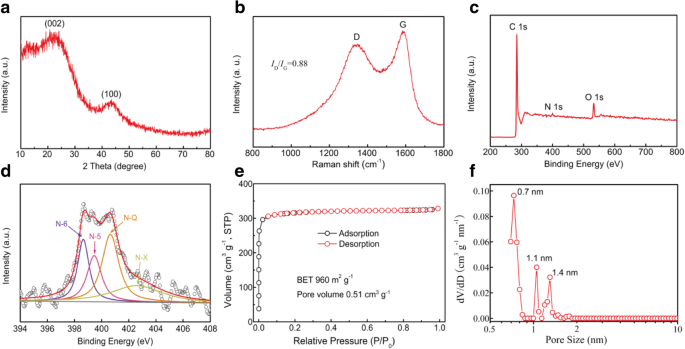
un modèle XRD. b spectres Raman. c Spectre d'enquête XPS. d Spectres N 1s haute résolution. e Isothermes d'adsorption/désorption d'azote. f Courbe de distribution de la taille des pores du matériau aMCS-0.4
Comme le montre la figure 2c, le relevé XPS de l'aMCS-0,4 présente trois pics de C 1 (285,2 eV), N 1 (400,1 eV) et O 1 (532,7 eV). Les compositions élémentaires de C, N et O dans aMCS-0,4 sont respectivement de 92,54 at%, 1,04 at% et 6,42 at%. Les résultats suggèrent que l'ammoniac peut agir comme une source d'azote pour introduire l'élément N dans les charpentes carbonées. La figure 2d affiche le spectre N 1s haute résolution de aMCS-0.4. Quatre pics de type à 398,6 eV, 399,4 eV, 400,6 eV et 402,4 eV sont corrélés aux pyridinique-N (N-6), pyrrolique-N (N-5), quaternaire-N (NQ) et pyridine-N-oxydes (NX), respectivement [10]. Généralement, la présence de groupes fonctionnels à base d'azote peut non seulement contribuer à la pseudocapacité d'addition, mais peut également améliorer la mouillabilité de surface et la conductivité électrique des matériaux carbonés, et ainsi améliorer les performances électrochimiques [3, 26].
Le N2 des mesures d'adsorption/désorption ont été menées pour étudier les surfaces spécifiques et la structure des pores internes des matériaux préparés. Comme le montre la figure 2e, l'isotherme de l'aMCS-0.4 appartient à une courbe de type I typique avec une forte absorption à de faibles pressions relatives, et un plateau presque horizontal à des pressions relatives plus élevées révèle la structure microporeuse. Les surfaces BET et le volume poreux total des aMCS-0,4 sont déterminés à 960 m 2 g −1 et 0,51 m 3 g −1 , respectivement. La courbe de distribution de la taille des pores de l'aMCS-0,4 est illustrée à la figure 2f, qui présente la structure des micropores avec des diamètres de 0,7 nm, 1,1 nm et 1,4 nm. L'image MET haute résolution (Fichier supplémentaire 1 :Figure S3) est également en bon accord avec ce résultat. Les structures carbonées microporeuses sont générées à partir de la décomposition du F108 lors de la carbonisation et de l'activité chimique du KOH [27, 28].
Ici, nous utilisons les aMCS-0.4 comme matériaux d'électrode pour les condensateurs électriques à double couche (EDLC) afin de démontrer leurs avantages structurels et de performance. Les courbes CV de l'électrode aMCS-0.4 présentent des formes rectangulaires à différentes vitesses de balayage de 10 à 100 mV s -1 (Fig. 3a), et les courbes GCD affichent des profils triangulaires typiques (Fig. 3b). Ceux-ci révèlent que les matériaux aMCS-0.4 ont une performance EDLC parfaite. Comme le montre la figure 3c, l'électrode aMCS-0.4 présente une excellente capacité spécifique de 310 F g −1 à une densité de courant de 0,5 A g −1 , ce qui est plus élevé que d'autres électrodes MCS similaires [12,13,14]. La capacité spécifique élevée bénéficie des grandes surfaces et des hétéroatomes dopés. De plus, la capacité spécifique maintient toujours 200 F g −1 même à une densité de courant élevée de 20 A g −1 ; il présente une bonne rétention de capacité. Les comportements de transport de charge et de cinétique de transfert peuvent être examinés par EIS. Le tracé de Nyquist de l'électrode aMCS-0.4 (Fig. 3d) présente une petite résistance interne (0,45 ) et une résistance de transfert de charge (0,12 ) révélant la conductivité électronique élevée des matériaux aMCS-0.4 préparés et une bonne interface de contact électrode/électrolyte . La ligne presque verticale dans la région des basses fréquences suggère que l'électrode aMCS-0.4 a une propriété de condensateur idéale et une diffusion efficace des ions électrolytiques. Ce résultat a été confirmé par les tracés de Bode (Fig. 3e), qui affichent l'angle de phase (− 80,5°) proche de - 90°. De plus, l'électrode aMCSs-0,4 présente une bonne stabilité de cycle avec une rétention de 92 % sur 10 000 cycles à une densité de courant de 20 A g −1 (Fig. 3f). Par conséquent, d'en haut, tous les résultats mettent clairement en évidence les applications potentielles attrayantes des MCS pour les électrodes des EDLC.
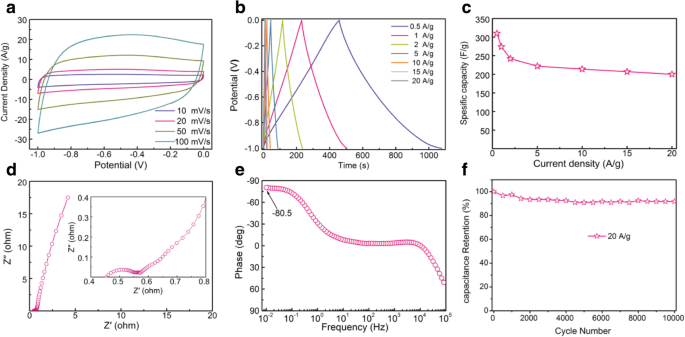
Les caractéristiques électrochimiques de l'électrode aMCS-0.4. un Courbes CV à différentes vitesses de balayage de 10 à 100 mV s −1 . b Courbes GCD à différentes densités de courant de 0,5 à 20 A g −1 . c Capacité spécifique en fonction des densités de courant. d Le tracé de Nyquist et l'encart montrent les tracés d'agrandissement à une plage de hautes fréquences. e intrigue de Bode. f Performances de cyclisme à une densité de courant de 20 A g −1 pour 10 000 cycles
Conclusions
En résumé, nous avons démontré une méthode hydrothermale assistée par surfactant facile pour synthétiser efficacement les MCS. Les MCS préparés ont une morphologie sphérique parfaite, une taille uniforme, une surface lisse et des tailles de particules réglables dans une large gamme de 500 à 2400 nm. En particulier, cette méthodologie permet aux aMCS-0.4 d'avoir des caractéristiques structurelles uniques avec une grande surface (960 m 2 g −1 ) et une fonctionnalité de surface appropriée de N et O co-dopé. Une électrode haute performance d'EDLC a été fabriquée en utilisant l'aMCS-0.4 comme matériau actif qui a fourni une excellente capacité spécifique (310 F g −1 à 0,5 A g −1 ) et une stabilité de cycle exceptionnelle (rétention de capacité de 92 % après 10 000 cycles). Cette recherche offre une nouvelle opportunité pour la fabrication de MCS avec des applications potentielles.
Abréviations
- CV :
-
Voltamétrie cyclique
- EDLC :
-
Condensateurs électriques double couche
- EIS :
-
Spectroscopie d'impédance électrochimique
- GCD :
-
Charge/décharge galvanostatique
- MCS :
-
Sphères de carbone monodispersées
- PF :
-
Phénol et formaldéhyde
Nanomatériaux
- Synthèse facile et propriétés optiques de petits nanocristaux et nanotiges de sélénium
- Composite hybride nanostructuré silice/or-cellulose Amino-POSS par procédé Sol-Gel et ses propriétés
- Synthèse et propriétés électrochimiques des matériaux cathodiques LiNi0.5Mn1.5O4 avec dopage composite Cr3+ et F− pour batteries lithium-ion
- Synthèse de points quantiques de sulfure d'antimoine solubles dans l'eau et de leurs propriétés photoélectriques
- Synthèse facile d'oxyde d'étain mésoporeux semblable à un trou de ver via l'auto-assemblage induit par l'évaporation et les propriétés de détection de gaz améliorées
- Effet de la méthode de synthèse des nanoparticules de manganite La1 − xSr x MnO3 sur leurs propriétés
- Synthèse en un seul pot de nanoplaques Cu2ZnSnSe4 et leur activité photocatalytique induite par la lumière visible
- Synthèse écologique et facile de nanofils de Co3O4 et leur application prometteuse avec du graphène dans les batteries lithium-ion
- Dépendance de la toxicité des nanoparticules sur leurs propriétés physiques et chimiques



