Dépôt chimique en phase vapeur de réseaux de nanotubes de carbone alignés verticalement :effets critiques des couches tampons d'oxyde
Résumé
Des nanotubes de carbone alignés verticalement (VACNT) ont été synthétisés sur différentes couches tampons d'oxyde en utilisant le dépôt chimique en phase vapeur (CVD). La croissance des VACNTs a été principalement déterminée par trois facteurs :la maturation d'Ostwald des nanoparticules de catalyseur, la diffusion souterraine de Fe et leur énergie d'activation pour la nucléation et la croissance initiale. La rugosité de surface des couches tampons a largement influencé le diamètre et la densité des nanoparticules de catalyseur après recuit, ce qui a apparemment affecté la durée de vie des nanoparticules et l'épaisseur des VACNTs préparés. De plus, la croissance des VACNTs était également affectée par la température de dépôt, et la durée de vie des nanoparticules de catalyseur diminuait apparemment lorsque la température de dépôt était supérieure à 600 °C en raison de leur mûrissement d'Ostwald. De plus, en plus du nombre de nanoparticules de catalyseur, la densité des VACNTs était également largement dépendante de leur énergie d'activation pour la nucléation et la croissance initiale.
Contexte
Les nanotubes de carbone alignés verticalement (VACNT) présentent de nombreuses propriétés excellentes, notamment des propriétés mécaniques extraordinaires, des caractéristiques électriques attrayantes et une conductivité thermique élevée [1,2,3]. Par conséquent, les VACNTs présentent un grand potentiel d'utilisation dans une grande variété d'applications, y compris les émetteurs de champ d'affichage, les capteurs biologiques, les dispositifs microélectroniques et les matériaux de stockage d'hydrogène et d'interface thermique [4,5,6,7,8,9,10,11 ]. Parmi les méthodes existantes, le dépôt chimique en phase vapeur (CVD) semble être le plus adapté à la croissance des VACNTs; il offre un meilleur contrôle des paramètres de croissance et de la croissance sur des sites prédéfinis d'un substrat à motifs [12,13,14,15,16,17]. Pour obtenir des VACNTs de haute qualité par CVD, des nanoparticules de catalyseur doivent être formées et empêchées de réagir avec le substrat sous-jacent [18]. Généralement, pour éviter la formation indésirable de siliciure métallique à des températures de traitement élevées, une couche tampon est généralement déposée sur le substrat avant le dépôt du catalyseur [19, 20].
De nombreux chercheurs ont découvert que la couche tampon est essentielle à la croissance des VACNTs, et différentes couches tampons montrent divers effets [21]. La croissance effective des VACNTs dépend largement du type, de la qualité en termes de porosité et de la stoechiométrie de la couche tampon [22,23,24,25]. Lee et al. ont rapporté que les couches tampons métalliques étaient inefficaces pour la croissance des VACNTs car elles ne pouvaient pas empêcher la diffusion du catalyseur dans le substrat, entraînant la formation de phases carbure ou siliciure [26]. Par rapport aux films métalliques, les films non métalliques tels que les films d'oxyde se sont avérés plus bénéfiques pour la synthèse des VACNTs. de los Arcos et al. a affirmé que, par rapport à Al, Al2 O3 a entraîné une croissance plus efficace des VACNT lorsqu'ils sont utilisés comme couche tampon [27, 28]. De plus, par rapport à SiO2 , TiO2 , et ZrO2 , Al2 O3 s'est avéré être un meilleur matériau de couche tampon pour la croissance des VACNTs lorsque Fe était utilisé comme catalyseur [29]. Bien que diverses couches tampons d'oxyde aient été introduites pour augmenter l'efficacité de croissance des VACNTs, leur rôle détaillé n'est pas clair.
Dans cet article, nous avons utilisé le CVD pour synthétiser des VACNTs avec différents films d'oxyde comme couches tampons. L'activité et la durée de vie des nanoparticules de catalyseur ont été analysées sur différentes couches tampons d'oxyde pour obtenir des VACNTs de haute qualité. Le mécanisme de croissance possible des VACNTs est également discuté.
Méthodes
SiO2 oxydé thermiquement et trois types d'Al2 O3 des films minces ont été utilisés comme couches tampons d'oxyde. L'Al2 O3 des films ont été déposés sur des substrats de Si par dépôt de couche atomique (ALD), évaporation par faisceau d'électrons (EB) et pulvérisation cathodique. Pour ALD Al2 O3 films, triméthylaluminium (TMA) et H2 O ont été utilisés comme précurseur et source d'oxygène, respectivement. La température de dépôt a été fixée à 200°C. L'épaisseur de l'Al2 O3 et SiO2 films utilisés comme couches tampons était de 20 nm. Un film de Fe de 1 nm d'épaisseur a été déposé sur chacun d'eux par évaporation EB; il a été utilisé comme catalyseur. Ensuite, les VACNTs ont été synthétisés par CVD (AIXTRON Black Magic II). Tout d'abord, de l'hydrogène a été introduit dans la chambre de réaction et la pression a été fixée à 0,2 µmbar. Avant la croissance des VACNTs, le catalyseur a été recuit à 550°C sous hydrogène. Le débit d'hydrogène a été fixé à 700 µsccm, et la période était de 3 µmin. Deuxièmement, de l'acétylène et de l'hydrogène ont été introduits simultanément dans la chambre et des VACNT ont été préparés sur des nanoparticules de catalyseur. Les débits d'acétylène et d'hydrogène étaient respectivement de 100 et 700 µsccm. La température de croissance a été augmentée de 500 à 650°C, et la période de croissance a été fixée à 30 min.
La résine époxy (412813) a été achetée auprès de Sigma-Aldrich Co., Ltd. L'agent de durcissement (C1486) et le diluant (E0342) ont été achetés auprès de TCI Chemical Industrial Development Co., Ltd. Après la croissance des VACNT, les films composites VACNT/époxy ont également été préparés. Tout d'abord, la résine époxy, l'agent de durcissement et les diluants ont été mélangés en tant que matrice à l'aide d'un mélangeur à dispersion à grande vitesse (MIX500D). Deuxièmement, les VACNTs ont été immergés dans la matrice, qui a ensuite été durcie dans une étuve à vide à 120 °C pendant 1 h puis à 150 °C pendant 1 h. Les films composites obtenus ont été décollés du substrat de Si et polis à une épaisseur d'environ 300 µm. Les pointes des VACNTs dépassaient des deux surfaces du film composite.
La microscopie électronique à balayage à émission de champ (FESEM; Merlin Compact) a été utilisée pour caractériser le diamètre et la distribution des nanoparticules de catalyseur ainsi que la section transversale des VACNTs et des films composites. Les spectres Raman des VACNTs ont été enregistrés avec un spectromètre inVia Reflex, et la microscopie électronique à transmission (MET; Tecnai G2 F20 S-TWIN) a été utilisée pour caractériser la morphologie des nanotubes de carbone. La composition chimique et la densité de différentes couches tampons ont été caractérisées par spectroscopie photoélectronique aux rayons X (XPS ; ESCALAB 250Xi) et par réflectivité des rayons X (XRR ; Bruker D8 Discover), respectivement. La rugosité de surface de différentes couches tampons a été analysée par microscopie à force atomique (AFM; SPM9700). L'analyse thermique par flash laser (Netzsch LFA 447) et la calorimétrie différentielle à balayage (DSC; Mettler Toledo DSC1) ont été utilisées pour mesurer la diffusivité thermique et la capacité thermique spécifique des films composites, respectivement. La conductivité thermique a ensuite été calculée en utilisant l'Eq. 1 :
$$ \lambda =\alpha \times \mathrm{Cp}\times \rho, $$ (1)où λ , α , Cp et ρ sont la conductivité thermique (W m −1 K −1 ), diffusivité thermique (mm 2 s −1 ), capacité thermique massique (J kg −1 K −1 ), et la densité (kg m −3 ) de films composites, respectivement.
Résultats et discussion
La figure 1a–d montre les spectres Raman de VACNTs cultivés sur différentes couches tampons d'oxyde. Généralement, le pic G, qui est la vibration symétrique du mode optique et de l'expansion du plan à six anneaux, était situé à environ 1580 cm −1 [30]. Le pic D, qui est un mode de vibration causé par le bord ou le défaut du plan du microcristal, était situé à environ 1360 cm −1 [30]. De plus, le pic G′ était typiquement situé à ~ 2700 cm −1 [31]. Pour différentes couches tampons d'oxyde, le rapport de I D et Je G a été calculé comme étant approximativement égal ou supérieur à 1, et aucun mode de respiration radiale (RBM) n'a été observé à ~ 200 cm −1 . Ces résultats indiquent que tous les VACNT préparés sur différentes couches tampons étaient à parois multiples. La figure 2a–d montre la morphologie des VACNTs sur différentes couches tampons, qui ont été analysées par MET. Les VACNTs étaient à parois multiples sur chacun d'eux, conformément aux résultats de l'analyse Raman. Les nanotubes de carbone étaient à triple paroi sur ALD et EB Al2 O3 mais quadruple ou quintuple parois sur Al2 pulvérisé O3 et SiO2 .
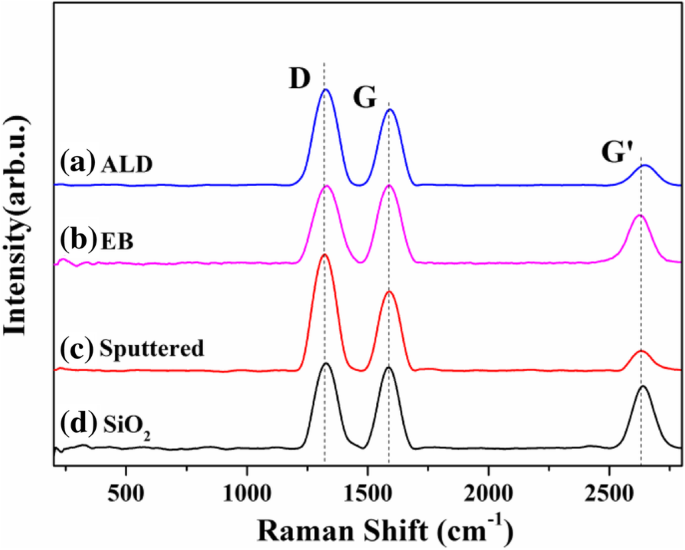
Spectres Raman de VACNT cultivés sur différentes couches tampons :a ALD Al2 O3 , b EB Al2 O3 , c pulvérisé Al2 O3 , et d SiO2 . Les spectres ont été normalisés à l'intensité de la bande G pour faciliter la comparaison

Images MET de VACNT cultivés sur différentes couches tampons :a ALD Al2 O3 , b EB Al2 O3 , c pulvérisé Al2 O3 , et d SiO2
La figure 3a–f montre les images SEM en coupe transversale des VACNT cultivés sur différentes couches tampons d'oxyde à 600 °C. Les VACNTs ont été synthétisés avec succès sur ALD et EB Al2 O3 , comme le montrent les Fig. 3a, b, e et f. L'épaisseur des VACNTs sur ALD Al2 O3 était plus petit que celui sur EB Al2 O3 , ce qui peut s'expliquer par des durées de vie différentes des nanoparticules de catalyseur sur elles pendant la période de croissance. La durée de vie des nanoparticules de catalyseur, qui représente le temps après lequel la nanoparticule de catalyseur a essentiellement perdu sa fonction catalytique pour faire croître des nanotubes de carbone, a été déduite de l'épaisseur des VACNTs [24]. Les résultats montrent que la durée de vie des nanoparticules de catalyseur sur EB Al2 O3 était plus long que celui sur ALD Al2 O3 , qui était en grande partie liée à la maturation d'Ostwald des nanoparticules de catalyseur sur les substrats. La maturation d'Ostwald est un phénomène par lequel les nanoparticules plus grosses augmentent en taille tandis que les nanoparticules plus petites, qui ont une plus grande énergie de déformation, rétrécissent en taille et finissent par disparaître par interdiffusion atomique [32]. Lorsqu'une nanoparticule de catalyseur disparaissait, ou lorsqu'une trop grande quantité de catalyseur était perdue, les nanotubes de carbone en croissance s'arrêtaient [32]. Lorsqu'un nombre suffisant de nanotubes de carbone a cessé de croître, la croissance des VACNTs s'est arrêtée collectivement parce que chaque nanotube de carbone terminé a conféré une force de traînée mécanique aux nanotubes en croissance adjacents en raison des forces de van der Waals et du verrouillage [32]. Par conséquent, la durée de vie des nanoparticules de catalyseur dépendait principalement de leur taux de maturation d'Ostwald. La figure 3c montre que presque aucun VACNT n'était présent sur l'Al2 pulvérisé O3 . Comme le montre le tableau 1, la densité et la composition chimique de l'Al2 pulvérisé O3 était presque similaire à ALD et EB Al2 O3 , qui indiquait que les différents Al2 O3 pourrait avoir une propriété de barrière similaire contre Fe. Par conséquent, la principale raison de l'échec de la croissance des VACNTs pourrait ne pas être la diffusion souterraine de Fe, mais la sérieuse maturation d'Ostwald des nanoparticules de catalyseur sur celui-ci [33]. Au fur et à mesure de la maturation d'Ostwald, le nombre de nanoparticules diminue tandis que le diamètre moyen du catalyseur augmente et que la distribution de la taille des nanoparticules s'élargit [32]. Par conséquent, une maturation sérieuse d'Ostwald des nanoparticules de catalyseur entraînerait directement une faible densité de nanotubes de carbone. Généralement, tout alignement marginal observé dans les échantillons CVD était dû à un effet d'encombrement, et les nanotubes de carbone se soutiennent mutuellement par attraction de van der Waals [34]. En conséquence, les VACNTs n'ont pas pu être obtenus sur des Al2 pulvérisés O3 . Par rapport aux VACNTs sur ALD et EB Al2 O3 , ceux sur SiO2 étaient très minces, ce qui pourrait être causé par la diffusion souterraine de Fe, comme le montre la figure 3d [33].

Images SEM en coupe de VACNT cultivés sur différentes couches tampons à 600 °C :a ALD Al2 O3 , b EB Al2 O3 , c pulvérisé Al2 O3 , et d SiO2 . Images e et f montrer la structure interne de a et b à fort grossissement
La figure 4a–d montre des images SEM de nanoparticules de catalyseur sur différentes couches tampons d'oxyde après recuit à 550 °C pendant 3 min en l'absence de C2 H2 . Par rapport aux autres, les nanoparticules avaient un diamètre beaucoup plus grand sur Al2 pulvérisé O3 avant la croissance des VACNTs. La figure 4e montre le nombre de nanoparticules de catalyseur sur un 200 × 200 nm 2 zone de différentes couches tampons. Le nombre de nanoparticules était le plus élevé sur EB Al2 O3 , et le moins sur l'Al2 pulvérisé O3 . Le plus grand diamètre et le plus petit nombre de nanoparticules pourraient entraîner leur durée de vie la plus courte sur Al2 pulvérisé O3 en raison de l'effet de la maturation d'Ostwald. Cela explique également pourquoi presque aucun VACNT n'a poussé sur de l'Al2 pulvérisé. O3 (Fig. 3c). De plus, le diamètre moyen et la distribution de taille des nanoparticules de catalyseur ont également été analysés, comme le montre la figure 5a–d. La figure 5b montre que le diamètre moyen des nanoparticules était le plus petit sur EB Al2 O3 , ce qui a conduit au catalyseur Fe présentant la durée de vie la plus longue [35]. Le résultat de la figure 3b confirme que les VACNTs les plus épais ont été cultivés sur EB Al2 O3 . La figure 5c montre que le diamètre moyen des nanoparticules était le plus grand sur Al2 pulvérisé O3 , ce qui a été confirmé par le résultat de la Fig. 4c. La figure 5a, d montre que le diamètre moyen des nanoparticules sur ALD Al2 O3 et SiO2 était similaire, alors que la Fig. 3a, d montre que leur épaisseur était assez différente. Les atomes de Fe pourraient diffuser plus facilement à travers SiO2 et dans le substrat Si que par ALD Al2 O3 [33]. La diffusion souterraine de Fe se traduirait par peu de nanoparticules de catalyseur existant à la surface de SiO2 pendant la période de croissance, ce qui a conduit aux VACNTs minces.
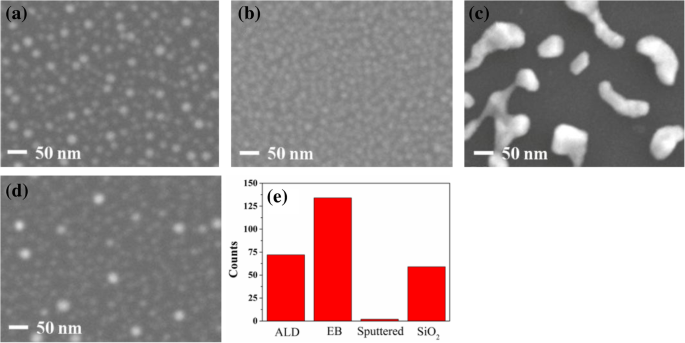
Images SEM en plan de nanoparticules de catalyseur formées sur différentes couches tampons après recuit à 550 °C en l'absence de C2 H2 :a ALD Al2 O3 , b EB Al2 O3 , c pulvérisé Al2 O3 , et d SiO2. L'image en e montre la quantité de nanoparticules de catalyseur sur une couche tampon différente avec un 200 × 200 nm 2 zone
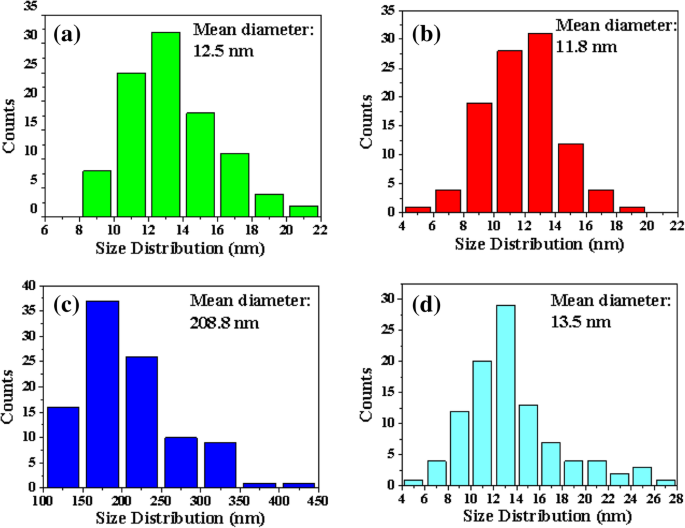
Distribution de taille de nanoparticules de catalyseur mesurée à partir des données FESEM par analyse manuelle de 100 particules sur différentes couches tampons :a ALD Al2 O3 , b EB Al2 O3 , c pulvérisé Al2 O3 , et d SiO2
La figure 6a–d montre la rugosité de surface de différentes couches tampons avant le dépôt du catalyseur. La rugosité de surface de EB Al2 O3 était le plus grand; sa valeur de rugosité quadratique moyenne (RMS) était de 2,53 nm, comme indiqué sur la figure 6b et le tableau 1. Comme mentionné précédemment, le plus petit diamètre et le plus grand nombre de nanoparticules de catalyseur ont été obtenus sur EB Al2 O3 . La surface rugueuse se traduirait par un petit diamètre et une densité élevée de nanoparticules de catalyseur après recuit. La figure 6c montre que la surface de l'Al2 pulvérisé O3 , dont la valeur RMS était de 0,68 nm, était la plus douce. Ce résultat indique que le plus grand diamètre et la plus faible densité de nanoparticules pourraient également être liés à la surface lisse de l'Al2 pulvérisé. O3 . D'après les Fig. 6a, d, la valeur RMS de l'ALD Al2 O3 était plus grand que celui de SiO2 . Par rapport aux nanoparticules sur SiO2 , ceux sur ALD Al2 O3 présentait une plus grande densité et un diamètre plus petit, comme le confirment les résultats des Fig. 4e et 5a, d. Par conséquent, la rugosité de surface des couches tampons était critique et a fortement influencé la croissance des VACNTs dans le processus CVD.
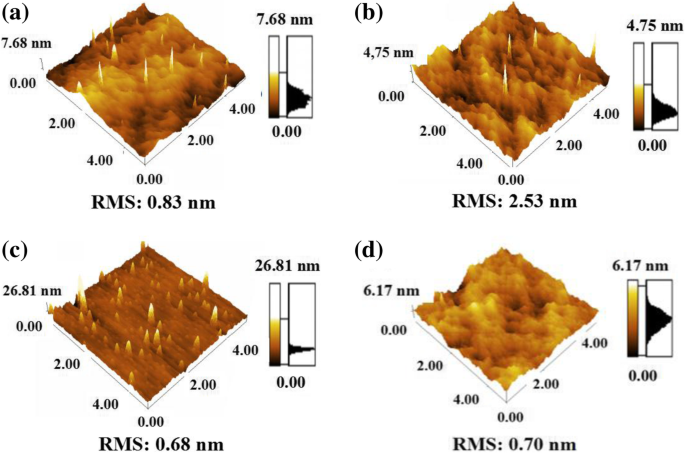
Images topographiques AFM des couches tampons exposées :a ALD Al2 O3 , b EB Al2 O3 , c pulvérisé Al2 O3 , et d SiO2
La figure 7 montre l'effet de la température de dépôt sur le taux de croissance des VACNTs sur EB et ALD Al2 O3 . A des températures inférieures à 600°C, le taux de croissance augmente avec l'augmentation de la température. Cependant, lorsque la température était supérieure à 600°C, le taux de croissance a apparemment diminué. Ce comportement pourrait être lié à la maturation d'Ostwald grave des nanoparticules de catalyseur, qui a largement réduit la durée de vie des nanoparticules et le taux de croissance [32]. De plus, la figure 7 montre également la dépendance du taux de croissance sur 1/T ; l'énergie d'activation a été directement calculée à partir de la pente de l'ajustement linéaire aux données [36]. Les énergies d'activation pour la nucléation et la croissance initiale des VACNTs sur ALD et EB Al2 O3 étaient de 39,1 et 66,5 kJ mol −1 , respectivement. Ce résultat indique que l'énergie d'activation pour la nucléation et la croissance initiale en utilisant ALD Al2 O3 est bien inférieur à celui utilisant EB Al2 O3 . Par conséquent, nous avons pu conclure que la nucléation et la croissance initiale des VACNTs étaient plus facilement réalisées sur ALD Al2 O3 , comparé à EB Al2 O3 . À partir du tableau 1, nous avons pu savoir qu'il y avait des impuretés dans l'ALD Al2 O3 , comme le carbone, qui pourrait offrir des sites supplémentaires pour la nucléation des VACNTs, puis réduire son énergie d'activation.
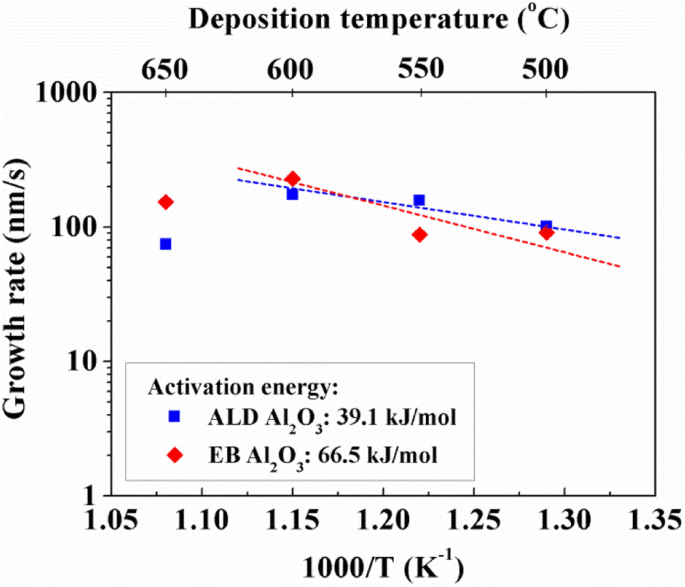
Variation du taux de croissance sur ALD et EB Al2 O3 couches tampons en fonction de la température de dépôt. Les énergies d'activation ont été calculées à partir d'une interpolation linéaire des pentes
La figure 8a, b montre les images SEM en coupe transversale des films composites préparés en remplissant la matrice dans les VACNTs. Les VACNT et la matrice ont été entièrement mis en contact et les films composites à base de VACNT ont été synthétisés avec succès. Leurs conductivités thermiques longitudinales ont ensuite été analysées, comme le montre la figure 9. Par rapport à la résine époxy pure, les VACNTs ont évidemment amélioré la conductivité thermique des films composites. De plus, le film composite avait une conductivité thermique plus élevée avec les VACNT cultivés sur ALD Al2 O3 par rapport à celui sur EB Al2 O3 . Généralement, la conductivité thermique de la résine époxy était bien inférieure à celle des nanotubes de carbone multiparois, dont la conductivité thermique expérimentale a été signalée comme étant supérieure à 3000 W m −1 K −1 à température ambiante [37]. Chaque nanotube de carbone était une voie de dissipation thermique dans les films composites, et une conductivité thermique plus élevée signifie plus de voies de dissipation thermique. Les résultats indiquent qu'une plus grande quantité de nanotubes de carbone et des VACNTs plus denses pourraient être obtenus sur ALD Al2 O3 . Généralement, chaque nanoparticule de catalyseur pourrait produire au plus un nanotube de carbone, et le nombre de nanoparticules de catalyseur pourrait fournir une prédiction de limite supérieure de la densité de VACNTs [35, 38]. Cependant, toutes les nanoparticules de catalyseur n'ont pas pu atteindre la formation d'un nanotube de carbone car l'énergie d'activation doit être surmontée pour sa nucléation et sa croissance initiale. Bien que l'EB Al2 O3 contenait un plus grand nombre de nanoparticules de catalyseur que l'ALD Al2 O3 , comme mentionné dans la Fig. 4e, le nombre de nanotubes de carbone sur EB Al2 O3 était encore inférieur à celui sur ALD Al2 O3 . Ce résultat pourrait s'expliquer par une énergie d'activation plus faible pour la nucléation et la croissance initiale des VACNTs sur ALD Al2 O3 , comme le montre la figure 7. Par conséquent, en plus du nombre de nanoparticules de catalyseur, la densité des VACNTs dépendait encore largement de l'énergie d'activation pour leur nucléation et leur croissance initiale.

Images SEM en coupe transversale de films composites avec des VACNT cultivés sur différentes couches tampons :a ALD Al2 O3 et (b ) EB Al2 O3
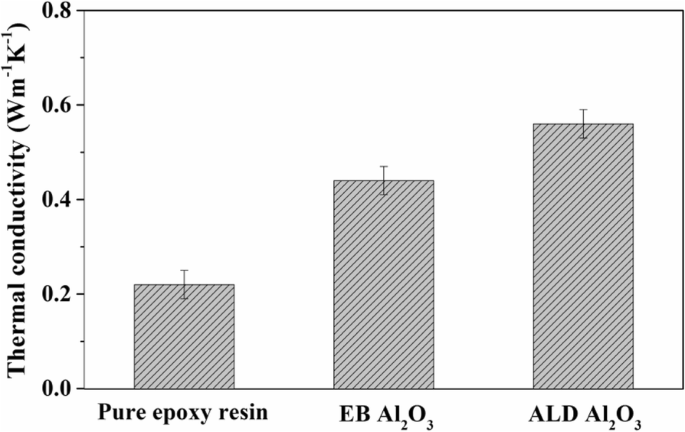
Analyse de conductivité thermique de différents films :le film avec résine époxy pure et les films composites avec VACNTs cultivés sur EB et ALD Al2 O3
Conclusions
Dans cette étude, nous avons étudié la croissance des VACNTs sur différentes couches tampons d'oxyde et leur mécanisme de croissance possible. La durée de vie des nanoparticules de catalyseur et l'épaisseur des VACNTs préparés dépendaient largement du diamètre et de la densité des nanoparticules après recuit. Le plus petit diamètre et la plus haute densité de nanoparticules ont été obtenus sur EB Al2 O3 , et les VACNTs les plus épais ont également été préparés sur ce substrat. A l'inverse, le plus grand diamètre et la plus faible densité de nanoparticules ont été obtenus sur de l'Al2 pulvérisé O3 , et presque aucun VACNT n'a été préparé dessus. Ces observations pourraient s'expliquer par un mûrissement d'Ostwald important de nanoparticules de catalyseur sur Al2 pulvérisé O3 . Par rapport à EB et ALD Al2 O3 , les VACNTs préparés étaient beaucoup plus fins sur SiO2 , ce qui pourrait être lié à la diffusion souterraine de Fe. De plus, la rugosité de surface des couches tampons a largement influencé le diamètre et la densité des nanoparticules de catalyseur. Par rapport à la surface de l'Al2 pulvérisé O3 , la surface rugueuse de EB Al2 O3 favorisé un petit diamètre et une haute densité de nanoparticules de catalyseur.
De plus, la croissance des VACNTs dépendait largement de la température de dépôt. À une température supérieure à 600 °C, le taux de croissance des VACNTs a apparemment diminué, ce qui pourrait être causé par une maturation grave d'Ostwald des nanoparticules de catalyseur, réduisant leur durée de vie. Par rapport à l'énergie d'activation sur EB Al2 O3 , que sur ALD Al2 O3 était beaucoup plus faible, ce qui suggère que la nucléation et la croissance initiale des VACNTs étaient plus facilement réalisées sur celui-ci. Cette énergie d'activation plus faible peut entraîner des VACNTs plus denses sur ALD Al2 O3 , ce qui a été confirmé par la conductivité thermique longitudinale plus élevée du film composite les comprenant. Par conséquent, en plus du nombre de nanoparticules de catalyseur, l'énergie d'activation pour la nucléation et la croissance initiale des VACNTs a encore fortement influencé leur densité.
Abréviations
- AFM :
-
Microscopie à force atomique
- ALD :
-
Dépôt de couche atomique
- CVD :
-
Dépôt chimique en phase vapeur
- DSC :
-
Calorimètre différentiel à balayage
- EB :
-
Faisceau d'électrons
- FESEM :
-
Microscopie électronique à balayage à émission de champ
- LFA :
-
Analyseur thermique flash laser
- RBM :
-
Modes de respiration radiale
- RMS :
-
Moyenne quadratique
- TEM :
-
Microscopie électronique à transmission
- TMA :
-
Triméthylaluminium
- VACNTs :
-
Nanotubes de carbone alignés verticalement
- XPS :
-
Spectroscopie photoélectronique aux rayons X
- XRR :
-
Réflectivité des rayons X
Nanomatériaux
- Qu'est-ce que le dépôt chimique en phase vapeur?
- Des articles récents détaillent l'évolutivité des nanotubes de carbone, les avancées en matière d'intégration
- Fil de nanotubes de carbone, muscle et feuilles transparentes
- Effets du forgeage sur l'acier au carbone
- Technologies avancées de dépôt de couche atomique pour les micro-LED et les VCSEL
- Matrices de nanopiliers GaAs à capuchon Au fabriqués par gravure chimique assistée par métal
- Diélectrophorèse assistée par chauffage pour film de nanotubes de carbone à paroi unique alignés de très haute densité
- Croissance auto-catalysée de nanofils verticaux de GaSb sur des tiges d'InAs par dépôt en phase vapeur de produits chimiques organo-métalliques
- Effets du pH micro-environnemental du liposome sur la stabilité chimique du médicament chargé



