Matrices de nanopiliers GaAs à capuchon Au fabriqués par gravure chimique assistée par métal
Résumé
Des matrices de nanopiliers de GaAs ont été fabriquées avec succès par gravure chimique assistée par métal à l'aide de matrices de nanopoints d'Au. Les réseaux de nanopoints ont été formés sur des substrats par dépôt sous vide à travers un masque d'alumine poreux avec un réseau ordonné d'ouvertures. En utilisant un agent de gravure avec une concentration élevée en acide et une faible concentration en oxydant à une température relativement basse, la zone entourant l'interface Au/GaAs pourrait être gravée sélectivement. Dans des conditions optimales, des matrices de nanopiliers GaAs coiffés d'Au ont été formées avec une périodicité ordonnée de 100 nm et des hauteurs de pilier de 50 nm.
Contexte
Les semi-conducteurs composés III-V ont attiré l'attention en tant que matériaux de nouvelle génération et alternatives potentielles aux semi-conducteurs à base de silicium en raison de leurs excellentes propriétés, notamment une mobilité supérieure des porteurs et une bande interdite directe. Les nanostructures avec une périodicité ordonnée et/ou un rapport d'aspect élevé sont considérées comme un élément important dans diverses applications, y compris les dispositifs optiques et optoélectroniques en raison de leur faible coût et de leur efficacité de conversion élevée par rapport aux dispositifs conventionnels à couche mince [1,2,3,4] . En général, pour fabriquer des semi-conducteurs de faible dimension (par exemple, des nanofils), des procédés à sec tels que l'épitaxie par faisceau moléculaire, l'épitaxie vapeur-liquide-solide et l'épitaxie métal-organique en phase vapeur sont utilisés [1, 5, 6, 7]. Bien que ces méthodes présentent de nombreux avantages, notamment une précision élevée de la structuration, leurs inconvénients incluent des limitations de coût et de taille élevées de la zone de structuration dans les applications pratiques. Par conséquent, des méthodes alternatives permettant la fabrication simple et rentable de nanostructures sont nécessaires.
La gravure chimique assistée par métal, qui a été proposée par Li et Bohn en 2000 [8], est une méthode de fabrication couramment utilisée en raison de sa relative simplicité et de son faible coût. Des études récentes ont démontré que la gravure chimique assistée par métal peut être appliquée pour fabriquer des nanostructures complexes telles que des nanopores profonds et droits, des nanopores hélicoïdaux, des canaux en pente, des cycloïdes et des spirales [4, 9,10,11,12]. Cependant, depuis le rapport de Li et al., la plupart des études ont rapporté la fabrication de nanostructures de silicium; peu d'études se sont concentrées sur la nanofabrication de semi-conducteurs composés III-V [13, 14], et la formation de structures ordonnées à l'échelle nanométrique sur des substrats de GaAs est particulièrement mal comprise. Pour élargir la gamme d'applications de la gravure chimique assistée par métal, il est souhaitable de développer une méthode de nanofabrication pour les semi-conducteurs composés III-V qui ne dépend pas des dimensions des motifs résultants.
Dans une étude précédente, nous avons fabriqué des matrices de microbosses d'InP [15] et des motifs de lignes et des matrices de piliers de GaAs [16] en utilisant une gravure chimique assistée par métal. Cependant, les dimensions des motifs résultants (par exemple, la périodicité et les largeurs des motifs de lignes) variaient de plusieurs micromètres à plusieurs dizaines de micromètres. À notre connaissance, aucune étude n'a rapporté la formation de nanostructures ordonnées de GaAs avec une périodicité submicronique ou inférieure à l'aide d'une gravure chimique assistée par métal pour les raisons suivantes :(1) il est difficile de contrôler la forme et la taille des métaux nobles utilisé comme catalyseur à l'échelle nanométrique et (2) le phénomène de gravure du GaAs est moins bien compris par rapport au cas du silicium. Ainsi, nous avons tenté de clarifier le mécanisme de gravure du GaAs à l'échelle nanométrique. Dans cette étude, nous démontrons que des réseaux de nanopiliers ordonnés avec une périodicité de 100 nm peuvent être fabriqués sur des substrats de GaAs en utilisant une gravure chimique assistée par métal avec un catalyseur Au à motifs. Les effets de la composition de l'agent de gravure et du temps de gravure sur la morphologie du substrat GaAs gravé sont également étudiés.
Méthodes
Le principe de la fabrication de réseaux de nanopiliers GaAs via une gravure chimique assistée par métal est représenté schématiquement sur la Fig. 1. Un masque d'alumine poreux traversant avec un réseau ordonné d'ouvertures a été préparé par anodisation en deux étapes suivie d'une anodisation en deux couches [ 17]. La première anodisation a été réalisée sur de l'aluminium poli électrochimiquement (pureté 99,99 %) à une tension constante de 40 V dans 0,3 mol dm −3 acide oxalique à 30 °C pendant 3 h. La tension d'anodisation de 40 V est bien établie en tant que condition d'auto-commande qui produit un arrangement de pores hautement ordonné dans l'alumine anodique [18].
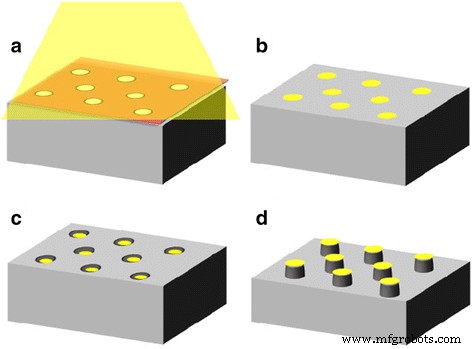
Modèle schématique de la fabrication de réseaux de nanopiliers GaAs. un Dépôt sous vide d'Au sur un substrat de GaAs à travers un masque d'alumine poreux. b Retrait du masque. c , d Gravure chimique de GaAs utilisant des matrices de nanodots d'Au comme catalyseur
Après la première anodisation, la première couche d'alumine anodisée a été retirée dans une solution mixte d'acide phosphorique et d'acide chromique à 80 °C. Par la suite, la deuxième anodisation a été réalisée pendant 1,5 min dans les mêmes conditions que la première anodisation. Sur la base du principe de l'anodisation à deux couches, l'échantillon a été à nouveau anodisé à une tension constante de 40 V dans 12 mol dm −3 acide sulfurique à 5 °C pendant 8 min pour préparer une couche d'alumine sacrificielle. Le masque d'alumine poreux à trou traversant a été formé en dissolvant la couche d'alumine sacrificielle dans 2 % en poids d'acide phosphorique à 30 °C pendant 20 min. Une gravure chimique supplémentaire a été réalisée dans de l'acide phosphorique à 5 % en poids à 30 °C pendant 15 min pour augmenter le diamètre des pores du masque en alumine.
Après rinçage du masque d'alumine dans de l'eau distillée, le masque d'alumine obtenu a été déposé sur un substrat GaAs de type n [dopé Si, 2,35-2,67 × 10 −3 Ω cm, (100) orientation cristalline]. Par la suite, une couche d'Au de 30 nm d'épaisseur a été évaporée à travers le masque d'alumine à l'aide d'un système de dépôt sous vide par la formule de chauffage par résistance (ULVAC KIKO Inc., VPC-410) avec une pression inférieure à 1 × 10 −3 Pa (Fig. 1a). L'épaisseur de la couche d'Au a été mesurée à l'aide d'une microbalance à cristal de quartz et le taux de dépôt d'Au était de 0,02 nm s −1 . Après dépôt de métal, le masque d'alumine a été retiré dans de l'acide phosphorique à 5 % en poids à 25 °C pendant 30 min (Fig. 1b).
Le substrat GaAs revêtu d'Au a été gravé chimiquement dans du HF contenant du KMnO4 (Fig. 1c). KMnO4 agit comme un agent oxydant dans une solution acide [19,20,21,22]. Les morphologies du masque d'alumine, de la couche d'Au déposée et du substrat GaAs gravé ont été évaluées par microscopie électronique à balayage à émission de champ (FE-SEM; JEOL JSM-6701F). La composition chimique du substrat GaAs gravé a été évaluée par spectroscopie électronique à vis sans fin (AES; JEOL JAMP-9500F). Les spectres électroniques Auger sont facilement acquis à partir de points ou de zones sélectionnés de la surface. Ici, l'image de cartographie élémentaire AES a été acquise avec une tension d'accélération et un courant d'émission de 30 kV et 15 nA, respectivement.
Résultats et discussion
Dans la gravure chimique assistée par métal, il est essentiel de contrôler avec précision les dimensions du catalyseur métallique pour obtenir la conception souhaitée sur la surface du substrat. Étant donné que la morphologie de la structure résultante dépend du motif géométrique initial et des dimensions du catalyseur métallique, un catalyseur métallique à motifs est nécessaire pour fabriquer des nanostructures ordonnées sur des surfaces semi-conductrices. Dans cette étude, un masque d'alumine avec un réseau ordonné d'ouvertures a été utilisé pour contrôler la taille et la disposition du catalyseur métallique. Pour un procédé de dépôt de métal à sec, l'épaisseur du masque est critique car le dépôt de métal à travers un masque épais avec des ouvertures étroites est physiquement difficile. Dans le cas de l'alumine poreuse, l'épaisseur du masque peut être ajustée avec une grande reproductibilité en modifiant le temps d'anodisation. Ici, un masque d'alumine poreuse traversant d'environ 300 nm d'épaisseur a été préparé sur un substrat de GaAs. Le masque d'alumine a été fixé avec sa surface tournée vers le haut. Les diamètres supérieur et inférieur des ouvertures dans le masque d'alumine étaient respectivement d'environ 80 et 70 nm. Le diamètre légèrement plus grand de l'ouverture supérieure par rapport à l'ouverture inférieure a été attribué à une attaque chimique lors de la préparation du masque en alumine.
La figure 2 montre un réseau de nanopoints Au bien ordonné typique sur un substrat de GaAs. Le réseau de nanopoints correspond à la configuration du réseau de pores auto-ordonné dans le masque d'alumine anodique, comme le montre la figure 2a. Bien que la contrôlabilité du dépôt d'Au doive être encore améliorée, le dépôt de métal à travers le masque d'alumine démontré ici convient à la production à grande échelle de motifs de points de métal noble ordonnés sur des substrats semi-conducteurs en termes de simplicité et d'efficacité du processus de fabrication. Notez que chaque nanopoint Au avait presque le même diamètre d'environ 70 nm ; ce diamètre a été déterminé par la taille des pores de la partie inférieure du masque d'alumine, tandis que les hauteurs de nanodots d'Au ont été principalement déterminées par le temps de dépôt. Dans cette étude, la hauteur de chaque nanopoint d'Au a été ajustée pour être d'environ 30 nm, comme le montre la figure 2b.

un Surface et b images SEM en coupe transversale d'un réseau de nanopoints d'Au formé sur un substrat de GaAs à travers un masque d'alumine poreuse anodique
Après la formation de réseaux de points Au sur des substrats de GaAs, les spécimens ont été immergés dans une solution de HF et de KMnO4 pour la gravure chimique assistée par métal. Dans la gravure chimique classique assistée par métal, la gravure se déroule localement à l'interface entre le catalyseur et le substrat sous-jacent, entraînant la formation de pores ou de tranchées dans la direction perpendiculaire au substrat, et le catalyseur métallique s'enfonce dans le semi-conducteur comme indiqué dans 1c. L'utilisation d'un agent de gravure composé d'une forte concentration en acide et d'une faible concentration en oxydant est considérée comme favorisant une consommation douce des trous positifs générés (h + ) à l'interface métal/semi-conducteur. Dans cette étude, l'oxydation de GaAs à l'interface Au/GaAs devrait se faire directement par le h + généré .
La figure 3 montre une image SEM typique de la surface de GaAs gravée à l'aide du catalyseur Au à motifs. La gravure chimique a été réalisée dans une solution contenant 0,001 mol dm −3 KMnO4 et 20 mol dm −3 HF à une température relativement élevée de 45 °C. Dans cette étude, la concentration de KMnO4 était faible (0,001 mol dm −3 ) pour supprimer la gravure latérale. Selon les rapports précédents de DeJarld et al. et Cheung et al., la vitesse de gravure latérale augmentait avec l'augmentation de l'agent oxydant (KMnO4 ) concentration [19, 21].

Image SEM de la surface supérieure du substrat GaAs après gravure chimique assistée par Au dans une solution contenant 0,001 mol dm −3 KMnO4 et 20 mol dm −3 HF pendant 600 s à 45 °C
Les catalyseurs Au, qui ont été détectés sous forme de points lumineux circulaires, ont été observés à l'intérieur des pores dans de nombreuses zones du substrat GaAs, comme le montre la figure 3. Le diamètre des pores observés sur la figure 3 coïncidait avec la taille des nanopoints d'Au déposés montrés sur la figure 2. Ces résultats indiquent que la gravure chimique classique assistée par métal, qui est représentée schématiquement sur la figure 1c, s'est produite uniquement à l'interface Au/GaAs et s'est déroulée de manière anisotrope perpendiculairement au substrat, c'est-à-dire dans la direction <100>.
Dans la gravure chimique assistée par métal, la composition de l'agent de gravure et la température de gravure affectent la dynamique de la diffusion des porteurs, de l'oxydation et de l'élimination du produit [19]. Pour ouvrir de nouvelles applications du substrat GaAs gravé, nous avons tenté de fabriquer des matrices de nanopiliers GaAs en modifiant les conditions de la gravure chimique assistée par métal. La figure 4 montre des images SEM en coupe transversale typiques de surfaces GaAs gravées obtenues à l'aide du catalyseur Au à motifs. En augmentant la concentration de KMnO4 , la morphologie de la structure résultante pourrait être modifiée. Dans tous les cas, des nanopiliers de GaAs disposés de manière hexagonale sur toute la surface de l'échantillon ont été obtenus. Les pointes des piliers étaient légèrement effilées à la suite d'une gravure latérale. Les périodicités des réseaux de nanopiliers de GaAs étaient d'environ 100 nm, correspondant à celles des réseaux de points Au utilisé comme catalyseur et aux pores de l'alumine poreuse utilisée comme masque initial. À notre connaissance, les dimensions (par exemple, la périodicité) des structures obtenues sur GaAs via une gravure chimique assistée par métal dans cette étude sont plus petites que celles rapportées pour d'autres structures GaAs [19,20,21,22].

Images SEM de réseaux de nanopiliers GaAs fabriqués par gravure chimique assistée par Au dans des solutions contenant 0,01 mol dm −3 KMnO4 et 5, 10 ou 20 mol dm −3 HF pendant 5 s à a 20 et b 45 °C
Lorsque la gravure a été effectuée à une température relativement basse de 20 °C, un catalyseur Au a été observé à l'extrémité de chaque pilier, comme indiqué par des flèches. La figure 4a montre que la vitesse de gravure augmente avec l'augmentation de la concentration de HF à la même concentration d'oxydant. À la concentration élevée en HF de 20 mol dm −3 , la hauteur résiduelle du pilier GaAs était la plus élevée.
Contrairement à l'attente que l'oxydation de GaAs à l'interface Au/GaAs procède par le h + généré , aucune dissolution chimique dans la zone de contact entre le catalyseur Au et le substrat GaAs sous-jacent n'a été observée dans le cas de la figure 4. Le motif de gravure est considéré comme dépendant de la température de l'agent de gravure. À basse température (par exemple, 20 °C), le taux de h + la consommation à l'interface Au/GaAs serait inférieure au taux de h + injection; ainsi, h + diffusé dans la zone entourant le GaAs revêtu d'Au. Finalement, un nanopilier de GaAs s'est formé sous la zone de contact entre le catalyseur Au et le substrat de GaAs sous-jacent, car une gravure sélective s'est produite sur la surface de GaAs exposée. En d'autres termes, les nanodots d'Au ont également agi comme un masque protecteur pour empêcher la dissolution du substrat de GaAs. Ce phénomène de gravure, illustré schématiquement sur la figure 1d, est appelé gravure chimique assistée par métal inverse [19, 22]. En 2010, nous avons également démontré la formation de réseaux de microbumps InP en utilisant une gravure chimique assistée par métal inverse sous irradiation UV [15]. Contrairement à la gravure chimique conventionnelle assistée par métal, la gravure chimique assistée par métal inverse se déroule dans les surfaces exposées des semi-conducteurs composés III-V autour des zones revêtues de métal par la diffusion de h + à partir d'un catalyseur métallique et d'une attaque chimique sélective de site subséquente. Un tel comportement de gravure unique n'a pas été observé dans les matériaux en silicium.
Lorsque la gravure chimique assistée par métal est effectuée à une température élevée de 45 °C, le h + généré devrait être consommé dès qu'il atteint la limite entre Au, GaAs et l'agent d'attaque, entraînant la promotion de l'attaque verticale. Même dans ce cas, cependant, une attaque chimique inversée assistée par un métal s'est produite. Comme le montre la figure 4b, la vitesse de gravure a augmenté avec l'augmentation de la concentration de HF de la même manière que le comportement de gravure de la figure 4a. Cependant, à une température de gravure élevée de 45 °C et une concentration élevée en HF de 20 mol dm −3 , les catalyseurs Au se sont détachés des pointes des piliers de GaAs car l'excès h + généré par la température relativement élevée, même dans le court temps de gravure de 5 s, a favorisé la gravure latérale de GaAs en présence du catalyseur Au. La contrôlabilité de la forme des piliers sera améliorée par l'optimisation supplémentaire des conditions de gravure (par exemple, la composition de l'agent de gravure, la concentration et la température). Tentatives de clarification des effets de la concentration d'agent oxydant sur la génération de h + et la morphologie des GaA gravés sont actuellement en cours.
Pour examiner l'effet du temps de gravure sur la géométrie de la structure GaAs gravée, la gravure chimique a été prolongée dans 20 mol dm −3 HF et 0,01 mol dm −3 KMnO4 à une température relativement basse de 20 °C. Comme le montre l'image en coupe transversale de la Fig. 5a, la profondeur des nanopiliers de GaAs a atteint ~ 50 nm. L'une des caractéristiques notables des réseaux de nanopiliers GaAs obtenus dans cette étude est que la pointe de chaque pilier était recouverte d'Au, comme le montre l'encart de la figure 5a. La figure 6 montre l'analyse élémentaire AES du même spécimen. Les cartes AES pour Ga et Au des GaAs gravés indiquent la présence d'Au à la pointe de chaque pilier même après une gravure chimique assistée par métal pendant 10 s.

Images SEM en coupe transversale d'un réseau de nanopiliers GaAs fabriqué par gravure chimique assistée par Au à 20 °C pour a 10 et b 60 s dans une solution contenant 20 mol dm −3 HF et 0,01 mol dm −3 KMnO4 . Encart montre une image de surface d'un réseau de nanopiliers GaAs coiffé d'Au

un Image du substrat GaAs après gravure chimique assistée par Au et cartes AES correspondantes pour b Ga et c Au. Les conditions de gravure étaient les mêmes que celles de la Fig. 5a
Étant donné que la hauteur du pilier a été déterminée principalement par le temps de gravure, la gravure a été prolongée de 10 s à 1 min pour former des réseaux de piliers plus élevés sur GaAs. Cependant, le temps de gravure prolongé de 1 min a entraîné une diminution de la hauteur du pilier, comme le montre la figure 5b. La diminution de la hauteur des piliers a été attribuée à la gravure latérale en présence de catalyseur Au et au détachement ultérieur des points Au utilisés comme catalyseur.
Bien que gravure chimique assistée par métal, qui contrôle précisément la diffusion de h + à partir d'un catalyseur métallique, n'a pas encore été entièrement réalisée, la nanofabrication de semi-conducteurs composés III-V à l'aide d'une gravure chimique assistée par métal offre une alternative prometteuse pour la conception de structures tridimensionnelles ordonnées sans l'utilisation de procédés secs. De plus, les réseaux de nanopiliers GaAs à capuchon Au obtenus ont des applications technologiques et scientifiques potentielles dans les dispositifs optoélectroniques tels que les cellules solaires qui utilisent des nanostructures plasmoniques pour améliorer le piégeage de la lumière [23, 24].
Conclusions
En résumé, nous avons démontré la fabrication de réseaux de nanopiliers de GaAs ordonnés sur des substrats de GaAs (100) via une gravure chimique assistée par Au. Des réseaux de nanodots Au avec des motifs en réseau hexagonal et des périodicités ordonnées de 100 nm ont été formés par dépôt sous vide à travers un masque d'alumine poreux. Les nanodots d'Au avaient des diamètres d'environ 70 nm, correspondant au diamètre de la partie inférieure du masque d'alumine, et servaient de catalyseur et de masque protecteur. À une température relativement basse, des réseaux de nanopiliers GaAs recouverts d'Au pourraient être formés par gravure sélective de site dans la surface de GaAs exposée environnante. Ces résultats fournissent la première preuve d'un contrôle plus précis des nanostructures sur des substrats de GaAs en utilisant une approche réalisable basée sur la gravure chimique assistée par métal. La technique de lithographie non conventionnelle pour la nanofabrication de semi-conducteurs composés III-V présentée dans cette communication surmonte les inconvénients des méthodes conventionnelles et a des applications technologiques et scientifiques potentielles dans divers domaines de recherche.
Abréviations
- AES :
-
Spectroscopie électronique Auger
- FE-SEM :
-
Microscopie électronique à balayage à émission de champ
Nanomatériaux
- Propriétés chimiques du titane
- Tableaux C#
- Tableaux C++
- Tableaux C
- C Tableaux multidimensionnels
- Tableaux Java
- Décryptage de l'évolution morphologique et de la cinétique de gravure de nanofils de silicium poreux lors d'une gravure chimique assistée par métal
- Effets du pH micro-environnemental du liposome sur la stabilité chimique du médicament chargé
- MATLAB - Tableaux



