Composites CoSe/NC dérivés du ZIF-67 comme matériaux d'anode pour batteries lithium-ion
Résumé
En tant que séléniure métallique typique, le CoSe est une sorte de matériau d'anode de premier plan pour les batteries lithium-ion (LIB) en raison de sa structure en couches bidimensionnelle, de sa bonne conductivité électrique et de sa capacité théorique élevée. Dans ce travail, les composites originaux de carbone dopé CoSe/N (CoSe/NC) ont été synthétisés en utilisant le ZIF-67 comme précurseur, dans lequel les nanoparticules de CoSe sont encapsulées dans des nanocouches NC et elles sont connectées par des liaisons C-Se. La structure du revêtement et le fort couplage chimique font que les nanocouches NC pourraient améliorer efficacement les propriétés de stockage du lithium des composites CoSe/NC. En conséquence, les composites CoSe/NC délivrent une capacité réversible de 310,11 mAh g −1 après 500 cycles à 1,0 A g −1 . En outre, les composites CoSe/NC présentent un comportement incrémental distinct de la capacité.
Contexte
Avec l'épuisement de l'énergie fossile représentée par le pétrole et la pollution croissante de l'environnement causée par la combustion de combustibles fossiles, il existe un besoin urgent d'une source d'énergie renouvelable durable. Les batteries lithium-ion (LIB) se distinguent de nombreuses nouvelles sources d'énergie en raison de leur densité énergétique élevée, de leur longue durée de vie et de leur respect de l'environnement [1, 2]. Ils sont largement utilisés dans les appareils électroniques mobiles et les véhicules électriques. Cependant, le matériau d'anode des LIB commerciaux est du graphite, et la capacité théorique du graphite n'est que de 372 mAh g −1 , qui ne peut pas répondre aux exigences de capacité des équipements électroniques à grande échelle tels que les véhicules électriques, et limite l'application et le développement des LIB [3,4,5,6]. Par conséquent, les scientifiques ont développé une variété de matériaux d'anode pour augmenter la capacité et les performances de vitesse des LIB, tels que les matériaux carbonés [7,8,9], les oxydes de métaux de transition [10,11,12,13], les sulfures métalliques [14, 15,16,17], les phosphures métalliques [18,19,20,21] et le séléniure métallique [22,23,24,25].
Le sélénium a une densité et une conductivité plus élevées, de sorte que le séléniure métallique a une densité énergétique et des performances de vitesse plus élevées que les oxydes et sulfures de métaux de transition [26]. Comparé aux oxydes et sulfures largement étudiés, le séléniure est relativement rare dans le domaine des LIB. Parmi les séléniures, le CoSe est considéré comme un excellent matériau d'anode pour les LIB en raison de sa structure en couches bidimensionnelle, de sa bonne conductivité électrique et de sa capacité théorique élevée [22]. Cependant, en tant que matériau d'électrode négative pour le stockage du lithium basé sur une réaction de conversion, comme les oxydes et les sulfures de métaux de transition, le CoSe subit une importante expansion de volume pendant la charge et la décharge, entraînant la rupture et la pulvérisation des matériaux actifs et la perte de la connexion avec le collecteur de courant, provoquant en outre l'atténuation aiguë de la capacité [10]. Selon la littérature précédente [25, 26], la préparation de nanostructures et la recombinaison avec des matériaux carbonés peuvent efficacement soulager les problèmes mentionnés ci-dessus. Les nanostructures poreuses sont avantageuses pour la perméation de l'électrolyte dans les matériaux d'électrode et raccourcissent la diffusion des ions lithium. Pendant ce temps, la structure poreuse pourrait fournir un espace libre pour l'expansion du volume afin d'empêcher la destruction de la structure, ce qui améliore la stabilité cyclique. En outre, la recombinaison de composés métalliques avec des matériaux carbonés pourrait utiliser pleinement l'excellente conductivité et les propriétés mécaniques des matériaux carbonés pour améliorer la conductivité des composés métalliques et amortir la contrainte causée par l'expansion du volume, ce qui est favorable à la vitesse et aux performances de cyclage. Cependant, à l'heure actuelle, les composés métalliques et la matrice carbonée sont liés par adsorption physique. Par rapport au couplage fort, tel que les liaisons chimiques, la connexion faible fera tomber les nanoparticules de composés métalliques de la matrice carbonée dans des conditions de forte densité de courant et de cycle à long terme [4, 22]. La construction d'un couplage fort entre les composés métalliques et la matrice carbonée reste un défi.
Les charpentes organométalliques (MOF) sont une classe de matériaux poreux formés par la fixation d'ions métalliques à des composés organiques via des liaisons de coordination [27,28,29,30]. En raison de sa structure poreuse, de sa surface spécifique élevée et de sa contrôlabilité structurelle, il a de larges perspectives d'application dans la séparation du stockage de gaz, la catalyse, les capteurs et le transport de médicaments [31, 32]. Le ZIF-67 est un matériau MOF à base de Co typique formé de Co 2+ et 2-méthylimidazole et a une structure poreuse similaire à la zéolite. Le 2-méthylimidazole possède un groupe fonctionnel contenant de l'azote qui se carbonise pour former du carbone dopé N (NC) par pyrolyse [9, 33]. D'une part, la CN peut atténuer l'expansion du volume et améliorer la stabilité du cycle ; d'autre part, le dopage des atomes N peut améliorer la conductivité tout en réfléchissant le site actif et en augmentant sa capacité de stockage du lithium [8]. En outre, les matériaux dérivés des MOF pourraient rester la structure poreuse. Par conséquent, le ZIF-67 est souvent utilisé comme précurseur pour préparer des matériaux composites à base de composés à base de cobalt tels que le Co3 O4 [34, 35], CoS [36, 37], CoP [38,39,40] et carbone dopé N.
Nous rapportons ici une méthode facile pour préparer des composites de carbone dopé CoSe/N (CoSe/NC) grâce à la sélénisation de ZIF-67 avec de la poudre de sélénium en atmosphère inerte. La figure 1 montre le processus de synthèse des composites CoSe/NC. Dans le processus de sélénisation, le Co 2+ au sein de ZIF-67 réagit avec le sélénium pour former des nanoparticules de CoSe, qui sont enveloppées par des nanocouches NC qui proviennent de la carbonisation du 2-méthylimidazole. Les nanocouches NC pourraient améliorer la conductivité du CoSe et supprimer l'expansion du volume, et offrir un stockage de lithium supplémentaire en tant que siège actif. La structure poreuse du ZIF-67 pourrait raccourcir le chemin de diffusion des électrons et des ions lithium. Plus important encore, les liaisons C-Se entre les nanoparticules de CoSe et les nanocouches NC ; la connexion chimique unique pourrait non seulement mieux favoriser la connexion électrique active entre CoSe et NC, mais aussi mieux atténuer la variation de volume. En conséquence, les composites CoSe/NC présentent de superbes propriétés de stockage du lithium.
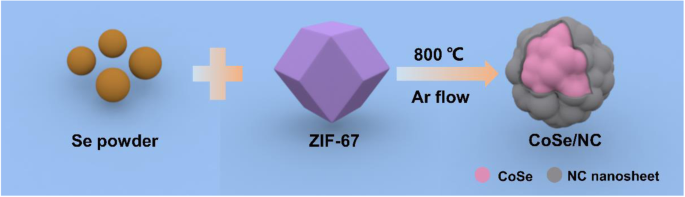
Schéma de principe pour la synthèse de composites CoSe/NC
Méthodes
Préparation du ZIF-67
Tous les produits chimiques sont de qualité analytique et utilisés sans autre purification. Dans une synthèse typique, 1,436 g de Co(NO3 )2 ·6H2 O et 3,244 g de 2-méthylimidazole ont été dissous dans 100 ml de solution de méthanol, respectivement. Par la suite, le Co(NO3 )2 ·6H2 La solution O a été versée dans une solution de 2-méthylimidazole sous agitation pendant 12 min, puis vieillie pendant 20 h. Enfin, les précipités violets résultants ont été collectés par centrifugation, lavés plusieurs fois au méthanol et séchés à l'air à 60 °C.
Préparation de CoSe/NC
Le CoSe/NC a été préparé par la sélénisation de ZIF-67 avec de la poudre de sélénium. Dans une synthèse typique, le ZIF-67 et la poudre de sélénium ont été mélangés avec un rapport massique de 1:1. Par la suite, la poudre de mélange a été placée dans une nacelle en céramique au four tubulaire sous atmosphère d'Ar et chauffée à 800 °C pendant 4 h avec une vitesse de chauffage de 2 °C min −1 . À titre de comparaison, du CoSe pur a été préparé par une procédure similaire, sauf en utilisant de la poudre de cobalt comme matériau de départ.
Caractérisation des matériaux
Les diagrammes XRD de poudre des échantillons ont été obtenus sur un diffractomètre à rayons X TD-3500X avec un rayonnement Cu Kα (λ =1,5418 Å) à une vitesse de balayage de 0,05 s −1 . Les spectres Raman ont été enregistrés sur un spectromètre LabRAM HR800 Raman avec une lumière laser à 532 nm. L'ATG a été réalisée sur un thermoanalyseur STA 449 F3 sous atmosphère ambiante et à une vitesse de chauffe de 10 °C min −1 de la température ambiante à 900 °C. Les mesures XPS ont été effectuées sur un spectromètre photoélectronique à rayons X Thermo ESCALAB 250XI avec un rayonnement monochromatique Al Kα (hν =1486,6 eV). Les isothermes d'adsorption/désorption d'azote ont été recueillies à 77 K à l'aide d'un instrument BELSORP-Max, qui ont été utilisés pour évaluer la surface spécifique (BET) et la distribution de la taille des pores (BJH). Les images FESEM ont été collectées par microscopie électronique à balayage Quanta 250 et microscopie électronique à balayage SIGMA 500, respectivement. Les images MET et SAED ont été prises sur une microscopie électronique à transmission Tacnai G2 F20.
Mesures électrochimiques
Tous les comportements électrochimiques des échantillons tels que synthétisés ont été effectués à l'aide d'une cellule de type pièce CR2032. Les électrodes de travail ont été préparées en mélangeant 80 % en poids de matières actives, 10 % en poids de noir d'acétylène et 10 % en poids de liant fluorure de polyvinylidène (PVDF) dans un N approprié. -méthyl-2-pyrrolidone (NMP) pour former une suspension. Par la suite, la suspension a été uniformément enduite sur une feuille de Cu et séchée à 80 °C pendant 4 h à l'air, puis poinçonnée dans des disques d'un diamètre de 14 mm et séchée à 120 °C pendant 12 h sous vide. La feuille de lithium métallique a été utilisée à la fois comme contre-électrode et électrode de référence. L'électrolyte était de 1,00 M de LiPF6 dans du carbonate d'éthylène et du carbonate de diéthyle (EC :DEC =1:1) et le séparateur était un film Celgard 2500. Toutes les cellules ont été assemblées dans une boîte à gants remplie d'argon avec une teneur en oxygène et en humidité inférieure à 1 ppm. Les tests de charge-décharge galvanostatique ont été effectués sur un système de test de batterie Neware CT-3008W entre 0,01 et 3,0 V à température ambiante. Les mesures de voltamétrie cyclique (CV) entre 0,01 et 3,0 V à une vitesse de balayage de 0,2 mV s −1 et la spectroscopie d'impédance électrochimique (EIS) avec la plage de fréquences de 0,01 à 100 kHz ont toutes été réalisées sur un poste de travail électrochimique CHI 760E.
Résultats et discussion
La structure cristalline et la morphologie du ZIF-67 tel que synthétisé ont été confirmées par XRD et SEM, respectivement, comme le montre la Fig. 2. Le diagramme de diffraction du ZIF-67 est identique au modèle simulé et aux rapports précédents (Fig. 2a) [41 , 42]. Le ZIF-67 présente une morphologie décaédrique avec une taille de 300 nm, qui pourrait être vue à partir de l'image SEM (Fig. 2b et fichier supplémentaire 1 :Figure S1). Pendant ce temps, le ZIF-67 affiche un aspect violet similaire à la synthèse précédente. Ces résultats montrent la synthèse réussie de ZIF-67.
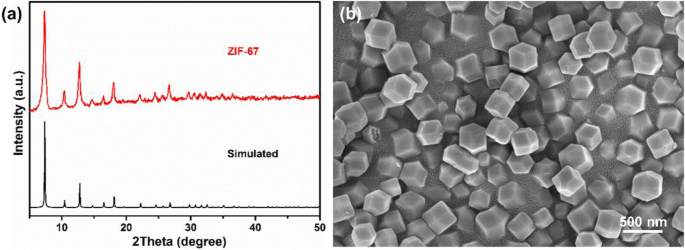
un Modèles XRD de ZIF-67 tel que synthétisé et modèles XRD simulés de ZIF-67. b Image SEM du ZIF-67 tel que synthétisé
La figure 3a présente les modèles XRD de CoSe/NC et de CoSe pur, dans lesquels tous les pics peuvent être attribués à CoSe (JCPDS 70-2870). En outre, les pics sont intenses et aucun autre pic ne peut être observé, suggérant la haute cristallisation et la pureté. Cependant, il n'y a pas de bosse ou de pic de matériaux carbonés dans le modèle XRD de CoSe/NC, ce qui pourrait être lié au degré de graphitisation et à la teneur en carbone. Pour confirmer la présence de carbone dans CoSe/NC, les spectres Raman ont été obtenus. Comme on peut le voir sur la Fig. 3b, deux larges pics à 1360 et 1590 cm −1 sont attribuées individuellement aux défauts (bande D) et au carbone graphitique ordonné (bande G), indiquant la présence de matériaux carbonés dans CoSe/NC [8]. La valeur de ID/IG est de 1,05, suggérant les matériaux carbonés avec des défauts riches. De plus, il y a un pic net et fort à 675 cm −1 , qui est liée à la liaison C–Se [22, 43]. La présence d'une liaison C-Se indique que la connexion entre CoSe et NC n'est pas une adsorption physique courante ; au lieu de cela, il s'agit d'une sorte de connexion chimique via une liaison C-Se. Par rapport à l'adsorption physique, la connexion chimique unique pourrait non seulement mieux favoriser la connexion électrique active entre CoSe et NC, mais également mieux atténuer la variation de volume. Le TGA a été utilisé pour déterminer la teneur en NC dans CoSe/NC. Selon la courbe TGA et l'équation chimique (Fig. 3c), le pourcentage massique de NC dans CoSe/NC est évalué à 11,7%. La figure 3d montre le N2 isotherme d'adsorption/désorption de CoSe/NC avec une isotherme typique de type IV et une boucle d'hystérésis de type H3, suggérant la caractéristique mésoporeuse. Le CoSe/NC présente une grande surface spécifique (BET) de 49,958 m 2 g −1 . Cependant, la surface spécifique de CoSe/NC est bien inférieure à celle du précurseur ZIF-67, ce qui peut être causé par l'effondrement de la structure de ZIF-67 pendant le processus de calcination et l'expansion de volume due à la formation de CoSe. La distribution de la taille des pores (BJH) affiche les pores primaires dans une plage de 1 à 10 nm avec une taille moyenne de 7,238 nm. La grande surface spécifique et la structure mésoporeuse sont avantageuses pour la pénétration de l'électrolyte et le transport rapide de Li + .
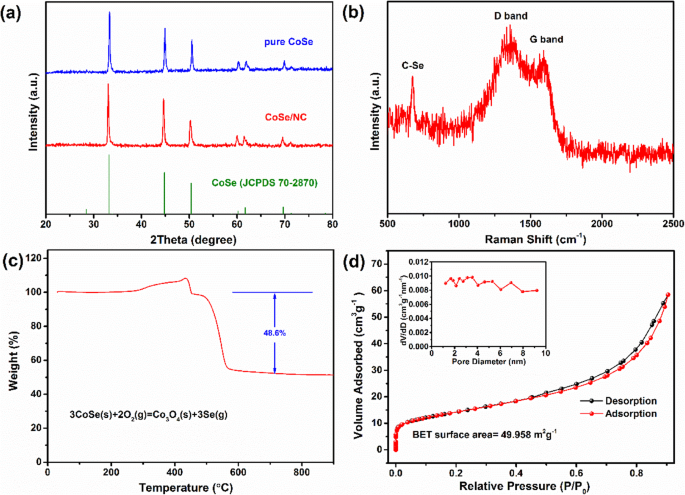
un Modèles XRD de CoSe/NC et de CoSe pur. b Spectres Raman de CoSe/NC. c Courbe TGA de CoSe/NC. d Isotherme d'adsorption-désorption d'azote et profils de distribution de diamètre de CoSe/NC.
XPS a été introduit pour caractériser la composante élémentaire et l'état de valence dans CoSe/NC, comme le montre la Fig. 4. L'étude de CoSe/NC montre la présence d'éléments Co, Se, C, N et O (Fig. 4a). Les pics caractéristiques du Co 2p1/2 et Co 2p3/2 a pu être observé à 796.92 et 780.94 eV dans le spectre Co 2p, qui pourrait être attribué au CoSe (Fig. 4b). Les deux pics situés à 785.55 et 802.53 eV sont les satellites shakeup de Co 2+ [22, 44, 45]. De plus, les deux autres pics à 793.03 et 778 eV sont probablement liés à CoOx , qui est causée par l'environnement oxydé. Le spectre Se 3d affiche deux pics à 54,94 et 54,08 eV, qui pourraient être attribués à Se 3d3/2 et Se 3d5/2 , respectivement (Fig. 4c). Le spectre C 1s (Fichier supplémentaire 1 :Figure S2) présente trois pics, qui pourraient être indexés sur C 1s, Nsp 2 -C, et Nsp 3 -C, respectivement. Le spectre N 1s de la figure 4d présente un pic N graphitique à 287,6 eV, un pic N pyrrole à 286 eV et un pic N pyridine à 284,7 eV, respectivement, indiquant que le lieur organique a été converti en carbone dopé à l'azote par calcination [8, 46]. Les résultats sont identiques au spectre C 1s. En outre, l'analyse quantitative de XPS a été menée. Les résultats sont présentés dans le tableau 1, qui suggère que la teneur en azote dans CoSe/NC est de 12,08 % (% atomique) et les teneurs en N graphitique, pyrrole N et pyridine N sont de 35,02 %, 37,46 % et 27,52 % (atomes %), respectivement. Sur la base des rapports précédents, d'une part, l'azote dopé est bénéfique pour améliorer la conductivité; d'autre part, le pyrrole N et la pyridine N peuvent augmenter le stockage du lithium en tant que site électrochimiquement actif.
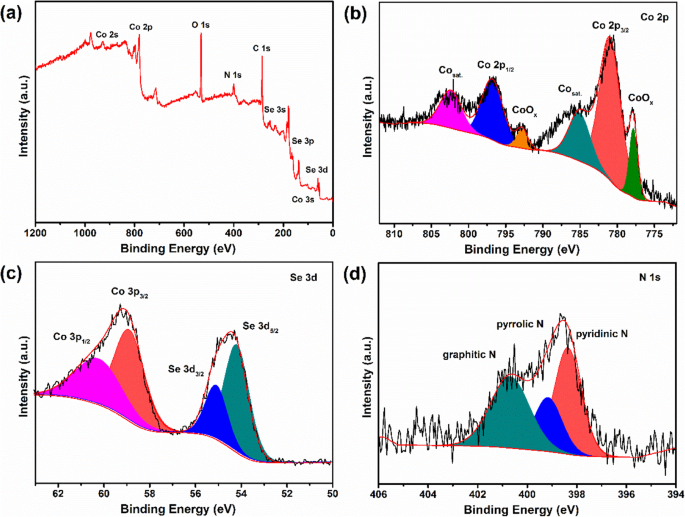
Spectres XPS de CoSe/NC :a sondage, b Co 2p, c Se 3d, et d N 1s
La morphologie et la microstructure de CoSe/NC ont été caractérisées par SEM et MET. Comme le montre la figure 5a, l'image SEM de CoSe/NC montre que les nanoparticules de CoSe sont enveloppées par NC avec une taille de 30 à 70 nm. Cependant, le CoSe/NC ne peut pas hériter de la morphologie décaédrique du précurseur ZIF-67 en raison de l'effondrement de la structure et de l'expansion de volume, comme mentionné précédemment. Les résultats du spectromètre à dispersion d'énergie (EDS) suggèrent la présence de Se, Co, C, N et O dans CoSe/NC, et le pourcentage d'azote est de 0,27 % (% en poids) (Fichier supplémentaire 1 :Figure S3 et tableau S1) . En outre, les images de cartographie élémentaire sont présentées sur la figure 5b, qui suggèrent la distribution uniforme de Se, Co, C et N. L'image TEM révèle en outre la structure, dans laquelle la structure de revêtement des nanoparticules de CoSe enveloppées de nanocouches NC pourrait être clairement observé (Fig. 5c, d). Dans la structure de revêtement, les nanocouches NC pourraient de préférence améliorer la conductivité et restreindre l'expansion de volume pendant le processus d'insertion de lithium. L'image HRTEM présente un espacement intercouche distinct de 2,69 Å, qui pourrait être bien indexé au plan de réseau (101) de CoSe (Fig. 5e). Pendant ce temps, notez que les nanocouches NC périphériques sont amorphes, ce qui est cohérent avec le résultat de Raman. Le diagramme SAED montre plusieurs anneaux de diffraction et non des taches, indiquant que le CoSe/NC tel que synthétisé est polycristallin. Ces anneaux pourraient correspondre aux plans de réseau (101), (110) et (112) de CoSe, qui est pris en charge par XRD (Fig. 5f).

un Image SEM de CoSe/NC. b Images de cartographie élémentaire de CoSe/NC. c , d Images MET de CoSe/NC. e Images HRTEM de CoSe/NC. f Modèle SAED de CoSe/NC
Pour explorer le comportement électrochimique du CoSe/NC, les courbes CV ont été réalisées avec une vitesse de balayage de 0,2 mV s −1 (Fig. 6a). Comme on peut le voir, il y a un pic de réduction net à 1,15 V et une faible bosse à 0,64 V dans le balayage cathodique initial, correspondant à la conversion de CoSe en Co et Li2 Se et la constitution de la couche SEI [22, 44, 45, 47]. Quant au balayage anodique, le pic d'oxydation se situe à 2.15 V qui est attribué à la formation de CoSe à partir de Co et Li2 Se, et se chevauchent bien avec ceux des balayages consécutifs, suggérant l'excellente stabilité cyclique. Dans les deuxième et troisième balayages cathodiques, les pics de réduction passent à 1,37 à partir de 1,15 V. Les courbes CV du CoSe pur montrent la même caractéristique avec CoSe/NC (Fichier supplémentaire 1 :Figure S4). Pour évaluer les performances de stockage du lithium du CoSe/NC, le test de décharge/charge galvanostatique a été réalisé. Comme indiqué dans les courbes de décharge/charge galvanostatique de CoSe/NC à 0,1 A g −1 , il existe des plates-formes de décharge et de charge évidentes à 1,4 et 2,0 V, qui sont en accord avec les positions des pics de réduction et d'oxydation dans les courbes CV susmentionnées (Fig. 6b). De plus, les capacités initiales de décharge et de charge sont de 1049,42 et 535,18 mAh g −1 , séparément, avec un CE de 50,99 %. La grande capacité irréversible et le faible CE sont attribués à la constitution de la couche SEI dans le processus de décharge initial. Il est à noter que les 100e capacités de décharge et de charge atteignent 1199,34 et 1158,88 mAh g −1 , qui est supérieure à la capacité de décharge initiale, et il n'y a pas de plates-formes évidentes.
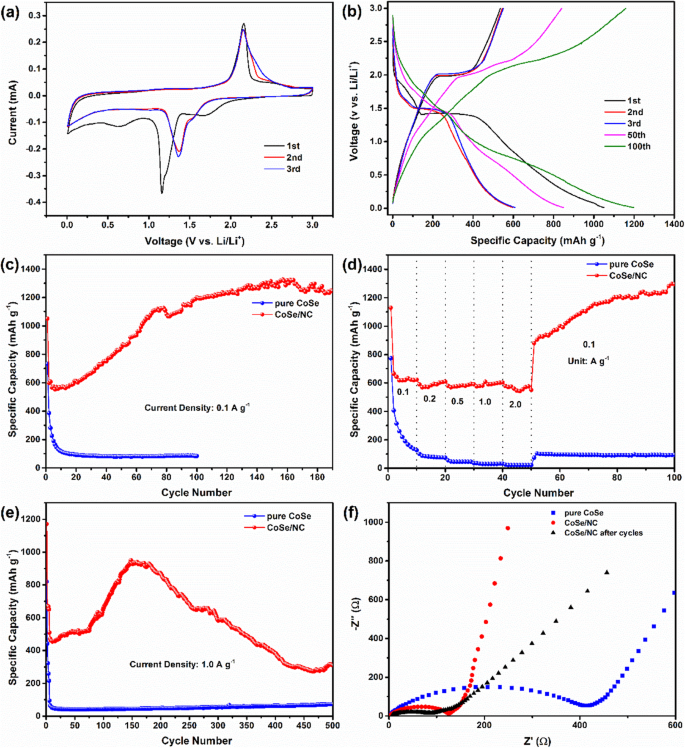
un Les courbes CV de CoSe/NC à 0.2 mV s −1 . b Profils de tension de décharge/charge galvanostatique de CoSe/NC à 0,1 A g −1 . c Performances de cyclage du CoSe/NC et du CoSe pur à 0,1 A g −1 . d Performances de taux de CoSe/NC et de CoSe pur à 0,1 à 1,0 A g −1 . e Performances cycliques à courant long du CoSe/NC et du CoSe pur à 1,0 A g −1 . f Spectres EIS de CoSe pur et CoSe/NC avant et après cyclage
La figure 6c affiche la propriété cyclique de CoSe/NC à 0,1 A g −1 . On a pu observer qu'il existe un comportement incrémentiel distinct de la capacité de décharge pendant tout le cycle, combiné à l'absence de plates-formes susmentionnées dans les 100e courbes, qui peut être attribué à une pseudocapacité qui est une sorte de réaction redox se produisant à l'extérieur des matériaux d'électrode. [45, 47]. Au cours des plusieurs cycles initiaux, la surface pour la pseudocapacité est moindre. Au cours des cycles suivants, les nanoparticules de CoSe se sont pulvérisées en petits morceaux à cause de l'expansion de volume. Par conséquent, il y a plus de sites actifs pour la pseudocapacité. Du fait que les nanoparticules de CoSe sont recouvertes de nanocouches NC, l'intégrité de la structure totale est maintenue. Le CoSe/NC affiche une première capacité de décharge de 1049,42 mAh g −1 . Au 157e cycle, la capacité spécifique atteint la valeur maximale de 1325 mAh g −1 . Dans les cycles suivants, la capacité spécifique diminue progressivement. Après 190 cycles, il reste 1244 mAh g −1 . La performance de débit de CoSe/NC a été évaluée à des densités de courant distinctes de 0,1, 0,2, 0,5, 1,0 et 2,0 A g −1 (Fig. 6d). Après 10 cycles au-dessus d'une série de densités de courant, les capacités correspondantes sont de 623,21, 609,72, 590,34, 603,77 et 551,33 mAh g −1 , séparément. Notamment, la densité de courant passe de 0,1 à 2,0 A g −1 , et la capacité diminue simplement de 11,5%, indiquant que CoSe/NC possède des performances de débit exceptionnelles. Lorsque la densité de courant revient à 0,1 A g −1 , la capacité revient rapidement à 880,09 mAh g −1 et monte progressivement jusqu'à 1295,81 mAh g −1 après 50 cycles, ce qui suggère que le CoSe/NC conserve toujours l'intégrité structurelle même à 2,0 A g −1 .
La propriété de stockage du lithium du CoSe/NC à une grande densité de courant de 1,0 A g −1 a également été réalisée, comme le montre la figure 6e. Pour générer une couche SEI homogène et compacte, CoSe/NC a été cyclé à 0,05 A g −1 pour les 5 premiers cycles. Généralement, d'une part, la forte densité de courant va conduire à un comportement de polarisation important qui limite le dégagement de capacité; d'autre part, cela endommagera la structure des matériaux des électrodes, ce qui entraînera une décoloration rapide de la capacité. Cependant, lorsque la densité de courant atteint 1,0 A g −1 , la capacité réversible est de 509,09 mAh g −1 . Dans les cycles suivants, la capacité réversible de CoSe/NC présente un comportement croissant similaire à ceux à 0,1 A g −1 et les performances de taux. Au 148e cycle, la capacité réversible atteint au maximum 950,27 mAh g −1 . Après 500 cycles, CoSe/NC reste une capacité réversible relativement importante de 310,11 mAh g −1 . Quant au CoSe pur, la capacité réversible n'est que d'environ 72,75 mAh g −1 , ce qui est bien inférieur à celui de CoSe/NC. Une telle performance exceptionnelle de stockage du lithium de CoSe/NC pourrait être attribuée aux nanocouches NC, qui pourraient fournir une capacité supplémentaire en tant que sites actifs et améliorer la conductivité, et les liaisons C-Se entre les nanocouches NC et les nanoparticules de CoSe qui pourraient aider les nanocouches NC à mieux tamponner le contrainte causée par le changement de volume pendant le processus de cyclage.
La figure 6f montre l'EIS du CoSe pur et du CoSe/NC (avant et après 100 cycles à 0,1 A g −1 ). Les trois parcelles de Nyquist présentent les mêmes caractéristiques, un demi-cercle et une ligne inclinée. Le diamètre du demi-cercle est lié à la résistance de transfert de charge et à la résistance interne. Comme on peut le voir, le demi-cercle dans CoSe/NC est clairement plus petit que celui de CoSe, suggérant que CoSe/NC possède une meilleure conductivité électrique, qui devrait être attribuée aux nanocouches NC. De plus, après 100 cycles à 0,1 A g −1 , le diamètre de CoSe/NC diminue qu'auparavant, ce qui peut être associé à la constitution de couche SEI sur l'apparition des matériaux d'électrode et à la pulvérisation de nanoparticules de CoSe pour augmenter la surface de contact entre l'électrode et l'électrolyte.
Pour étudier et analyser davantage le comportement d'augmentation de capacité de CoSe/NC, la cinétique électrochimique a été menée sur la base des mesures CV à diverses vitesses de balayage de 0,2 à 1,0 mV s −1 après 100 cycles à 0,1 A g −1 (Fig. 7a). Selon le mécanisme de génération de capacité, la capacité pourrait être divisée en deux types, la capacité à diffusion contrôlée qui est une sorte de réaction redox en phase globale (insertion/extraction typique d'ions lithium) et la capacité à contrôle capacitif qui comprend une double couche capacité et pseudocapacité. Au contraire, la capacité à contrôle capacitif se produit à la surface des matériaux d'électrode, la capacité à double couche est un processus d'adsorption physique, mais la pseudocapacité est une réaction redox hautement réversible. Dans les courbes CV, la pertinence entre le courant (i) et la vitesse de balayage (ν) pourrait être représentée par une équation, comme suit [48,49,50,51] :
$$ i=a{\nu}^b $$ (1) $$ \mathit{\log}i=blog\nu +\mathit{\log}a $$ (2)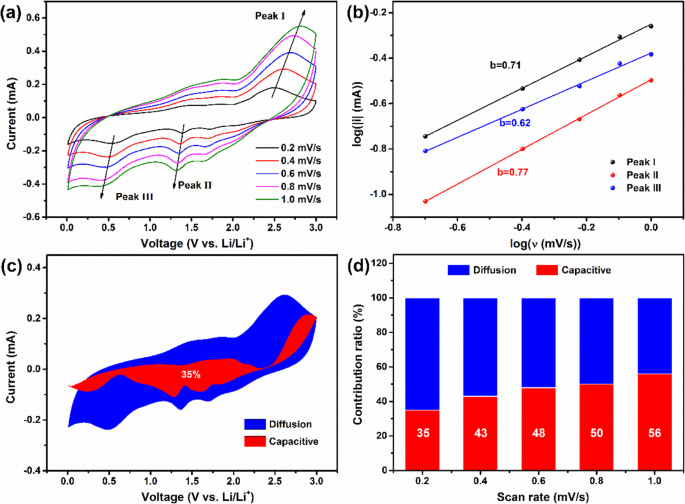
un Courbes CV de CoSe/NC après 100 cycles à 0,2 à 1,0 mV s −1 . b Diagrammes de log ν en fonction de log |i| pour les trois pics des courbes CV. c Contribution capacitive et diffusion contrôlée au stockage de charge à 0,2 mV/s. d Rapport de contribution des capacités capacitives et contrôlées par diffusion à 0,2 à 1,0 mV s −1
où a et b sont des valeurs ajustables. Si b =0,5, suggérant un processus contrôlé par la diffusion. Cependant, la valeur de b est de 1,0, correspondant au processus à commande capacitive. Pour déterminer la valeur de b , Éq. (1) est transformé en Eq. (2). La valeur de b pourrait être obtenu en calculant la pente de log (ν) par rapport à log (i ). Selon la méthode mentionnée ci-dessus, le b les valeurs des pics I, II et III dans les courbes CV sont quantifiées à 0,71, 0,62 et 0,77, séparément, ce qui suggère que la capacité est due à un processus de contrôle hybride, comme le montre la figure 7b. La contribution de capacité spécifique de deux processus de contrôle pourrait également être obtenue sur la base de l'équation suivante :
$$ i(V)={k}_1\nu +{k}_2{\nu}^{1/2} $$ (3) $$ i(V)/{\nu}^{1/2} ={k}_1{\nu}^{1/2}+{k}_2 $$ (4)où k 1 et k 2 sont des valeurs ajustables. Le courant (i ) est composé de composants à commande capacitive (k 1 ν ) et procédé à diffusion contrôlée (k 2 ν 1/2 ). Afin de calculer les valeurs de k1 et k 2 ν 1/2 , Éq. (3) est converti en Eq. (4). Les valeurs de k 1 et k 2 correspondent à la pente et à l'interception de i(V )/ν 1/2 contre ν 1/2 , respectivement. Selon cette méthode, k 1 ν et k 2 ν 1/2 à divers potentiels pourraient être acquises. Comme le montre la figure 7c, la zone représente le rapport de contribution ; la contribution du procédé à contrôle capacitif est de 37% à 0.2 mV s −1 . Les ratios de contribution à d'autres taux de balayage sont également effectués (Fig. 7d). Les taux de contribution du processus à commande capacitive sont de 43 %, 48 %, 50 % et 56 % à 0,4, 0,6, 0,8 et 1,0 mV s −1 , respectivement. Les résultats ci-dessus démontrent que le processus électrochimique de CoSe/NC est un processus de contrôle hybride.
Conclusions
En résumé, les composites CoSe/NC d'origine ont été préparés en utilisant le ZIF-67 comme précurseur, dans lequel les nanoparticules de CoSe sont recouvertes de nanocouches NC et elles sont reliées par des liaisons C-Se. Dans les composites tels que préparés, les nanocouches NC pourraient améliorer la conductivité du CoSe, tamponner l'expansion volumique et participer à la réaction de stockage du lithium en tant que siège actif. La structure du revêtement et les liaisons C-Se rapprochent les nanoparticules de CoSe et les nanocouches NC, ce qui est bénéfique pour le travail des nanocouches NC pour améliorer les propriétés électrochimiques. Par conséquent, les composites CoSe/NC présentent une capacité cyclique et des performances de taux exceptionnelles en tant que matériaux d'anode pour les LIB. Les composites CoSe/NC pourraient offrir une capacité réversible de 1244 mAh g −1 après 190 cycles à 0,1 A g −1 . Même à une densité de courant élevée de 1,0 A g −1 , il peut rester 310,11 mAh g −1 après 500 cycles. Par ailleurs, selon les résultats de la cinétique électrochimique, le processus électrochimique de CoSe/NC est un processus de contrôle hybride. Ces résultats indiquent que la préparation de composés métalliques/composites carbonés en utilisant des MOF, en tant que précurseur, est une stratégie valable pour améliorer les propriétés de stockage du lithium des composés métalliques.
Disponibilité des données et des matériaux
Toutes les données sont entièrement disponibles sans restriction.
Abréviations
- BET :
-
Brunauer-Emmett-Teller
- BJH :
-
Barrett-Joyner-Halenda
- CV :
-
Voltamétrie cyclique
- DMC :
-
Carbonate de diéthyle
- CE :
-
Carbonate d'éthylène
- EDS :
-
Spectromètre à dispersion d'énergie
- EIS :
-
Spectroscopie d'impédance électrochimique
- LIB :
-
Batteries lithium-ion
- MOF :
-
Charpentes organométalliques
- NC :
-
Carbone dopé N
- PVDF :
-
Fluorure de polyvinylidène
- TEM :
-
Microscopie électronique à transmission
- TGA :
-
Analyse thermogravimétrique
- XPS :
-
Spectroscopie photoélectronique aux rayons X
- XRD :
-
Diffraction de puissance des rayons X
Nanomatériaux
- Les meilleurs matériaux d'impression 3D en métal pour la fabrication additive
- Qualités PVDF renouvelables pour batteries lithium-ion
- Synthèse facile de nanoparticules SiO2@C ancrées sur MWNT en tant que matériaux anodiques hautes performances pour batteries Li-ion
- Synthèse et propriétés électrochimiques des matériaux cathodiques LiNi0.5Mn1.5O4 avec dopage composite Cr3+ et F− pour batteries lithium-ion
- Composite MoS2/noir d'acétylène à quelques couches comme matériau d'anode efficace pour les batteries lithium-ion
- Préparation de micromatériaux hybrides MnO2 revêtus de PPy et de leurs performances cycliques améliorées en tant qu'anode pour batteries lithium-ion
- Effet de différents liants sur les performances électrochimiques des anodes à oxyde métallique pour les batteries lithium-ion
- Composite Si/Graphène intégré fabriqué par réduction thermique au magnésium comme matériau d'anode pour les batteries lithium-ion
- Option métal pour l'usinage CNC



