Synthèse ionothermique de silicium nanoporeux cristallin et son utilisation comme matériaux d'anode dans les batteries lithium-ion
Résumé
Le silicium a un grand potentiel en tant que matériau d'anode pour les batteries lithium-ion (LIB) hautes performances. Ce travail rapporte une approche facile, à haut rendement et évolutive pour préparer du silicium nanoporeux, dans lequel le siliciure de magnésium commercial (Mg2 Si) a réagi avec le liquide ionique acide à 100°C et à pression ambiante. Le silicium obtenu est constitué d'une structure cristalline et poreuse d'une surface BET de 450 m 2 /g et taille de pores de 1,27 nm. Lorsqu'ils sont recouverts de la couche de carbone dopé à l'azote et appliqués comme anode LIB, les composites nanoporeux silicium-carbone obtenus présentent une efficacité coulombienne initiale élevée de 72,9% et possèdent une capacité spécifique de 1000 mA h g −1 à 1 A g −1 après 100 cycles. Cette méthode de préparation n'implique pas de récipients à haute température et pression et peut être facilement appliquée pour la production de masse de matériaux de silicium nanoporeux pour batterie lithium-ion ou pour d'autres applications.
Introduction
L'augmentation rapide de la consommation et la forte dépendance à l'égard des énergies fossiles dans la société contemporaine ont provoqué un malaise croissant à l'égard de l'environnement, du climat et de l'approvisionnement énergétique. Il existe une demande pressante pour le développement de dispositifs et de systèmes énergétiques durables et portables à haute énergie et à haute densité de puissance pour résoudre l'inadéquation entre la source d'énergie temporelle et l'environnement pour les modes de vie modernes [1]. Les batteries lithium-ion rechargeables (LIB) sont très prometteuses pour les dispositifs de stockage d'énergie en raison de leur densité d'énergie relativement élevée et de leur stabilité à long cycle [2, 3]. Pour répondre aux exigences croissantes des LIB hautes performances, divers matériaux d'électrodes à haute capacité sont largement développés, tels que les matériaux carbonés amorphes poreux [4, 5], les composites à base de phosphore [6, 7], les composites à base de silicium [8 ], et les oxydes de métaux de transition [9, 10]. En tant que composant vital, le silicium (Si) est l'un des matériaux anodiques les plus impressionnants en raison de sa grande capacité théorique (4 200 mAh g −1 ), des sources naturelles abondantes et une tension d'absorption Li relativement sûre [11]. Néanmoins, la commercialisation pratique à grande échelle du matériau anodique de silicium est en proie à deux problèmes complexes. D'une part, l'énorme expansion et contraction volumétriques dans les processus de charge et de décharge conduisent à la rupture de la matière active silicium, un évanouissement rapide et irréversible de la capacité de la batterie [12]. D'autre part, la faible électroconductivité intrinsèque (1,6 × 10 −3 S/m) de silicium élémentaire entrave également considérablement le transfert d'électrons et diminue la capacité de débit de l'électrode.
Récemment, des efforts considérables ont été déployés pour contourner les problèmes de stabilité mentionnés ci-dessus [13]. Un grand nombre de matériaux de silicium nanostructurés, notamment des nanotubes [14], des nanofils/nanorods [15, 16] et des nanofeuilles [17, 18, 19] ont été conçus pour obtenir une intégrité structurelle et des performances de cycle améliorées. De plus, la préparation de composites poreux à base de Si est également considérée comme une méthode efficace, car les espaces poreux appropriés dans les composites de silicium poreux pourraient agir comme des tampons pour atténuer l'expansion de volume et ainsi améliorer les performances de cyclage dans les LIB [20, 21]. Par exemple, Kim et al. a fabriqué des particules de silicium poreux tridimensionnelles par recuit thermique et gravure de gels de Si coiffés de butyle et de SiO2 nanoparticules à 900 °C sous atmosphère d'Ar, qui présentaient une capacité stable de plus de 2800 mA h g −1 après 100 cycles à 1 °C [22]. An et al. a signalé une voie verte, évolutive et contrôlable pour préparer du silicium nanoporeux (NP-Si) avec d'excellentes propriétés électrochimiques à partir du Mg2 commercial Alliage de Si par distillation sous vide à haute température [23]. Bien que d'énormes progrès dans les performances électrochimiques aient été démontrés, la plupart des méthodes de préparation de ces structures nanoporeuses de Si sont généralement trop compliquées pour être mises à l'échelle.
Une autre tactique efficace pour augmenter les performances électrochimiques de l'anode de silicium consiste à enduire du carbone électroniquement conducteur sur des particules de nanosilicium pour former des nanocomposites silicium-carbone [19, 24], tels que le jaune-enveloppe [25], la pastèque [26] et les structures creuses [ 27]. Par exemple, Pan et al. conçu des nanocomposites Si–C à structure jaune-coquille avec une capacité spécifique élevée et une bonne stabilité au cyclage par une méthode simple et peu coûteuse basée sur la technologie de gravure NaOH [28]. Chen et al. développé un Si/B4 structuré noyau-coque C avec revêtement en graphite et a démontré que ces composites possédaient une bonne stabilité au cyclage à long terme [29]. Diverses études ont démontré que le carbone conducteur pouvait non seulement constituer la faible conductivité électrique du silicium, mais aussi servir d'intermédiaire élastique pour retarder le grand changement de volume et empêcher le contact direct entre les matériaux actifs du silicium et l'électrolyte, conduisant à une stabilité de cyclage améliorée. [30].
À ce jour, les voies de synthèse vers les nanoparticules de silicium (Si NPs) ou le silicium poreux (pSi) impliquent généralement la décomposition thermique des silanes [31], la gravure chimique des plaquettes de Si et la réduction magnésiothermique de SiO2 modèles [32, 33]. Ces préparations nécessitent généralement plusieurs étapes, une température élevée, des gabarits relativement coûteux, etc., ce qui entraîne un coût élevé et des difficultés de mise à l'échelle [34]. Récemment, la préparation de Si NPs en solution a également fait l'objet d'une grande attention [35, 36]. Par exemple, Kauzlarich et al. a signalé que SiCl4 réagi avec NaSi ou KSi dans des solvants organiques pour obtenir des nanoparticules de silicium [37]. Liang et al. préparé les nanosphères de silicium en forme de nid via une réaction solvothermique, dans laquelle NaSi a réagi avec NH4 Br dans le solvant mixte pyridine et diméthoxyéthane en autoclave à 80°C pendant 24h [38]. La synthèse de solution rapportée impliquait généralement des agents réducteurs hautement actifs tels que les métaux alcalins, LiAlH4 , et NaSi et ont souvent produit de faibles rendements ou de petites quantités de Si NP. À cet égard, pour la fabrication de masse de nanosilicium, une approche simple, évolutive et peu coûteuse est toujours impérative. Nous présentons ici une préparation pratique et à haut rendement de silicium poreux par oxydation de Mg2 Si dans un liquide ionique acide à 100°C et pression ambiante. Lorsqu'ils sont recouverts d'une couche de carbone dopé à l'azote et ont servi d'anode de batterie lithium-ion, les composites nanoporeux silicium-carbone obtenus présentaient une efficacité coulombienne initiale (CE) élevée de 72,9% et délivraient une capacité spécifique de 1000 mA h g −1 après 100 cycles à 1 A g −1 .
Méthodes
Matériaux
Le chlorure de 1-butyl-3-méthylimidazolium ([Bmim]Cl) a été fourni par Shanghai Cheng Jie Chemical Co. LTD. Chlorure d'aluminium (AlCl3 ) a été acheté auprès de Sinopharm Chemical Reagent Co., Ltd. Siliciure de magnésium (Mg2 Si) et de la poudre de silicium commerciale (1 à 5 µm) ont été achetées à Alfa Aesar. Carbonate d'éthylène (EC), carbonate de diéthyle (DEC), carbonate de fluoroéthylène (FEC) et LiPF6 de qualité batterie ont été achetés à Shenzhen Kejingstar Technology Ltd., Chine. Tous les produits chimiques et réactifs ont été utilisés directement tels qu'ils ont été reçus.
Synthèse de nanoparticules de silicium poreux (pSi)
Dans une procédure typique, [Bmim]Cl (1.5 g) et AlCl3 (4,5 g) avec un rapport molaire de ~ 1:4 ont été mélangés et chargés dans un tube de verre Schlenk. Par la suite, 500 mg de siliciure de magnésium (Mg2 Si) ont été ajoutés dans le tube en verre et vigoureusement agités à 100°C pendant 10h. La procédure ci-dessus a été menée dans une boîte à gants remplie d'Ar. Après refroidissement, le précipité a été récupéré et lavé avec de l'acide chlorhydrique 1 M, de l'eau distillée et de l'éthanol. Enfin, le produit (150 mg, 82% de rendement) a été séché sous vide pour une caractérisation plus poussée.
Synthèse de carbone dopé à l'azote enrobé de nanoparticules de silicium poreux (pSi@NC)
La procédure de préparation est référencée dans la littérature rapportée [39, 40]. Tout d'abord, 0,1 g des nanoparticules de silicium poreux (pSi) obtenues ont été dispersées dans 250 mL d'eau déminéralisée contenant du dodécylbenzènesulfonate de sodium (SDBS; 5 mg) par ultrasonication pendant 30 min. Le mélange a été vigoureusement agité pendant 1 h à température ambiante. Après cela, 200 μL de monomère de pyrrole, 0,34 g de (NH4 )2 S2 O8 , et 1,25 mL de HCl 1 M ont été ajoutés dans la solution ci-dessus. Après agitation du mélange dans un bain de glace/eau pendant 24 h, les poudres noires formées (notées pSi@PPy) ont été recueillies par filtration, lavées avec de l'eau déminéralisée et séchées sous vide. Enfin, l'échantillon pSi@PPy a été chauffé à une vitesse de rampe de 5 °C min −1 dans un four tubulaire à 700 °C pendant 3 h sous un courant d'atmosphère d'Ar pour obtenir le composite pSi@NC. La teneur en carbone a été estimée par des études thermogravimétriques.
Mesures électrochimiques
Les propriétés électrochimiques des nanoparticules de silicium poreux ont été étudiées en utilisant une demi-pile bouton CR2032, dans laquelle des feuilles métalliques de lithium servaient de contre-électrodes et d'électrode de référence, le pSi@NC tel que préparé comme électrode de travail, des films macroporeux de polypropylène (Celgard 2400) comme séparateurs. , et 1,0 M LiPF6 dans un mélange 1:1 (v/v) de carbonate d'éthylène (EC)/carbonate de diéthyle (DEC) comme électrolyte. Les cellules CR2032 ont été assemblées en boîte à gants sous atmosphère d'argon (teneurs en oxygène et en eau inférieures à 0,1 ppm). Les électrodes d'anode de travail ont été préparées en mélangeant le composite pSi@NC obtenu, du carbone super P et de l'alginate de sodium dans un rapport pondéral de 70:20:10 dans de l'eau déminéralisée pour former une suspension homogène. Ensuite, la suspension a été appliquée sur une feuille de Cu et séchée sous vide à 80°C pendant 12h. La masse totale de chargement des matériaux actifs sur l'électrode était d'environ 0,5 mg cm −2 . Les cycles de charge-décharge des demi-cellules ont été effectués sur un testeur de batterie Neware (Shenzhen, Chine) à un mode de courant constant sur la plage de 0,01 à 1,5 V. La voltamétrie cyclique (CV) des anodes telles que préparées a été mesurée sur un poste de travail électrochimique CHI650d (Shanghai Chenhua Instruments Inc., Chine), utilisant une cellule à trois électrodes avec un taux de balayage de tension de 0,2 mV s −1 à température ambiante. La capacité spécifique a été calculée sur la base de la masse totale des composites pSi@NC.
Méthodes de caractérisation
Les mesures de diffraction des rayons X de puissance (PXRD) ont été réalisées sur un diffractomètre à rayons X Bruker D8 ADVANCE (rayonnement Cu Kα, 40 kV, 40 mA, λ = 1,5418 Å). La morphologie et la microstructure des échantillons ont été obtenues par microscopie électronique à balayage (microscope électronique à balayage à émission de champ Hitachi, S-4800), et la spectroscopie à rayons X à dispersion d'énergie a été utilisée pour analyser la distribution élémentaire. Des images de microscopie électronique à transmission (MET) et de MET haute résolution ont été enregistrées sur un équipement JEM-2100. Les paramètres poreux ont été déterminés à l'aide d'un analyseur Micromeritics ASAP 2020 à 77 K après dégazage de l'échantillon à 150 °C pendant 10 h. La surface spécifique a été calculée à l'aide de la méthode Brunauer-Emmett-Teller (BET) à points multiples et la distribution de la taille des pores a été analysée par la méthode de la théorie fonctionnelle de la densité (DFT) basée sur les données d'adsorption. La spectroscopie Raman (LabRAM Aramis, Horiba, équipée d'un laser de longueur d'onde de 633 nm) a été utilisée pour étudier la structure du silicium nanoporeux, qui a d'abord été calibré avec une plaquette de Si (520 cm −1 ). Le spectromètre PHI 5000 VersaProbe a été utilisé pour les mesures de spectroscopie photoélectronique à rayons X (XPS). L'analyse thermogravimétrique (TGA) a été réalisée sur un analyseur thermique simultané STA449F3 (Netzche) sous atmosphère d'air à 10 °C min −1 de 30 à 800°C dans l'air circulant. Des tests de voltamétrie cyclique (CV) ont été effectués sur une station électrochimique CHI650d (Shanghai Chenhua Instruments Inc., Chine).
Résultats et discussion
La préparation de nanoparticules de silicium poreux (pSi) à partir de Mg2 Si dans le liquide ionique peut être exprimé en tant que réaction 1, comme indiqué dans le schéma 1. Pour comprendre le processus de réaction, les produits vierges de la réaction 1 proposée sans aucun traitement de lavage ont été directement collectés et analysés par PXRD (Fichier supplémentaire 1 :Figure S1) . L'analyse PXRD a montré que le produit vierge était principalement composé de Si cristallin, sous-produit de sels inorganiques MgCl2 , et réactifs Mg2 Si et AlCl3 . Dans le processus de préparation de nanoparticules de silicium poreux, du chlorure de 1-butyl-3-méthylimidazole et du trichlorure d'aluminium dans un rapport molaire de 1:4 ont été mélangés pour garantir que le système réactionnel est acide. Ensuite, Mg2 Si a réagi avec le système acide pour former les nanoparticules de silicium. Le rendement en nanoparticules de silicium poreux était supérieur à 82 % sur la base de la quantité d'atomes de Si dans Mg2 Si. La réaction a été effectuée dans un ballon, permettant une production de masse de pSi facilement évolutive. L'utilisation de liquide ionique [BmimCl]-AlCl3 était nécessaire pour la préparation du pSi. Sans AlCl3 , la réaction de Mg2 Si avec [BmimCl] n'a pas pu avoir lieu. De même, le Mg2 Si n'a pas pu réagir avec AlCl3 seul ou dans d'autres solvants organiques tels que le tétrahydrofurane pour produire du pSi. Nous avons noté que le pSi avait été préalablement préparé par décomposition thermique de silanes ou d'halogénures de silicium à haute température, ou de leurs réactions avec des agents réducteurs hautement actifs tels que les métaux alcalins, LiAlH4 , et NaSi [37, 41]. L'utilisation de Mg2 Le Si dans la préparation de silicium nanostructuré par distillation du Mg à haute température est également connu [23, 42, 43]. Cependant, ces réactions ont souvent produit de faibles rendements ou de petites quantités de pSi. En revanche, la méthode rapportée dans ce travail est applicable pour la production de masse de pSi.
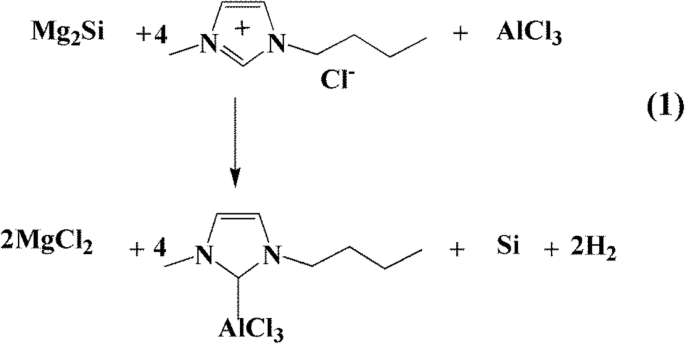
La réaction proposée pour la préparation du pSi
Le modèle PXRD du produit est illustré à la Fig. 1a. Ces cinq pics étroits et pointus à 2θ 28,4, 47,3, 56,1, 69,1 et 76,4° sont attribués aux plans de réseau (111), (220), (311), (400) et (331) de la phase de silicium cubique (JCPDS n° 27-1402), ce qui suggère que le silicium obtenu est hautement cristallin. La taille moyenne des cristallites des particules de silicium obtenues était d'environ 40 nm sur la base de l'équation de Scherrer. La figure 1b représente les spectres Raman des nanoparticules de silicium. Le pic caractéristique typique situé à environ 518 cm −1 correspond au mode d'étirement Si-Si du Si cristallin. La large bande entre 900 et 1050 cm −1 doit être attribué au spectre de second ordre du silicium [44]. Et le petit pic à ~ 303 cm −1 a été attribuée à l'oxyde de surface. Les surfaces spécifiques et la caractérisation de la porosité des échantillons obtenus ont été élucidés par N2 isothermes d'adsorption/désorption à 77 K. L'échantillon de pSi présente des courbes de sorption isothermes de type IV(a) avec une boucle d'hystérésis hybride H2(b)/H3, caractéristique d'un matériau à structure poreuse [45]. Il possédait une surface élevée Brunauer−Emmett−Teller (BET) de 450 m 2 g −1 . L'analyse de la distribution de la taille des pores basée sur la méthode DFT a montré que le produit consistait en des micropores relativement étroits (1,27 nm) et des mésopores (5,4 nm) avec une large distribution de la taille des pores. La présence de ces pores pourrait faciliter Li + diffusion d'ions.
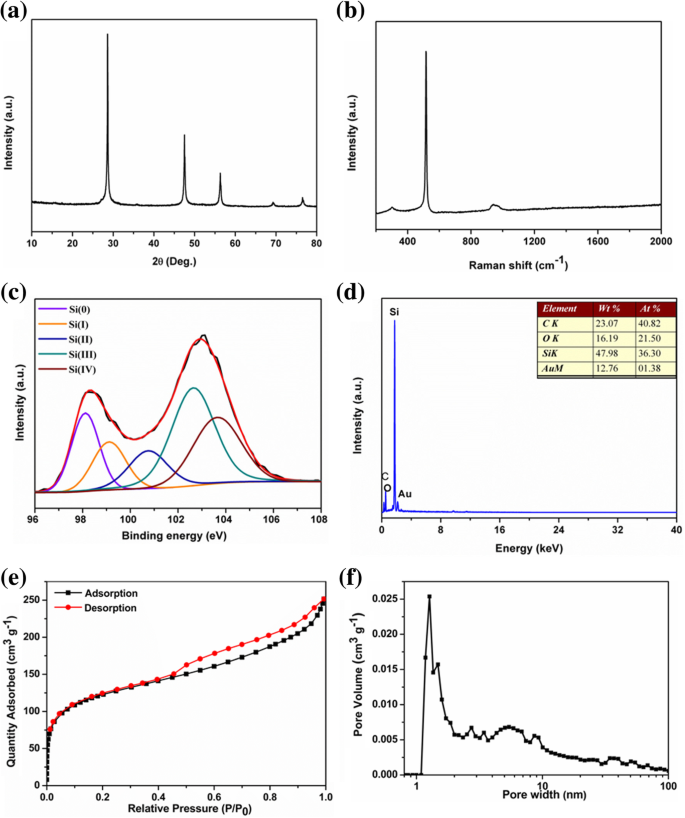
un Modèles PXRD, b Spectres Raman, c Spectre XPS, d Spectre EDS, e courbes d'adsorption-désorption d'azote, et f la courbe de distribution de la taille des pores du pSi
La morphologie des échantillons de silicium obtenus a été étudiée en utilisant la microscopie électronique à balayage (MEB) et la microscopie électronique à transmission (MET). Les images SEM (Fig. 2a, b, Fichier supplémentaire 1 :Figure S2) et MET (Fig. 2c, d) montrent que la taille globale des particules des particules de silicium nanoporeux obtenues varie de plusieurs dizaines à environ 100 nm de diamètre. L'image MET de la figure 2c montre que l'échantillon est composé de particules de silicium interconnectées, ce qui donne une structure poreuse. Nous avons postulé que le Si 4− étroitement arrangé dans le précurseur micrométrique Mg2 Si a réagi avec un liquide ionique acide pour former du Si entouré de MgCl2 nanoparticules. Ces derniers ont été lavés par HCl dilué, laissant du pSi interconnecté avec des lacunes. Le pSi obtenu a montré une grande surface BET de 450 m 2 g −1 avec une distribution uniforme de la taille des pores à 1,27 nm, soutenant la postulation ci-dessus. L'image HRTEM de pSi sur la Fig. 2d révèle que la frange claire du réseau avec un d typique -l'espacement de 0,31 nm, attribué aux plans cristallins (111) du Si cubique, est en bon accord avec les résultats du PXRD. Les nanoparticules de silicium interconnectées sont recouvertes d'une fine couche d'oxyde sur la surface externe, en raison de l'oxydation. La composition de surface et l'état de valence des nanoparticules de Si ont été identifiés par analyse de dispersion d'énergie (EDS) et spectroscopie photoélectronique aux rayons X (XPS). Le spectre Si 2p XPS (Fig. 1c) a montré deux larges pics superposés à 98,2 eV et 103,0 eV. Les deux pics peuvent être divisés en cinq composants à 98,11, 99,11, 100,75, 102,64 et 103,64 eV, qui ont été attribués à Si(0), Si(I), Si(II), Si(III) et Si(IV ), respectivement. La présence d'un fort pic Si(0) implique la formation de silicium poreux. Les pics Si(III) et Si(IV) plus forts suggèrent que la surface du silicium poreux était recouverte d'oxyde de silicium [46]. De manière cohérente, l'analyse par dispersion d'énergie (EDS) du pSi a montré que le rapport atomique Si/O à la surface était d'environ 3:2 (Fig. 1d).

un , b Images SEM et c , d Images TEM de pSi (encart dans d montre les modèles SAED)
Pour être utilisés comme matériaux d'anode LIB, le pSi a été encapsulé avec du polypyrrole conducteur pour former des composites pSi@NC. Le motif PXRD du composite pSi@NC a montré un large pic supplémentaire à environ 23° (Fig. 3a), suggérant que la couche de carbone dopé à l'azote est amorphe [39]. Le spectre Raman du composite pSi@NC (Fig. 3b) a montré deux larges pics à 1335 et 1585 cm −1 attribué aux bandes D et G du carbone graphitique [47], respectivement, ce qui confirme le résultat PXRD. Le rapport d'intensité de la bande D et de la bande G (ID /IG ) du composite pSi@NC est d'environ 1,07, ce qui implique un faible degré de graphitisation de la couche de carbone. Les spectres XPS C 1 s de pSi@NC ont montré l'existence d'une liaison N–C (285,85 eV sur la figure 3c), confirmant que l'azote était dopé dans la charpente carbonée [48]. Le pic N 1 s XPS (Fig. 3d) peut être divisé en trois pics se centralisant respectivement à 397,85, 398,72 et 400,57 eV, qui appartiennent aux types pyridinique, pyrrolique et graphitique d'atomes d'azote dopés dans la charpente carbonée [39 , 49]. La teneur en carbone du composite pSi@NC a été déterminée par TGA à environ 20 % en poids (Fichier supplémentaire 1 :Figure S3).
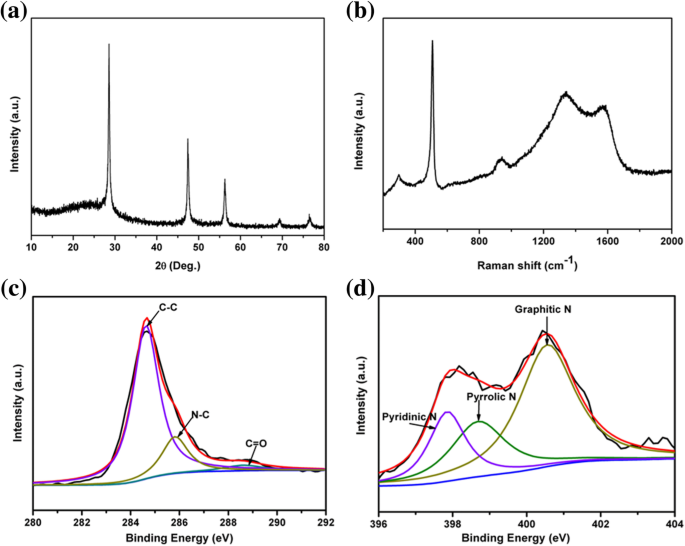
un Modèles PXRD, b Spectres Raman, c spectres XPS C 1 s haute résolution et d spectres XPS haute résolution N 1 s du composite pSi@NC
Pour caractériser les performances électrochimiques du composite pSi@NC en tant qu'anode des LIB, mesures de voltamétrie cyclique (CV) entre et 2,5 V à une vitesse de balayage de 0,2 mV s −1 ont été effectués. Comme le montre la figure 4a, le premier pic de réduction autour de 1,5 V dans les courbes CV a été attribué à la décomposition de l'additif électrolytique (carbonate de fluoroéthylène FEC) [50]. Le pic de réduction irréversible était visible au potentiel autour de 0,6 V lors de la première décharge et a disparu dans les cycles suivants, ce qui était associé à la génération de la membrane d'interface électrolyte solide (SEI) [51]. La formation de SEI était due à la décomposition de solvants organiques de l'électrolyte tels que EC et DEC et a conduit à la perte de capacité initiale irréversible [50, 52]. Le pic près de 0,1 V dans les courbes CV suivantes représentait la transition du silicium cristallin au Lix amorphe Si [53]. Pendant ce temps, pendant le processus de charge, deux pics redox typiques à environ 0,28 et 0,53 V ont été observés, qui étaient liés au processus d'extraction de Li à partir de Lix Si [54, 55]. Notamment, les intensités de courant des pics anodiques et cathodiques ont progressivement augmenté après les premiers cycles. Ce phénomène d'« activation » doit être principalement attribué à la dégradation progressive de la structure cristalline du silicium [54, 56].
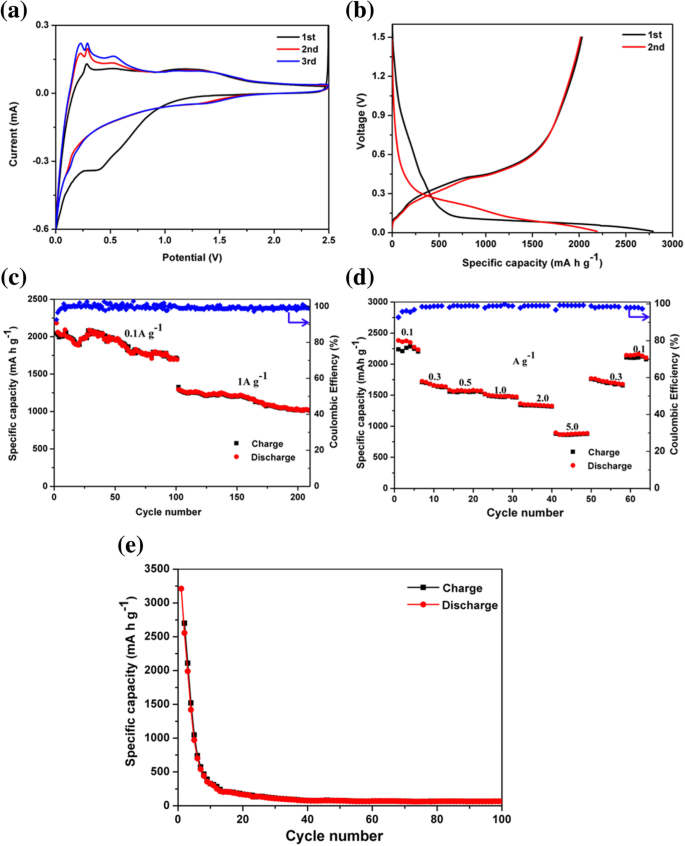
un Courbes CV, b courbes de charge-décharge, c performances cyclistes à long terme à 0,1 A g −1 et 1 A g −1 pour 100 cycles, respectivement (densités de courant) et d performances de débit cyclées à diverses densités de courant de l'électrode composite pSi@NC. e Performances de cyclage du composite Si@NC commercial à 0,1 A g −1 pour 100 cycles
La figure 4b illustre les deux premières courbes de décharge-charge des anodes composites pSi@NC cyclées à une densité de courant de 0,1 A g −1 . Le composite pSi@NC avait une terrasse de décharge longue et plate autour de 0,1 V lors de la première décharge, ce qui est conforme à la terrasse caractéristique des insertions de Li du Si cristallin. Le silicium bien cristallisé est devenu amorphe et a montré les profils de charge/décharge représentatifs du silicium amorphe dans les cycles suivants. Les autres plateaux potentiels apparus vers 0,6 V lors du premier processus de lithiation résultaient de la formation de SEI [57]. Les résultats étaient en bon accord avec les courbes CV. Les capacités initiales de décharge et de charge étaient de 2790 et 2036 mA h g −1 , délivrant une efficacité coulombienne initiale (CE) élevée de 72,9%. La capacité de charge plus faible pourrait être due en partie à l'effet contraignant de la couche d'oxyde SiOx , qui ont servi de tampons pour limiter l'expansion volumique et l'étendue de la lithiation [58, 59]. Il est important de noter qu'aucune diminution de capacité évidente n'a été observée dans les cycles suivants, et l'efficacité coulombienne a été maintenue presque constante à environ 100 %.
La figure 4c montre les performances de cyclage des anodes composites pSi@NC, qui ont été conduites à une densité de courant de 0,1 A g −1 pour 100 cycles et à une densité de courant de 1 A g −1 pour les 100 cycles suivants. Les anodes nanocomposites pSi@NC ont montré une capacité de 1720 mA h g −1 après 110 cycles à une densité de courant de 0,1 A g −1 , correspondant à une rétention de capacité de 79 %. De plus, les électrodes composites pSi@NC délivraient une capacité réversible de 1010 mA h g −1 à 1 A g −1 après les 110 cycles suivants, avec un taux de décroissance de la capacité de 0,2 % par cycle du 101 au 210e cycle. La figure 4d montre les performances de débit de l'électrode pSi@NC. L'électrode pSi@NC a atteint des capacités de décharge de 2360, 1690, 1570, 1470, 1320 et 850 mA h g −1 à la densité de courant de 0,1, 0,3, 0,5, 1,0, 2,0 et 5,0 A g −1 , respectivement. La capacité de décharge pourrait être récupérée à environ 2160 mA h g −1 lorsque la densité de courant est revenue à 0,1 A g −1 , prouvant que l'anode composite pSi@NC avait une réversibilité électrochimique exceptionnelle. En comparaison, la poudre de silicium commerciale (Fig. 4e) recouverte de carbone conducteur dopé à l'azote en tant qu'anode a atteint une capacité de décharge initiale élevée de 3230 mA h g −1 , mais a subi une grave détérioration de la capacité à 110 mA h g − 1 après 100 cycles à 0,1 A g −1 . Ces résultats suggèrent que la couche conductrice de carbone dopé à l'azote et la structure poreuse de pSi@NC pourraient fournir les voies rapides de transport ion/électron et maintenir la stabilité structurelle, conférant ainsi à l'anode composite pSi@NC de bonnes performances de débit et une excellente réversibilité [ 21, 39, 60]. De plus, l'oxydation de surface dans le pSi pourrait également contribuer à améliorer l'efficacité de cyclage des batteries lithium-ion, ce qui a limité l'expansion volumique des particules de silicium et évité certaines réactions secondaires selon les études précédentes [58].
Conclusions
En résumé, nous avons développé une nouvelle méthode pour préparer du silicium nanoporeux avec des rendements élevés basée sur la réaction du siliciure de magnésium (Mg2 Si) dans un liquide ionique acide. Lorsqu'ils sont recouverts de la couche de carbone dopé à l'azote et appliqués comme anode de batterie lithium-ion, les composites silicium-carbone obtenus présentent une capacité réversible élevée, une stabilité de cycle à long terme et une efficacité initiale élevée de Columbic. La couche de revêtement de carbone dopé N a fourni les voies conductrices efficaces pour le transport rapide des ions lithium et le transfert d'électrons, ce qui est bénéfique pour améliorer les propriétés électrochimiques des particules de silicium. Étant donné que les conditions de réaction sont relativement douces et que le rendement des produits est supérieur à 82 %, cette méthode de préparation pourrait être étendue à la production en série de matériaux d'anode en silicium.
Abréviations
- [Bmim]Cl :
-
Chlorure de 1-butyl-3-méthylimidazolium
- AlCl3 :
-
Chlorure d'aluminium
- CV :
-
Voltamétrie cyclique
- EDS :
-
Spectroscopie à dispersion d'énergie
- Mg2 Oui :
-
Siliciure de magnésium
- pSi :
-
Nanoparticules de silicium poreux
- pSi@NC :
-
Carbone dopé à l'azote enrobé de nanoparticules de silicium poreux
- PXRD :
-
Diffraction des rayons X sur poudre
- SEM :
-
Microscopie électronique à balayage
- TEM :
-
Microscopie électronique à transmission
- TGA :
-
Analyse thermogravimétrique
- XPS :
-
Spectroscopie photoélectronique aux rayons X
Nanomatériaux
- Composite hybride nanostructuré silice/or-cellulose Amino-POSS par procédé Sol-Gel et ses propriétés
- Synthèse facile de nanoparticules SiO2@C ancrées sur MWNT en tant que matériaux anodiques hautes performances pour batteries Li-ion
- Synthèse et propriétés électrochimiques des matériaux cathodiques LiNi0.5Mn1.5O4 avec dopage composite Cr3+ et F− pour batteries lithium-ion
- Composite MoS2/noir d'acétylène à quelques couches comme matériau d'anode efficace pour les batteries lithium-ion
- Préparation de micromatériaux hybrides MnO2 revêtus de PPy et de leurs performances cycliques améliorées en tant qu'anode pour batteries lithium-ion
- Composite Si/Graphène intégré fabriqué par réduction thermique au magnésium comme matériau d'anode pour les batteries lithium-ion
- Synthèse écologique et facile de nanofils de Co3O4 et leur application prometteuse avec du graphène dans les batteries lithium-ion
- Synthèse sonochimique en une étape facile et propriétés photocatalytiques des composites graphène/Ag3PO4 Quantum Dots
- Anode à film nanocristallin Fe2O3 préparée par dépôt laser pulsé pour batteries lithium-ion



