Cathodes à feuilles carbonisées imprégnées de sélénium autonomes pour batteries sodium-sélénium hautes performances
Résumé
Une nouvelle approche de carbonisation des feuilles par pyrolyse thermique avec diffusion à l'état fondu suivie d'un dépôt en phase vapeur de sélénium est développée pour préparer les cathodes composites carbone-sélénium pour batteries sodium-sélénium. La feuille carbonisée possède une porosité hiérarchique interne et une charge massique élevée; par conséquent, le composite est appliqué comme cathode sans liant ni collecteur de courant, présentant une excellente capacité de débit et une capacité spécifique réversible élevée de 520 mA h g −1 à 100 mA g −1 après 120 cycles et 300 mA h g −1 même à 2 A g −1 après 500 cycles sans aucune perte de capacité. De plus, la structure tridimensionnelle naturelle unique et le degré de graphitisation modéré du carbone à base de feuilles facilitent le Na + /e − transport pour activer le sélénium qui peut garantir une utilisation élevée du sélénium pendant le processus de décharge/charge, démontrant une stratégie prometteuse pour fabriquer des électrodes avancées vers les batteries sodium-sélénium.
Introduction
Avec la croissance rapide des appareils électroniques, des batteries rechargeables de manière durable sont nécessaires de toute urgence, d'où l'urgence d'exploiter des dispositifs de stockage d'énergie à haute capacité et à des performances de débit satisfaisantes [1,2,3,4,5]. Les batteries lithium-ion (LIB) sont la puissance dominante pour les appareils électroniques en raison des avantages d'une densité d'énergie/puissance élevée et d'une stabilité à long terme [4, 6]. Alors que les LIB commerciaux ne peuvent pas répondre aux futurs besoins énergétiques des véhicules électriques, les batteries lithium-soufre (Li-S) ont été considérablement développées en raison du faible coût et de la densité énergétique théorique élevée du S [7,8,9,10]. Cependant, la nature isolée du S et la dissolution des polysulfures sont des défis majeurs, entraînant une réaction électrochimique lente et une faible utilisation du S, ce qui entrave leurs applications pratiques [11,12,13,14,15].
Les batteries sodium-ion (SIB) sont considérées comme une alternative prometteuse pour les LIB en raison des applications de stockage d'énergie électrique à faible coût et à grande échelle [2, 16, 17, 18, 19]. En particulier, les batteries sodium-sélénium (Na-Se) ont suscité un intérêt croissant ces dernières années [20,21,22]. L'élément Se est dans le même groupe que S et a une électrochimie similaire à celle de Na tandis que la densité d'énergie de Na2 Se (3254 mAh cm −3 ) est comparable à Li2 Se (3467 mAh cm −3 ) [23,24,25,26]. De plus, la conductivité électrique du Se (10 −3 S cm −1 ) est bien supérieur à celui de S (10 −30 S cm −1 à 25°C) [27]. L'effet navette des polyséléniures (qui est similaire aux polysulfures, Na2 Sen , 3 < n < 8) peut également détériorer la durée de vie des batteries Na-Se ; par conséquent, c'est un défi clé de surmonter l'obstacle de la navette des polyséléniures [28,29,30]. Les matrices de carbone avec une porosité appropriée et une conductivité électrique élevée, qui sont toujours utilisées pour charger le Se, ont été considérées comme un moyen efficace de résoudre les problèmes ci-dessus ces dernières années [20, 21, 31, 32]. De nombreux efforts ont été déployés pour piéger les polyséléniures solubles dans divers carbones, notamment les nanofibres de carbone [33, 34], les sphères de carbone [35, 36] et les nanofeuilles de carbone [22], qui se sont avérées efficaces pour améliorer les performances électrochimiques de Na- Se piles. Néanmoins, les matériaux rapportés impliquent des processus complexes à plusieurs étapes et des composants supplémentaires (noir de carbone et liants) ; de plus, ils sont généralement nocifs pour l'environnement et coûteux sur le plan économique.
Heureusement, des matériaux renouvelables aux propriétés remarquables fournies par la nature peuvent répondre à nos besoins [5, 37]. Par exemple, les feuilles naturelles sont diversifiées avec un dopage hétéroatome et une structure poreuse exceptionnelle et ces carbones durs naturels, qui possèdent la capacité impressionnante de stocker des ions sodium, peuvent agir comme substituts alternatifs des matériaux traditionnels en tant que matériaux d'électrode pour les dispositifs SIB [32, 37] . Les feuilles de Ficus peuvent être carbonisées par pyrolyse thermique, et il est extrêmement satisfaisant que les feuilles obtenues possèdent une structure poreuse hiérarchique et une surface moyenne. En bref, les vides poreux peuvent doter les produits de pyrolyse d'une capacité de charge élevée et servir de réservoirs tampons ioniques pendant le processus électrochimique, améliorant la capacité de débit et la densité de puissance [5, 38].
Ici, nous avons préparé un nouveau type d'électrode autoportante imprégnée de Se par diffusion de fusion suivie d'un dépôt de vapeur de Se dans une feuille carbonisée qui est obtenue par pyrolyse thermique de feuilles naturelles d'une manière facile. La capacité spécifique hautement réversible (84 % de la capacité théorique du Se) est atteinte pour la première fois lorsque le composite biochar-sélénium est appliqué comme cathodes sans liant ni collecteur de courant pour les batteries Na-Se. De plus, l'électrode composite telle que préparée présente une capacité de vitesse et une stabilité de cyclage satisfaisantes. Avec les propriétés de supériorité, l'électrode à feuille carbonisée a démontré des performances électrochimiques souhaitables, qui sont un matériau d'anode potentiel pour les batteries Na-Se.
Méthodes
Préparation de la feuille carbonisée
Les feuilles sèches ont été découpées en plaques circulaires (17 mm de diamètre). Les plaquettes de feuilles ont été fixées entre des lames de céramique pour éviter le gondolage ou la pulvérisation pendant le processus de carbonisation, comme le montre la figure 1a. Les plaquettes de feuilles ont été placées dans le four tubulaire pour carboniser à 800 °C pendant 2 h avec une vitesse de montée de 5 °C min −1 sous N2 couler. La feuille carbonisée (notée R800) a été immergée dans 3,0 M de HCl pendant 12 h pour éliminer les sels inorganiques. Les échantillons R800 ont été immergés dans du KOH 1,0 M pendant 12 h, puis placés dans le four tubulaire et activés à 600 °C pendant 2 h avec une vitesse de montée en puissance de 5 °C min −1 sous N2 flux pour obtenir des matériaux poreux (notés R800A). Les échantillons ont été lavés plusieurs fois avec de l'eau déminéralisée et séchés à 70°C pendant une nuit dans une étuve à vide.

un Illustration schématique montrant les processus de préparation de l'électrode autonome Se-R800A. Photographies numériques de b le R séché, c le R800, d le R800A, et e le Se-R800A
Préparation du Se-R800A
La poudre de Se a été placée au fond du bateau en porcelaine, et les films R800A autonomes ont été suspendus par un support ironique dans les airs juste au-dessus de la poudre de Se, et le rapport pondéral de Se:C n'est pas inférieur à 2:1 afin de assurer un excès de poudre de Se comme indiqué sur la Fig. 1a. Ensuite, le Se a été fondu à 260°C sous N2 atmosphère et maintenue pendant 10 h pour assurer une bonne pénétration du Se. Le poids de Se dans l'électrode Se-R800A finale a été mesuré par analyse thermogravimétrique.
Caractérisation des matériaux
La morphologie et la microstructure ont été observées par microscopie électronique à balayage (SEM, Hitachi SU-70), microscopie électronique à balayage à émission de champ (FESEM, JSM-7800F et TEAM Octane Plus) et microscopie électronique à transmission (TEM, JEM-2100, et X-Max80). La structure et les spectres Raman ont été collectés sur la diffraction des rayons X (XRD, PANalytical Empyrean avec rayonnement Cu-Kα) et le microscope Raman (Renishaw, inVia), respectivement. L'analyse thermogravimétrique (TGA, STA409PC) a été testée de la température ambiante à 700 °C avec une vitesse de chauffe de 10 °C min −1 sous N2 atmosphère. L'instrument de surface et de porosimétrie BELSORP-max a été utilisé pour mesurer le N2 isothermes d'adsorption/désorption des électrodes. Des tests de spectroscopie photoélectronique à rayons X (XPS) ont été réalisés à l'aide d'un Thermo K-Alpha + système.
Mesures électrochimiques
Les tests électrochimiques ont été effectués à l'aide de piles bouton CR2032, qui ont été assemblées avec une feuille de Na manuelle préparée par presse à comprimés comme contre-électrode à l'intérieur d'une boîte à gants remplie d'argon (MBRAUN, UNILab2000) avec des niveaux d'humidité et d'oxygène inférieurs à 1 ppm. La fibre de verre (Whatman) a été utilisée comme séparateur. L'électrolyte était 1 M de NaClO4 dans un mélange carbonate d'éthylène/carbonate de diéthyle (EC/DEC, 1:1 en volume). Le Se-R800A autonome a été directement utilisé comme électrode de travail sans aucun liant ni conducteur en carbone. Les mesures du voltamogramme cyclique (CV) ont été effectuées sur une station de travail électrochimique (CHI660D). Les tests de charge-décharge galvanostatique ont été effectués sur une plage de tension de 0,005 à 3,0 V (vs Na + /Na) sur un système de test de batterie (Land, CT-2001A). Les mesures de spectroscopie d'impédance électrochimique (EIS) ont été testées à l'aide de la station de travail électrochimique (CHI 760D) en appliquant une tension de 5 mV sur une fréquence de 10 −2 –10 5 Hz. Le test de la technique de titrage intermittent galvanostatique (GITT) a été réalisé par le processus de décharge/charge des cellules pendant 10 min à 10 mA g −1 et suivi d'une relaxation de 40 minutes au maximum 50 cycles. Toutes les cellules ont été maintenues à température ambiante pendant au moins 12 h avant les tests. Toute la capacité spécifique dans ce travail a été calculée sur la base du poids Se de chargement. Pour les tests SEM ex situ, les électrodes testées ont été soigneusement lavées avec du solvant DEC trois fois et séchées pendant la nuit dans une étuve à vide.
Résultats et discussion
L'électrode autonome Se-R800A a été fabriquée par des procédés de carbonisation, d'activation de KOH et d'imprégnation de Se, qui sont présentés sur la figure 1.
Après le processus de carbonisation à 800 °C, la taille du R800 (Fig. 1b) a à peine diminué (17 mm à 12 mm de diamètre) et l'épaisseur a énormément changé (800 μm à 240 μm) avec une perte de poids de 74%. La figure 1c montre que le R800 est devenu noir, indiquant que R a été transformé avec succès en carbone. Après le processus d'activation, le poids de R800 a continué à diminuer d'environ 9 %. Cependant, après le processus d'imprégnation au Se, le poids du R800A (Fig. 1d) a augmenté de 90 % pour se transformer en Se-R800A, comme le montre la Fig. 1e. Il est à noter que les films R800A suspendus dans les airs juste au-dessus de la poudre de Se étaient entourés de vapeur de Se. Il s'agit d'une idée originale de diffusion à l'état fondu et de dépôt en phase vapeur en évitant les dispersions isolées de Se dans les matrices de carbone [20]. Enfin, le Se-R800A conserve une bonne résistance mécanique en tant qu'électrode autonome pour les batteries Na-Se.
La figure 2a montre la structure typique d'une feuille naturelle avec deux surfaces différentes, où la surface supérieure est plate tandis que la surface arrière contient des stomates uniformes. La figure 2b montre que la section transversale de la feuille est très poreuse avec une palissade et des cellules d'éponge à l'intérieur pour créer suffisamment d'espace pour l'échange de O2 et CO2 [37]. La feuille carbonisée montre une structure similaire à la structure poreuse d'origine de la feuille ; par conséquent, toute la structure à porosité hiérarchique est adaptée au stockage des ions sodium. La figure 2c montre l'intérieur de la feuille carbonisée où est rempli de feuilles réticulées superposées. L'épaisseur de la feuille interconnectée est inférieure à 100 nm, ce qui peut faciliter l'infiltration de l'électrolyte et raccourcir la longueur de diffusion des ions. L'épaisseur totale du Se-R800A est d'environ 240 μm, comme le montre la figure 2d, et les stomates de la surface arrière fournissent suffisamment de canaux pour l'électrolyte et le Na + ions pour passer la couche d'éponge disposée de la feuille carbonisée, puis entrer à travers les feuilles de carbone superposées remplies de Se (Fig. 2e) pour accomplir la réaction électrochimique principale et cette couche se concatène avec une couche de palissade bien alignée. La surface supérieure est considérée comme le collecteur de courant et les électrons se déplacent le long de la feuille de carbone conductrice, puis sont collectés par la couche de surface supérieure [37]. La figure 2f montre un aperçu de la microstructure du Se-R800A, où des particules de Se et du carbone amorphe ont été trouvés. L'image en médaillon montre les franges du réseau pour la région ordonnée mesurées à 0,2 nm, qui pourraient être attribuées au plan cristallin (111) de Se. Le Se-R800A à structure de feuille multicouche vise à atténuer considérablement l'effet navette pour améliorer le cycle à long terme et à activer le Se pour assurer une utilisation élevée du Se, ce qui améliorera les performances électrochimiques des batteries Na-Se.

Images SEM du R800 a surface supérieure et surface arrière et b vue en coupe. c Image SEM agrandie de la feuille de carbone dans la couche d'éponge du R800A. d Image FESEM de la coupe transversale. e Image agrandie de la FESEM. f Image HRTEM du Se-R800A
Comme le montre la figure 3a, le Se-R800A conserve la morphologie du R800 et aucun Se isolé n'a pu être observé, tandis que la cartographie élémentaire EDX du Se-R800A vérifie la distribution homogène du Se comme le montre la figure 3, qui s'avère complète pénétration du Se dans le R800A. Cela confirme que les composites C-Se ont été fabriqués avec succès. Le signal Se est uniforme à travers la section efficace, le Se-R800A avec des mappages d'éléments C, N et O correspondants dans la même région (Fig. 3b). Comme mentionné ci-dessus, le dopage par hétéroatome de N et O provenant du biochar facilite le processus électrochimique et la sédimentation des polyséléniures [6, 39, 40, 41].

un Images FESEM du Se-R800A. b Images de cartographie élémentaire de C, N, O et Se du Se-R800A et les résultats EDX correspondants
Pour approfondir l'étude de la structure des poudres Se-R800A, R800 et Se, les modèles XRD sont illustrés à la figure 4a. Après l'infiltration du Se dans le R800A, les pics de diffraction du Se cristallin dans le Se-R800A disparaissent pour la plupart et seules des bosses amorphes (ressemblant au R800) peuvent être observées, ce qui implique une dispersion complète du Se amorphe dans le R800A. Il est prouvé que le Se amorphe facilite la stabilité du cycle et retarde la formation de polyséléniures solubles dans l'électrolyte à base de carbonate [21, 22, 31]. Cependant, le pic agrandi à 29,7° (l'encart sur la Fig. 4a) dans le Se-R800A est clairement observé, démontrant qu'une petite quantité de Se cristallin existe toujours. La spectroscopie Raman a été appliquée pour étudier les trois échantillons. Comme indiqué sur la Fig. 4b, le Se brut affiche un pic pointu situé à 234 cm −1 , qui correspond à l'équilibre trigonal Se [27]. Cependant, pour le Se-R800A, ces pics caractéristiques disparaissent et laisse un large pic à 250–300 cm −1 en raison de la vibration d'étirement C-Se et de la vibration du groupe C-Se-Se [21]. La faible intensité du pic de Se est décalée vers le bleu jusqu'à 260 cm −1 (l'encart sur la Fig. 4b), qui est associée à la transformation de cristallin en moléculaire de Se [22, 24, 28, 39]. De plus, le R800 et le Se-R800A disposent tous deux de la bande D à 1346 cm −1 et la bande G à 1598 cm −1 , relatifs respectivement au carbone désordonné et graphitique. Le rapport d'intensité de I D /Je G dans Se-R800A est d'environ 0,92 et supérieur à 0,88 de R800, révélant que Se insère et impacte la graphitisation du R800A tout en maintenant une excellente conductivité électrique [32]. Cela confirme en outre que le Se-R800A peut être utilisé comme cathode satisfaisante pour les batteries Na-Se. Pour examiner les effets de l'activation de KOH et de l'imprégnation de Se, la figure 4d montre la structure de surface du R800, R800A et Se-R800A, qui sont tous l'isotherme de type IV similaire à l'adsorption des matériaux microporeux [31]. La surface calculée de Brunauer-Emmett-Teller (BET) est de 270, 934 et 434 m 2 g − 1 respectivement, révélant que KOH est capable d'agrandir la surface spécifique en créant des pores pour piéger efficacement Se [5]. Remarquablement, après l'imprégnation de Se, la surface spécifique du Se-R800A diminue de 54 % sur la figure 4c, accompagnée d'une diminution remarquable de la distribution de la taille des pores dans la plage de 0,5 à 2 nm, comme le montre la figure 4d, impliquant la diffusion de Se dans les micropores du R800A. Ces micropores abondants ont été confirmés pour confiner efficacement le Se amorphe dans le rapport précédent [22, 27, 42]. Le TGA est appliqué dans le but d'affirmer le poids de charge de Se dans le matériau composite final. Le Se dans le Se-R800A a commencé à s'évaporer de manière significative à 300 °C, entraînant une perte de poids de 47 % de Se à 550 °C. Comme illustré sur la Fig. 4e, le Se-R800 présente la courbe similaire du Se-R800A mais seulement 11% de chargement de Se est obtenu, suggérant qu'il est nécessaire d'activer le biochar et de former des micropores par KOH pour charger le Se. Jusqu'à 700°C, le R800 a présenté une légère perte de poids (< 2%) causée par la pyrolyse thermique profonde et une graphitisation supplémentaire. L'état chimique du Se a été étudié plus en détail par XPS, comme indiqué sur la figure 4f. Le pic 3d de Se est divisé en 3d3/2 et 3d5/2 avec des énergies de liaison de 56,23 et 55,38 eV, respectivement. Celles-ci sont légèrement supérieures à celles du Se 3d brut (55,95 et 55,15 eV), indiquant l'intense interaction chimique entre le Se et la matrice R800 [34]. En règle générale, le R800 en tant que biomasse possède des hétéroatomes (par exemple, N et O comme le montre la figure 3 pour N, O), en particulier O, offre une forte liaison entre Se et R800. Ceci est prouvé par l'apparition du pic Se-O (58,33 eV) dans le spectre. De toute évidence, deux nouveaux pics centrés à 57,18 et 55,88 eV apparaissent pour le composite Se-R800A, indiquant la génération de liaisons Se-O-C au cours du processus d'imprégnation. Les nouveaux pics pourraient être impliqués dans la formation de liaisons Se-O-C, ce qui conduit à une densité électronique plus faible du site O. Cette liaison chimique de pontage (-O-) permet à C de se coupler fortement avec Se et supprime l'effet navette des polyséléniures pendant le cyclage [24, 27, 39, 43].
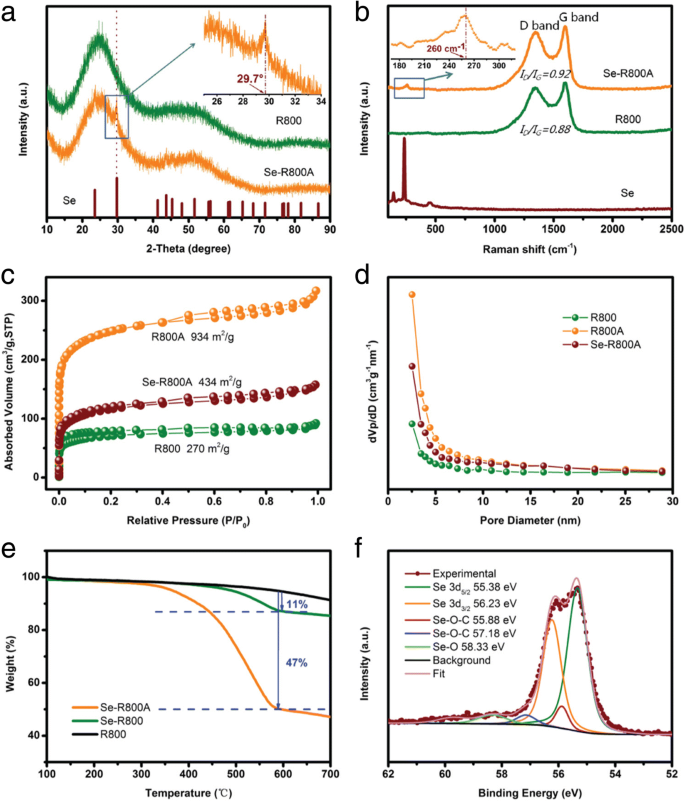
un Modèles XRD et b spectres Raman. c N2 isothermes d'adsorption/désorption et d courbes de distribution de la taille des pores obtenues par la méthode DFT. e Analyse thermogravimétrique. f Spectres XPS de Se dans le Se-R800A
Afin d'évaluer les performances électrochimiques des batteries Na-Se, le Se-R800A a été directement utilisé comme cathode dans la pile bouton CR2032. Il convient de mentionner que la surface arrière du Se-R800A fait face au métal Na et que la surface supérieure est comme le collecteur de courant.
La figure 5a montre les courbes CV dans la plage de 0,005 à 3,0 V à une vitesse de balayage de 0,2 mV s −1 . Dans le processus de décharge initial, en plus du pic près de 0 V qui est l'adsorption de Na + au niveau des sites défectueux et des micropores de la matrice carbonée [44] comme les échantillons R800A et R800, seul un pic cathodique apparaît à environ 1,2 V, indiquant que la conversion de Se en Na2 Se (Se ↔ Na2 Se) n'est qu'une réaction à une étape, ce qui est très différent du mécanisme des réactions à plusieurs étapes (Se ↔ Na2 Sen , 3 < n < 8 ↔ Na2 Se) entre Se et Na [21, 24, 39]. Et puis le pic passe à un 1,1 V plus stable résultant du processus d'activation électrochimique [27]. Pour le processus de charge, un seul pic anodique est observé et reste stable à 1,7 V en trois cycles, indiquant qu'il s'agit d'une transformation directe de Na2 Se dans Se (Na2 Se Se) à 1,7 µV; par conséquent, le Se-R800A permet de faciliter efficacement la suppression de l'effet navette et le maintien de la capacité spécifique. Les profils de tension de décharge/charge à 50 mA g −1 montrent les mêmes tendances dans la Fig. 5b, qui coïncide avec l'analyse du CV. Le plateau unique est lié à la conversion de Se en Na2 insoluble Voir [27]. Les courbes de charge se chevauchent presque pendant trois cycles, tandis que les courbes de décharge changent par rapport à l'initiale avec une capacité de 1100 mA h g −1 aux cycles suivants avec une capacité réversible de 700 mA h g −1 . Cela pourrait expliquer la formation du film d'interface d'électrolyte solide (SEI) sur Se-R800A avec piégeage partiellement irréversible de Na + dans les pores [22]. Après les cycles suivants, les courbes de décharge se chevauchent également, démontrant que le Se-R800A atteint une stabilité de cycle supérieure. Les performances de cyclage de l'électrode Se-R800A sont illustrées à la Fig. 5c. La capacité délivrée à la capacité initiale de 620 mA h g −1 et retenu 520 mA h g −1 à 100 mA g −1 après 120 cycles, soit 84% de la capacité théorique de Se, indiquant l'excellente stabilité en cyclage, et l'efficacité coulombienne a été maintenue à 100% sauf que l'efficacité coulombique initiale est inférieure à 80% en raison de Na + piégé dans le biochar poreux. En revanche, la capacité spécifique du R800A n'est que de 18 mA h g −1 , ce qui peut être attribué à une résistance sévère au SEI en raison de l'énorme surface spécifique. Il convient de mentionner que la capacité spécifique du R800 est de 80 mA h g −1 à 100 mA g −1 après 120 cycles mais exceptionnellement stable, il est essentiel de valider la supériorité naturelle unique des matériaux multicouches dérivés de la biomasse pour prolonger la durée de vie des batteries Na-Se. Les performances de débit de l'électrode Se-R800A à différentes densités de courant sont étudiées plus en détail et illustrées à la Fig. 5d. Lorsque la densité de courant est passée de 20, 60, 100, 200, 300 à 600 mA g −1 , l'électrode Se-R800A fourni une capacité spécifique était de 745, 674, 655, 610, 573 à 486 mA h g −1 , respectivement. Lorsque la densité de courant a été réglée sur 20 mA g −1 , la capacité réversible récupérée à 711 mA h g −1 , offrant une capacité de débit remarquable de l'électrode. Surtout, même à une densité de courant élevée de 2 A g −1 , le Se-R800A offrait toujours une excellente capacité réversible élevée de 300 mA h g −1 après 500 cycles longs sans évanouissement de capacité (Fig. 5e). Cette capacité spécifique supérieure et cette performance de débit surpassent la plupart des cathodes C-Se typiques signalées pour les batteries Na-Se (tableau 1).
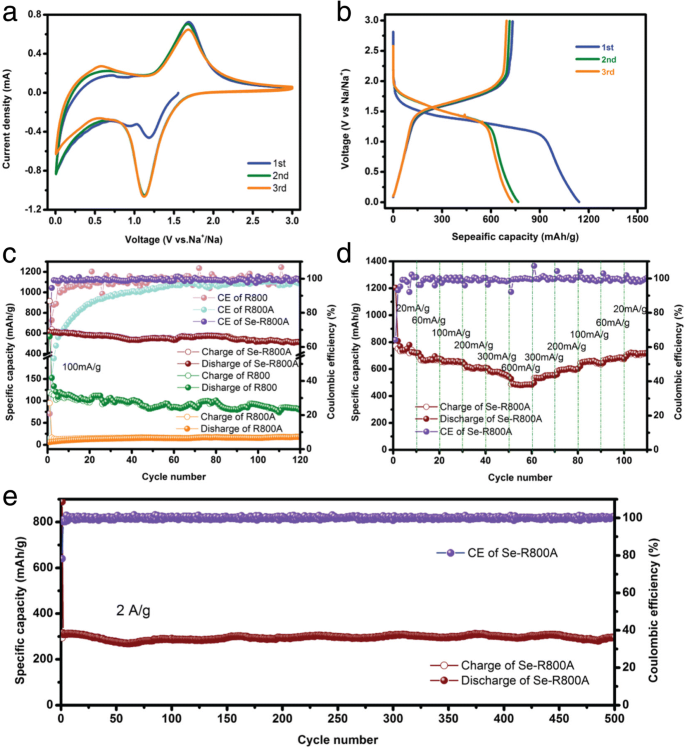
Les performances électrochimiques de la cathode Se-R800A dans les batteries Na-Se, a les courbes CV à une vitesse de balayage de 0,2 mV s −1 , b les profils de tension de décharge/charge galvanostatique testés à 50 mA g −1 , c les performances de cyclisme des Se-R800A, R800A et R800 à 100 mA g −1 , d la capacité de débit à diverses densités de courant, et e les performances cyclistes du Se-R800A à 2 A g −1
Il est à noter que la stabilité du cyclage à haute densité de courant, même à 2 A g −1 , est meilleur que celui à 0,1 A g −1 . Cela peut être dû aux raisons suivantes :(i) le biochar non artificiellement hiérarchisé et le degré de graphitisation modéré du Se-R800A accélèrent considérablement le Na + et e − le transport pour activer le Se amorphe, assurant ainsi une cinétique électrochimique facile même à haute densité de courant ; (ii) les intermédiaires (Na2 Sen , 3 < n < 8) à faible densité de courant ont plus de chances de se dissoudre dans l'électrolyte carbonate, mais les polyséléniures sont fermement confinés dans les micropores et retenus par des feuilles de carbone qui se chevauchent, ce qui est efficace pour atténuer l'effet navette, résultant en une utilisation très efficace de Se pendant le cyclisme à long terme [27].
Afin d'obtenir de plus amples informations sur les performances électrochimiques améliorées du Se-R800A, la résistance de transfert de charge (R ct ) et la résistance à la diffusion ionique (R identifiant ) des R800, R800A et Se-R800A ont été mesurés par EIS. Comme le montre la figure 6, le tracé de Nyquist de la cathode R800 présente le demi-cercle dans les régions haute fréquence attribuées à R ct contenant la couche SEI et l'interface électrode-électrolyte [45, 46] et une ligne inclinée dans la région des basses fréquences correspondant à R identifiant représentant l'impédance de Na + diffusion [47]. L'électrode R800A présente un demi-cercle de rayon plus grand après activation par KOH, indiquant que des micropores abondants contribuent à accélérer le processus cinétique des réactions électrochimiques, mais augmenteront nettement la résistance de la couche SEI en raison de la surface énorme [22, 27, 31, 39, 40 ]. De plus, par rapport à l'électrode R800 du tableau 2, le plus petit R identifiant implique des micropores car les réservoirs tampons ioniques raccourcissent efficacement la distance de diffusion des ions.
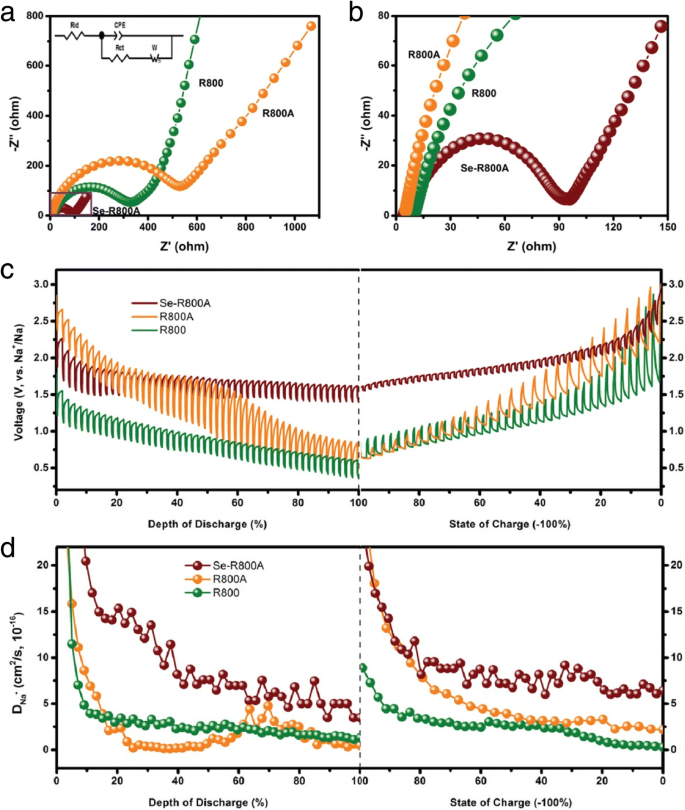
un Tracés de Nyquist de batteries Na-Se assemblées avec les R800, R800A et Se-R800A comme cathodes pour l'analyse d'impédance et l'encart est le circuit équivalent. b Agrandi la section du Se-R800A. c Profils de tension et d le Na + coefficients de diffusion du R800, R800A et Se-R800A obtenus via la technique GITT lors des processus de décharge/charge
Lorsque le Se chargé occupe la plupart des micropores, l'électrode Se-R800A montre évidemment un R plus petit ct et R identifiant confirmé par les excellentes performances électrochimiques. Les pores de la feuille carbonisée sont pour la plupart dans la plage de 0,1 à 2 nm, et ces micropores abondants sont plus adaptés pour charger et confiner Se, apportant enfin une surface modérée pour une efficacité coulombienne plus élevée [31, 37]. Le Na + les coefficients de diffusion des trois échantillons sont calculés par la méthode GITT pendant le processus de décharge/charge sur la Fig. 6c, d [48]. On peut observer que le Na + les coefficients de diffusion de R800, R800A et Se-R800A sont du même ordre de grandeur (10 −16 cm 2 /s) mais le Se-R800A est plus haut que les autres, ce qui révèle que le Na + la diffusion dans les matrices carbonées est notablement améliorée grâce à la présence de Se [49, 50]. Avec ces propriétés, la conductivité électronique et l'efficacité de diffusion ionique dans le composite carbone-sélénium ont été efficacement améliorées, résultant en une excellente performance électrochimique de l'électrode Se-R800A pour les batteries Na-Se.
Après démontage de la cellule de test, la morphologie du Se-R800A (Fig. 7b) reste la même que l'antériorité (Fig. 7a), suggérant que la feuille carbonisée est qualifiée pour servir de cadre favorable aux batteries Na-Se. La figure 7c montre la structure hiérarchique de l'électrode Se-R800A après 500 cycles, et elle a également conservé la morphologie d'origine. Par conséquent, on peut souligner que les excellentes performances de cyclage et de vitesse peuvent être dues aux raisons suivantes :premièrement, le Se-R800A autonome avec des hétéroatomes abondants (tels que N, O) pour accueillir Se peut supprimer l'effet navette de les polyséléniures. Deuxièmement, la structure hiérarchique de la feuille carbonisée à surface anisotrope pourrait répondre au besoin de l'e − et Na + transport pour activer le Se intérieur. Les polyséléniures sont confinés dans les micropores et retenus par des feuilles de carbone superposées pour augmenter la barrière énergétique de la diffusion des polyséléniures [42]. Enfin, en tant que cathodes sans liant ni collecteur de courant, la structure interconnectée en 3D et les feuilles de carbone interconnectées peuvent grandement faciliter l'infiltration de l'électrolyte et raccourcir la distance de diffusion des ions [22]. Ces avantages sont essentiels pour une capacité améliorée et une durée de vie prolongée.
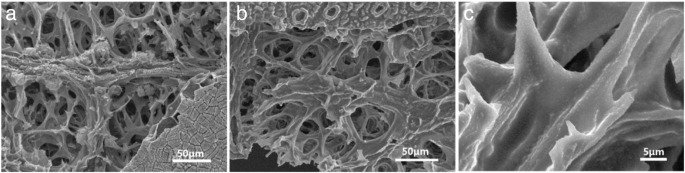
Images SEM du film d'électrode Se-R800A a avant et b après les cycles. c Image SEM agrandie de la feuille de carbone après cycles
Conclusions
En conclusion, il a été démontré qu'une nouvelle fabrication du Se-R8000A peut être terminée par un four tubulaire. Il a été possible de confiner le Se dans la feuille carbonisée microporeuse par des méthodes courantes d'infusion par fusion, ce qui peut réduire efficacement l'effet navette des polyséléniures, ce qui se traduit par d'excellentes performances électrochimiques pour les batteries Na-Se. Le Se-R8000A affiche une capacité réversible aussi élevée que 520 mA h g −1 à 100 mA g −1 après 120 cycles, ce qui prend en charge la stabilité de cyclisme et la capacité de cadence supérieures. Il a été prouvé que la structure des feuilles hiérarchiquement non artificielle et le degré de graphitisation modéré du Se-R800A favorisent considérablement l'utilisation efficace du Se. En général, le Se-R800A, en raison de ses caractéristiques autonomes, performantes et économiques, s'est avéré être une alternative prometteuse aux matériaux d'électrode conventionnels et substantiels dans les batteries Na-Se.
Abréviations
- BET :
-
Brunauer-Emmett-Teller
- CV :
-
Voltammogramme cyclique
- DEC :
-
Carbonate de diéthyle
- CE :
-
Carbonate d'éthylène
- EIS :
-
Spectroscopie d'impédance électrochimique
- FESEM :
-
Microscopie électronique à balayage à émission de champ
- GITT :
-
Technique de titrage galvanostatique intermittent
- LIB :
-
Batteries lithium-ion
- Li-S :
-
Lithium-soufre
- Na-Se :
-
Sodium-sélénium
- SEI :
-
Interface à électrolyte solide
- SEM :
-
Microscopie électronique à balayage
- SIB :
-
Batteries sodium-ion
- TEM :
-
Microscopie électronique à transmission
- TGA :
-
Analyse thermogravimétrique
- XPS :
-
Spectroscopie photoélectronique aux rayons X
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- Nanocristaux d'étain pour la future batterie
- Qualités PVDF renouvelables pour batteries lithium-ion
- Synthèse facile de nanoparticules SiO2@C ancrées sur MWNT en tant que matériaux anodiques hautes performances pour batteries Li-ion
- Composite aérogel/soufre de charbon actif revêtu de polyaniline pour batterie lithium-soufre hautes performances
- Nanofeuilles V6O13 interconnectées 3D cultivées sur du textile carbonisé via un processus hydrothermique assisté par des semences en tant que cathodes flexibles hautes performances pour les batter…
- Anode à film nanocristallin Fe2O3 préparée par dépôt laser pulsé pour batteries lithium-ion
- Microarrays mésoporeux VO2 bidimensionnel pour supercondensateur hautes performances
- Microsphères de silicium mésoporeux produites à partir de la réduction magnésiothermique in situ d'oxyde de silicium pour un matériau d'anode à hautes performances dans les batteries sodium-ion…
- Préparation et propriétés électrochimiques des anodes Fe2O3/C en forme de grenade pour batteries Li-ion



