Nanoscopie basée sur la microscopie à force atomique de cellules souches dérivées de tissus adipeux humains à différenciation chondrogène :expression de la nanostructure et de l'intégrine β1
Résumé
L'intégrine β1 est connue pour être impliquée dans la différenciation, la migration, la prolifération, la réparation des plaies, le développement des tissus et l'organogenèse. Afin d'analyser la probabilité de liaison entre le ligand de l'intégrine 1 et les récepteurs du cluster de différenciation 29 (CD29), la microscopie à force atomique (AFM) a été utilisée pour détecter les récepteurs natifs couplés à l'intégrine 1 à la surface des cellules souches humaines dérivées du tissu adipeux (hADSc) . La probabilité de liaison de l'interaction ligand-récepteur de l'intégrine 1 a été sondée par des pointes fonctionnalisées par l'intégrine 1 sur hADSc au cours de la différenciation chondrogénique précoce au niveau de la culture cellulaire bidimensionnelle. La morphologie cellulaire et l'ultrastructure de l'hADSc ont été mesurées par AFM, qui a démontré que les cellules à long fuseau devenaient des cellules polygonales avec des rapports longueur/largeur diminués et une rugosité accrue pendant l'induction chondrogénique. La liaison du ligand integr1 de l'intégrine et des récepteurs CD29 a été détectée par des pointes fonctionnalisées 1 pour hADSc vivant. Un total de 1200 courbes ont été enregistrées à 0, 6 et 12 jours d'induction chondrogénique. Les forces de rupture moyennes étaient respectivement de 61,8 ± 22,2 pN, 60 ± 20,2 pN et 67,2 ± 22,0 pN. Les événements de rupture étaient de 19,58 ± 1,74%, 28,03 ± 2,05 % et 33,4 ± 1,89 %, respectivement, ce qui a démontré que la probabilité de liaison était augmentée entre le ligand de l'intégrine 1 et les récepteurs à la surface de l'hADSc pendant l'induction chondrogénique. L'intégrine β1 et la voie de signalisation β-caténine/SOX étaient corrélées au cours de la différenciation chondrogénique. Les résultats de cette enquête impliquent que l'AFM offre un aperçu cinétique et visuel des changements dans la liaison du ligand de l'intégrine 1 au récepteur CD29 sur hADSc au cours de la chondrogenèse. Il a été démontré que les changements dans la morphologie cellulaire, l'ultrastructure membranaire et la probabilité de liaison ligand-récepteur transmembranaire sont des marqueurs utiles pour l'évaluation du processus de différenciation chondrogénique.
Contexte
L'arthrose (OA) est une maladie articulaire dégénérative fréquente chez les personnes âgées [1], avec une arthrose dégénérative caractérisée par une destruction progressive du cartilage articulaire. Le cartilage est hautement organisé sans vaisseaux sanguins, nerfs ou tissu lymphatique [2]. La matrice extracellulaire (MEC) est principalement composée de collagène II et de glycoprotéine, et elle est très importante pour l'homéostasie du cartilage. Le cartilage étant avasculaire, sa capacité d'auto-renouvellement est limitée. Bien que les traitements de l'arthrose (chirurgicaux et non chirurgicaux) puissent rapidement soulager les symptômes des patients arthrosiques, en particulier la douleur, ils ne peuvent pas restaurer la structure et la fonction normales du cartilage articulaire [3]. À l'avenir, le traitement inclura probablement l'ingénierie tissulaire avec des cellules souches et des échafaudages pour réparer les défauts et le cartilage articulaire dégénératif [4]. Les cellules souches mésenchymateuses sont des cellules stromales multipotentes qui ont un potentiel ostéogénique, adipogène, chondrogénique et myogénique, en fonction des combinaisons de facteurs de croissance [5]. L'analyse de la différenciation des cellules souches mésenchymateuses a montré que la Wnt/β-caténine, la cible mammifère de la rapamycine (mTOR), la phosphoinositide 3-kinase (PI3K) et d'autres voies jouent un rôle important dans la différenciation [6,7,8]. Cependant, le mécanisme sous-jacent par lequel la différenciation chondrogénique est induite reste insaisissable. Ceci est particulièrement vrai pour le mécanisme par lequel les signaux extracellulaires activent les voies de signalisation intracellulaires. Nous avons trouvé que l'intégrine β1 subit des changements au cours de la différenciation chondrogénique. Par conséquent, nous avons émis l'hypothèse que l'intégrine β1 pourrait jouer un rôle important dans la différenciation chondrogénique des cellules souches dérivées de tissus adipeux (hADSc) en raison de son implication dans diverses voies de signalisation de différenciation tissulaire. Dans cette enquête, l'accent a été mis sur la voie de signalisation Wnt/β-caténine.
De nombreuses études ont montré que les interactions entre les cellules et l'environnement extracellulaire sont régulées par les protéines transmembranaires, en particulier les membres de la famille des intégrines [9]. Les intégrines sont composées de glycoprotéines hétérodimères transmembranaires de chaînes α et liées de manière non covalente [10]. Théoriquement, il existe 64 intégrines connues dont seulement 24 ont été trouvées. Les intégrines jouent un rôle vital dans l'adhésion cellule-cellule, l'adhésion cellule-ECM, la signalisation cellulaire et l'organisation du cytosquelette d'actine [11]. L'ECM joue un rôle important dans l'homéostasie tissulaire, et que l'ECM régule les intégrines. Les intégrines interviennent dans de nombreux processus fondamentaux, notamment l'adhésion cellulaire, la migration, la prolifération, la différenciation, la mort cellulaire, la réparation des plaies, le développement des tissus et l'organogenèse. Au cours de la différenciation chondrogénique des cellules souches mésenchymateuses, l'expression de l'intégrine β1 est connectée à la voie de signalisation SOX et au collagène II. Cette étude s'est concentrée sur le dimère 1 de l'intégrine, car il s'agit du dimère le plus important parmi les hétérodimères du cartilage et est connu pour interagir avec de nombreux dimères α différents [12]. Le cluster de différenciation 29 (CD29) est une sous-unité d'intégrine β1 associée à des récepteurs antigéniques très tardifs, exprimés sur presque tous les types de cellules et de tissus.
Ici, la microscopie à force atomique (AFM) a été utilisée pour nous aider à mesurer les changements au cours de la différenciation chondrogénique hADSc. En tant que type de microscopie à sonde à balayage à très haute résolution, l'AFM a fourni une nouvelle opportunité de détecter la morphologie et la membrane cellulaire de cellules individuelles dans un fluide à l'échelle nanométrique. Pendant ce temps, le système de spectroscopie de force à molécule unique (SMFS) combiné à la microscopie à force atomique (AFM) a été utilisé pour mesurer la liaison ligand-récepteur sur les cellules vivantes. Le système de SMFS était plus sensible aux changements de récepteurs dans la membrane cellulaire, et les images de la force de liaison ont été visualisées. Dans ce travail, la liaison ligand-récepteur de l'intégrine 1 a été sondée par des pointes AFM fonctionnalisées par l'intégrine 1. En appliquant l'AFM, la différenciation chondrogénique s'est avérée modifier la forme des cellules hADSc et augmenter la rugosité cellulaire. Cette application a fourni une méthode permettant d'évaluer la différenciation chondrogénique par mesure directe des interactions ligand-récepteur de l'intégrine 1 et de l'altération de l'ultrastructure de la surface cellulaire, améliorant ainsi l'investigation de la surface cellulaire et le dépistage de manière visualisée. La différenciation chondrogénique modifie la composition et la structure de la membrane, ainsi que les interactions cytosquelettiques intracellulaires. Ces changements dans la morphologie cellulaire, l'ultrastructure et la liaison ligand-récepteur transmembranaire servent de marqueurs utiles pour l'évaluation des mécanismes de différenciation chondrogénique.
Méthodes
Culture cellulaire et réactifs
Pour cette enquête, des cellules ont été isolées de trois patients chirurgicaux (âge moyen 20 ans) comme décrit précédemment [13]. Des consentements éclairés ont été obtenus de tous les patients. L'approbation éthique de cette étude a été obtenue auprès du premier hôpital affilié de l'Université de Jinan (formulaire de supplément). Les cellules ont été maintenues dans un milieu basal, qui comprenait du milieu d'Eagle modifié de Dulbecco à faible teneur en glucose (DMEM, Life Technologies, CA, USA) complété avec 10 % de sérum bovin fœtal inactivé par la chaleur (FBS, Life Technologies, CA, USA), 100 unités/ ml de pénicilline (Life Technologies, CA, USA), 100 μg/ml de streptomycine (Life Technologies, CA, USA), 0,11 mg/ml de pyruvate de sodium (Life Technologies, CA, USA) et de la L-glutamine (Life Technologies, CA, ETATS-UNIS). Les cellules ont été maintenues à 37 °C dans un incubateur humidifié contenant 5 % de CO2 avec un support changé tous les 3 jours.
Différence in vitro
Pour l'induction chondrogénique, des hADSc de quatrième à huitième passage ont été ensemencées à une densité cellulaire élevée (2 × 105/10 ml) et cultivées dans un milieu chondrogénique contenant du DMEM/F12 supplémenté avec 1% de FBS, 1% d'insuline-transferrine-sélénium ( ITS) + supplément (Cyagen, Guangzhou, Chine), 10 ng/ml transforming growth factor-beta1 (TGF-β1) (Peprotech, Rocky Hill, New Jersey, USA), 100 ng/ml insulin-like growth factor-1 ( IGF-1) (Peprotech, Peprotech, Rocky Hill, New Jersey, États-Unis), 10-7 M dexaméthasone (Sigma, St. Louis, MO, États-Unis) et 50 μg/ml d'acide ascorbique (Sigma, St. Louis, MO , ETATS-UNIS). Le milieu a été changé tous les 2 jours avec du TGF-β1 et de l'IGF-1 fraîchement ajoutés. La chondrogenèse a été évaluée par coloration au bleu alcian et au bleu de toluidine.
Pour induire une différenciation ostéogénique et adipogène, les cellules du quatrième au huitième passage ont été traitées avec le milieu ostéogénique et adipogène pendant 2 semaines, respectivement. Milieu ostéogénique composé de DMEM additionné de 10-7 M dexaméthasone (Sigma, St. Louis, MO, USA), 50 μg/ml d'acide ascorbique (Sigma, St. Louis, MO, USA) et 10 mmol/l de β-glycérol phosphate (Sigma, St. Louis, MO, USA). L'ostéogenèse a été évaluée par coloration au rouge alizarine.
Milieu adipogène constitué de DMEM additionné de 0,5 mmol/l de 3-isobutyl-1-méthylxanthine (IBMX) (Sigma, St. Louis, MO, USA), 1 μmol/l d'hydrocortisone (Sigma, St. Louis, MO, USA), 0,1 mmol/l d'indométacine (Sigma, St. Louis, MO, USA). La différenciation adipogène a été évaluée par coloration Oil Red O.
Identification des antigènes de surface hADSc par cytométrie en flux
Les hADSC ont été digérés avec de la trypsine puis rincés deux fois avec du DMEM, avant remise en suspension à une densité cellulaire de 2 × 10 7 cellules/ml. La suspension cellulaire (50 μl ; 1 × 10 6 cellules) a été ajouté à des tubes d'époxyde d'époxyde de 1,5 ml puis incubé avec des anticorps anti-CD34, anti-CD44, anti-CD45, anti-CD73, anti-CD90, anti-CD106, anti-HLA-DR et anti-CD105 pour 20 min à 37 °C dans le noir. L'anti-CD34, l'anti-CD44 et l'anti-CD45 ont été obtenus auprès de CST (Beverly, MA, USA); d'autres anticorps ont été obtenus auprès d'Abcam (Cambridge, MA, USA). Ensuite, la suspension cellulaire a été centrifugée à × 500g pendant 5 min, suivi de l'élimination du surnageant et de la remise en suspension des cellules dans 200 μl de Stain Buffer. Toutes les étapes ont été répétées deux fois avant l'analyse par cytométrie en flux.
Analyse d'immunotransfert (IB)
Les cellules ont été collectées pour l'immunotransfert comme décrit précédemment [14]. Les anticorps primaires utilisés étaient l'anti-β-caténine (ab32572), l'anti-intégrine 1 (ab30394) et l'anti-collagène II (ab34712), obtenus auprès d'Abcam (Cambridge, MA, USA). L'anti-β-actine (8H10D10, 1:2000), l'anti-GSK-3β (27C10, 1:1000) et l'anti-SOX (92G2, 1:1000) ont été obtenus auprès de Cell Signaling Technology (CST, Beverly, MA, ETATS-UNIS). Les anticorps secondaires conjugués à la HRP (1 : 1000–1 : 3000) ont été achetés auprès de CST.
Immunofluorescence
Pour la différenciation chondrogénique, les cellules ont été traitées pendant 0, 6 et 12 jours, digérées et cultivées sur le verre dans des plaques à 24 puits (Costar353047, Corning, New York, États-Unis) pendant 24 h. Les cellules ont été lavées deux fois avec une solution tampon phosphate glacée (PBS), fixées avec du paraformaldéhyde à 4 % pendant 15 minutes à température ambiante. Après blocage, les cellules ont été incubées avec l'anticorps primaire réactif avec l'intégrine 1 pendant 1 h, suivie d'une incubation pendant 1 h dans l'obscurité avec des IgG anti-souris marqués Alexa Fluor 488 (H + L) (CST #4408, MA, USA ), 4',6-diamidino-2-phénylindole (DAPI, Sigma, MO, USA). Pour la coloration à la phalloïdine, après blocage, les cellules ont été perméabilisées avec 0,2% de Triton X-100 pendant 30 min, puis les cellules ont été incubées avec du DAPI et de la phalloïdine-Alexa Flour 573 (Life technologies, CA, USA) pendant 1 h. Après trois lavages, la localisation subcellulaire de l'intégrine β1 et le changement d'actine filamenteuse (actine F) ont été évalués au cours de la différenciation du cartilage avec un microscope confocal à balayage laser (ZEISS, LSM 700, Oberkochen, Allemagne).
Préparation des conseils AFM
Les pointes Si3N4 (DNP-10, Bruker Corp) avec une constante de ressort (0,06 N/m) ont été modifiées chimiquement par l'anticorps anti-CD29 comme suit [15]. Les pointes ont été nettoyées avec de l'acétone, de la lumière ultraviolette et une solution de piranha (H2 SO4 :H2 O2 = 3:1, v /v ) pour des durées différentes (5 min, 30 min et 10 min). Après un rinçage abondant à l'eau purifiée, des pointes ont été formées par incubation avec une solution à 1% de 3-APTES (Sigma, St. Louis, MO, USA) dans de l'éthanol pendant 30 min. Les pointes ont été lavées trois fois avec de l'eau ultrapure et traitées avec une solution de glutaraldéhyde à 2,5 % (Sigma, St. Louis, MO, USA) pendant 1 h. Le glutaraldéhyde superflu a été lavé trois fois avec de l'eau. Enfin, les pointes ont été insérées dans une solution anti-intégrine 1 (1 mg/ml) et incubées une nuit à 4 °C. Les sondes modifiées ont été lavées avec du PBS avant les expériences.
Mesures AFM
L'AFM (Bioscope Catalyst, Bruker, USA) a été utilisé pour étudier la morphologie de l'hADSc et les changements ultrastructuraux au cours de la différenciation chondrogénique. La constante de force exacte des pointes AFM a été mesurée dans du PBS. Pour évaluer la morphologie et l'ultrastructure, les cellules ont été lavées plusieurs fois avec du PBS. Ensuite, une solution de paraformaldéhyde à 4 % a été ajoutée dans un tube de 3,5 cm 2 boîte de culture pendant 15 min. Après que les cellules aient été lavées avec du PBS, les cellules ont été stockées dans du PBS à 4 °C jusqu'à leur utilisation. La constante de ressort des pointes variait de 4,2 à 5,8 N/m en mode contact. Les images morphologiques et ultrastructurales de hADSc ont été prises dans du PBS à température ambiante par AFM. Les images d'ultrastructure entourant les noyaux de hADSc ont été obtenues en mode contact. Le logiciel d'analyse au nanoscope a été utilisé pour évaluer l'ultrastructure de la surface cellulaire pour plus de 15 images différentes de 10 × 10 μm pour au moins 15 cellules différentes dans des groupes (jours 0, 6, 12). La force de liaison entre les pointes AFM modifiées par l'intégrine 1 et les récepteurs CD29 de hADSc vivant a été analysée au cours de différentes périodes chondrogéniques (0, 6 et 12 jours). La force de liaison a été mesurée dans le mode approche-rétraction du système AFM (Bioscope Catalyst, Bruker, USA). Pour étudier les événements de séparation de l'intégrine 1–cellules vivantes, les pointes modifiées par l'anticorps intégrine β1 ont été utilisées à des vitesses d'approche-rétraction de 500 nm/s. La constante de force des pointes fonctionnalisées était de 0,058 ± 0,006 N/m. La force de seuil sur les cellules était de 800 pN. L'anticorps anti-intégrine 1 (100 μg/ml) a été ajouté aux cellules pendant 30 min avant les expériences de mesure de force. Le blocage de l'intégrine 1 et des sondes nues ont également été utilisés comme témoins pour détecter la force de rupture non spécifique entre les pointes modifiées par l'anticorps intégrine β1 et les cellules. Pour la quantification de la probabilité de liaison ligand-récepteur de l'intégrine 1, des courbes de force d'interaction spécifique ont été mesurées par des sondes fonctionnalisées par anticorps intégrine β1. Plus de 400 courbes de force ont été mesurées dans une seule expérience avec des résultats résumés à partir d'au moins trois expériences indépendantes. Ainsi, environ 1200 courbes force-distance d'origine dans chaque expérience de comparaison ont été acquises à partir de 30 à 40 cellules différentes à l'aide du logiciel d'analyse Nanoscope de l'instrument. En faisant la moyenne des valeurs de force pour au moins trois expériences indépendantes, l'effet de l'induction chondrogénique sur la force d'interaction entre le ligand de l'intégrine 1 et les récepteurs CD29 à la surface cellulaire a été déterminé.
Transcription inverse et PCR en temps réel
Des kits de purification d'ARN TRIzol® Plus (Life Technologies, CA, USA) ont été utilisés et 1 μg d'ARN a été rétrotranscrit en ADNc à l'aide d'un kit de transcription inverse d'ADNc à haute capacité (Invitrogen) selon le protocole du fabricant avec une modification mineure. L'intégrine β1 et la GAPDH ont été quantifiées par qRT-PCR avec des amorces spécifiques du gène :5′-TGGAGGAAATGGTGTTTTGC-3′ (intégrine β1-sens) et 5′-CGTTGCTGGCTTCACAAGTA-3′ (intégrine β1-antisens); 5′-CTGACTTCAACAGCGACACC-3′ (GAPDH-sens) et 5′-CCCTTGTTGCTGTAGCCAAAT-3′ (GAPDH-antisens). Pour la PCR en temps réel, la PCR en temps réel Step One (Applied Biosystems) a été réalisée en utilisant Fast SYBR@GREEN Master Mix (Life Technologies, CA, USA). L'expression du gène cible a été normalisée par rapport à la GAPDH en tant qu'étalon interne et calculée à l'aide de la méthode comparative 2-ΔΔCT. Chaque essai a été réalisé en triple.
Analyse statistique
Toutes les expériences ont été réalisées au moins trois fois, avec des données exprimées comme la moyenne ± écart type (SD). La comparaison entre deux groupes a été réalisée par t test. Des différences significatives entre les moyennes des groupes ont été déterminées par une analyse ANOVA à un facteur, suivie du test T2 de Bonferroni et Tamhane (des variances égales n'ont pas été supposées). Valeurs de p < 0,05 ont été considérés comme statistiquement significatifs.
Résultats et discussion
Évaluation de l'hADSc
Les cellules souches mésenchymateuses sont des cellules stromales multipotentes qui ont un potentiel ostéogénique, adipogène, chondrogénique et myogénique. Il existe deux principaux moyens d'identifier hADSc, les marqueurs CD de surface cellulaire et la capacité à se différencier [16]. Comme indiqué dans le fichier supplémentaire 1 : Figure S1 et le fichier supplémentaire 2 : Figure S2, les cellules dérivées étaient hADSc. Ensuite, la prolifération cellulaire du passage 3 hADSc a été déterminée par le test MTT (Fichier supplémentaire 3 : Figure S3).
Modifications induites de la morphologie et de l'ultrastructure de surface au cours de la chondrogenèse hADSc
L'AFM est toujours utilisé pour détecter la morphologie et l'ultrastructure des cellules à l'échelle nanométrique [17]. La forme d'une cellule est liée à sa fonction cellulaire spécialisée et à l'organisation des tissus. Dans certaines recherches sur le cancer, l'AFM peut être utilisée comme technique d'imagerie élevée pour analyser les changements morphologiques afin d'évaluer les effets des médicaments. De plus, la forme des cellules souches mésenchymateuses est modifiée au cours de l'induction chondrogénique [18]. Alors que des changements de forme cellulaire semblent être nécessaires à la différenciation, on sait peu de choses sur le fait que la morphologie cellulaire affecte les premiers stades de développement de la différenciation des cellules souches mésenchymateuses. Par conséquent, les changements de morphologie et d'ultrastructure membranaire au cours de la chondrogenèse hADSc ont été évalués par AFM, car ces changements sont importants [19] et peuvent influencer directement la fonction des cellules [20]. La morphologie de surface et la structure ultrafine de hADSc ont été étudiées au cours de la différenciation chondrogénique pour différentes périodes de temps (Fig. 1 et Fig. 2). La morphologie et l'ultrastructure de surface étaient évidemment différentes dans chaque groupe de comparaison. Au jour 0, les cellules avaient une forme de fuseau allongé avec une surface relativement lisse. L'architecture de la membrane cellulaire était homogène. Après induction chondrogénique, aux jours 6 et 12, des changements significatifs de la morphologie cellulaire ont été observés. La plupart des cellules se sont progressivement réduites en une forme polygonale (Fig. 1a) avec une diminution du rapport longueur/largeur cellulaire moyen au cours de la différenciation chondrogénique (Fig. 1b). De nombreuses études montrent que les changements de morphologie cellulaire sont compatibles avec le cytosquelette des cellules [21]. Nous avons également trouvé les changements du cytosquelette au cours de la différenciation chondrogénique, ce qui a été expliqué dans ces derniers résultats.
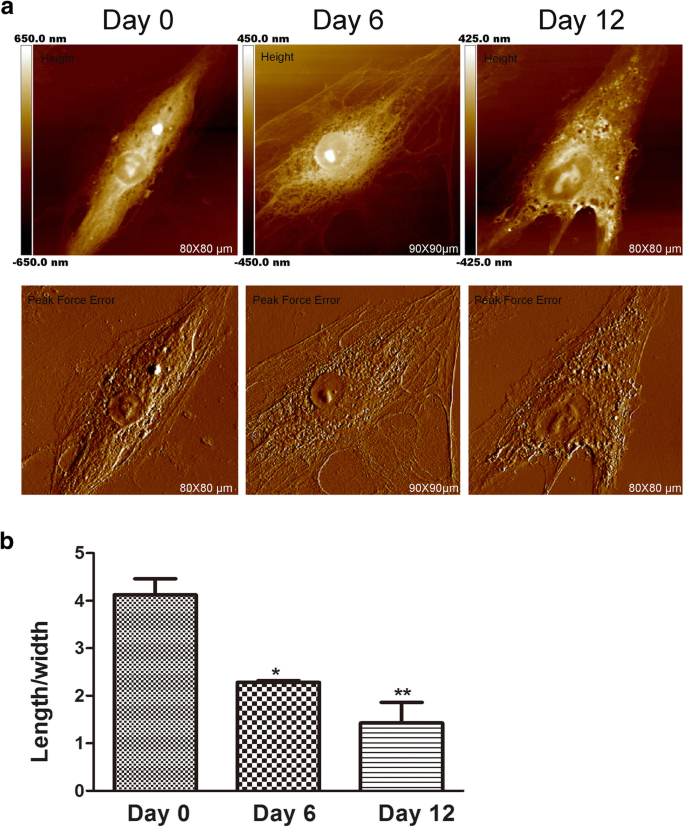
Caractéristiques de la morphologie de l'hADSc au cours de la chondrogenèse. un Des images morphologiques de hADSc entières ont été obtenues à 0, 6 et 12 jours de différenciation chondrogénique. Les images ont été analysées par un modèle d'image d'erreur de hauteur et de force maximale par Nanoscope. b Le rapport longueur/largeur moyen des cellules a été mesuré après un traitement de différenciation chondrogénique à 0, 6 et 12 jours. *p < 0,05, ***i>p < 0,01
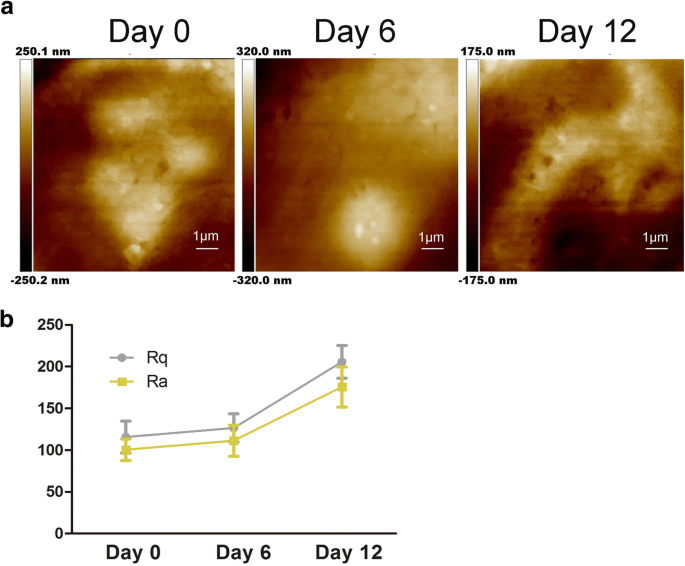
Caractéristiques de l'ultrastructure membranaire hADSc au cours de la différenciation chondrogénique. un Les changements dans l'ultrastructure de la membrane cellulaire ont été évalués après différenciation chondrogénique pendant 0, 6 et 12 jours. b Les paramètres de rugosité de surface Ra et Rq des cellules ont été mesurés pendant l'induction chondrogénique de hADSc pendant 0, 6 et 12 jours
Comme le montre la figure 2a, l'ultrastructure de la membrane cellulaire a également changé ; les particules grossissaient et étaient hétérogènes. Des études antérieures ont démontré que Ra et Rq étaient les créateurs de la valeur de rugosité pour évaluer le changement dans les membranes cellulaires traitées différemment [22]. Rq concerne la rugosité quadratique moyenne, \( \mathrm{Rq}=\sqrt{\frac{\sum_{t-1}^N{\left( Zn-\overline{Z}\right)}^2 }{N-1}} \); \( \mathrm{Rq}=\sqrt{\frac{\sum_{\mathrm{t}-1}^{\mathrm{N}}{\left(\mathrm{Zn}-\overline{\mathrm{Z }}\right)}^2}{\mathrm{N}-1}} ; \) Ra est à peu près la rugosité moyenne, \( \mathrm{Ra}=\frac{1}{N}{\sum}_{ t-1}^N1\mid Zi-\overline{Z}\mid \). Pour obtenir la rugosité, la taille de numérisation est de 10 μm × 10 μm. Comme le montre la figure 2b, le Ra et le Rq de deux zones différentes ont augmenté au cours de la chondrogenèse de hADSc. Les valeurs Ra et Rq des cellules au jour 0 étaient faibles, indiquant une surface lisse (Fig. 2b). Les valeurs de Ra et Rq ont augmenté simultanément avec la différenciation chondrogénique, montrant une plus grande hétérogénéité et plus rugueuse sur les surfaces cellulaires (Fig. 2a). Sur la base des changements observés, la différenciation chondrogénique a entraîné des changements dans la morphologie cellulaire et le rapport hauteur/largeur des cellules (Fig. 1a, b). Il existe des études montrant que la MEC pourrait réguler l'adhésion cellulaire en régulant les intégrines [11]. Par conséquent, des valeurs de rugosité accrues suggèrent des changements dans l'ECM et l'ultrastructure de la membrane cellulaire au cours de la chondrogenèse. Ces données démontrent que la différenciation chondrogénique affecte la morphologie cellulaire, la MEC et la structure de la membrane cellulaire.
Modifications cytosquelettiques pendant l'induction chondrogénique de hADSc
Au cours de la différenciation des cellules souches, la morphologie cellulaire et les changements structurels membranaires sont liés au cytosquelette de la cellule, suite au développement de caractéristiques cellulaires spécifiques à la lignée [21]. Comme le montre la figure 3a, les signaux de fluorescence rouge et bleu indiquent respectivement la F-actine et le DAPI. Le cytosquelette cellulaire a beaucoup changé au cours de l'induction chondrogénique sur la figure 3a. D'une part, les microfilaments du cytosquelette se sont déplacés le long de l'axe cellulaire long dans le groupe au jour 0, tandis que les microfilaments du cytosquelette se sont propagés dans un réseau radial lorsque hADSc a été traité par différenciation chondrogénique pendant 12 jours. D'autre part, la distribution des microfilaments cellulaires était homogène dans le groupe du jour 0 mais les microfilaments étaient principalement distribués à la périphérie des hADSc traités par différenciation chondrogénique pendant 12 jours.
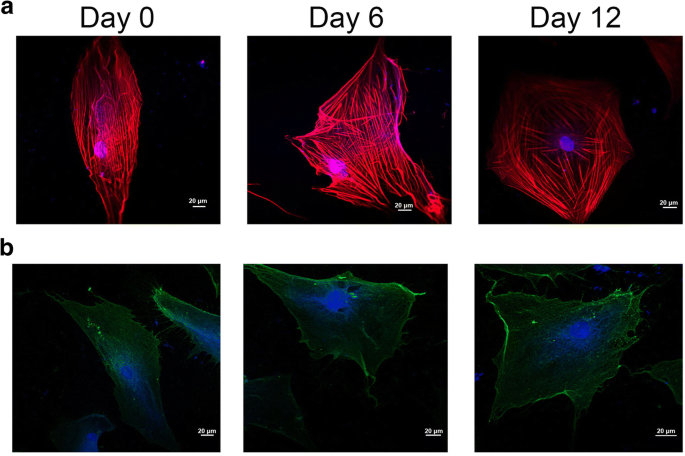
Organisation du cytosquelette et localisation de l'intégrine β1 sur hADSc à différenciation chondrogénique. un Des changements dans le cytosquelette ont été détectés au cours de la chondrogenèse de hADSc par microscopie confocale. b La localisation de l'intégrine β1 a été mesurée au cours de la différenciation chondrogénique par microscopie confocale. Le cytosquelette et le noyau ont été colorés avec la F-actine et le DAPI, respectivement. Les signaux de fluorescence rouge et bleu indiquent respectivement la F-actine et le DAPI
La différenciation chondrogène a modifié la probabilité de liaison de l'intégrine β1 aux récepteurs sur hADSc
L'AFM est également un outil utile pour l'étude de la force de liaison entre les ligands et leurs récepteurs, rendant la transduction du signal membrane-récepteur claire à la surface des cellules [23]. Par AFM, les changements entre l'intégrine β1 et ses récepteurs sont mesurés de manière visuelle, simple et spécifique. L'interaction du ligand-récepteur de l'intégrine 1 sur les cellules vivantes est un moyen d'explorer le processus de liaison sur la membrane cellulaire. La procédure de fonctionnalisation des pointes AFM est le couplage de l'intégrine 1 aux pointes AFM par liaison d'APTES et de glutaraldéhyde. Ces pointes ont été utilisées pour la détection de la liaison de l'intégrine β1 aux récepteurs CD29 sur les surfaces cellulaires (Fig. 4a). La spectroscopie de force à molécule unique (SMFS) a été utilisée pour évaluer la distribution de la force de séparation des cellules vivantes anti-intégrine 1 dans les régions localisées de l'hADSc vivant individuel (Fig. 4b). Des courbes de force représentatives sont présentées sur les figures 4c, d, qui représentent une courbe à molécule unique (figure 4c) et deux paires de courbes de pic de rupture (figure 4d). Des expériences de blocage et des expériences de pointes nues AFM ont été réalisées pour vérifier la spécificité des courbes de force obtenues. Les pointes AFM nues n'ont détecté aucun pic de force spécifique (Fig. 4e). Des expériences AFM nues ont montré que la probabilité de liaison non spécifique de l'interaction ligand-récepteur de l'intégrine β1 à la surface de l'hADSc était inférieure à 1%. Pour les expériences de blocage, l'anticorps anti-intégrine 1 a été incubé avec des cellules pendant 30 min, puis les courbes de force ont été enregistrées à l'aide d'embouts fonctionnalisés à l'intégrine 1. L'anticorps bloquant a réduit les courbes de force de 90 % (Fig. 4f). Il n'y avait pas de différence dans la probabilité de liaison du ligand-récepteur de l'intégrine 1 sur les surfaces cellulaires entre les trois groupes après traitement par anticorps anti-intégrine β1 (Fig. 4g). Ces résultats démontrent que les pointes AFM modifiées par anticorps étaient très utiles pour détecter la force, et que les pointes AFM fonctionnalisées par l'intégrine β1 étaient spécifiques.
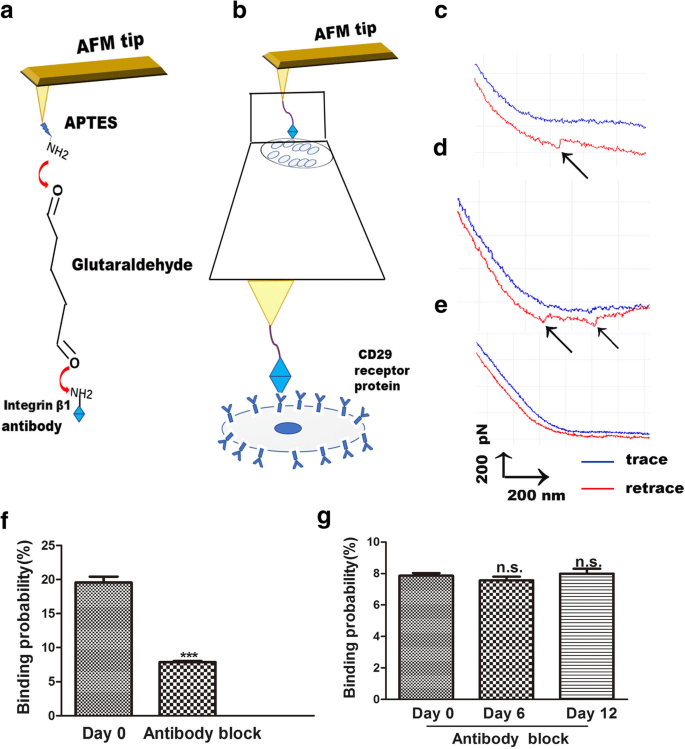
Mesures de force AFM avec une pointe AFM fonctionnalisée par l'intégrine 1 sur un hADSc vivant. un Représentation schématique de la stratégie utilisée pour l'immobilisation de l'intégrine 1 sur une pointe AFM. b Représentation schématique de la force d'une molécule unique mesurée entre les pointes AFM fonctionnalisées par l'intégrine 1 et l'hADSc vivant. c, d Courbes de force représentatives obtenues avec des pointes AFM modifiées à l'intégrine β1 sur hADSc et e après que le système a été bloqué avec la solution d'anticorps monoclonal d'intégrine 1. f La probabilité de liaison des pointes fonctionnalisées par l'intégrine 1 sur hADSc avant et après le blocage par l'anticorps intégrine β1 au jour 0. g La probabilité de liaison des pointes fonctionnalisées par CD29 sur hADSc après blocage par l'anticorps intégrine β1 à 0, 6 et 12 jours. ***p < 0.001, n.s.. aucune différence significative
La force de liaison (force de rupture) est la force d'interaction entre les ligands et leurs récepteurs [24]. Les changements de morphologie et d'ultrastructure de surface des membranes plasmiques sont liés à de nombreux processus de biologie cellulaire, tels que la différenciation, l'apoptose et la migration cellulaire. Au cours de la différenciation, on pense que les modifications du cytosquelette sont liées aux modifications de l'intégrine, en particulier de l'intégrine β1. L'intégrine β1 (CD29) est très importante dans l'adhésion cellulaire à l'ECM et dans l'adhésion cellule-cellule. Il peut également interagir avec des protéines intracellulaires, stimulant des molécules de signalisation liées au cytosquelette d'actine [25]. Dans cette étude, des modifications de la morphologie du cytosquelette et des cellules ont été observées au cours de la chondrogenèse hADSc par microscopie confocale à balayage laser (CLSM) et AFM. Au cours de la différenciation chondrogénique, les changements dans le cytosquelette, la morphologie et l'ultrastructure de surface peuvent être un nouvel indicateur fiable de l'état cellulaire. L'intégrine β1, le récepteur CD29, est distribuée sur la surface cellulaire comme jugé par immunofluorescence (Fig. 3b). La force de liaison et la stabilité des complexes ligand-récepteur de l'intégrine β1 au cours de la chondrogenèse hADSc ont été évaluées à 0, 6 et 12 jours de différenciation. Un total de 1200 courbes ont été enregistrées pour chaque jour, avec des forces de rupture moyennes de 61,8 ± 22,2 pN, 60 ± 20,2 pN et 67,2 ± 22,0 pN, respectivement (Fig. 5a–c). La distribution de l'amplitude de la force a été analysée en tant que force moyenne + SD (Fig. 5d). Il n'y avait pas de différence significative de force moyenne entre les jours 0 et 6. Il y avait une différence de force moyenne entre les jours 0 et 12. L'amplitude de la force de liaison a augmenté au jour 12. Pendant ce temps, les événements de rupture à 0, 6 et 12 jours étaient respectivement de 19,58 ± 1,74%, 28,03 ± 2,05 % et 33,4 ± 1,89 % (Fig. 5e). La probabilité de liaison accrue a également indiqué que l'intégrine 1 (CD29) a joué un rôle important dans la différenciation chondrogénique et peut fournir des informations pour la différenciation chondrogénique, via des voies de signalisation. Par conséquent, l'augmentation des nanodomaines d'intégrine β1 au cours de la différenciation chondrogénique peut affecter fondamentalement la force de liaison du ligand-récepteur CD29 sur hADSc vivant. Des changements dans la morphologie et l'ultrastructure de surface des membranes plasmiques ont accompagné des changements dans la structure, la conformation, la force de liaison et la stabilité des complexes ligand-récepteur de l'intégrine 1 sur les cellules. En résumé, l'intégrine β1 joue un rôle nécessaire dans la différenciation chondrogénique hADSc.
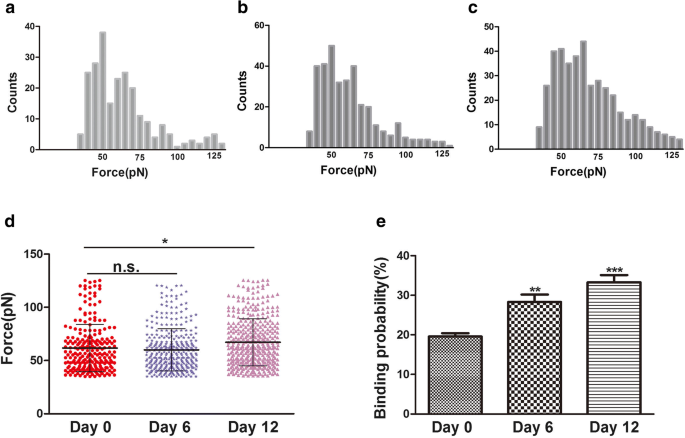
Force de liaison et probabilité de liaison mesurées à la surface d'hADSc vivants par des pointes AFM fonctionnalisées par l'intégrine β1. a–c Histogrammes de la force de liaison de l'anticorps-récepteur intégrine 1 obtenus lors de la différenciation chondrogénique hADSc pendant 0, 6 et 12 jours. d Les forces de liaison pour les récepteurs de l'intégrine 1 ont été obtenues à 0, 6 et 12 jours de différenciation chondrogénique de hADSc. e La probabilité de liaison du récepteur integr1 de l'intégrine a été détectée pendant la différenciation chondrogénique de hADSc pendant 0, 6 et 12 jours. *p < 0,05, ***i>p < 0,01, ****p < 0,001, n.s. pas de différence significative
Suppression de l'intégrine β1 pendant la différenciation chondrogène hADSc
De nombreuses études ont montré que les membres de la famille des intégrines jouent un rôle important dans la différenciation cellulaire. De plus, les intégrines peuvent réguler l'interaction entre l'environnement extracellulaire et les cellules, contrôlant les voies de transduction du signal via des protéines connectées [26]. Des études antérieures ont montré que la probabilité de liaison peut être affectée par la densité et la conformation de la protéine transmembranaire (récepteurs) à la surface cellulaire [27]. La conformation de l'intégrine peut être un casque fermé, qui a une faible affinité pour le ligand, ou un casque ouvert, qui a une forte affinité pour le ligand [28, 29]. L'expression de l'intégrine β1 était régulée à la hausse aux niveaux transcriptionnel et traductionnel avec une expression accrue du collagène II, caractéristique des chondrocytes (Fig. 6a, b). En tant que telle, l'expression de l'intégrine β1 régulée à la hausse était cohérente avec une probabilité de liaison accrue sans tenir compte de la conformation.
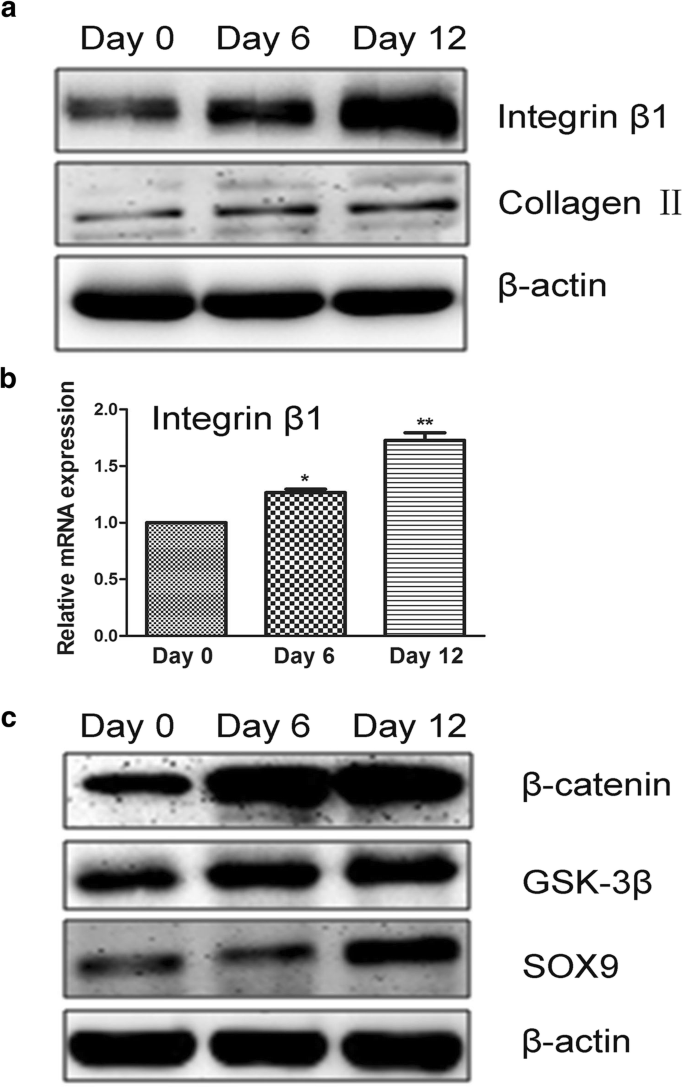
The role of integrin β1 and β-catenin/SOX pathway in regulating hADSc chondrogenic differentiation. un Protein integrin β1 was up-regulated during chondrogenesis of hADSc as assessed by western blotting. Cartilage differentiation up-regulated collagen II expression at different days. b The mRNA of integrin β1 was up-regulated during chondrogenic differentiation of hADSc. c Measurement of proteins associated with the β-catenin/SOX pathway during chondrogenic differentiation of hADSc for 0, 6, and 12 days. *p < 0,05, ***i>p < 0.01
The Role of Integrin β1 in Chondrogenic Differentiation Regulated by the β-catenin/SOX Signaling Pathway
Previous studies have shown Wnt/β-catenin, PI3K, and mTOR signaling pathways to be related to integrin β1 [30,31,32]. Each is important in mesenchymal stem cell differentiation. Likewise, studies have demonstrated SOX and collagen II to be regulated by integrin β1 during chondrogenesis of hADSc. SOX is a hallmark component of the Wnt/β-catenin signaling pathway. Hence, we hypothesized that chondrogenic differentiation was regulated by the β-catenin/SOX pathway via integrin β1. SOX, GSK-3β, β-catenin, and integrin β1 were all increased during chondrogenesis of hADSc (Fig. 6c), with integrin β1 inducing cell signaling. These data demonstrate chondrogenic differentiation to be regulated by the β-catenin/SOX pathway via integrin β1.
Prospective and Limitations
In this work, changes in cellular morphology, the structure of the membrane, and the binding probability of integrin β1 ligand–receptors were demonstrated to be useful image markers to evaluate the chondrogenic differentiation process. This is a new method for evaluation of morphology, membrane ultrastructure, and changes in transmembrane proteins during chondrogenic differentiation. There are limitations to this study. Although increased binding probability was related to the high expression of integrin β1, the conformation of integrin β1 during chondrogenesis was not investigated. Further work is necessary to determine the conformation of integrin β1 during chondrogenic differentiation. Integrin β1 was demonstrated to participate in the β-catenin/SOX signaling pathway during chondrogenesis of hADSc. However, the relationship between integrin β1 and β-catenin/SOX signaling pathway is still not fully established. Further work is necessary to identify the exact role of integrin β1 in this pathway.
Conclusions
In the present work, a novel method (AFM) was employed to evaluate chondrogenic induction in hADSc. Cell surface ultrastructural changes were assessed by AFM imaging. AFM was used to investigate the binding force and binding probability between integrin β1 ligand and its receptors on the surface of hADSc by integrin β1-functionalized AFM tips. Based on AFM data, during chondrogenesis, cell morphology was changed from an elongated spindle shape to a polygonal shape with increased cell roughness. By use of integrin β1-functionalized AFM tips, the binding probability and force magnitude of integrin β1 ligand–receptor on the surface of hADSc were found to increase during chondrogenic induction. By immunoblot, integrin β1 was demonstrated to participate in the β-catenin/SOX signaling pathway, which regulated the chondrogenesis of hADSc. Taken together, these results and the established methodology contribute to a better understanding of cell morphology and roughness. Further, the data provide thermodynamic and kinetic insight into the integrin β1 ligand-binding process, at the single-molecule level. This AFM method will be useful for investigation of signaling pathways in living hADSc during chondrogenesis. Changes in the cellular nanostructure, as well as structure of the membrane, and the binding probability of transmembrane proteins are useful markers to evaluate chondrogenic differentiation mechanisms. This AFM method can be used to understand the mechanism of mesenchymal stem cell differentiation in tissue engineering and will be useful for an enhanced understanding of mesenchymal stem cell chondrogenic differentiation.
Abréviations
- AFM :
-
Microscopie à force atomique
- CD:
-
Cluster of differentiation
- DAPI:
-
4′,6-diamidino-2-phenylindole
- DMEM :
-
Dulbecco’s Modified Eagle’s Medium
- ECM:
-
Extracellular matrix
- F-actine :
-
Actine filamenteuse
- FBS :
-
Sérum fœtal bovin
- hADSc:
-
Human adipose-deprived stem cells
- IB:
-
Immunoblotting analysis
- IBMX:
-
3-isobutyl-1-methylxanthine
- IGF-1:
-
Insulin-like growth factors-1
- ITS:
-
Insulin transferrin selenium
- mTOR:
-
Mammalian target of rapamycin
- OA :
-
Osteoarthritis
- PBS :
-
Phosphate buffer solution
- PI3K:
-
Phosphoinositide 3-kinase
- SD :
-
Écart type
- SMFS:
-
Single-molecule force spectroscopy
- TGF-β1:
-
Transforming growth factor-beta1
Nanomatériaux
- Démonstration d'un biocapteur flexible à base de graphène pour la détection sensible et rapide des cellules cancéreuses de l'ovaire
- Technologies avancées de dépôt de couche atomique pour les micro-LED et les VCSEL
- Les nanoparticules de phosphore noir favorisent la différenciation ostéogénique des CSEM grâce à l'expression TG2 régulée à la hausse
- Dévoilement de la structure atomique et électronique des nanofibres de carbone empilées
- Analyse de l'actine et de l'organisation de l'adhésion focale dans des cellules U2OS sur des nanostructures polymères
- Les nanotechniques inactivent les cellules souches cancéreuses
- Comparaison des électrodes métalliques à motifs de type nanotrou et de type nanopilier incorporées dans des cellules solaires organiques
- Synthèse de nanocristaux de ZnO et application dans des cellules solaires polymères inversées
- Étude de la force d'adhérence et de la transition vitreuse de films minces de polystyrène par microscopie à force atomique



