Fabrication et propriété photocatalytique de nouveaux nanocomposites SrTiO3/Bi5O7I
Résumé
Le roman SrTiO3 /Bi5 O7 I nanocomposites ont été fabriqués avec succès par une approche de décomposition thermique. Les échantillons tels que préparés ont été caractérisés par les spectres XRD, XPS, SEM, EDS, FTIR, DRS et PL. Les résultats montrent que le SrTiO3 /Bi5 O7 I les nanocomposites sont composés de pérovskite SrTiO3 nanoparticules et tétragonale Bi5 O7 Je nanotiges. Le SrTiO3 /Bi5 O7 Les nanocomposites présentent une excellente performance photocatalytique pour la dégradation de la solution de RhB sous irradiation solaire simulée, supérieure à celle du Bi5 vierge O7 I et SrTiO3 . En particulier, les 30 % en poids de SrTiO3 /Bi5 O7 I nanocomposite se trouve comme les composites optimaux, sur lesquels la dégradation du colorant atteint 89,6% pour 150 min de photocatalyse. Le taux de dégradation photocatalytique de 30 % en poids de SrTiO3 /Bi5 O7 Le nanocomposite est 3,97 fois et 12,5 fois supérieur à celui du Bi5 nu O7 I et SrTiO3 , respectivement. Les expériences de piégeage d'espèces réactives suggèrent que \( \bullet {\mathrm{O}}_2^{-} \) et les trous sont les principales espèces actives responsables de la dégradation de RhB. De plus, les spectres PL élucident la séparation efficace des paires électron-trou photoinduites. De plus, le mécanisme photocatalytique possible du SrTiO3 /Bi5 O7 I nanocomposites est également élucidé sur la base des preuves expérimentales.
Contexte
Les teintures issues des industries textiles ou colorantes ont suscité de nombreuses inquiétudes quant à l'impact sur la qualité des ressources en eau et les produits de dégradation toxiques et cancérigènes [1]. Par conséquent, des techniques de traitement plus compétentes sont nécessaires pour l'élimination complète des colorants des eaux usées. Plusieurs méthodes conventionnelles impliquant des méthodes physiques, chimiques et biologiques ont été appliquées pour la décoloration des eaux usées [2]. Ces méthodes peuvent éliminer les colorants des eaux usées, mais elles sont souvent coûteuses, inefficaces et produisent des déchets secondaires [3, 4]. Parmi les diverses technologies de traitement des eaux usées par colorant, la photocatalyse à base de semi-conducteurs a suscité un grand intérêt et a attiré l'attention du monde entier [5,6,7]. En effet, il utilise l'énergie solaire pour la décomposition des polluants colorants, dont la source d'énergie est abondante, inépuisable, non polluante et gratuite [8, 9]. Actuellement, TiO2 est le photocatalyseur semi-conducteur le plus largement utilisé en raison de sa photoactivité élevée, de son faible coût, de sa stabilité chimique et photochimique, de sa non-toxicité et de ses caractéristiques respectueuses de l'environnement. Cependant, il a montré une très faible activité photocatalytique sous irradiation de lumière visible en raison de sa large bande interdite de 3,2 eV et de la recombinaison rapide des porteurs photogénérés [10]. Pour résoudre efficacement les problèmes mentionnés ci-dessus, de nombreux travaux ont été consacrés à la modification de surface ou à la combinaison de photocatalyseurs semi-conducteurs [11]. Néanmoins, le développement de photocatalyseurs innovants et hautement efficaces reste un défi majeur [12].
Bi5 O7 I est un semi-conducteur de type p nouvellement trouvé, qui montre un niveau de bande de valence (VB) relativement plus positif que les autres oxyiodures de bismuth en fournissant plus de trous photo-excités et facilite par la suite la séparation des porteurs photogénérés [13]. Par conséquent, le Bi5 O7 Le photocatalyseur I présente une activité élevée pour la photodégradation de la Rhodamine B (RhB) dans l'eau et l'acétaldéhyde sous irradiation de lumière visible [14]. Malheureusement, l'application pratique de Bi5 O7 Le photocatalyseur dans la décontamination environnementale est encore limité, ce qui est attribué à sa faible efficacité de transfert causée par la recombinaison d'électrons photogénérés et de trous [15]. Dans le but d'améliorer encore la photoactivité de Bi5 O7 I, de nombreuses tentatives ont été réalisées comme le dopage avec des métaux ou des non-métaux [16], ou le couplage avec d'autres semi-conducteurs. Par exemple, Huang et al. synthétisé g-C3 N4 /Bi5 O7 I hétérojonction via une méthode de co-cristallisation, et le composite présentait un taux de dégradation 2,9 fois supérieur à celui du Bi5 pur O7 je [17]; Cheng et al. fabriqué Bi5 O7 I/Bi2 O3 composite via une méthode de gravure chimique, qui a montré une activité photocatalytique élevée dans la décomposition du vert de malachite [18]; Hu et al. ont signalé qu'un composite comprenant Sr2 de type n TiO4 et p-type Bi5 O7 J'ai montré une photoactivité accrue en raison de l'inhibition de la recombinaison électron-trou [19]; Cui et al. fabriqué AgI/Bi5 O7 J'hybride via une simple réaction ionique en une étape, et l'AgI/Bi5 O7 Je composite amélioré l'activité photocatalytique [20], et ainsi de suite. Ces résultats ont montré que Bi5 O7 Les composites à base d'I ont présenté une performance photocatalytique améliorée sous irradiation de lumière visible. Par conséquent, nous pouvons fabriquer Bi5 O7 Composites à base d'I par couplage à un autre semi-conducteur avec des positions de bande de conduction (CB) et VB appropriées en tant que photocatalyseur prometteur piloté par la lumière visible. Parmi les différents candidats, le titanate de strontium (SrTiO3 ) est un matériau semi-conducteur de type n, qui a été largement étudié en raison de ses nombreuses excellentes propriétés, par exemple, stabilité thermique, bonne résistance à la chaleur, corrosion et résistance [21,22,23]. Pur SrTiO3 absorbe uniquement la lumière UV en raison de sa large bande interdite de 3,1 à 3,4 eV [24]. Heureusement, le VB de SrTiO3 est positionné entre le CB et le VB de Bi5 O7 I, tandis que son CB est positionné au dessus du CB de Bi5 O7 I. Considérant les mérites structurels de Bi5 O7 I, combinaison de SrTiO3 avec Bi5 O7 I pour former le SrTiO3 /Bi5 O7 I composite peut être un moyen viable et conseillé de réaliser l'activité photocatalytique élevée.
Dans ce travail, une série de SrTiO3 /Bi5 O7 Les photocatalyseurs nanocomposites ont d'abord été synthétisés. Leur phase cristalline, leur microstructure et leurs propriétés optiques ont été étudiées par une série de techniques. Le SrTiO3 /Bi5 O7 Les nanocomposites ont affiché une performance photocatalytique améliorée dans la dégradation de la solution de Rhodamine B (RhB) sous une irradiation solaire simulée. De plus, le mécanisme photocatalytique possible du SrTiO3 /Bi5 O7 I nanocomposites a également été élucidé sur la base des preuves expérimentales.
Méthodes
Préparation du SrTiO3 /Bi5 O7 I Composites
SrTiO3 nanoparticules et SrTiO3 Les composites /BiOI ont d'abord été synthétisés via une méthode sol-gel telle que décrite dans la littérature [25, 26]. SrTiO3 /Bi5 O7 I composites ont ensuite été synthétisés par une voie de décomposition thermique. Tous les réactifs chimiques ont été utilisés directement pour les expériences sans autre purification. Pendant la décomposition thermique, le SrTiO3 tel que préparé Les composites /BiOI ont été placés dans un four tubulaire et le programme de chauffage a été défini comme suit :rampe à 5 °C min − 1 à 500 °C en continu et maintien à 500 °C pendant 3 h. Ensuite, le four a été naturellement refroidi à température ambiante pour obtenir 10 % en poids de SrTiO3 /Bi5 O7 Je nanocomposite. Autre SrTiO3 /Bi5 O7 I matériaux nanocomposites avec différents SrTiO3 le contenu a été fabriqué par la même méthode.
Caractérisation de l'échantillon
Les structures cristallines des échantillons synthétisés ont été caractérisées par diffraction des rayons X (XRD) avec Cu Kα rayonnement (D/max-2500, Rigaku). La morphologie des échantillons a été étudiée par un microscope électronique à balayage à émission de champ ultra-haute résolution (FE-SEM; SUAPR55, Allemagne Zeiss) avec spectroscopie de rayons X à dispersion d'énergie (EDS). La composante élémentaire de surface et l'état chimique des échantillons ont été analysés par spectroscopie photoélectronique à rayons X (XPS ; Axis Ultra DLD, Kratos Analytical, UK) avec un Al Kα monochromatisé Source de rayons X (hν = 1486.6 eV). Les spectres de réflectance diffuse (DRS) ultraviolet-visible (UV-vis) ont été obtenus à l'aide d'un spectrophotomètre UV-vis (UV-2450, Shimadzu). Les groupes fonctionnels à la surface des échantillons ont été étudiés dans une spectroscopie infrarouge à transformée de Fourier Nicolet iS50 (FTIR; Thermo Fisher Scientific, USA). Les spectres d'émission de photoluminescence (PL) ont été mesurés sur un spectromètre à fluorescence en régime permanent LH110911.
Études d'évaluation photocatalytique
L'activité photocatalytique des matériaux a été évaluée via la décomposition de RhB sous irradiation solaire simulée (lumière UV) dans un appareil de photoréaction. Après 30 min d'adsorption dans l'obscurité, l'adsorption-désorption est à l'équilibre entre le photocatalyseur et les molécules RhB. Une lampe au xénon de 500 W a été utilisée comme source de lumière solaire simulée (lampe UV). Cent milligrammes de photocatalyseur ont été complètement dispersés dans 100 mL de solution de RhB (20 mg/L). Au cours de chaque expérience photocatalytique, 3 ml de la suspension ont été pipetés toutes les 30 minutes et centrifugés pour éliminer les particules de catalyseur. La concentration de RhB a été mesurée à l'aide d'un spectrophotomètre UV-vis.
Résultats et discussion
Analyse XRD
Les modèles de poudre XRD fournissent la structure cristalline et les informations de phase des échantillons synthétisés, comme le montre la figure 1. Le SrTiO3 l'échantillon est fortement cristallisé avec une structure pérovskite (JCPDS n° 35-0734). La diffraction culmine au 2θ les valeurs de 22,75°, 32,39°, 39,95°, 46,47°, 52,34°, 57,78°, 67,82° et 77,18° peuvent être indexées sur (100), (110), (111), (200), (210), (211), (220) et (310) plans cristallins, respectivement [27]. Aucun autre pic de diffraction spécifique n'est détecté. Du modèle XRD de pur Bi5 O7 I, on peut voir que les principaux pics de diffraction à 7,71°, 13,31°, 15,38°, 23,19°, 28,08°, 31,09°, 33,43°, 46,28°, 47,69°, 53,45°, 56,51° et 58,02° sont conformes aux (001), (201), (002), (401), (312), (004), (020), (024), (224), (714), (332) et (624) avions du Bi5 O7 I (JCPDS n° 10-0548), respectivement [28]. Le pic le plus fort correspond au plan cristallin (312) de Bi5 O7 I. À partir du modèle XRD de 30 % en poids de SrTiO3 /Bi5 O7 I nanocomposite, il peut être constaté que tous les pics de diffraction importants proviennent du tétragonal Bi5 O7 Moi et pérovskite SrTiO3 . Il n'y a pas d'autres pics évidents d'impureté observés, ce qui indique que le Bi5 O7 I et SrTiO3 phases coexistent dans le composite.
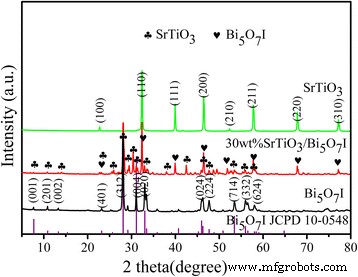
Modèles XRD de pur Bi5 O7 Moi, SrTiO3 et 30 % en poids de SrTiO3 /Bi5 O7 Je nanocomposite
Analyse XPS
Les mesures XPS fournissent des informations supplémentaires pour l'évaluation de la composition élémentaire de surface et de la pureté des 30 % en poids de SrTiO3 /Bi5 O7 Je nanocomposite. L'énergie de liaison obtenue dans l'analyse XPS a été corrigée pour la charge de l'échantillon en référençant C 1 s à 284,65 eV, et les résultats sont affichés sur la figure 2. Le spectre de balayage XPS du composite est illustré sur la figure 2a, qui révèle la existence d'éléments Ti, Sr, Bi, I et O dans le composite. Les deux pics forts à 159,02 et 164,25 eV sont respectivement attribués à Bi 4f5/2 et Bi 4f7/2 pics de Bi 3+ dans le SrTiO3 /Bi5 O7 I nanocomposites comme le montre la Fig. 2b [29]. Dans les spectres XPS de I 3d illustrés à la Fig. 2c, les deux pics forts à 617,88 et 630,22 eV, correspondant à I 3d5/2 et je 3d3/2 , respectivement, suggèrent l'état d'oxydation − 1 de l'iode [30]. Comme le montre la Fig. 2d, les énergies de liaison de Ti 2p3/2 et Ti 2p1/2 correspondent aux pics à 457,90 et 463,80 eV dans le spectre de Ti 2p, respectivement. La séparation des pics entre le Ti 2p3/2 et Ti 2p1/2 est de 5,90 eV, ce qui indique un état d'oxydation + 4 du Ti dans le SrTiO3/Bi5 O7 Je composite [31]. Sur la figure 2e, les pics à 132,50 et 134,25 eV correspondent aux énergies de liaison de Sr 3d5/2 et Sr 3d3/2 , respectivement, indiquant son existence dans le Sr 2+ état [32]. Sur la figure 2f, les pics à 529,65 et 531,25 eV sont attribués à O 1 s. Le pic à 529,65 eV est attribué à l'oxygène du réseau de SrTiO3 /Bi5 O7 I nanocomposites, et le pic à 531,25 eV est généralement attribué à l'oxygène chimisorbé causé par les lacunes en oxygène [33]. Le résultat XPS confirme en outre la formation de SrTiO3 /Bi5 O7 I nanocomposites, et une intégration intime a été réalisée, ce qui concorde bien avec les résultats de XRD.
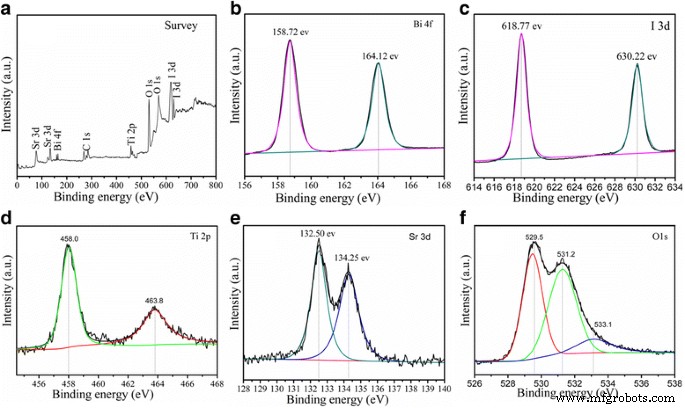
Modèles XPS du SrTiO à 30 % en poids3 /Bi5 O7 I nanocomposites :a sondage, b Bi 4f, c Je 3d , d Ti 2p, e Sr 3d, et f O1
Analyse SEM et EDS
Les compositions de surface et les morphologies du SrTiO3 pur tel que préparé , Bi5 O7 I et 30 % en poids de SrTiO3 /Bi5 O7 Je nanocomposite ont été observés par FE-SEM. Comme le montre la figure 3a, du SrTiO3 pur est composé de particules sphéroïdales ou sphériques d'un diamètre compris entre 50 et 300 nm. Le SrTiO3 de plus petite taille les particules sont évidemment agrégées ensemble dans une certaine mesure. Dans la Fig. 3b, pour le Bi5 O7 En nanofeuillets, ils ont une taille moyenne d'environ 1 μm et une épaisseur comprise entre 80 et 100 nm, ce qui est similaire à celui rapporté précédemment [13]. En revanche, après la combinaison le Bi5 O7 I n'est pas de nanofeuilles mais de morphologie de nanotiges, qui est construite par beaucoup de nanotiges, comme le montre la figure 3c. Pour le Bi5 O7 I nanotiges, la longueur est comprise entre 100 et 300 nm et le diamètre moyen est d'environ 80 nm. On voit clairement que SrTiO3 les particules adhèrent étroitement à la surface de Bi5 O7 I nanotiges, et on pense qu'il est favorable aux performances photocatalytiques. De plus, l'EDS a été utilisé pour analyser la composition chimique des 30 % en poids de SrTiO3 /Bi5 O7 Je nanocomposite. Comme le montre la figure 3d, le signal C observé peut être dérivé de l'adhésif conducteur qui est utilisé pour fixer l'échantillon. Il est à noter que l'EDS est convenablement utilisé pour la détermination quantitative de la teneur en éléments lourds (par exemple, Bi, Ti, I et Sr), mais pas pour les éléments légers (par exemple, P et O) [34]. Le rapport atomique de Bi à I est obtenu comme 11/63 à partir du spectre EDS, ce qui est bien en accord avec le rapport atomique Bi/I de Bi5 O7 Je phase. Le rapport atomique Sr/Bi est très proche de 1/12,5, ce qui implique que SrTiO3 La phase représente environ 30 % de la teneur molaire totale du composite.
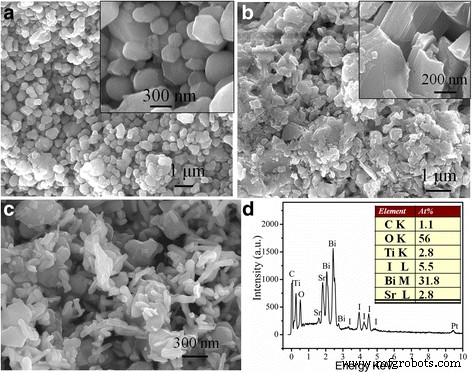
Images SEM de a pur SrTiO3 , b pur Bi5 O7 Je, c 30 % en poids de SrTiO3 /Bi5 O7 Je nanocomposite, et d Spectre EDS de 30 % en poids de SrTiO3 /Bi5 O7 Je nanocomposite
Analyse des propriétés optiques
Les spectres UV-vis DRS des différents catalyseurs sont présentés sur la figure 4a. Le pur SrTiO3 présente un bord de bande d'absorption à 380 nm dans la région UV, ce qui pourrait être attribué à l'énergie à large bande interdite [35, 36]. Le Bi5 O7 I montre un bord d'absorption beaucoup plus long de 520 nm, qui peut répondre à la lumière visible. Le bord d'absorption du SrTiO3 /Bi5 O7 Je nanocomposites sont 480 ~ 520 nm. Par rapport au SrTiO3 pur , après couplage avec Bi5 O7 I nanofeuillets, l'intensité du pic d'absorption du SrTiO3 /Bi5 O7 I nanocomposites amélioré de manière significative.
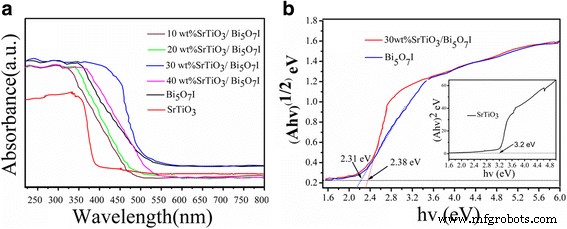
un Spectres DRS de SrTiO3 /Bi5 O7 I nanocomposites et b la parcelle Tauc de (Ahν) 1/2 versus hν le Bi5 pur O7 I et 30 % en poids de SrTiO3 /Bi5 O7 Je nanocomposite, le tracé de Tauc de (Ahν) 2 versus hν le SrTiO3 pur photo en médaillon de b
Sur la base des spectres d'absorption, le E g du semi-conducteur peut être calculé à partir de Aһν = A (һν − E g ) n /2 équation [37]. Les valeurs de n pour SrTiO3 et Bi5 O7 J'ai 4 et 1 ans respectivement. L'énergie de bande interdite du SrTiO3 peut être estimé à partir du tracé (Aһν) 2 en fonction de l'énergie du ploton (һν), et de l'énergie de la bande interdite du Bi5 O7 Je peux être estimé à partir du tracé (Aһν) 1/2 contre һν. L'interception de la tangente au X L'axe donne une approximation de l'énergie de la bande interdite des échantillons, comme indiqué sur la Fig. 4b. Les valeurs de l'énergie de la bande interdite du Bi5 pur O7 I, 30 % en poids de SrTiO3 /Bi5 O7 Je nanocomposite et pur SrTiO3 sont d'environ 2,31, 2,38 et 3,2 eV, respectivement, ce qui correspond aux valeurs rapportées dans la littérature pertinente [38, 39].
Analyse par spectroscopie FTIR
Le Bi5 O7 I et SrTiO3 /Bi5 O7 Les nanocomposites ont été davantage caractérisés à l'aide de la spectroscopie FTIR pour analyser leur liaison chimique. Comme le montre la Fig. 5. On peut voir que dans presque tous les échantillons, les bandes d'adsorption de 3445,5 et 1621,9 cm −1 étaient dues à la vibration d'étirement O–H et à la vibration de déformation des molécules d'eau chimisorbées [40]. La bande à 2906,5 cm −1 est attribuée à la vibration d'étirement Ti-O [41]. Les autres pics dans la plage de 1471,6 à 500 cm −1 correspondent aux modes d'étirement et de déformation impliqués dans les liaisons Bi-O [42].
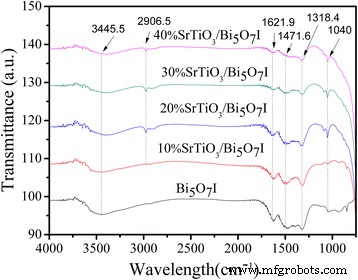
Spectres FTIR du Bi5 pur O7 I et SrTiO3 /Bi5 O7 Je nanocomposites
Activité photocatalytique
Comme Bi5 O7 I et SrTiO3 ont une photo absorption et SrTiO3 très distincts réagit principalement à la lumière UV, la lumière solaire simulée et la lumière UV dans les mêmes conditions sont utilisées séparément comme source lumineuse pour explorer les performances photocatalytiques de Bi5 O7 Moi, SrTiO3 , et SrTiO3 /Bi5 O7 Je nanocomposites. La figure 6a affiche les courbes de dégradation de RhB sous une irradiation solaire simulée. On observe que RhB est stable et à peine décomposé sans le catalyseur sous irradiation solaire simulée pendant 150 min. Le pur SrTiO3 montre une activité catalytique modérée, et seulement 18 % de réduction de RhB ont été obtenus après 150 min d'irradiation. Elle est attribuée à la faible absorption lumineuse de SrTiO3 dans la région de la lumière visible ou ses grandes énergies de bande interdite. Bi5 pur O7 I affiche une activité très distincte qui dégrade plus de 52 % de RhB en 150 min. Par rapport au SrTiO3 pur et Bi5 O7 Moi, le SrTiO3 /Bi5 O7 Les nanocomposites présentent une activité photocatalytique significativement améliorée dans les mêmes conditions. Avec l'augmentation de SrTiO3 teneur de 10 à 40 %, l'activité photocatalytique des composites augmente d'abord puis diminue, et l'activité photocatalytique la plus élevée est observée pour les 30 % en poids de SrTiO3 /Bi5 O7 Je nanocomposite. Pour ce composite optimal, la dégradation du colorant atteint environ 89,6 % sous une irradiation solaire simulée pendant 150 min. Une activité aussi élevée peut être attribuée aux électrons photogénérés ayant une mobilité et une séparation plus rapides.
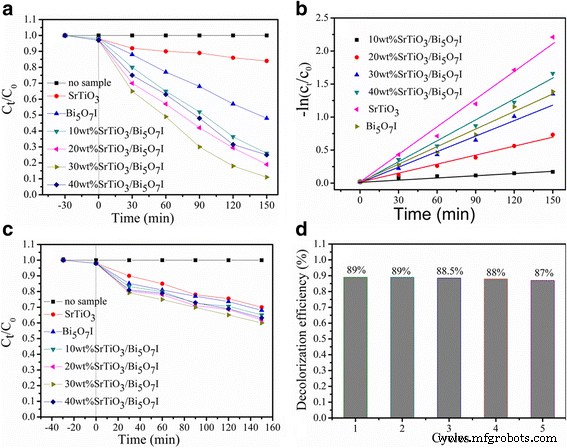
un Dégradation photocatalytique de la solution de RhB pour tous les échantillons sous irradiation solaire simulée. b Parcelles de -ln(Ct /C0 ) en fonction du temps pour tous les échantillons. c Dégradation photocatalytique de la solution de RhB pour tous les échantillons sous éclairage UV. d Efficacité de dégradation cyclique de RhB sur le SrTiO3 /Bi5 O7 Je nanocomposites
Pour mieux comprendre la cinétique de réaction de la dégradation photocatalytique RhB pour différents photocatalyseurs, l'efficacité de la dégradation photocatalytique a été calculée à l'aide de l'équation suivante :ln(C 0 /C t ) = K application t , où C 0 , C t , et K application sont représentatifs de la concentration initiale, de la concentration au temps t et de la constante de vitesse apparente de pseudo-premier ordre, respectivement [43]. Le -ln(Ct /C0 ) présente une relation bien linéaire avec le temps d'irradiation et la réaction photocatalytique appartient à la réaction de pseudo-premier ordre comme le montre la figure 6b. Le k application valeurs obtenues pour Bi5 O7 Moi, SrTiO3 , 10 % en poids de SrTiO3 /Bi5 O7 I, 20 % en poids de SrTiO3 /Bi5 O7 I, 30 % en poids de SrTiO3 /Bi5 O7 I, et 40 % en poids de SrTiO3 /Bi5 O7 I les nanocomposites sont 1,16 × 10 −3 , 4,88 × 10 −3 , 9 × 10 −3 , 1,06 × 10 −2 , 1,45 × 10 −2 , et 9,24 × 10 −3 min −1 , respectivement. Il est évident que les 30 % en poids de SrTiO3 /Bi5 O7 Le nanocomposite présente la constante de vitesse de réaction photocatalytique maximale, qui est environ 2,97 fois supérieure à celle du Bi5 nu O7 I, et 12,5 fois supérieur à celui du SrTiO3 pur .
Les courbes de dégradation RhB sur tous les échantillons sous irradiation de lumière UV sont illustrées plus en détail sur la figure 6c. On peut clairement voir que le phénomène est similaire à celui de la Fig. 6a. Cependant, tous les échantillons présentent une efficacité photocatalytique très faible en raison de la faible absorption de la lumière UV, et la sensibilisation aux colorants a un effet sur l'activité photocatalytique. Comme le montre la figure 6a, les 30 % en poids de SrTiO3 /Bi5 O7 I nanocomposite affiche toujours la meilleure activité; cependant, la photodégradation de RhB n'est que de 40 % en 150 min. Ces résultats démontrent que le SrTiO3 /Bi5 O7 Les nanocomposites possèdent une activité photocatalytique plus efficace sous irradiation solaire simulée.
La stabilité et la réutilisation du SrTiO3 à 30 % en poids /Bi5 O7 I nanocomposite a été réalisé en répétant les tests de dégradation de RhB. Après chaque cycle, le SrTiO3 /Bi5 O7 Les nanocomposites ont été réutilisés dans le cycle suivant avant d'être collectés par centrifugation, lavés plusieurs fois avec de l'eau déminéralisée et de l'alcool éthylique, et enfin séchés à 80 °C pendant 3 h. Comme le montre la Fig. 6d, l'activité photocatalytique du composite ne diminue pas évidemment même après le cinquième recyclage sous irradiation solaire simulée, ce qui suggère une bonne stabilité pour recycler les 30 % en poids de SrTiO3 /Bi5 O7 Je nanocomposite.
Discussion sur le mécanisme photocatalytique
Afin de mieux comprendre les espèces actives impliquées dans la photodégradation de SrTiO3 /Bi5 O7 Dans les nanocomposites, nous avons réalisé des expériences de piégeage d'espèces réactives sur les 30 % en poids de SrTiO3 /Bi5 O7 Je nanocomposite pour déterminer les principales espèces actives dans la réaction photocatalytique. Comme le montre la Fig. 7, l'ajout d'isopropanol (IPA) n'a pratiquement aucun effet sur la dégradation de RhB par rapport au SrTiO3 /Bi5 O7 I nanocomposites, ce qui indique qu'aucun radical •OH n'est généré. Au contraire, une diminution significative de la dégradation du colorant est observée après l'ajout de benzoquinone (BQ) ou de sel disodique d'acide éthylènediaminetétraacétique (EDTA-2Na), ce qui implique que \( \bullet {\mathrm{O}}_2^{- } \) et les trous sont les principales substances réactives pour la photodégradation RhB.
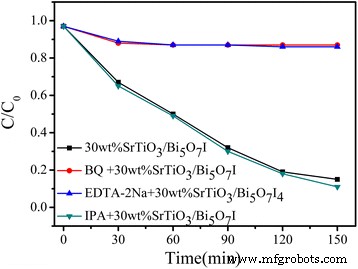
La constante d'efficacité de dégradation de RhB sur les 30 % en poids de SrTiO3 /Bi5 O7 Je nanocomposite en présence de divers charognards
Afin d'étudier la séparation de charge des photocatalyseurs tels que préparés, la spectroscopie PL a été en outre introduite. La figure 8 montre la comparaison des spectres PL entre Bi5 O7 I et 30 % en poids de SrTiO3 /Bi5 O7 Je nanocomposite sous excitation à 320 nm. Les spectres PL des deux échantillons sont caractérisés par un pic à 497 nm, qui est attribué à l'émission d'énergie de transition de bande interdite de Bi5 O7 I. Cependant, il y a une forte diminution de l'intensité de 30 % en poids de SrTiO3 /Bi5 O7 Je nanocomposite. Ce phénomène démontre une séparation efficace des porteurs photogénérés au sein du composite entre SrTiO3 et Bi5 O7 Je.
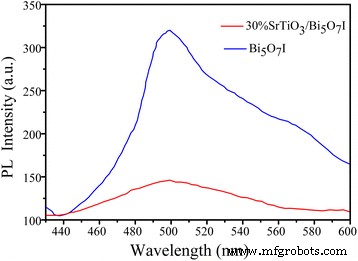
Spectres PL de Bi5 pur O7 I nanofeuilles et 30 % en poids de SrTiO3 /Bi5 O7 Je nanocomposite
Mieux comprendre le mécanisme de l'activité photocatalytique renforcée du SrTiO3 /Bi5 O7 I nanocomposites sous irradiation solaire simulée, les positions CB et VB correspondantes pour SrTiO3 et Bi5 O7 Je suis théoriquement calculé selon \( {E}_{VB}=\chi -{E}_0+\frac{1}{2}{E}_g \) et E CB = E VB − E g , où E VB est le potentiel VB, E CB est le potentiel CB, E 0 est l'énergie des électrons libres sur l'échelle de l'hydrogène (environ 4,5 eV), E g est l'énergie de la bande interdite, et χ est calculé comme la moyenne géométrique des électronégativités de Mulliken des composants dans le semi-conducteur [44]. Par conséquent, le E VB et E CB de Bi5 O7 J'ai été calculé à 2,92 et 0,56 eV, alors que les énergies de SrTiO3 étaient d'environ 2,03 et − 1,15 eV, respectivement. Ces deux semi-conducteurs ont des potentiels de bande appropriés et peuvent donc construire une structure composite.
D'après les résultats ci-dessus, une illustration schématique des bandes d'énergie correspondant entre SrTiO3 et Bi5 O7 I et les modes possibles de transfert de charges sont illustrés à la Fig. 9. Les deux SrTiO3 et Bi5 O7 Je suis excité sous la lumière solaire simulée (lumière UV), et les électrons dans le VB des deux SrTiO3 et Bi5 O7 Je serais ravi de la CB, les trous sont restés dans sa VB. Comme le potentiel CB de SrTiO3 (− 1.15 eV) est plus négative que celle de Bi5 O7 I (+ 0,56 eV), les électrons de SrTiO3 sont facilement injectés dans le CB de Bi5 O7 I. Les électrons photogénérés pourraient réagir avec O2 pour produire des espèces actives d'oxygène radical superoxyde (\( \bullet {\mathrm{O}}_2^{-} \)), qui induit alors la dégradation de RhB [45]. Par contre, les trous dans le VB de Bi5 O7 Je migre vers le VB de SrTiO3 , entraînant une séparation efficace des électrons et des trous photoinduits. De cette façon, les électrons et les trous photogénérés sont séparés efficacement dans le SrTiO3 /Bi5 O7 Je nanocomposites. Le VB de SrTiO3 est de 2,23 eV, inférieur au potentiel redox de •OH/H2 O (+ 2,27 eV). Selon les rapports pertinents [46, 47], le VB de SrTiO3 est insuffisant pour oxyder H2 O dans •OH. Il indique que \( \bullet {\mathrm{O}}_2^{-} \) et les trous sont les principales espèces actives d'oxygène pour SrTiO3 /Bi5 O7 I nanocomposites dans la décoloration RhB, sous irradiation solaire simulée. Par conséquent, le SrTiO3 synthétisé /Bi5 O7 Le photocatalyseur nanocomposite présente une performance photocatalytique bien supérieure à celle du SrTiO3 et Bi5 O7 Je.
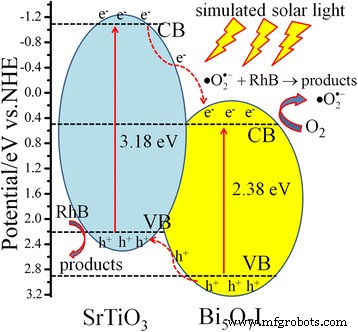
Le diagramme schématique des bandes d'énergie et le processus photocatalytique possible de SrTiO3 /Bi5 O7 Je nanocomposites
Conclusions
En résumé, le roman SrTiO3 /Bi5 O7 Les photocatalyseurs nanocomposites ont été conçus et fabriqués par une approche solvothermique couplée à une décomposition thermique. Les mesures XRD, XPS et EDS montrent que les produits sont bien SrTiO3 /Bi5 O7 Je nanocomposites. L'analyse UV-vis DRS montre que le SrTiO3 /Bi5 O7 I nanocomposites have a good performance of light absorption. The results of PL spectra show that the recombination of photoinduced electron-hole pairs is obviously inhibited in SrTiO3 /Bi5 O7 I nanocomposites. The obtained nanocomposites show a good stability and a recycling capacity in the photocatalytic process. The as-synthesized SrTiO3 /Bi5 O7 I photocatalysts exhibit a highly efficient photocatalytic property for the degradation of RhB under simulated solar light irradiation, which is superior to that of SrTiO3 and Bi5 O7 I. The outstanding photocatalytic activity of the photocatalysts is ascribed to the efficient separation and migration of photogenerated charge carriers. The \( \bullet {\mathrm{O}}_2^{-} \) and holes are the main oxygen-active species causing the dye degradation. This work could provide insights into the design and development of other excellent photocatalytic materials for environmental and energy applications.
Abréviations
- BQ:
-
Benzoquinone
- CB:
-
Conduction band
- DRS:
-
Diffuse reflectance spectra
- EDS:
-
Energy-disperse X-ray spectroscopy
- EDTA-2Na:
-
Ethylenediaminetetraacetic acid disodium salt
- FE-SEM:
-
Field-emission scanning electron microscope
- FTIR :
-
Fourier-transform infrared spectroscopy
- IPA:
-
Isopropanol
- PL:
-
Photoluminescence
- RhB:
-
Rhodamine B
- UV-vis:
-
Ultraviolet-visible
- VB:
-
Valence band
- XPS:
-
X-ray photoelectron spectroscopy
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- Performances photocatalytiques induites par la lumière visible des nanocomposites ZnO/g-C3N4 dopés N
- Préparation et performances photocatalytiques des photocatalyseurs à structure creuse LiNb3O8
- Un nouveau photocatalyseur à hétérojonction Bi4Ti3O12/Ag3PO4 avec des performances photocatalytiques améliorées
- Fabrication de couches minces SrGe2 sur des substrats Ge (100), (110) et (111)
- Synthèse en un seul pot de nanoplaques Cu2ZnSnSe4 et leur activité photocatalytique induite par la lumière visible
- La fabrication et les performances d'absorption des ondes électromagnétiques à haute efficacité des nanocomposites structurés CoFe/C Core-Shell
- Fabrication et caractérisation de nano-clips de ZnO par le procédé à médiation par polyol
- Fabrication de nanofibres hélicoïdales CA/TPU et son analyse de mécanisme
- Modulation de la morphologie et des propriétés optiques des nanostructures multimétalliques PdAuAg et alliages PdAg



