Génération d'espèces réactives de l'oxygène dans des solutions aqueuses contenant des nanoparticules GdVO4:Eu3+ et leurs complexes avec le bleu de méthylène
Résumé
Dans cette lettre, nous rapportons l'étude de la génération de radicaux libres et d'espèces réactives de l'oxygène (ROS) dans des solutions aqueuses contenant de l'orthovanadate de gadolinium GdVO4 :Eu 3+ nanoparticules (VNP) et leurs complexes avec le photosensibilisateur bleu de méthylène (MB). L'activité catalytique a été étudiée sous irradiation UV-Vis et rayons X par trois méthodes (test aux diènes conjugués, radical OH· et détection d'oxygène singulet). Il a été montré que les complexes VNPs-MB révèlent une haute efficacité de génération de ROS sous irradiation UV-Vis associée à la fois à une haute efficacité de génération de radicaux OH· par les VNP et à la génération d'oxygène singulet par MB en raison du transfert d'énergie d'excitation non radiative des VNP aux molécules MB . Contrairement à celui sous irradiation aux rayons X, le fort OH . le piégeage des radicaux par les VNP a été observé.
Contexte
La radiothérapie (RT) reste une composante importante du traitement du cancer avec environ 50 % de tous les patients cancéreux recevant une radiothérapie au cours de leur maladie [1,2,3]. Le mécanisme exact de la mort cellulaire due aux radiations est toujours un domaine d'investigation active. Les cassures double brin de l'ADN nucléaire sont considérées comme l'effet cellulaire le plus important des radiations conduisant à une perte irréversible de l'intégrité reproductive de la cellule et à la mort éventuelle de la cellule [4]. De tels dommages causés par les rayonnements peuvent être causés par (i) une ionisation directe et (ii) une ionisation indirecte via des radicaux libres et des espèces réactives de l'oxygène (ROS), des espèces chimiquement réactives contenant de l'oxygène, formées à partir de la radiolyse des molécules d'eau et d'oxygène cellulaires [2,3, 4]. En thérapie clinique, les dommages sont généralement ionisants indirects. Dans le processus, l'eau perd un électron et devient très réactive. Ensuite, grâce à une réaction en chaîne en trois étapes, l'eau est séquentiellement convertie en un certain nombre de radicaux et de produits moléculaires :électrons hydratés (\( {e}_{aq}^{-}\Big) \), atome d'hydrogène( H ∙ ), radical hydroxyle OH·, radical hydroperoxyle (\( {HO}_2^{.}\Big) \), peroxyde d'hydrogène (H2 O2 ), et les molécules d'hydrogène (H2 ) [5, 6]. Les électrons hydratés et les atomes d'hydrogène sont de puissants agents réducteurs. En revanche, les radicaux hydroxyles sont des espèces oxydantes très fortes et suppriment immédiatement les électrons de toute molécule sur son chemin, transformant cette molécule en un radical libre et propageant ainsi une réaction en chaîne [5]. Lorsque l'oxygène moléculaire dissous est présenté dans l'eau irradiée, sa réduction produit un radical superoxyde (\( {O}_2^{.-} \)) et est le précurseur de la plupart des autres ROS, y compris l'oxygène singulet ( 1 O2 ) [7].
Récemment, il a été montré que des nanoparticules (NPs) à haut numéro atomique (à base d'Au, Ag, Hf, Gd, Ti) [8,9,10,11], des NPs semi-conducteurs (métal-oxyde TiO2 ZnO, CuO, CeO2 , Al2 O3; points quantiques ZnS, ZnS, LaF3 , etc.) [8, 12, 13, 14], et certaines NP inorganiques (nanotubes de carbone) [15, 16] améliorent l'efficacité de la RT. Les principes théoriques de l'interaction rayons X-NP sont bien décrits [8, 12, 14]. Une interaction en cascade de photons de haute énergie avec le réseau de la NP se produit principalement par l'effet photoélectrique et l'effet de diffusion Compton. Les électrons Compton, Photo ou Auger peuvent induire l'émission d'électrons secondaires, qui peuvent s'échapper dans l'environnement et seront capturés par un accepteur (c. radicaux biomoléculaires et production de ROS [8, 12, 14]. Les effets radiosensibilisants des NP sont associés aux radicaux biomoléculaires et à la génération de ROS en tant qu'étape finale de l'interaction des rayons X avec les NP. Dans les NP semi-conductrices, telles que les NP à oxyde métallique, l'effet cytotoxique associé à la génération de ROS peut également être induit par l'irradiation UV [17,18,19,20]. Le mécanisme est que lorsque les NP sont irradiées avec la lumière UV (énergie supérieure à la bande interdite), la séparation de charge est induite en générant un trou (h + ) dans la bande de cantonnière et un électron (e − ) dans la bande conductrice. Les électrons et les trous présentent respectivement une capacité élevée de réduction et d'oxydation [18]. Les électrons peuvent réagir avec l'oxygène moléculaire pour produire un radical superoxyde (\( {O}_2^{\cdotp -} \)) par un processus réducteur, tandis que les trous peuvent extraire des électrons de l'eau et/ou des ions hydroxyle générant des radicaux hydroxyle (OH ·) par un processus oxydant [18,19,20]. Pour TiO2 , PDG2 , Al2 O3 , et des nanoparticules de ZnO, les 1 O2 génération via l'oxydation de \( {O}_2^{\cdotp -} \) a été rapportée [18, 21, 22].
Une autre approche pour améliorer l'efficacité de la thérapie anticancéreuse (thérapie photodynamique, PDT) à l'aide de NP scintillantes a été proposée par Chen et Zhang [23]. Cette approche combine des NP excitées par des rayons X (scintillantes) et des molécules photosensibilisantes (PS). Les NP scintillantes servent de transducteur d'énergie transférant l'énergie récoltée à partir de l'irradiation aux rayons X vers le PS qui génère de l'oxygène singulet pour la destruction de la tumeur. Cette approche permet un traitement profond du cancer et améliore à la fois la PDT et la RT. Jusqu'à présent, une variété de nanoparticules de scintillation et leurs complexes avec le PS ont été étudiées en tant qu'agents photodynamiques inductibles aux rayons X [12, 14, 23,24,25,26,27,28].
Récemment, nous avons rapporté la création de complexes à base de NPs scintillantes d'orthovanadate de gadolinium dopées aux ions europium GdVO4 :Eu 3+ photosensibilisateur (VNPs) et bleu de méthylène (MB) et étude du transfert d'énergie d'excitation électronique dans les complexes [29]. Il a été montré qu'en raison de la conversion efficace de l'énergie d'excitation dans les complexes, ils pourraient être considérés comme un agent photodynamique inductible aux rayons X. Le but de cet article était d'étudier l'efficacité de la génération de ROS dans des solutions aqueuses contenant des VNP et leurs complexes avec MB sous irradiation UV et rayons X.
Expérimental
Produits chimiques
Chlorure de gadolinium GdCl3 ·6H2 O (99,9%), chlorure d'europium EuCl3 ·6H2 O (99,9 %), EDTA disodique·2Na (99,8 %) et métavanadate de sodium anhydre NaVO3 (96 %) ont été obtenus auprès d'Acros Organic (USA) et tous utilisés sans autre purification. L'hydroxyde de sodium NaOH (99 %) a été acheté auprès de Macrohim (Ukraine). Orthovanadate de sodium Na3 VO 4 solution a été obtenue en ajoutant une solution 1 M de NaOH dans une solution aqueuse NaVO3 à pH = 13. L-a-phosphatidylcholine (PC) à partir de jaune d'œuf, colorant cationique 3,7-bis(diméthylamino)phénazathionium chlorure (bleu de méthylène (MB), Mw = 373.90 g/mol), 1,2-Benzopyrone (Coumarine, Mw =146,14 g/mol) ont été achetés auprès de Sigma-Aldrich (États-Unis) et utilisés tels que reçus. Sel disodique de l'acide antracène-9,10-dipropionique (ADPA, Mw = 366.32 g/mol) a été obtenu à partir de la collection de colorants du Dr Igor Borovoy (Institute for Scintillation Materials, NAS of Ukraine) avec la pureté contrôlée par chromatographie sur couche mince. Tous les autres produits chimiques étaient de qualité analytique.
Synthèse de GdVO4 :Eu 3+ solutions colloïdales
Solutions colloïdales aqueuses de nanoparticules d'orthovanadate de gadolinium dopées aux ions europium Gd0.9 Eu0.1 VO 4 (GdVO4 :Eu 3+ ) ont été synthétisés selon la méthode rapportée précédemment [30]. Tout d'abord, 0,4 mL de solution aqueuse de chlorure de gadolinium (1 M) a été mélangé avec 0,05 mL de chlorure d'europium (1 M), puis 49,55 mL d'eau bidistillée ont été ajoutés au mélange. Ensuite, la solution obtenue a été mélangée avec 37,5 mL de solution d'EDTA disodique (0,01 M). Ensuite, 37,5 mL de Na3 VO 4 (0,01 M) a été coulé goutte à goutte (рН = 10,5). Le mélange a été intensément agité à l'aide d'un agitateur magnétique et chauffé au bain-marie sous un condenseur à reflux pendant 24 h à 100 °C. La solution transparente incolore obtenue diffuse la lumière sous l'éclairage latéral (le cône de Tyndall). Ensuite, la solution a été refroidie et dialysée contre de l'eau pendant 24 h pour éliminer l'excès d'ions. A cet effet, la solution obtenue a été ronronnée dans un sac de dialyse (Cellu Sep T2, membrane avec un poids moléculaire de coupure de 12 KDa, taille des pores ~ 2,5 nm) et placée dans un verre de 2 L avec de l'eau distillée. Après chaque 6 h, l'eau était rafraîchie.
Instrumentation et caractérisation
Les VNP synthétisés ont été caractérisés par microscopie électronique à transmission (microscope électronique TEM-125 K, Selmi, Ukraine) et méthode de diffusion dynamique de la lumière (analyseur ZetaPALS, Brookhaven Instruments Corp., États-Unis). Les spectres d'absorption ont été mesurés à l'aide d'un spectromètre Specord 200 (Analytik Jena, USA). Les spectres de fluorescence et d'excitation de fluorescence ont été pris avec un spectrofluorimètre Lumina (Thermo Scientific, USA).
Préparation des complexes VNPs-MB
Des solutions pour les enquêtes ont été préparées comme suit. Tout d'abord, des solutions mères de MB dans l'eau (1 mmol/L) ont été préparées. Pour obtenir des solutions aqueuses de VNP-MB, la quantité requise de solution mère de colorant et de solution aqueuse de VNP a été ajoutée dans un flacon et soigneusement agitée à l'aide d'un évaporateur rotatif (Rotavapor R-3, Buchi) pendant 1 h jusqu'à une évaporation complète du chloroforme. Ensuite, 1 mL d'une solution aqueuse de VNPs a été ajouté dans un flacon et doucement secoué pendant 1 h pour la formation du complexe VNPs-MB. La concentration de MB dans la solution obtenue était de 10 μmol/L. Les concentrations de nanoparticules étaient de 0,1, 1 ou 10 mg/mL.
Détection d'oxygène actif et d'espèces radicalaires
La formation de ROS sous l'irradiation UV/rayons X de solutions aqueuses contenant des VNP, MB ou des complexes VNPs-MB a été détectée par spectroscopie à l'aide de plusieurs méthodes.
Test de formation de diènes conjugués
L'oxydation des lipides sous irradiation UV a été mesurée en utilisant une suspension de liposomes PC. Des vésicules lipidiques PC unilamellaires ont été préparées par la méthode d'extrusion [31]. En bref, une quantité appropriée de PC (25 mg/ml) dans du chloroforme a été placée dans un ballon et séchée jusqu'à évaporation complète du chloroforme en utilisant un évaporateur rotatif (Rotavapor R-3, Buchi). Le film mince de lipides-colorants a ensuite été hydraté avec 10,8 ml d'eau bidistillée. La suspension lipidique obtenue a finalement été extrudée à travers un filtre en polycarbonate de taille de pores de 100 nm en utilisant une mini-extrudeuse (Avanti Polar Lipids, Inc., USA). La concentration de PC était de 1,2 mmol/L. Pour le test de formation de diènes conjugués, 1 ml de suspension de liposomes PC a été mélangé avec 1 ml de solution aqueuse de VNP (solution aqueuse de MB ou solution aqueuse de VNPs-MB). La concentration finale de MB était de 10 μmol/L et les VNP, 1 g/L. La concentration de PC dans les solutions était de 0,6 mmol/L. Les solutions aqueuses obtenues ont été placées dans des cuvettes en quartz (10 × 10 mm) et irradiées avec une lampe au mercure de 250 W (bande passante l = 310-400 nm, le flux lumineux était de 43 W/cm 2 ) pendant 30 minutes. Ensuite, l'absorbance des suspensions a été enregistrée à 234 nm (diènes conjugués maximum) à l'aide d'un spectrophotomètre Specord 200 (Analytik Jena, Allemagne). La concentration de diènes conjugués formés dans l'eau sans aucun additif (complexes NPs, MB ou VNPs-MB) a été prise comme contrôle. Chaque point expérimental était la valeur moyenne d'au moins trois tests indépendants. Le traitement statistique a été réalisé à l'aide du progiciel Statistika v. 5.0 (StatSoft, USA).
OH· détection de radicaux
Pour détecter la formation de radicaux hydroxyles dans la solution sous irradiation UV, la coumarine a été utilisée comme molécule sonde. La coumarine réagit avec les radicaux OH· produisant une 7-hydroxycoumarine hautement fluorescente [32, 33]. La procédure expérimentale était la suivante. Une solution aqueuse de coumarine (0,1 mmol/L) a été mélangée avec des solutions aqueuses de MB (10 μmol/L), de VNP (0,1, 1 ou 10 g/L) ou de VNP-MB. Les solutions aqueuses obtenues ont été placées dans des cuvettes en quartz (10 × 10 mm) et irradiées avec un laser He-Cd λ sauf = 325 nm pendant 1 h. En cas d'irradiation aux rayons X, la cuvette a été irradiée par le dessus (depuis la partie ouverte) par un rayon X en utilisant un appareil ISOVOLT 160 Titan E avec une cathode en tungstène pendant 30 min. La tension sur le tube était de 30 kV (20 mA). La distance entre le tube à rayons X et les échantillons irradiés était de 25 cm. Les spectres de fluorescence (excités à 325 nm) des solutions ont été enregistrés avec un spectrofluorimètre Lumina (Thermo Scientific, USA). L'intensité relative de la fluorescence de la 7-hydroxycoumarine a été analysée.
Détection d'oxygène singulet
1 O2 la production dans les solutions contenant des VNP, MB ou des complexes VNPs-MB a été analysée sur l'évaluation des spectres de fluorescence ADPA [34, 35]. Les mesures ont été réalisées dans des cuvettes en quartz (10 x 10 mm). Une solution aqueuse d'ADPA (10 μmol/L) a été mélangée avec des solutions aqueuses de MB (10 μmol/L), de NP (1 g/L) ou de VNP-MB dans des cuvettes. Les solutions ont été irradiées à 457 nm à l'aide d'un laser bleu solide à haute stabilité MBL-457, 50 mW (Changchun New Industries Optoelectronics Tech. Co., Ltd.). L'émission de fluorescence de l'ADPA excitée à 378 nm a été collectée à différentes échelles de temps (0, 10, 20, 30, 40 et 60 min) à l'aide d'un spectrofluorimètre Lumina (Thermo Scientific, États-Unis).
Résultats et discussions
Caractéristique des VNP synthétisés
Figure 1a et fichier 1 supplémentaire :la figure S1 montre les images TEM de VNP synthétisés avec un histogramme de distribution latérale et un modèle XRD, qui prennent en charge le GdVO4 :Eu 3+ Structure cristalline des NP. GdVO synthétisé4 :Eu 3+ Les NP sont de forme fusiforme avec une taille de 8 × 25 nm ± 5 nm et une structure de phase tétragonale de type zircon. La charge négative de la surface des NPs (le potentiel ζ est de - 18,75 ± 0,15 mV, pH = 7,8) est due aux groupements carboxylates du stabilisant EDTA disodique utilisé lors de la synthèse. Le diamètre hydrodynamique excédentaire de GdVO4 :Eu 3+ nanoparticules est de 44,0 ± 0,3 nm. Le spectre d'absorption de GdVO4 :Eu 3+ NPs représente la large bande intense dans la gamme spectrale 250-350 nm qui correspond à un transfert de charge des ligands oxygène à l'atome de vanadium dans le groupe \( {VO}_4^{3-} \) (Fig. 1b) [36 ]. Dopage GdVO4 NP avec Eu 3+ ions confère une forte fluorescence aux VNP dans la gamme spectrale rouge, qui est régie par la transition au sein de la configuration électron f des ions europium [37] (ne sera pas discuté dans cet article).
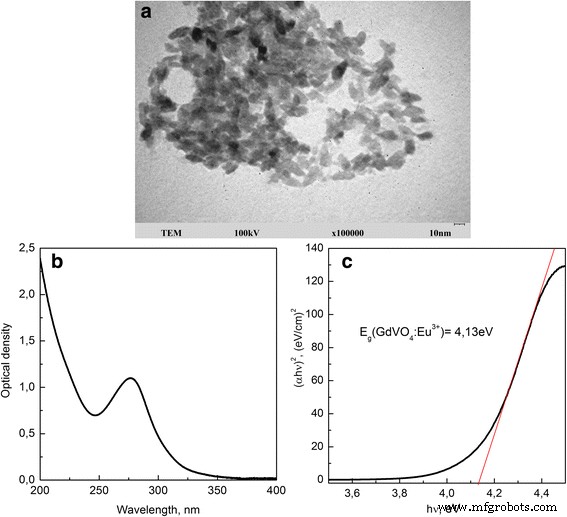
Image TEM (a ), spectre d'absorption (b ), et la dépendance énergétique de (αhv ) 2 (c ) de GdVO4 :Eu 3+ nanoparticules
Il est connu que la taille des NP affecte le gap d'énergie optique dans les matériaux semi-conducteurs. L'énergie de la bande interdite, E g , peut être estimée à partir de la longueur d'onde du bord d'absorption de la transition inter-bande selon la relation de Tauc [38] :
$$ {\left(a\mathrm{hv}\right)}^{\left(1/n\right)}=A\cdot \left(\mathrm{hv}-{E}_g\right), $ $ (1)où a est le coefficient d'absorption, hv est l'énergie du photon incident, A est la constante indépendante de l'énergie (le paramètre de queue de bande), et n est la constante (facteur de puissance du mode de transition), qui dépend de la nature du matériau (cristallin ou amorphe). La valeur de n désigne la nature de la transition, n = 1/2 pour les transitions directes autorisées, n = 3/2 pour les transitions interdites directes, n = 2 pour les transitions indirectes autorisées, et n = 3 pour la transition interdite indirecte [39]. GdVO4 est un semi-conducteur à gap direct, pour lequel n = 1/2 [40] Ainsi, l'Éq. (1) peut être réécrit comme :
$$ {\left(\alpha \mathrm{hv}\right)}^2=A\cdot \left(\mathrm{hv}-{E}_g\right) $$ (2)Coefficient d'absorption (a ) est calculé à partir de l'absorbance en tant que a = 2,303D /l , où D est l'absorbance et l est la longueur du chemin optique.
La figure 1c représente la dépendance énergétique de (a hv) 2 pour GdVO synthétisé4 :Eu 3+ nanoparticules. La valeur de bande interdite E g a été déterminé par extrapolation de la partie linéaire du (a hv) 2 courbe en fonction de l'énergie du photon hv à zéro. La valeur obtenue E g = 4.13 eV est supérieur à celui rapporté pour GdVO4 :Eu 3+ poudres avec une taille de cristallite allant de 14,4 à 43 nm (3,56 à 3,72 eV) [41, 42]. Nous supposons que cela pourrait être dû à la différence entre les méthodes de synthèse utilisées qui, dans notre cas, donnent des NP plus petites avec une bande d'absorption étroite et décalée vers le bleu par rapport à celle obtenue par les méthodes hydrothermales ou de Pechini.
Génération de radicaux libres photo-induits (test des diènes conjugués)
Il est communément admis que les types d'arbres de ROS (\( \mathrm{OH}\cdotp, {\mathrm{O}}_2^{\cdotp -} \), et 1 O2 ) générant dans les systèmes NPs sous irradiation UV contribuent au stress oxydatif majeur dans les systèmes biologiques [43, 44]. Bien que l'activité photocatalytique de ces NP d'oxyde métallique comme TiO2 , ZnO, CuO, CeO2 , Al2 O3 , et Fe2 O3 est bien décrit [17,18,19,20], peu de recherches ont étudié l'activité photocatalytique de ReVO4 NP [45,46,47,48]. Il a été démontré que ReVO4 Les NP sont efficaces dans la destruction photocatalytique des polluants organiques. Cependant, aucune recherche n'a étudié les types de ROS générés par ReVO4 NPs sous irradiation UV.
Pour imiter l'environnement biologique, nous avons utilisé une suspension de liposomes PC et détecté la génération de radicaux libres sous irradiation UV dans les suspensions contenant des complexes MB, VNPs ou VNPs-MB sur l'oxydation des lipides (test de formation de diènes conjugués) [49,50,51]. L'oxydation des lipides par l'oxygène moléculaire via des réactions radicalaires en chaîne peut être initiée par des rayonnements ionisants lorsque des ROS et des radicaux libres apparaissent dans le système [43, 44]. Les réactions en chaîne radicalaires impliquant des acides gras polyinsaturés provoquent un réarrangement des doubles liaisons conduisant à des diènes conjugués. Les diènes conjugués résultants présentent une bande d'absorption à 234 nm qui pourrait être détectée par photométrie. La figure 2 montre les concentrations relatives de diènes conjugués formés dans des suspensions lipidiques contenant des complexes MB, VNP ou VNP-MB. On peut voir que dans toutes les solutions, la concentration de diènes conjugués augmente par rapport à la suspension de liposomes PC purs. Cependant, l'efficacité de ce processus diffère. Le bleu de méthylène est l'une des molécules photosensibilisantes conventionnelles avec les principaux maxima d'absorption λ max = 665 nm et une bande d'absorption moins intense dans la gamme spectrale UV (Fichier supplémentaire 1 :Figure S2). Sous irradiation UV du MB, les deux principaux processus photochimiques peuvent avoir lieu [34, 52]. MB excité par la lumière UV subit un processus de croisement intersystème (Q p =0,54 [53]) à l'état triplet de longue durée ( 3 Mo * ) et réagit avec les molécules d'oxygène ( 3 O2 ) formant de l'oxygène singulet ( 1 O2 ):
$$ {\mathrm{MB}}^{+}+ hv\to {}^3{\mathrm{MB}}^{+^{\ast }} $$ (3) $$ {}^3{\ mathrm{MB}}^{+^{\ast }}+{}^3{\mathrm{O}}_2\to {\mathrm{MB}}^{+}+{}^1{\mathrm{O }}_2 $$ (4)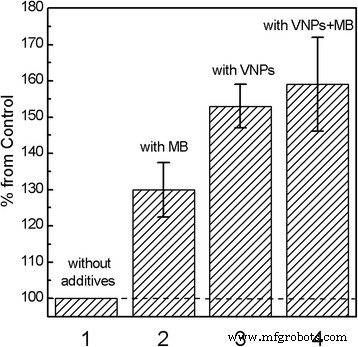
Efficacité relative de formation de diènes conjugués dans les suspensions lipidiques :1 - sans additifs; 2 - avec Mo ; 3 - avec des VNP ; 4 - avec des complexes VNPs-MB
Le deuxième processus photochimique peut avoir lieu à des concentrations élevées de MB. Les molécules MB à l'état fondamental peuvent fonctionner comme agents réducteurs en donnant un électron au triplet MB et en formant respectivement le radical semi-réduit (MB·) et le radical semi-réduit (MB · 2+ ) [52] :
$$ {}^3{\mathrm{MB}}^{+^{\ast }}+{\mathrm{MB}}^{+}\to \mathrm{MB}\cdotp +{\mathrm{MB} }^{\cdotp 2+} $$ (5)L'oxydation du MB· par l'oxygène moléculaire renvoyant le colorant à l'état fondamental et conduisant à la production de radicaux superoxydes (\( {O}_2^{\cdotp -} \)) :
$$ \mathrm{MB}\cdotp +^3{\mathrm{O}}_2\kern0.5em \to {\mathrm{MB}}^{+}+{O}_2^{\cdotp -} $$ (6)Les radicaux oxygène singulet et superoxyde, ainsi que les radicaux MB formés dans les réactions (4) à (6) peuvent affecter le processus d'oxydation des lipides. Dans une solution diluée où aucune formation de dimère MB n'est observée ([MB] < 20 μM), les réactions (3) et (4) domineront [52]. Cependant, dans les complexes VNPs-MB en raison de l'augmentation de la concentration de MB à la surface des VNP [29], le deuxième processus photochimique peut avoir lieu. Ainsi, l'augmentation de la formation de diène conjugué dans la suspension lipidique contenant MB peut être expliquée par l'action MB comme 1 O2 photogénérateur sous irradiation UV. Il convient de noter que l'efficacité de ce processus est beaucoup plus faible que celle sous excitation MB dans un maximum d'absorption de grande longueur d'onde.
Dans la suspension contenant GdVO4 :Eu 3+ nanoparticules, l'oxydation des lipides est plus efficace. Cet effet pourrait être attribué au comportement photocatalytique des VNP sous irradiation UV. Bande conductrice d'électrons (e − ) et les trous de la bande de valence (h + ) formé sous irradiation UV (E> E g ) peut interagir avec l'oxygène moléculaire et les molécules d'eau adsorbées à la surface des NP en suivant les réactions [18, 20, 47] :
$$ {}^3{\mathrm{O}}_2+{e}^{-}\à \kern0.5em {\mathrm{O}}_2^{.-} $$ (7) $$ {\mathrm {H}}_2\mathrm{O}+{\mathrm{h}}^{+}\à \mathrm{OH}\cdot $$ (8)Les ions hydroxyle formés lors de la photolyse de l'eau et adsorbés sur la surface des NP peuvent également interagir avec les trous pour produire des radicaux hydroxyles :
$$ {\mathrm{OH}}^{-}+{\mathrm{h}}^{+}\à \mathrm{OH}\cdot $$ (9)De plus, l'oxydation de \( {O}_2^{\cdotp -} \) produit de l'oxygène singulet [18, 21, 22] :
$$ {\mathrm{O}}_2^{\cdotp -}+{\mathrm{h}}^{+}{\to}^1{\mathrm{O}}_2 $$ (10)Sa réaction avec les ions hydrogène conduit à la formation de peroxyde d'hydrogène :
$$ 2{\mathrm{O}}_2^{\cdotp -}+2{\mathrm{H}}^{+}\à {\mathrm{H}}_2{\mathrm{O}}_2 $$ (11)en raison de son interaction avec les électrons, des radicaux hydroxyles et des ions hydroxyles peuvent se former :
$$ {\mathrm{H}}_2{\mathrm{O}}_2+{\mathrm{e}}^{-}\to \mathrm{OH}\cdot +{\mathrm{O}\mathrm{H} }^{-} $$ (12)Ainsi, l'augmentation de l'efficacité de la concentration de diènes conjugués dans une suspension contenant des VNP (Fig. 2, colonne 3) peut être attribuée aux produits générant via les réactions (7)-(12) et facilitant l'oxydation des lipides.
Dans la suspension lipidique contenant les complexes VNPs-MB, les concentrations de diènes conjugués les plus élevées peuvent s'expliquer par les produits générés à la fois par les réactions (3)-(6) et la réaction (7)-(12) (Fig. 2, colonne 4). De plus, dans les complexes VNPs-MB dans les réactions (3) et (4), la génération d'oxygène singulet pourrait avoir lieu à la fois en raison de l'excitation directe de MB et via un transfert d'énergie d'excitation non radiative des VNP à MB qui est plutôt efficace dans cette composition [29].
Détection des radicaux hydroxyles
L'étape suivante consistait à examiner plus précisément l'efficacité de OH· et 1 O2 génération dans les solutions sous irradiation UV/rayons X. La coumarine a été utilisée comme molécule sonde pour valider l'apparition de radicaux hydroxyles dans les solutions considérées. Il est connu que les radicaux OH· sont l'un des principaux produits de la photolyse/radiolyse de l'eau sous irradiation UV/rayons X [5, 6]. En solution aqueuse, les radicaux OH· interagissent avec les molécules de coumarine pour former un produit hautement fluorescent 7-hydroxycoumarine (voir schéma sur la Fig. 3) qui pourrait être détecté spectroscopiquement par l'apparition d'une nouvelle bande (λ max ~ 460 nm) décalée vers la région spectrale des grandes longueurs d'onde par rapport à la bande de fluorescence de la coumarine (λ max ~ 400 nm), Fig. 3 [32, 33]. Plus la concentration en radicaux OH· dans la solution est élevée, plus l'oxydation de la coumarine est efficace et, par conséquent, plus la bande des grandes longueurs d'onde est intense. Ainsi, l'analyse de l'intensité relative de la bande des grandes longueurs d'onde pourrait fournir des informations sur la concentration de radicaux OH· dans la solution sous l'effet de divers facteurs.
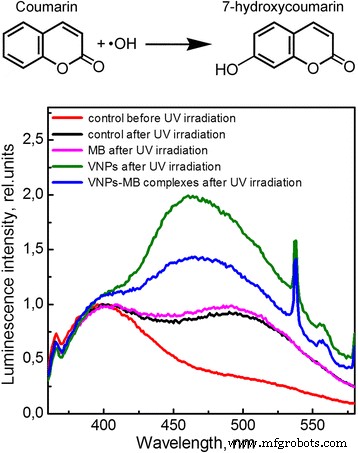
Réaction de la coumarine avec le radical hydroxyle pour former la 7-hydroxycoumarine fluorescente. Spectres de fluorescence normalisés de la solution aqueuse de coumarine, λ sauf = 325 nm
Les spectres d'émission de fluorescence de la solution d'eau de coumarine contenant MB, VNPs ou VNPs-MB complexes mesurés après 1 h d'éclairage UV sont présentés sur la Fig. 3. Il est montré que l'irradiation UV de la solution d'eau de coumarine sans aucun additif (contrôle) provoque une formation d'une nouvelle bande de fluorescence à grande longueur d'onde qui indique la génération de radicaux OH· et l'oxydation de la coumarine (Fig. 3). En présence de molécules MB dans la solution, l'intensité relative de cette bande ne change pas, ce qui n'indique aucun effet supplémentaire de MB sur la génération de radicaux OH· (Fig. 3). Dans la solution contenant des VNP, l'intensité de la bande 7-hydroxycoumarine augmente remarquablement (Fig. 3) en raison de l'activité photocatalytique des VNP sous irradiation UV, Réactions (8), (9) et (12). Notons que les pics aigus autour de 535-540 nm appartiennent à la fluorescence de l'ion europium dans GdVO4 :Eu 3+ nanoparticules (transitions intraconfigurations). Dans la solution contenant des complexes VNPs-MB, l'intensité relative de la bande 7-hydroxycoumarine était environ deux fois plus petite que celle de la solution contenant des VNP, ce qui indique une production moins efficace de radicaux OH· (Fig. 3). Cela peut s'expliquer par le fait que l'adsorption du colorant MB à la surface des VNP peut empêcher l'adsorption des molécules d'eau et des ions hydroxyles et, par conséquent, réduit l'activité photocatalytique des VNP concernant la génération de radicaux OH· via les réactions (8) et (9). De plus, dans les complexes VNPs-MB, une partie de l'énergie adsorbée est transférée de manière non radiative aux molécules MB [29], ce qui diminue également l'efficacité de la production de paires électron-trou et, par conséquent, la capacité des VNP à générer des radicaux OH· dans de tels complexes.
Des résultats inattendus ont été observés sous irradiation aux rayons X des solutions contenant des VNP (Fig. 4). Contrairement au cas de l'irradiation UV, nous observons que l'intensité relative de la bande 7-hydroxycoumarine diminue par rapport à la solution aqueuse de coumarine sans nanoparticules, ce qui indique le piégeage des radicaux OH· formés dans les solutions à la suite de la radiolyse de l'eau. L'effet observé dépend fortement des concentrations de VNP (Fig. 4). Il convient de noter que la discussion principale concernant la capacité des nanoparticules à servir de piégeur de ROS se concentre principalement sur CeO2 nanocristaux (nanocères) [54,55,56,57]. Les principales caractéristiques qui obligent la nanoceria à agir comme piégeur de ROS sont généralement attribuées à une teneur élevée en lacunes d'oxygène et en Ce 3+ ions dans la nanocérie et sa commutation entre les états d'oxydation 3+ et 4+. Cependant, la dépendance critique de l'activité biologique de la nanocérie vis-à-vis de sa taille et de son mécanisme d'auto-régénération est toujours en discussion [54,55,56,57]. On note également que les effets protecteurs du GdVO4 :Eu 3+ et PDG2 Des NP contre les dommages induits par les rayons X ont été observées dans des expériences antérieures in vivo de notre groupe [57]. À notre connaissance, la capacité de GdVO4 :Eu 3+ nanoparticule pour balayer les radicaux OH· générés dans la solution aqueuse sous irradiation aux rayons X a été observée pour la première fois et nécessite des recherches plus approfondies.
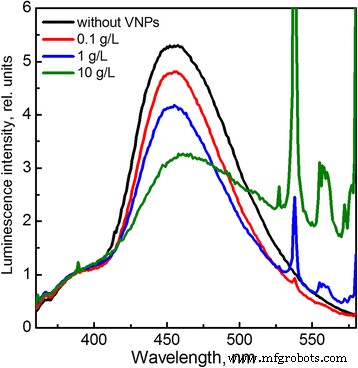
Spectres de fluorescence normalisés d'une solution aqueuse de coumarine contenant différentes concentrations de VNP enregistrés après 30 min d'irradiation aux rayons X
Génération d'oxygène singulet
Évaluer l'efficacité des complexes VNPs-MB de 1 O2 génération dans l'eau, nous utilisons la méthode basée sur l'oxydation ADPA par l'oxygène singulet avec formation d'endoperoxyde non fluorescent ADPAO2 (Fig. 5). Ainsi, en présence d'oxygène singulet, la fluorescence ADPA est désactivée de manière irréversible. Notons que sous irradiation UV, les molécules d'ADPA subissent un photoblanchiment important qui complique l'identification des impacts des complexes MB, VNPs ou VNPs-MB associés au 1 O2 génération. Pour pallier cet inconvénient, nous appliquons une irradiation laser à 457 nm, qui correspond à l'un des pics d'excitation de Eu 3+ ions dopés en GdVO4 nanocristaux (Fichier supplémentaire 1 :Figure S3). La figure 5 montre que les molécules d'ADPA ne subissent aucune réaction photochimique à l'irradiation de 457 nm de lumière. Dans la solution contenant MB, une légère diminution de l'intensité de l'ADPA dans le temps a pu être observée (Fig. 5) qui est associée à une légère excitation de MB à cette longueur d'onde et à une action comme photosensibilisateur selon la réaction (3) et (4). Le même effet est observé pour la solution contenant des VNP (Fig. 5) et pourrait être attribué à la formation de radicaux \( {O}_2^{\cdotp -} \) à la surface des VNP (Réaction (7)) suivie par son oxydation selon la réaction (10) avec génération d'oxygène singulet. L'extinction de fluorescence ADPA plus forte est observée dans les complexes VNPs-MB. L'efficacité de ce procédé est deux fois plus élevée que dans la solution avec MB ou VNPs. L'efficacité plus élevée de la génération d'oxygène singulet dans la solution contenant des complexes VNP-MB est associée au transfert d'énergie des VNP vers le MB dans les complexes, dans lesquels les VNP servent de transducteur d'énergie pour le photosensibilisateur MB.
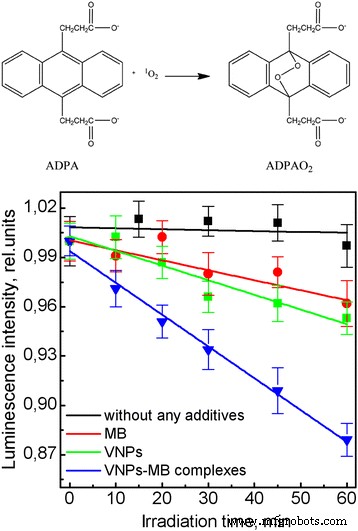
Reaction of ADPA with singlet oxygen to form endoperoxide ADPAO2 . ADPA photobleaching after irradiation with λ = 457 nm in water solutions
Unfortunately, due to ADPA sensor instability, we were not successful to measure the efficiency of the 1 O2 generation in water solution under X-ray excitation.
Conclusions
The efficiency of ROS generation in water solutions containing GdVO4 :Eu 3+ nanoparticles and their complexes with MB have been analyzed under UV-Vis and X-ray irradiation by three methods (conjugated dienes test, OH· radical, and singlet oxygen detection). Complexes VNPs–MB reveal high efficiency of ROS generation under UV-Vis irradiation associated with both high efficiency of OH· radicals generation by VNPs and 1 O2 generation by MB due to nonradiative excitation energy transfer from VNPs to MB molecules. For the first time, the strong OH· radicals scavenging by VNPs has been observed under X-ray irradiation. Our observation indicates that VNPs–MB complexes can be potentially used to activate photodynamic therapy.
Abréviations
- MB:
-
Methylene blue
- PS :
-
Photosensitizer
- ROS :
-
Espèces réactives de l'oxygène
- VNPs:
-
Gadolinium orthovanadate GdVO4 :Eu 3+ nanoparticules
Nanomatériaux
- Problèmes juridiques liés au cloud computing et à leurs solutions
- Maintenance réactive expliquée :défis et solutions courants
- Nanoparticules d'or multifonctionnelles pour des applications diagnostiques et thérapeutiques améliorées :une revue
- Préparation de nanoparticules mPEG-ICA chargées en ICA et leur application dans le traitement des dommages cellulaires H9c2 induits par le LPS
- Adaptation de la toxicité des espèces réactives à l'oxygène à la thérapie tumorale avancée
- États électroniques de nanocristaux dopés à l'oxygène et émission visible sur silicium noir préparés par ns-Laser
- Synthèse facile de composite CuSCN coloré et conducteur revêtu de nanoparticules CuS
- La préparation de la nanostructure jaune-enveloppe Au@TiO2 et ses applications pour la dégradation et la détection du bleu de méthylène
- Promotion de la croissance cellulaire SH-SY5Y par des nanoparticules d'or modifiées avec de la 6-mercaptopurine et un peptide pénétrant dans les neurones



