Nanopétales d'oxyde de nickel mésoporeux (NiO) pour la détection ultrasensible du glucose
Résumé
Les propriétés de détection du glucose de nanostructures mésoporeuses et denses d'oxyde de nickel (NiO) sous forme de nanopétales (NP) cultivées de manière hydrothermale sur le substrat de verre recouvert de FTO ont été démontrées. Les investigations basées sur l'étude structurelle des NiO-NPs ont été réalisées par diffraction des rayons X (XRD), microscopies à force électronique et atomique, rayons X à dispersion d'énergie (EDX) et photospectroscopie à rayons X (XPS). Les mesures de Brunauer-Emmett-Teller (BET), utilisées pour l'analyse de surface, suggèrent la pertinence de NiO pour les applications de détection de glucose basées sur l'activité de surface. Le capteur de glucose, qui a immobilisé le glucose sur l'électrode NiO-NPs@FTO, montre la détection d'une large gamme de concentrations de glucose avec une bonne linéarité et une sensibilité élevée de 3,9 μA/μM/cm 2 au potentiel de fonctionnement de 0,5 V. Une limite de détection aussi basse que 1 μΜ et un temps de réponse rapide inférieur à 1 s ont été observés. L'électrode du capteur de glucose possède une bonne capacité anti-interférence, stabilité, répétabilité et reproductibilité et montre un comportement inerte envers l'acide ascorbique (AA), l'acide urique (UA) et l'acide dopamine (DA), ce qui en fait un parfait capteur de glucose non enzymatique.
Contexte
Le diabète, une maladie chronique dans laquelle le taux de glucose dans le sang augmente et s'il n'est ni diagnostiqué ni traité, peut être très dangereux pour la santé et éventuellement entraîner la mort [1, 2]. Différents régimes thérapeutiques dans la gestion du diabète incluent l'ajustement de la dose des médicaments en fonction du taux de glucose dans le sang en raison d'un taux d'insuline compromis, principale cause de la maladie. Par conséquent, un capteur de glucose précis et fiable pour détecter le niveau dans le sang est le paramètre le plus important dans la gestion du diabète. Généralement, le capteur de glucose fonctionne sur l'utilisation d'une enzyme, la glucose oxydase (GOx), qui convertit le glucose en acide gluconique et H2 O2 [3,4,5,6,7]. La concentration de glucose est déterminée en surveillant le nombre d'électrons circulant à travers l'électrode pour la formation d'hydrogène sous forme de peroxyde [8]. Dans les biocapteurs enzymatiques, la détection quantitative se fait en contrôlant le potentiel et en mesurant le courant en raison de la substance (à détecter) réagissant avec la zone active du matériau (agissant comme capteur) sur l'électrode de travail. Les capteurs de glucose enzymatiques, fonctionnant sur le même principe, présentent une grande sensibilité au glucose. Les limites de ces capteurs incluent leur durée de vie plus courte, les conditions environnementales telles que la température, la valeur du pH et la toxicité du produit chimique utilisé. Pour résoudre ces problèmes, de nombreux capteurs de glucose non enzymatiques à base d'oxyde métallique ont été développés récemment [9,10,11,12,13,14]. Le mécanisme de détection de ces capteurs de glucose non enzymatiques est basé sur l'oxydation du glucose, par l'ion oxyde métallique près de la surface de l'électrode, en gluconolactone. En détection électrochimique, la voltamétrie cyclique (CV) s'avère être une technique efficace en raison de sa haute sensibilité à de faibles limites de détection, une analyse quantitative précise et une caractérisation rapide et claire [15, 16]. Ces capteurs de glucose à base d'oxyde ont certainement le potentiel d'être utilisés dans un diagnostic réel et nécessitent une étude plus approfondie.
Il existe un intérêt croissant pour la fabrication d'électrodes avec des matériaux d'oxyde métallique à faible coût, tels que NiO, CuO, TiO2 , ZnO et composites qui peuvent montrer une sensibilité élevée au glucose en améliorant l'activité électrocatalytique [17,18,19,20,21,22,23,24]. En ce qui concerne la détection basée sur la réaction, les nanomatériaux pourraient être intéressants car ils peuvent fournir une plus grande surface de réaction et donc une meilleure détection. Ces derniers temps, une variété de matériaux sous forme nanostructurée ont montré un grand potentiel dans la détection, l'électronique et l'optoélectronique [25,26,27]. Un fait établi à propos des nanostructures est la capacité d'adapter une propriété physique en modifiant sa taille et/ou sa morphologie, ce qui donne la polyvalence aux nanomatériaux à utiliser dans diverses applications. Par conséquent, pour les capteurs, la conception de la surface des électrodes est également l'un des paramètres clés. Parmi beaucoup, les nanomatériaux à base de Ni présentent des propriétés remarquables, telles que la catalyse [28,29,30] et une sensibilité élevée due à un rapport surface/volume élevé. Un capteur de glucose économique mais sensible peut être une réalité avec des capteurs à base de nanostructure NiO en concevant de manière appropriée le dispositif et en synthétisant le matériau. Dans cet article, une électrode de travail constituée de nanostructures de NiO en forme de pétale pour la détection du glucose via une étude électrochimique a été fabriquée pour être utilisée comme composé actif. Un substrat de verre conducteur revêtu d'oxyde d'étain dopé au fluor (FTO) a été utilisé pour faire croître les nanostructures de NiO (NS) par technique hydrothermale.
Expérimental
Un précurseur de nitrate de nickel mélangé avec du persulfate de potassium en présence d'une moindre quantité de solution d'ammonium a été utilisé pour l'alignement lors de la préparation de ces NiO NS. Après 5 h de chauffage continu à 150 °C, le film déposé a été rincé avec de l'eau déminéralisée et séché à l'air. Par la suite, le film NiO-NSs a été recuit à 250 °C pendant 2 h. Des NiO NS uniformes et bien alignés ont été obtenus sur la surface conductrice du verre recouvert de FTO. La microstructure du film a été étudiée par un XRD (diffractomètre à rayons X Rigaku SmartLab utilisant un rayonnement Cu-Kα monochromatique λ = 1,54 Å) ainsi que la microscopie électronique (Supra55 Zeiss). La spectroscopie à rayons X à dispersion d'énergie (Oxford Instrument) et le spectromètre de photoélectrons à rayons X (ESCA System, SPECS GmbH, Allemagne) avec un rayonnement Al Kα (1486,6 eV) ont été utilisés pour la confirmation élémentaire. La microscopie à force atomique a été réalisée sur une machine Bruker (MultiMode 8-HR) et l'analyse des nanostructures à haute résolution a été réalisée à l'aide du logiciel WSxM [31]. Pour la détection du glucose avec NiO-NS, des mesures électrochimiques appropriées ont été effectuées à l'aide de la station de travail électrochimique Keithley 2450-EC. La méthode Brunauer-Emmett-Teller (BET) a également été utilisée sur Autosorb iQ, version 1.11 (Quantachrome Instruments) pour l'analyse de surface.
Résultats et discussion
Les détails microstructuraux et la morphologie des NiO NS ont été étudiés en utilisant la microscopie électronique et la microscopie à force atomique (AFM). La figure 1a montre des structures très denses ressemblant à des pétales de rose cultivées sur le substrat de verre conducteur recouvert de FTO. L'épaisseur de ces pétales est d'environ 25 à 30 nm, recouverts d'épines très fines comme des structures sur le dessus. Le film est dense et homogène sur plus de cent microns. L'uniformité sur de plus grandes surfaces le rend éligible pour les applications de détection. Une vue en coupe transversale des NiO NS peut être vue dans l'encart de la Fig. 1a qui montre l'alignement vertical et la hauteur des pétales. Une micrographie MET de ces NiO NS peut être vue dans le fichier supplémentaire 1 :Figure S1. La figure 1b montre l'image SEM de nanopétales NiO montrant que des NP NiO uniformes sont cultivées sur une large zone. Plus de détails sur la forme et la taille de ces nanopétales ont été étudiés à l'aide d'images AFM sur la figure 1c–e. La figure 1c, d montre respectivement des images AFM bidimensionnelles et tridimensionnelles. Il montre des pétales à peu près uniformément répartis avec des nanopétales très denses (NP) alignés verticalement. Les images AFM de la figure 1e et l'encart de la figure 1c montrent des NS NiO à une résolution plus élevée. La ligne noire sur la figure 1e montre le profil de la ligne de la nanostructure, qui donne des informations sur l'épaisseur moyenne des NP. Il est évident que les nanopétales ont des largeurs comprises entre ~ 25-30 nm. Le spectre des rayons X à dispersion d'énergie (EDX) de la figure 1f montre la composition chimique des NiO NPs suggérant des NiO NSs de haute pureté avec un rapport Ni/O adéquat. Certains pics correspondant à l'étain élémentaire (Sn) peuvent également être observés sur le verre revêtu de FTO utilisé comme substrat. La figure 1, démontre clairement que des NS NiO denses en forme de pétale ont été fabriqués uniformément, avec une certaine porosité, sur un substrat de verre revêtu de FTO.

un , b Morphologies de surface des nanostructures NiO montrant une structure en forme de pétale avec sa vue en coupe (en médaillon). c –e Images AFM avec profilage de ligne. f Spectres EDX pour la conformation élémentaire
La spectroscopie photoélectronique aux rayons X (XPS) est réalisée pour l'analyse des constituants et des compositions chimiques de surface des nanopétales de NiO. Le scan de l'enquête XPS (Fig. 2a) décrit la composition du nickel et de l'oxygène avec le pic du substrat d'étain (Sn), ce qui est cohérent avec les résultats de l'EDX. Deux pics caractéristiques Ni 2p sont observés à environ 855,7 eV (2p3/2 ) et 873,4 eV (2p1/2 ) en scan haute résolution (Fig. 2b). Le spectre déconvolué contient sept pics avec deux pics plus forts à 855,7 et 873,4 eV correspondent à Ni 2+ dans les liaisons Ni–O, avec deux pics satellites (faibles) [32]. Le motif XRD sur la figure 2c montre clairement des pics de diffraction, dans l'ordre décroissant des intensités de pic XRD, à 43°, 37°, 63°, 76° et 79°, respectivement. Les positions des pics et leurs intensités relatives sont en bon accord avec la structure cubique à faces centrées (FCC) des NiO-NS révélant une nature cristalline des NPs [33]. La caractérisation morphologique et structurelle mentionnée ci-dessus du substrat préparé prédit la présence de structures de NiO semblables à des pétales de faible dimension et celles-ci seront étudiées pour d'éventuelles propriétés de détection du glucose.
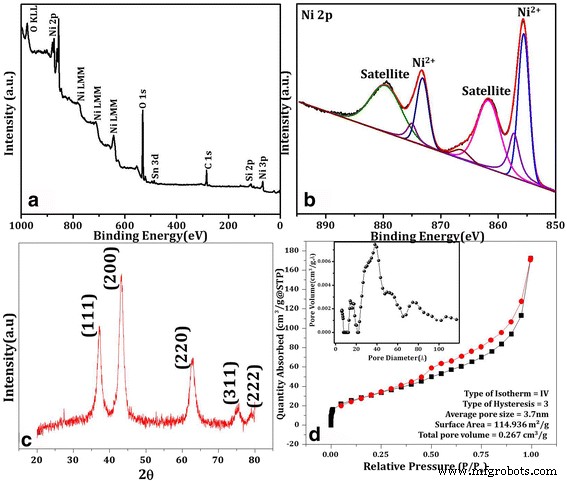
Analyse des constituants des nanopétales NiO fabriqués à l'aide de XPS a analyse de l'enquête, b balayage profond de 2p Ni, c XRD pour l'analyse structurelle, et d surface et étude textuelle utilisant la mesure de l'isotherme BET par N2 adsorption/désorption
Comme mentionné précédemment, la base du mécanisme de détection est la réactivité du glucose avec NiO nécessitant ainsi des surfaces plus élevées, qui doivent être analysées avant d'étudier les propriétés de détection. La surface spécifique et d'autres paramètres, comme le type d'isotherme, la taille moyenne des pores et le volume total des pores ont été obtenus par le N 2 adsorption/désorption en utilisant la méthode BET. La figure 2d révèle l'isotherme de type IV et l'hystérésis de type H3 lorsqu'elles sont mesurées à 77 K avec la plage de pression relative de 0,025 ≤ P /P 0 1,00 [18]. La surface mesurée, estimée par les méthodes BET et Langmuir dans le P /P 0 plage de 0,05 à 0,30, se trouve à 114,936 m 2 /g et distribution de la taille des pores autour de 3,7 nm. Cela indique que les NP NiO sont mésoporeuses avec une distribution de taille de pores relativement uniforme. Le volume total des pores de l'échantillon est de 0,267 cm 3 /g tel qu'estimé à une pression relative (P /P 0 ) de 0.99.
Une surface adéquate semble disponible pour la détection du glucose des NiO-NPs a été étudiée ci-dessous à l'aide de mesures CV électrochimiques, comme le montre la Fig. 3. Pour les mesures CV, un système à trois électrodes a été utilisé avec un échantillon NiO-NPs@FTO comme électrode de travail. , Ag/AgCl (1 M KCl) et fil de platine utilisés comme référence et contre-électrodes, respectivement. La figure 3a montre I –V courbes avec différents taux de balayage de tension variant entre 10 et 100 mV/s. L'électrode est très stable comme testé en répétant les scans CV pendant 3000 cycles (Fichier supplémentaire 1 :Figure S2). Il est évident d'après la figure 3a qu'un courant de ~ 0,25 mA/cm 2 coulait à une vitesse de balayage de 10 mV/s (courbe noire) et augmente jusqu'à ~ 2,5 mA/cm 2 lorsque la vitesse de balayage a été augmentée à 100 mV/s (courbe vert clair). Une augmentation du courant de dix fois en augmentant le taux de balayage de dix fois signifie une variation linéaire entre les deux. Une telle variation linéaire du courant en fonction d'une vitesse de balayage, comme le montre l'encart de la Fig. 3a, est le plus souvent attribuée à une réaction contrôlée par la surface et sera meilleure pour les applications de détection.
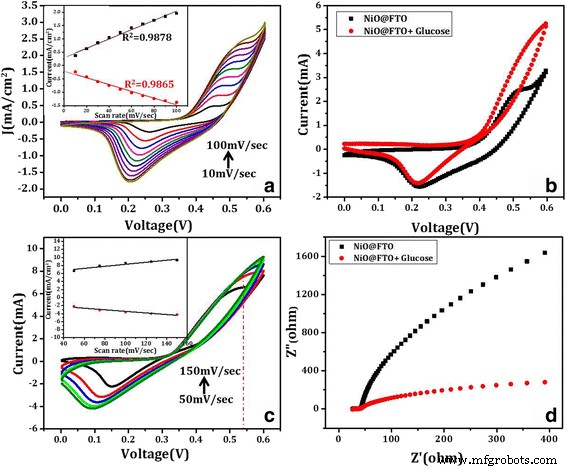
un Voltamétrie cyclique (CV) de NiO-NPs@FTO sur différentes vitesses de balayage. b Détection électrochimique du glucose (10 μM) à l'aide de la technique CV. c Balayage CV de l'électrode NiO-NPs@FTO immobilisée au glucose à différentes vitesses de balayage. b Spectroscopie d'impédance électrochimique (EIS) pour montrer la détection du glucose. Encarts dans a et c montrer une variation linéaire du courant en fonction de la vitesse de balayage
Pour l'étude de détection, des mesures CV ont été effectuées avec un film NiO NSs comme électrode de travail (NiO-NPs@FTO) à une vitesse de balayage de 50 mV/s avec (rouge) et sans (noir) glucose (5 mM), dans le présence d'électrolyte NaOH 0,1 M, comme le montre la figure 3b. Les tracés CV enregistrés à différentes vitesses de balayage en présence de glucose ont également été montrés sur la figure 3c qui montre également des valeurs de courant accrues par rapport au cas sans glucose et augmente encore avec l'augmentation des taux de balayage. Les courbes CV dépendantes de la vitesse de balayage de la figure 3c sont cohérentes avec les discussions ci-dessus concernant la détection du glucose et la réaction contrôlée par la surface. Comme on peut le voir sur les courbes noire et rouge de la Fig. 3b, un courant de crête de réaction est observé, indiquant que l'électrode NiO-NPs@FTO subit la réaction redox dans la plage de potentiel de 0,0 à 0,6 V. La valeur du courant de crête est doublée en présence de glucose, c'est-à-dire que le courant de l'électrode NiO-NPs@FTO avec du glucose est plus important que celui sans glucose, ce qui peut être attribué à l'oxydation de la molécule de glucose immobilisée dans une plus grande surface des NiO NS. Cela semble être le mécanisme le plus probable de détection du glucose, comme cela peut être confirmé par les réactions d'oxydoréduction suivantes qui se déroulent sur des sites appropriés.
$$ \mathrm{NiO}+{\mathrm{H}}_2\mathrm{O}\à \mathrm{NiO}\mathrm{OH} $$ (1) $$ \mathrm{NiO}\mathrm{OH} +\mathrm{glucose}\à \mathrm{NiO}+{\mathrm{H}}_2{\mathrm{O}}_2+\mathrm{gluconolactone} $$ (2) $$ \mathrm{Gluconolactone}\à \ mathrm{gluconique}\ \mathrm{acide} $$ (3) $$ \mathrm{Gluconic}\ \mathrm{acide}+{\mathrm{H}}_2\mathrm{O}\to {\mathrm{gluconate} }^{\hbox{-} }+{\mathrm{H}}^{+} $$ (4)Pendant la mesure CV, Ni 2+ s'oxyde en Ni 3+ par une solution électrolytique aqueuse présente dans la cellule au niveau de l'électrode NiO-NPs@FTO (réaction 1). Ni oxydé 3+ fonctionne comme catalyseur pour le glucose et oxyde le glucose en se réduisant (réaction 2). Lors de l'oxydation, le glucose se transforme en gluconolactone qui se transforme par conséquent immédiatement en acide gluconique (réaction 3) et ce composé réagit avec les molécules d'eau pour former des ions gluconate et hydronium (réaction 4). Ces ions près de la surface de l'électrode de travail entraînent une augmentation du courant en tant que signal détectable avec une très bonne sensibilité spécifique de 3,9 μA/μM/cm 2 .
Afin de soutenir davantage l'amélioration de la conductivité électrique induite par le «dopage au glucose», la spectroscopie d'impédance électrochimique (EIS) de l'électrode de travail fabriquée en NiO NP a été mesurée avec et sans glucose (Fig. 3d). Un seul demi-cercle enfoncé dans la région des hautes fréquences et une ligne inclinée dans la région des basses fréquences sont visibles sur le graphique de Nyquist (cole-cole) de la figure 3d. Généralement, le demi-cercle à haute fréquence montre l'impédance de réaction électrochimique entre le glucose présent dans la solution électrolytique et l'interface de nanostructure NiO, tandis que la ligne inclinée dans la région de basse fréquence montre le matériau actif (NiO) et l'impédance d'interface d'électrode conductrice [34]. L'effet du glucose sur le graphique cole-cole de la figure 3d est clairement distinguable, et ainsi, la même mesure peut être utilisée pour détecter la présence de glucose. Cela montre clairement la propriété de détection du glucose du matériau qui est des NiO NS en forme de nanopétale.
La répétabilité d'un appareil est l'un des paramètres importants pour des performances efficaces en tant que capteur réel. La figure 4a est la cellule électrochimique pour la détection du glucose à l'aide de techniques CV et ampérométriques. La figure 4b correspond à l'analyse CV de NiO-NPs@FTO en présence de diverses concentrations de glucose de 100 M à 1,2 mM. La figure 4c montre la relation linéaire de la concentration de glucose avec la densité de courant ayant un facteur d'ajustement linéaire (R 2 ) de 0.9948. La figure 4d montre le comportement ampérométrique de l'électrode NiO-NPs@FTO lors de l'ajout d'une solution aqueuse de glucose de différentes quantités dans un électrolyte NaOH 0,1 M détecté à + 0,5 V. À ce biais, l'électrode NiO-NPs@FTO présente des changements systématiques dans le courant lorsque 50 μL de solution de glucose de concentration, 1 μM est ajouté dans l'électrolyte. En outre, pour illustrer le comportement exclusif de détection du glucose, l'effet d'autres composés présents avec l'acide urique de type glucose (UA), l'acide ascorbique (AA) et l'acide folique (FA) a été vérifié en effectuant des expériences de contrôle. Les réponses des espèces mentionnées à diverses concentrations ont été étudiées en ajoutant ces enzymes aux 57e et 65e secondes (flèche marquée sur la figure 4d) qui ne montrent aucun changement significatif dans le courant pendant la mesure ampérométrique alors que le glucose a été détecté lorsqu'il est ajouté entre à 60e seconde. La sélectivité de la détection du glucose par rapport à d'autres composés peut être vue plus clairement dans le fichier supplémentaire 1 :Figure S3. Une autre observation importante est la réduction du courant après le pic induit par le glucose, ce qui rend le capteur réutilisable. L'électrode NiO NS présente une très bonne sensibilité par rapport à diverses autres électrodes de capteur, comme le montre le tableau 1 qui résume certaines des électrodes de détection de glucose récentes. Une sensibilité supérieure de l'électrode à base de NiO NS (rangée du bas du tableau 1) en fait un bon candidat pour les applications de détection du glucose sur lesquelles des études supplémentaires peuvent être effectuées sur des échantillons réels comme du sang ou des aliments, le cas échéant.
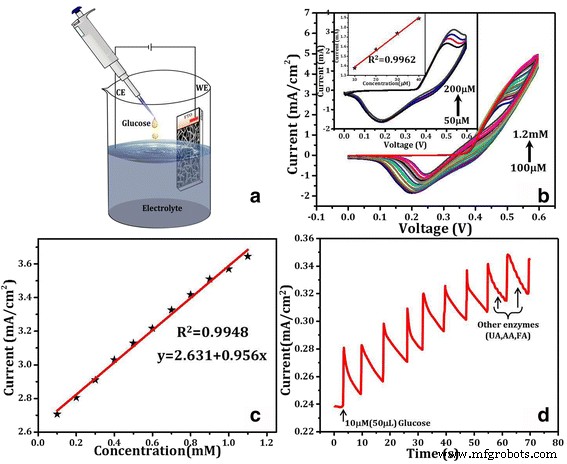
un Illustration schématique de la configuration de détection électrochimique du glucose utilisant NiO-NPs@FTO comme électrode de travail avec l'électrolyte de support NaOH (0,1 M). b Ajout séquentiel de glucose de 50 μM pendant le scan CV avec sa vue grossissante dans l'encart. c Relation linéaire de la concentration de glucose avec le courant d réponse ampérométrique (à + 0,5 V) sur une addition de glucose de 10 μM
Conclusions
En résumé, un excellent comportement de détection du glucose avec une sensibilité améliorée a été obtenu en utilisant une électrode avec des nanostructures de NiO (NSs) alignées très denses et de croissance hydrothermale, avec un rapport surface/volume élevé. Les NiO NS, développés par la technique simple, présentent de meilleures capacités de détection du glucose en termes de stabilité et de sensibilité par rapport à ses homologues développés par d'autres techniques. L'électrode de capteur proposée présente une large plage de détection des concentrations de glucose avec une sensibilité spécifique élevée de 3,9 μA/μM/cm 2 et un temps de réponse rapide inférieur à 1 s. En plus de cela, il montre une réponse inerte aux autres enzymes présentes avec le glucose comme l'acide ascorbique, l'acide folique et l'acide urique, ce qui en fait un capteur de glucose non enzymatique efficace. Tous ces résultats obtenus indiquent que le capteur de glucose proposé peut être un outil analytique efficace pour la surveillance des concentrations de glucose dans les médicaments, le sérum humain, et peut être utilisé dans des applications biomédicales.
Nanomatériaux
- Nanofibres polymères électrofilées décorées de nanoparticules de métaux nobles pour la détection chimique
- Dépôt en couche atomique de nano-films d'oxyde d'indium pour transistors à couche mince
- Détection du glucose électrochimique non enzymatique sensible basée sur du NiO poreux creux
- Manipulation de la température de sulfuration pour synthétiser un film de nanosphères α-NiS pour la conservation à long terme des capteurs de glucose non enzymatiques
- Développement d'un biocomposite électrofilé de chitosan-oxyde de polyéthylène/fibrinogène pour des applications potentielles de cicatrisation
- Microarrays mésoporeux VO2 bidimensionnel pour supercondensateur hautes performances
- Exfoliation à la meule :une véritable exfoliation par cisaillement pour l'oxyde de graphène à quelques couches de grande taille
- Dispositif à base de graphène pour biocapteurs ultrasensibles
- Applications pour l'alliage de nickel 400



