Amélioration de la sélectivité des transducteurs ampérométriques à l'aide de films nanométriques de phénylènediamine
Résumé
Dans ce travail, nous avons étudié les conditions de dépôt d'une membrane semi-perméable à base de polyphénylènediamine (PPD) sur des électrodes de platine à disques ampérométriques. En limitant l'accès des substances interférentes à la surface de l'électrode, la membrane empêche leur impact sur le fonctionnement du capteur. Deux méthodes de dépôt membranaire par électropolymérisation ont été comparées, à potentiel variable (voltamétrie cyclique) et à potentiel constant. La voltamétrie cyclique s'est avérée plus facile à exécuter et à fournir de meilleures propriétés de la membrane. La dépendance de l'efficacité de la membrane PPD sur le nombre de voltamogrammes cycliques et la concentration de phénylènediamine a été analysée. Il a été montré que l'impact des substances interférentes (acide ascorbique, dopamine, cystéine, acide urique) sur le fonctionnement du capteur pouvait être complètement évité en utilisant trois voltamogrammes cycliques dans 30 mM de phénylènediamine. D'autre part, lorsque l'on travaille avec des échantillons dilués, c'est-à-dire à des concentrations plus faibles de substances électroactives, il est raisonnable de diminuer la concentration de phénylènediamine à 5 mM, ce qui entraînerait une sensibilité plus élevée des transducteurs au peroxyde d'hydrogène en raison d'une couche de PPD plus mince. . La membrane PPD a été testée en fonctionnement continu et au stockage de 8 jours et s'est avérée efficace en capteur et biocapteurs.
Contexte
Les biocapteurs sont de nouveaux dispositifs analytiques; dont l'utilisation est une alternative à la chromatographie, la spectroscopie et la colorimétrie. Les biocapteurs sont beaucoup moins chers et plus faciles à utiliser que ces méthodes traditionnelles, cependant, souvent inférieurs à eux par les caractéristiques analytiques. À l'heure actuelle, la recherche dans le domaine de la biosensorité progresse activement [1].
Selon la définition classique de l'Association internationale des chercheurs en chimie fondamentale et appliquée, un biocapteur est un dispositif intégré basé sur un récepteur et un transducteur, capable de fournir une analyse quantitative ou semi-quantitative à l'aide d'un élément de reconnaissance biologique [2]. Par type de transducteur, les biocapteurs sont classés en plusieurs groupes (électrochimiques, optiques, piézoélectriques, etc.), parmi lesquels les biocapteurs électrochimiques sont l'un des plus grands groupes et sont à leur tour divisés en ampérométriques, potentiométriques, conductométriques et impédimétriques [3] .
L'une des caractéristiques analytiques importantes des biocapteurs est leur sélectivité, c'est-à-dire leur capacité à identifier uniquement le composé cible. La sélectivité du biocapteur est déterminée par la sélectivité du matériel biologique et la sélectivité du transducteur. Fondamentalement, les enzymes et les anticorps utilisés dans les biocapteurs électrochimiques en tant que biomatériau sont très sélectifs, alors que les électrodes, qui servent de transducteurs, sont plutôt non sélectives. La sélectivité du biocapteur est particulièrement importante lorsque l'on travaille avec de vrais fluides biologiques ou d'autres échantillons complexes ; par conséquent, son enquête est une étape nécessaire dans le développement de biocapteurs.
Dans le sérum sanguin, l'urine, le liquide céphalo-rachidien, etc., il existe des substances interférentes qui peuvent subir des réactions chimiques à la surface des transducteurs, provoquant ainsi de faux résultats dans la mesure par biocapteur de la substance cible. Les principaux interférents dans les échantillons biologiques sont l'acide ascorbique, la cystéine, l'homocystéine, l'acide urique, la dopamine, le glutathion, etc. Leurs concentrations dans le sérum sanguin humain sont indiquées dans le tableau 1.
Il existe deux approches principales pour empêcher l'oxydation des substances interférentes sur la surface de l'électrode :une diminution du potentiel de travail par l'introduction de substances supplémentaires dans la membrane biosélective ou le dépôt de membranes semi-perméables supplémentaires, ce qui permet un accès sélectif de la substance cible à la surface de l'électrode. 4]. Le dépôt de membranes semi-perméables est méthodologiquement plus simple et affecte légèrement le fonctionnement du biocapteur.
Dans les biocapteurs, le peroxyde d'hydrogène s'oxyde ou se réduit sur l'électrode et ainsi le signal du biocapteur est généré. Par conséquent, un problème réel est le développement de films nanoporeux, qui sont perméables au peroxyde d'hydrogène et empêchent la pénétration d'autres substances. Parmi ces membranes, les films polymères à base de phénylènediamine (PD) retiennent considérablement l'attention [5]. La membrane à base de polyphénylènediamine (PPD) a des nanopores; leur taille est suffisante pour pénétrer les composés de faible poids moléculaire, y compris le peroxyde d'hydrogène, à travers la membrane jusqu'à la surface de l'électrode. D'autre part, la membrane ne permet pas le passage ou l'oxydation de substances plus grosses comme l'acide ascorbique ou la dopamine. Ainsi, la membrane améliore la sélectivité vis-à-vis du peroxyde d'hydrogène, ce qui, à son tour, augmente la précision du biocapteur. Dans plusieurs travaux, différents isomères de PD et méthodes de polymérisation de PD ont été étudiés. En particulier, des membranes PPD ont été formées sur des microélectrodes en fibre de carbone recouvertes de ruthénium par électrodéposition à un potentiel constant (+ 0,7 V) lors de la création de biocapteurs basés sur la glucose oxydase, la lactate oxydase et la glutamate oxydase [6]. Trois isomères de PD ont été testés; les résultats avec le méta-isomère étaient les meilleurs. Puisqu'une certaine sensibilité à l'acide ascorbique subsistait encore, l'ascorbate oxydase a été ajoutée pour l'éliminer complètement. Dans [7], les auteurs ont étudié des membranes PPD déposées sur des cylindres de Pt-Ir par ampérométrie CV ou à potentiel constant. La sensibilité à l'acide ascorbique a notamment diminué avec les membranes à base d'isomères méta et ortho oxydés à potentiel constant alors que la sensibilité au peroxyde d'hydrogène n'a diminué que de 10 %. Les résultats obtenus avec des membranes PPD déposées sur des électrodes à disque de palladium étaient assez différents [8]. Électrodéposition de m -PD par CV a provoqué la formation de films avec une perméabilité au peroxyde d'hydrogène trois fois plus élevée par rapport à m -Oxydation du PD à potentiel constant. Ainsi, m -PD s'est avéré préférable parmi tous les isomères. Le capteur de peroxyde d'hydrogène récemment signalé utilisant des o déposés par CV -Le film PD avec des nanoparticules d'Au [9] a démontré une bonne prévention des effets interférents. Généralement, on peut conclure que m -PD est supérieur aux autres pour toutes les électrodes, alors que la procédure de polymérisation PD doit être optimisée dans chaque cas particulier. De plus, les membranes à base de PD peuvent également être utilisées dans des capteurs sans élément biologique. Comme cela a été récemment montré, la sérumalbumine bovine a pu être détectée par un capteur à base de copolymères conjugués de PD et d'autres composés aromatiques (une extinction de la fluorescence de la protéine après liaison avec le copolymère a été observée) [10].
Ainsi, le but du présent travail était de comparer différentes méthodes de m -déposition de phénylènediamine et sélection d'une procédure optimale de formation de PPD sur les électrodes à disque de platine.
Méthodes
Matériaux
Acide ascorbique, cystéine, acide urique, dopamine, peroxyde d'hydrogène, m -phénylènediamine et HEPES ont été achetés auprès de Sigma-Aldrich Chemie (USA). Tous les autres produits chimiques étaient de p.a. note.
Les échantillons de sérum sanguin humain ont été obtenus auprès du Centre municipal scientifique et pratique de néphrologie et d'hémodialyse de Kiev (Ukraine).
Conception de transducteurs ampérométriques
Dans ce travail, des électrodes à disque de platine fabriquées par nos soins ont servi de transducteurs ampérométriques. Un fil de platine de 0,4 mm de diamètre et de 3 mm de long a été scellé à une extrémité d'un capillaire en verre d'un diamètre extérieur de 3,5 mm. Une extrémité ouverte du fil était la surface de travail du transducteur. Une extrémité intérieure du fil de platine a été soudée par l'alliage de Wood à une extrémité d'un fil d'argent à l'intérieur du capillaire ; son autre extrémité était reliée à un potentiostat. Les électrodes ont été utilisées à plusieurs reprises; avant utilisation, leur surface de travail a été traitée avec HCl pendant 30 s, lavée à l'éthanol et broyée avec du papier abrasif P1500 PS 8A.
Méthodes de mesure
Les spectres d'absorption UV-vis des échantillons ont été mesurés sur le spectromètre Thermo Evolution 600 dans la gamme de longueurs d'onde de 200 à 900 nm en mode de réflexion diffuse à l'aide d'une sphère d'intégration. L'étalon de réflectance diffuse Spectralon et le disque de platine ont été utilisés comme échantillons blancs pour m -poudre de phénylènediamine et couche de PPD sur la surface de l'électrode de Pt respectivement.
Pour les mesures électrochimiques, des électrodes de travail ont été placées dans une cellule électrochimique classique avec des électrodes auxiliaires (fil de platine) et de référence (Ag/AgCl dans KCl saturé) connectées au potentiostat PalmSens (Palm Instruments BV, Pays-Bas). L'utilisation du multiplexeur à huit canaux (du même fabricant), connecté au potentiostat, a permis la surveillance simultanée des signaux de huit électrodes; cependant, dans notre travail, nous avons généralement utilisé trois électrodes en raison de la petite taille de la cellule de travail.
Les mesures chronoampérométriques (technique « détection ampérométrique ») ont été réalisées à température ambiante dans une cellule en verre ouverte de 3 mL sous agitation permanente par un agitateur magnétique et à un potentiel constant de 0,6 V par rapport à l'électrode de référence Ag/AgCl. Dix millimolaires d'HEPES, pH 7,4, ont été utilisées comme tampon de travail dans toutes les expériences. Les concentrations de substrat dans la cellule de travail ont été obtenues par addition d'aliquotes de solutions mères (50 mM de peroxyde d'hydrogène, 20 mM d'acide ascorbique, 3 mM de cystéine, 4,5 mM d'acide urique, 2,1 mM de dopamine). De nouvelles solutions ont été préparées juste avant l'expérience. Toutes les substances électroactives, à l'exception de l'acide urique, ont été dissoutes dans le tampon de travail ; l'acide urique en raison de sa faible solubilité a été dissous dans de l'eau distillée avec 5 mM de NaBrO3 . La phénylènediamine a été dissoute dans un tampon phosphate 40 mM, pH 7,4.
La voltamétrie cyclique a été réalisée dans la même cellule de mesure sans agitation. Le potentiel de démarrage était de 0 V, le potentiel final de +0,9 V, le taux de balayage (taux de changement de potentiel) de 20 mV/s et le pas de changement de potentiel de 5 mV.
Toutes les expériences ont été réalisées en trois répétitions. Les données dans les tableaux et les figures représentent une valeur moyenne des expériences ± écart type, calculée par le programme OriginLab OriginPro 8.5.
Résultats et discussion
Pour confirmer les raisons du dépôt de membrane supplémentaire sur le transducteur ampérométrique pour l'amélioration de sa sélectivité au peroxyde d'hydrogène, il était nécessaire de vérifier la sensibilité et la sélectivité de ce transducteur vis-à-vis d'éventuels interférents.
Les biocapteurs peuvent être utilisés pour les mesures dans les échantillons non dilués et dilués. L'option de dilution dépend de la concentration de substance à analyser et de la sensibilité du biocapteur :si le biocapteur peut identifier la substance cible à des concentrations, des dizaines de fois inférieures à celles réelles dans les échantillons, ces derniers doivent être dilués pour diminuer la contenu en interférents et ainsi améliorer la précision du réseau. De plus, il permet de réduire par des dizaines de fois le volume de substrat requis pour les mesures.
Parfois, la concentration de la substance analysée est trop faible ou la dilution n'est pas souhaitable pour des raisons techniques. Pour une meilleure compréhension de la fonction du transducteur ampérométrique, des matériaux électroactifs de trois concentrations ont été utilisés :(1) pertinent pour le sérum sanguin, (2) 20 fois inférieur à (1), c'est-à-dire dilution 20 fois, et (3) 100- dilution au pli. Les réponses du biocapteur aux substances électroactives de trois concentrations ont été reçues à l'aide du transducteur nu avant le dépôt du film PPD, et la sensibilité du transducteur a été calculée (tableau 2). Comme on le voit, la sensibilité à la dopamine et à l'acide ascorbique était la plus élevée, à la cystéine la plus faible. Cependant, les acides ascorbique et urique peuvent être considérés comme les principaux interférents en raison de leurs concentrations essentiellement plus élevées dans les échantillons biologiques. Les réponses du transducteur à ces substances sont d'un ordre de grandeur supérieur à la réponse à la substance cible, le peroxyde d'hydrogène. Par conséquent, le transducteur nu ne convient pas aux mesures dans des échantillons biologiques en raison de l'impact prononcé des interférents. D'autre part, après dilution 100 fois, les réponses à la cystéine et à la dopamine sont devenues négligeables, et la réponse à tous les interférents au total n'était que d'environ 20 % de la réponse au peroxyde d'hydrogène, ce qui signifie que dans certains cas, le capteur peut être utilisé même sans modifications supplémentaires.
Actuellement, il n'y a que des informations fragmentées concernant les méthodes de dépôt de membrane PPD sur les transducteurs. Par conséquent, à l'étape suivante des travaux, il a été évalué quelle méthode parmi les deux les plus courantes et les plus prometteuses est la plus réalisable.
Dans la première méthode, des membranes PPD ont été déposées sur la surface d'une électrode à disque de platine par électropolymérisation de molécules de monomère phénylènediamine en utilisant un potentiel variable (voltamétrie cyclique). Les transducteurs avec électrodes de référence et auxiliaires ont été placés dans une cellule de travail avec une solution de phénylènediamine, et un certain nombre de voltamogrammes cycliques ont été obtenus [7]. Un exemple de l'expérience est montré sur la figure 1. Au cours du premier voltamogramme cyclique (CVA), une augmentation significative du courant a été observée à un potentiel allant de 0,5 à 0,9 V en raison de l'oxydation de la phénylènediamine. Au cours de la deuxième CVA et des suivantes, le courant a considérablement diminué, indiquant une vitesse d'électropolymérisation plus faible. Cependant, comme l'ont montré les expériences suivantes, la formation de la membrane PPD a duré sur tout le CV.
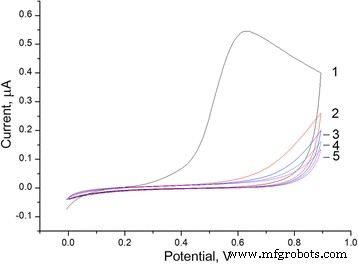
Voltammogrammes cycliques obtenus par électropolymérisation de phénylènediamine sur la surface du transducteur
La deuxième méthode de dépôt sur membrane PPD consiste en l'oxydation de la phénylènediamine à un potentiel constant de + 0,7 V sur un temps fixe (40 min) [11]. La comparaison des réponses des transducteurs lors de l'utilisation des deux méthodes de dépôt est présentée dans le tableau 3. Ci-après, les réponses aux substances électroactives sans la membrane PPD ont été considérées comme 100 %. Les membranes, déposées par les deux méthodes, ont empêché les interférents de manière assez efficace - seule une faible sensibilité à la cystéine a été observée. D'autre part, la sensibilité du transducteur au peroxyde d'hydrogène après voltamétrie a augmenté de 2,6 fois. Ceci peut s'expliquer par l'électro-activation du platine lors de la voltampérométrie, mais pas par l'effet de membrane PPD. Une telle augmentation de la sensibilité au peroxyde d'hydrogène a été observée également après l'obtention de voltamogrammes cycliques dans un tampon phosphate sans phénylènediamine. Après le dépôt membranaire à potentiel constant, aucune électro-activation n'a été révélée et les réponses au peroxyde d'hydrogène n'ont pas changé. Ainsi, l'utilisation de la voltampérométrie cyclique s'est révélée préférable pour trois raisons :moins de temps pour un dépôt (20 contre 40 min), une entrave plus efficace à la cystéine et des réponses croissantes au peroxyde d'hydrogène.
Cependant, la voltamétrie cyclique présente un inconvénient :les voltamogrammes peuvent être obtenus simultanément sur une seule électrode (même en utilisant un multiplexeur), tandis que le dépôt de membrane à potentiel constant permet la connexion simultanée de 8 à 16 électrodes de travail (selon le type de multiplexeur). Par conséquent, d'autres travaux devraient être axés sur l'optimisation des conditions des voltamogrammes cycliques pour réduire le temps de prétraitement du transducteur.
L'électropolymérisation PD par CV et ampérométrie à potentiel constant est supposée se produire par différentes voies à travers un mécanisme assez compliqué [12]. Ainsi, le CV implique un potentiel appliqué élevé, ce qui conduit à la génération d'oligomères moins conjugués de PD. Pour cette raison, il est supposé qu'à la polymérisation PD par CV, les pores sont plus grands et la perméabilité de la couche PPD est plus élevée par rapport à la polymérisation à potentiel constant [8, 13]. Cependant, comme indiqué dans la section « Contexte », différents auteurs sont parvenus à des conclusions contradictoires sur la méthode préférentielle de dépôt de DP et, dans de nombreux cas, le CV a donné de bons résultats. À notre avis, l'ampérométrie CV et l'ampérométrie à potentiel constant peuvent fournir la génération de membranes PPD avec de bonnes propriétés permsélectives, et une optimisation est nécessaire pour chaque cas particulier.
La membrane PPD était clairement visible sur la surface de l'électrode sous la forme d'un film brun doré transparent uniforme. Pour confirmer qu'il s'agit bien de PPD, la polymérisation de PD a en outre été confirmée par spectroscopie. Le spectre de réflectance diffuse UV-vis du film (Fig. 2) montre des bandes d'absorbance intenses à 222 et 315 nm, similaires aux bandes du monomère et liées aux transitions électroniques dans les cycles aromatiques [14], tandis que l'absorbance sans particularité à 400-800 nm, décroissant constamment avec la longueur d'onde se rapporte à π − π * transitions électroniques dans le système aromatique hautement conjugué du polymère conducteur PPD.
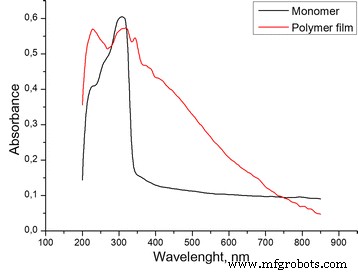
Spectres de réflectance diffuse UV-vis de m -membrane phénylènediamine et PPD, formée sur l'électrode Pt
Pour une meilleure interprétation des résultats obtenus, il serait utile d'estimer la taille des pores dans les membranes PPD produites par différentes méthodes. Cependant, la détermination directe de la taille des pores dans la membrane PPD est presque impossible, car la membrane se compose de plusieurs couches de PD et les pores des couches inférieures peuvent avoir des tailles différentes. Killoran et O'Neill ont déterminé que l'épaisseur de la membrane efficace de m -PD était de 15 nm, et la section transversale d'un brin de polymère oligomère estimée par del Valle et al. était de 1 nm [7, 15]. Ainsi, la membrane PPD contient environ 15 couches de polymère. Étant donné que la membrane PPD a des propriétés hydrophobes et isolantes, la membrane doit avoir des nanopores perforants qui s'étendent jusqu'à la surface de l'électrode et permettent le contournement des molécules de peroxyde d'hydrogène, sinon H2 O2 ne peut pas être oxydé et générer un signal ampérométrique. Les pores ne sont certainement pas uniformes et le diamètre minimal des pores doit être inférieur à 1 nm afin de rejeter les molécules électroactives, et il est donc assez difficile d'analyser les pores même avec des microscopes électroniques ou à force atomique. Pour ces raisons techniques, il est beaucoup plus facile d'estimer l'efficacité de la membrane PPD en évaluant la perméabilité membranaire pour différentes molécules. Une telle approche indirecte est répandue et permet de comparer les caractéristiques pratiques de différentes membranes.
L'efficacité des membranes PPD déposées en utilisant différents nombres de voltamogrammes cycliques a été testée (Fig. 3).
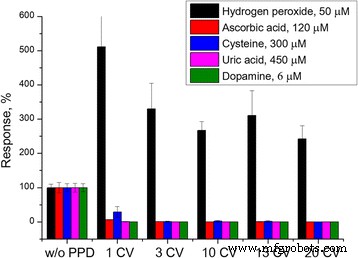
Efficacité des membranes PPD déposées en utilisant différents nombres de CVA
La membrane PPD déposée par un seul CVA était évidemment insuffisante pour éliminer l'influence des interférents. Cependant, ici, l'effet de l'électroactivation du platine était le plus fort. À une augmentation supplémentaire du nombre de voltamogrammes, les réponses aux interférents ont diminué, mais en même temps, la sensibilité du transducteur au peroxyde d'hydrogène a également diminué, probablement à cause d'une couche de PPD trop épaisse, qui entrave la diffusion de la substance. Trois CVA étaient suffisants pour une disparition complète des réponses à la dopamine et à l'acide urique, et une diminution significative des réponses à l'acide ascorbique et à la cystéine. Par conséquent, trois CVA ont été pris pour une valeur optimale, et la concentration de phénylènediamine a été augmentée jusqu'à l'élimination complète de l'impact interférentiel (Fig. 4).
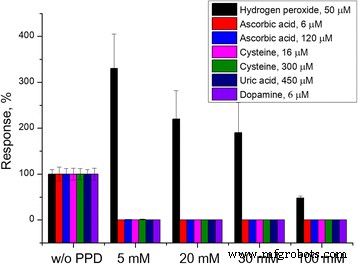
Efficacité des membranes PPD déposées à différentes concentrations de phénylènediamine
Notamment, l'utilisation de 5 mM de phénylènediamine était suffisante pour éliminer les réponses aux interférences de faibles concentrations restantes après dilution de l'échantillon, mais insuffisante pour travailler avec des échantillons non dilués. Une augmentation de la concentration de phénylènediamine à 20 mM et trois CVA se sont avérées suffisantes pour éliminer complètement l'impact de la cystéine et une diminution des réponses à l'acide ascorbique au niveau le plus bas (0,1 % de la réponse à l'acide ascorbique sans membrane PPD). L'utilisation d'une concentration plus élevée (jusqu'à 100 mM) de phénylènediamine a entraîné une double diminution de la sensibilité du transducteur au peroxyde d'hydrogène, probablement en raison d'une couche de PPD trop épaisse. Ainsi, le dépôt de membrane PPD à l'aide de trois CVA dans 30 mM de phénylènediamine est une procédure optimale. Comme un voltamogramme a duré environ 2 minutes, le dépôt de la membrane sur un capteur a pris 6 minutes.
Ensuite, la stabilité de la membrane PPD a été étudiée. Après le dépôt des membranes PPD, les capteurs ont été placés dans le tampon de travail pendant 2 h, et les réponses au peroxyde d'hydrogène, à l'acide ascorbique et à la cystéine ont été mesurées pour évaluer les changements de permsélectivité membranaire (Fig. 5). Il a été constaté que les réponses au peroxyde d'hydrogène augmentaient légèrement pendant le travail, tandis que les petites réponses aux interférents devenaient encore plus petites. Probablement, cela s'est produit parce que l'acide ascorbique et la cystéine ont progressivement obstrué quelques gros pores de la couche de PPD. Cette expérience a démontré que la membrane PPD peut être utilisée sans perte significative de sa sélectivité en peroxyde d'hydrogène pendant au moins 2 h.
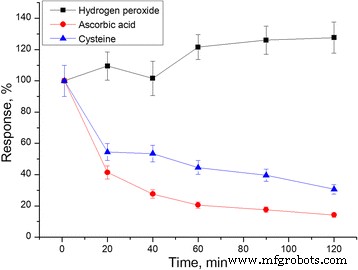
Stabilité de la membrane PPD pendant 2 heures. Les réponses à trois substances ont été normalisées par rapport à la réponse initiale à la substance correspondante après dépôt de PPD
La stabilité au stockage de la membrane PPD a été étudiée. Les capteurs avec membranes PPD déposées ont été stockés au sec pendant 8 jours à - 18 °C ; périodiquement, les capteurs étaient dégelés et les réponses au peroxyde d'hydrogène, à l'acide ascorbique et à la cystéine étaient mesurées (Fig. 6). Au cours de cette période, la sensibilité des capteurs au peroxyde d'hydrogène a été multipliée par 2,5; la sensibilité à l'acide ascorbique et à la cystéine n'a pas changé. Cet effet peut s'expliquer par un gonflement lent de la membrane PPD qui a conduit à une amélioration de la diffusion du peroxyde d'hydrogène à travers la couche de PPD.
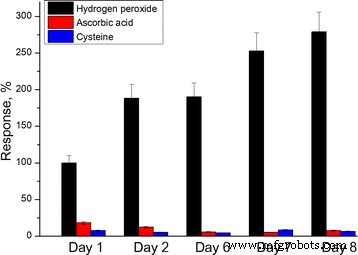
Stabilité au stockage de la membrane PPD. Les réponses ont été normalisées à la réponse à H2 O2 au premier jour
Enfin, l'efficacité de la membrane PPD a été validée lors de l'analyse d'échantillons biologiques réels. Les transducteurs sans membrane ont présenté des signaux faibles après addition de sérum sanguin à la cellule de travail en raison de la présence de composés électroactifs. Cependant, après dépôt de la membrane, aucune réponse n'a été obtenue. Des résultats similaires ont été obtenus avec le lysat de neurones. Ces expériences démontrent que la méthode développée de dépôt de PPD sur des électrodes à disque de platine est efficace et que les transducteurs modifiés peuvent être utilisés pour travailler avec des échantillons biologiques complexes.
Il est utile de comparer la méthode de dépôt de PPD développée dans ce travail avec les méthodes rapportées précédemment (tableau 4).
Comme on le voit, la méthode présentée est la plus rapide et les propriétés de blocage de la membrane obtenue sont meilleures ou du moins pas pires que celles des autres membranes PPD.
Conclusions
Nous avons étudié les conditions de dépôt d'une membrane semi-perméable à base de polyphénylènediamine visant à diminuer l'impact des substances interférentes sur le fonctionnement du biocapteur. Il a été montré que l'électropolymérisation de la phénylènediamine par voltamétrie cyclique était plus facile et offrait de meilleures propriétés de la membrane par rapport à l'électropolymérisation à potentiel constant. La dépendance de l'efficacité de la membrane PPD sur le nombre de voltamogrammes cycliques et la concentration de phénylènediamine a été étudiée. Il a été montré que l'impact des substances interférentes sur le fonctionnement du capteur peut être complètement éliminé en utilisant trois voltamogrammes cycliques dans 30 mM de phénylènediamine. D'un autre côté, lorsque l'on travaille avec des échantillons dilués, c'est-à-dire des concentrations plus faibles de substances électroactives, il est raisonnable de diminuer la concentration de phénylènediamine à 5 mM, ce qui entraînerait une sensibilité plus élevée du transducteur au peroxyde d'hydrogène en raison d'une couche de PPD plus mince. La membrane PPD peut être utilisée sans perte significative de sa sélectivité en peroxyde d'hydrogène pendant au moins 2 h de fonctionnement continu et peut être conservée au moins 8 jours. Il a été démontré que le transducteur avec la membrane PPD n'est pas sensible aux substances électroactives présentes dans les échantillons biologiques et peut être utilisé pour la création de biocapteurs.
Nanomatériaux
- C# en utilisant
- Avancement vers 7 nm
- Utiliser les angles pour améliorer l'avenir de l'électronique
- Béton intelligent utilisant des nanoparticules
- Revue sur l'application des biocapteurs et des nanocapteurs dans les agroécosystèmes
- Fabrication à haut débit de nanofibres de qualité à l'aide d'un électrofilage à surface libre modifiée
- Préparation et propriétés optiques des films GeBi à l'aide de la méthode d'épitaxie par faisceau moléculaire
- Élimination des antibiotiques de l'eau avec une membrane de nanofiltration 3D 100 % carbone
- Conception d'un capteur acoustique à membrane basilaire cochléaire bionique pour la sélectivité en fréquence basé sur un nanogénérateur triboélectrique à film



