Synthèse facile de WS2/Bi2MoO6 hétérostructurés en tant que photocatalyseurs hautes performances basés sur la lumière visible
Résumé
Dans cet article, le roman WS2 /Bi2 MoO6 des photocatalyseurs hétérostructurés ont été fabriqués avec succès via une méthode de croissance solvothermique facile à l'aide de couches pré-exfoliées WS2 nanotranches comme substrat. La structure, la morphologie et les propriétés optiques du WS2 tel que préparé /Bi2 MoO6 les échantillons ont été caractérisés par XRD, XPS, SEM, TEM (HRTEM) et spectres de réflectance diffuse (DRS) UV-vis. Les résultats ont confirmé l'existence d'une excellente interface de nanojonction entre les couches WS2 nanotranches et Bi2 MoO6 nanoflocons. En lumière visible (>420 nm), le WS2 /Bi2 MoO6 les composites présentent une activité photocatalytique significativement améliorée par rapport au Bi2 pur MoO6 vers la décomposition de la rhodamine B (RhB). Pendant ce temps, les expériences de piégeage d'espèces actives ont indiqué que les trous (h + ) étaient les principales espèces actives au cours de la réaction photocatalytique. Les performances photocatalytiques améliorées peuvent être attribuées à la récupération efficace de la lumière, à la séparation rapide des paires électron-trou photogénérées et à l'excellent transport des porteurs de charge du WS2 /Bi2 MoO6 hétérostructures. De plus, le WS2 préparé /Bi2 MoO6 les composites montrent également une bonne stabilité structurelle et d'activité dans les expériences de répétabilité.
Contexte
La photocatalyse est largement considérée comme l'une des techniques d'assainissement de l'environnement les plus prometteuses en raison de la méthode d'utilisation de l'énergie propre [1, 2]. En règle générale, certains ont accepté que les photocatalyseurs à haute efficacité avec un large espace interdit, tels que TiO2 et ZnO, ne peuvent utiliser qu'une irradiation de lumière ultraviolette [3]. Quant à l'application pratique, la stratégie de photocatalyse sera un énorme coup de pouce une fois qu'un photocatalyseur pourra absorber favorablement l'abondante énergie solaire dans la région visible. À cette fin, de nombreuses tentatives pour sonder le photocatalyseur à lumière visible pour une utilisation suffisante de l'énergie solaire en utilisant le semi-conducteur à bande étroite [4,5,6]. Bien que le photocatalyseur monophasé puisse être excité en douceur par la lumière visible, il présente toujours une faible efficacité de conversion d'énergie en raison d'une faible efficacité de séparation des charges résultant de la recombinaison rapide des électrons et des trous photo-induits [7]. Il est largement admis que l'hétérostructure peut améliorer la probabilité de séparation de la charge induite par la lumière car la région interfaciale de contact de l'hétérojonction fournira un champ électrique interne pour restreindre la probabilité de recombinaison, résultant ainsi en une performance photocatalytique efficace. En général, l'hétérostructure conçue adoptera au moins un semi-conducteur à bande étroite pour récolter plus d'énergie lumineuse visuelle, puis pour générer plus de charges photo-induites [8, 9].
En tant que nouveau photocatalyseur, Bi2 MoO6 a attiré l'attention dans le domaine de la photocatalyse à la lumière visuelle car elle possède une structure stratifiée distincte en sandwich [10, 11]. Comme mentionné précédemment, le pur Bi2 MoO6 n'est pas adapté à l'utilisation en tant que photocatalyseur efficace de la lumière visible en raison de la forte probabilité de recombinaison du porteur de charge photogénéré. Par conséquent, certaines stratégies efficaces pour relever ce défi en utilisant l'architecture d'une nanostructure hybride appropriée et en particulier l'introduction de nanofeuilles bidimensionnelles (2D) se sont avérées être une approche efficace pour renforcer le transfert de charge interfaciale entre deux composants dans le processus de réaction photocatalytique. De toute évidence, il est prévu que l'hétérostructure entre Bi2 MoO6 et le matériau en couches 2D augmentera l'efficacité photocatalytique par irradiation à la lumière visuelle [8].
Les dichalcogénures de métaux de transition en couches (TMD) sont largement considérés comme une sorte de matériau de chargement prometteur en raison de leur structure réticulaire de graphène analogue [12, 13]. En particulier, la monocouche et quelques couches de TMD ont une application importante pour la catalyse et le stockage d'énergie en raison de leurs propriétés électroniques distinctes et de leurs surfaces spécifiques élevées [14, 15]. Par exemple, MoS monocouche et à quelques couches2 ont récemment attiré l'attention de la communauté scientifique dans la recherche en photocatalyse, qui attribue le manque de couplage intercouche et l'absence de symétrie d'inversion résultant en des propriétés photoélectriques très différentes de celles de la masse [14, 16, 17]. Du point de vue de la conception des matériaux pour un photocatalyseur hétérojonctionnel sensibilisé à la lumière visible efficace, la principale préoccupation est que les bandes interdites hybrides (1,1 à 1,7 eV) peuvent correspondre étroitement au spectre solaire [18]. En fait, les semi-conducteurs en couches 2D typiques, tels que MoS2 ou g-C3 N4 , ont reçu une attention particulière pour explorer les applications potentielles de la photocatalyse, qui ont conduit à la nanofeuille TMD qui est souvent utilisée comme support pour établir les photocatalyseurs composites hétérostructurés via différentes stratégies hybrides de bandes d'énergie [19, 20]. Par exemple, le MoS hiérarchique2 /Bi2 MoO6 Les composites ont montré une performance efficace pour l'oxydation photocatalytique de la rhodamine B sous irradiation à la lumière visible [21]. Cependant, l'architecture hétérostructurée mono- ou peu-couches de WS2 /Bi2 MoO6 en tant que photocatalyseur à lumière visuelle n'a pas été signalé.
Ici, nous avons démontré une stratégie facile pour fabriquer des WS2 hétérostructurés /Bi2 MoO6 composite via une méthode de croissance solvothermique facile à l'aide de couches WS2 pré-exfoliées nanotranches comme support. Le WS2 /Bi2 MoO6 présente une excellente activité photocatalytique vis-à-vis de la dégradation de la rhodamine B (RhB) sous la lumière visible (λ> 420 nm) irradiation. Selon l'analyse de caractérisation de la microstructure de XRD, XPS, SEM et TEM, le mécanisme photocatalytique possible du WS2 à quelques couches /Bi2 MoO6 composite a également été élucidé. On pense que la formation de jonctions entre Bi2 MoO6 et WS2 peut permettre la migration rapide de la charge photogénérée et réduire l'auto-agglomération. Il est postulé que l'excellente activité photocatalytique de WS2 /Bi2 MoO6 devrait être attribuée à son efficacité de migration élevée des porteurs photo-induits et à l'interaction électronique interfaciale. Ces résultats fournissent également probablement une perspective précieuse pour mieux comprendre la conception d'autres photocatalyseurs hétérostructurés.
Méthodes
Préparation du WS Few-Layer2 Nanotranches
L'exfoliation liquide des couches commerciales WS2 a été réalisé selon la méthode du rapport modifié [22]. En bref, 50 mg de WS commercial2 de la poudre (achetée auprès d'Aladdin Industrial Corporation) a été ajoutée à 20 mL d'éthanol/eau avec des fractions en volume d'EtOH de 40 % ajoutées comme solvant de dispersion. Le flacon scellé a été soniqué pendant 10 h, puis la dispersion a été centrifugée à 3000 tr/min pendant 20 min pour éliminer les agrégats. Enfin, le surnageant a été collecté pour obtenir quelques couches WS2 nanotranches. Pour déterminer les concentrations de nanofeuillets 2D dans le surnageant, nous avons estimé la masse restante dans le surnageant en mesurant le spectre d'absorption UV-vis à une longueur d'onde fixe de 630 nm. Le résultat du calcul en vertu de la loi Lambert-Beer a indiqué que le WS2 exfolié la concentration de dispersion était d'environ 0,265 ± 0,02 mg/ml.
Synthèse du WS hiérarchique2 /Bi2 MoO6 Composites
Le WS2 /Bi2 MoO6 les échantillons ont été synthétisés à l'aide d'une méthode solvothermique facile. Typiquement, 2 mmol de Bi(NO3 )3 ·5H2 O a été ajouté à 10 mL de solution d'éthylène glycol contenant du Na2 dissous MoO4 ·2H2 O avec le rapport molaire Bi/Mo de 2:1 sous agitation magnétique. Une quantité appropriée de WS2 exfolié Les nanotranches ont été dispersées dans 20 mL d'éthanol et passées aux ultrasons à température ambiante pendant 45 min. Ensuite, il a été ajouté lentement dans la solution ci-dessus, suivi d'une agitation pendant 10 minutes pour former une phase homogène. La solution résultante a été transférée dans un autoclave en acier inoxydable revêtu de téflon de 50 ml et maintenue à 160 °C pendant 10 h. Ensuite, l'autoclave a été refroidi progressivement à température ambiante. Enfin, le précipité a été centrifugé et lavé plusieurs fois avec de l'éthanol et de l'eau déminéralisée et séché dans une étuve à vide à 80 °C pendant 6 h. Selon cette méthode, WS2 /Bi2 MoO6 composites avec différents WS2 des rapports de masse (1, 3, 5 et 7 % en poids) ont été synthétisés. A titre de comparaison, le blanc Bi2 MoO6 a été préparé en l'absence de WS2 en utilisant les mêmes conditions expérimentales.
Caractérisation des photocatalyseurs
La structure et la morphologie de l'échantillon ont été étudiées par microscopie électronique à balayage (SEM ; JEOL JSM-6701F, Japon), microscopie électronique à transmission (TEM ; JEOL 2100, Japon), microscopie électronique à transmission haute résolution (HRTEM ; JEOL 2100, Japon), et diffraction des rayons X sur poudre (XRD ; Bruker D8 Advance utilisant une source de rayonnement Cu-Kα, λ = 1,5406 Å, États-Unis). Les spectres de réflectance diffuse (DRS) ultraviolet-visible des échantillons ont été réalisés à température ambiante dans la plage de 200 à 800 nm sur un spectrophotomètre UV-vis (Cary 500 Scan Spectrophotometers, Varian, USA) équipé d'une sphère d'intégration. Les états électroniques des éléments de surface des catalyseurs ont été identifiés par spectroscopie photoélectronique à rayons X (XPS ; Shimadzu Corporation, Japon, source de rayons X Al-Kα).
Mesure de l'activité photocatalytique
Dans toutes les activités catalytiques des expériences, 50 mg des échantillons ont été ajoutés à une solution aqueuse de RhB (50 mL, 10 mg/L) agitée magnétiquement dans un récipient en verre Pyrex, puis irradiés radialement avec une lampe à arc 300 W Xe (PLS-SXE 300 , Beijing Perfect Company, Labsolar-III AG) pour fournir de la lumière visible avec λ ≥ 420 nm par un filtre de coupure ultraviolet UVCUT-420 nm (CE Aulight. Inc). La distance entre le filtre ultraviolet et la solution aqueuse de RhB était d'environ 6,5 mm. Et la densité de puissance de la lumière visible était de 150 mW/cm 2 , qui a été estimée par le wattmètre optique (PD130, Thorlabs, USA). Avant irradiation, la suspension a été maintenue à l'obscurité sous agitation magnétique pendant 30 min pour assurer l'établissement d'un équilibre adsorption/désorption. À des intervalles de temps donnés, 2 mL ont été prélevés dans la suspension et immédiatement centrifugés ; la concentration de RhB après illumination a été contrôlée à 553 nm en utilisant un spectrophotomètre UV-vis (Shimadzu UV-2550, Shimadzu Corporation, Japon). Les concentrations relatives (C /C 0 ) du RhB ont été déterminés par l'absorbance (A /Un 0 ) à 553 nm. Toutes les expériences ont été réalisées au moins en double. Les valeurs rapportées se situaient dans la plage d'erreur expérimentale de ±2 %. En combinant avec la loi de Lambert-Beer, la constante de vitesse de dégradation photocatalytique (k ) de RhB a été obtenu à l'aide de la formule suivante :
$$ \ln \left({C}_0/ C\right)\kern0.5em =\kern0.5em k t $$où C est la concentration de RhB au temps de réaction t , C 0 est la concentration à l'équilibre adsorption/désorption de RhB au début de la réaction, et A et A 0 sont les valeurs d'absorbance correspondantes.
De plus, pour identifier les espèces actives générées au cours de la réactivité photocatalytique, divers capteurs ont été ajoutés dans la solution de RhB, notamment 2 mM d'isopropanol (IPA, un quencher de ·OH), 2 mM d'acide éthylènediamine tétraacétique disodique (EDTA ; un quencher de h + ) et 2 mM p -benzoquinone (BQ ; a ·O2 − piégeur) et 40 mL/min N2 (un extincteur d'électrons). Les essais comparatifs de dégradation photocatalytique ont été réalisés dans les mêmes conditions réactionnelles que celles mentionnées ci-dessus.
Résultats et discussion
Analyse de la microstructure et de la morphologie
Afin de confirmer la composition et la structure cristalline des échantillons tels que préparés, une étude XRD a été réalisée. Comme le montre la figure 1, on peut constater que le pur WS2 , cinq pics situés à 14,4°, 33,6°, 39,6°, 49,8° et 58,5° ont été observés, ce qui correspond bien aux (002), (101), (103), (105) et (110) plans cristallins de WS2 (carte JCPDS n° 84-1398). Quant au pur Bi2 MoO6 , les pics de diffraction des plans (131), (200), (151), (260), (331) et (262) à 2θ = 28,2°, 32,5°, 36,0°, 47,1°, 55,4° et 58,5°, qui peuvent être indexés sur la phase orthorhombique de Bi2 MoO6 (carte JCPDS n° 76-2388). Dans le cas du WS2 à quelques couches /Bi2 MoO6 matériaux composites, le diagramme XRD n'affiche que les pics de diffraction caractéristiques de la phase hexagonale WS2 et phase orthorhombique Bi2 MoO6 . De plus, par rapport aux données standard pour Bi2 MoO6 (n°76-2388), l'existence de WS2 à quelques couches n'a pas modifié les positions des pics de diffraction de Bi2 MoO6 dans l'échantillon composite, indiquant Bi2 MoO6 nanoflocons cultivés sur quelques couches de WS2 nanotranches plutôt qu'incorporées dans le WS2 treillis. Il n'y a aucune trace de phase d'impureté dans la présente résolution, ce qui suggère la haute pureté des échantillons tels que préparés.
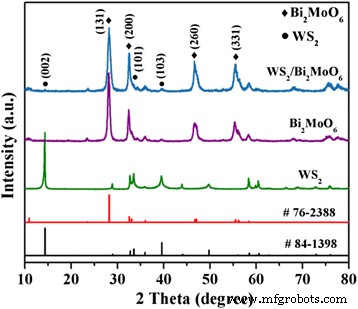
Diagrammes de diffraction des rayons X de Bi2 MoO6 , WS2 à quelques couches , et WS2 /Bi2 MoO6 (5 % en poids) composite
Les morphologies des échantillons tels que synthétisés ont été étudiées à l'aide de SEM. À titre de comparaison, des images SEM du WS brut en vrac2 sans traitement aux ultrasons et des nanotranches exfoliées sont illustrées à la Fig. 2a, b. Le premier présente une morphologie stratifiée multicouche distincte d'environ 20 μm d'épaisseur, tandis que le second présente une morphologie en forme de feuille 2D avec une épaisseur variant de dizaines de nanomètres à 1 à 2 μm. Les résultats démontrent que le WS commercial en couches2 ont été dépouillés de quelques couches WS2 nanotranches. La figure 2c montre l'image SEM de Bi2 pur MoO6 . On peut voir que le Bi2 MoO6 présentait une morphologie de microsphères avec des surfaces rugueuses. Un examen plus approfondi révèle que les microsphères sont constituées de nombreux Bi2 secondaires MoO6 nanoplaques. De plus, lorsque Bi2 MoO6 a été déposé sur le WS2 à quelques couches 2D via un processus solvothermique facile (Fig. 2d), on peut clairement voir que les surfaces de WS2 les nanotranches étaient uniformément recouvertes par de nombreux Bi2 bidimensionnels MoO6 nanoplaques (Fig. 2d) et qui formaient un WS2 /Bi2 MoO6 structure hiérarchique.

Images SEM du WS brut en vrac2 (un ), exfolié WS2 nanotranches (b ), pur Bi2 MoO6 (c ), et WS2 /Bi2 MoO6 (5 % en poids) composite (d )
Plus d'informations sur la nano-structure du WS2 à quelques couches /Bi2 MoO6 composites a été obtenu à partir d'images MET (HRTEM). Il est facile d'observer sur la figure 3a que WS2 (flèches violettes) montre une structure de nanofeuillet claire qui est similaire à celle du graphène, prouvant que le disulfure de tungstène semblable au graphène est obtenu. Pendant ce temps, Bi2 MoO6 des nanoplaques d'un diamètre d'environ 50 à 100 nm se sont développées sur le WS2 nanofeuillets. Les images HRTEM (Fig. 3b, c) tirées de la Fig. 3a affichent clairement les franges de réseau résolues de 0,274 et 0,227 nm, ce qui correspond aux (200) plans de phase orthorhombique de Bi2 MoO6 et les (103) plans de WS2 , respectivement. Par conséquent, les résultats expérimentaux ont indiqué qu'une interface d'hétérojonction cohérente et étroite entre les couches WS2 et Bi2 MoO6 s'est formé, ce qui peut bénéficier d'une meilleure séparation des charges et d'un transfert d'électrons efficace au sein de la structure hybride par rapport au Bi2 pur MoO6 .

TEM (a ) et HRTEM (b , c ) images de WS2 /Bi2 MoO6 (5 % en poids) composite
Analyse électronique de la structure et du spectre
La composition élémentaire et les états d'oxydation des quelques couches WS2 /Bi2 MoO6 les composites ont en outre été déterminés par des spectres XPS. La figure 4a montre les spectres XPS de l'enquête du WS2 à quelques couches /Bi2 MoO6 (5 % en poids), qui présente des pics W, S, O, Bi, Mo et C. Aucun pic correspondant à d'autres éléments n'est observé. Le pic pour Bi 4f dans le Bi2 MoO6 (Fig. 4b) qui apparaissait à 164,4 et 159,2 eV appartenait à Bi 4f5/2 et Bi 4f7/2 de Bi 3+ ions [23]. L'énergie de liaison Mo 3d (Fig. 4c) de 235,6 et 232,5 eV est cohérente avec le Mo 3d3/2 et Mo 3d5/2 de Mo 4+ ions [23]. Les pics asymétriques de O 1 s (Fig. 4d) se situent à 530,0 eV, caractéristiques du Mo-O [24]. Cependant, les énergies de liaison de Bi 4f, Mo 3d et O 1 s dans les spectres XPS (Fig. 4b–d) du WS hiérarchique2 /Bi2 MoO6 légèrement (environ 0,2 eV) vers des énergies de liaison inférieures par rapport au Bi2 pur MoO6 . Pendant ce temps, dans le WS2 hiérarchique /Bi2 MoO6 composite, les valeurs de W 4f5/2 (34,2 eV) et W 4f7/2 (32,0 eV) pics (Fig. 4e) correspondant à WS2 sont légèrement inférieurs (environ 0,2 eV) au WS2 pur (34,4 et 32,2 eV). De même, le spectre S 2p haute résolution (Fig. 4f) se déplace également légèrement vers des énergies de liaison inférieures de 0,3 eV. Ces résultats pourraient être attribués à la forte interaction entre WS2 et Bi2 MoO6 résultant en un décalage interne des orbites Bi 4f, Mo 3d, O 1 s W 4f et S 2p [21, 25]. Par conséquent, en combinant les enquêtes XRD, SEM, TEM et XPS, il a révélé qu'il existe à la fois WS2 et Bi2 MoO6 espèces dans le WS hiérarchique2 /Bi2 MoO6 composite et que les hétérojonctions sont formées dans leur interface de contact.
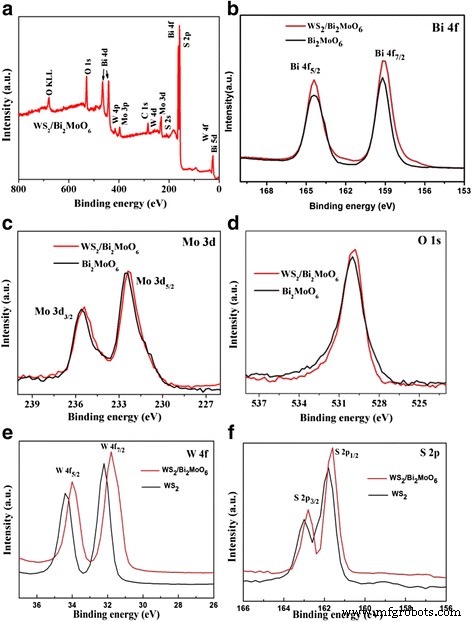
Enquête sur les spectres XPS du WS2 /Bi2 MoO6 composite (a ) et les spectres XPS haute résolution de Bi 4f (b ), Mo 3d (c ), O 1 s (d ), W 4f (e ), et S 2p (f ) de Bi2 MoO6 , WS2 , et le WS2 /Bi2 MoO6 composite (5 % en poids)
La figure 5a montre une comparaison des spectres de réflectance diffuse UV-vis (UV-Vis-DRS) du WS2 , Bi2 MoO6 et WS hiérarchique2 /Bi2 MoO6 composite avec différents WS2 Contenu. On peut clairement voir que le spectre d'absorption du Bi2 pur MoO6 s'étend de la région UV à la lumière visible à environ 450 nm. Lorsque WS2 combiné avec Bi2 MoO6 , le spectre d'absorption du composite hiérarchique présente un décalage vers le rouge évident et une absorption plus intense dans le domaine de la lumière visible par rapport au Bi2 pur MoO6 . Pendant ce temps, lorsque le contenu de WS2 augmenté à un niveau relativement élevé (3 à 7 % en poids), le composite hiérarchique affiche une absorption étonnamment forte autour de 450-800 nm. Ces résultats indiquent clairement que le photocatalyseur composite pourrait absorber plus de photons pendant la réaction photocatalytique. Par conséquent, il peut être révélé que l'ajout de WS2 nanoslices est bénéfique pour l'absorbance de la lumière visible du WS2 /Bi2 MoO6 composite.
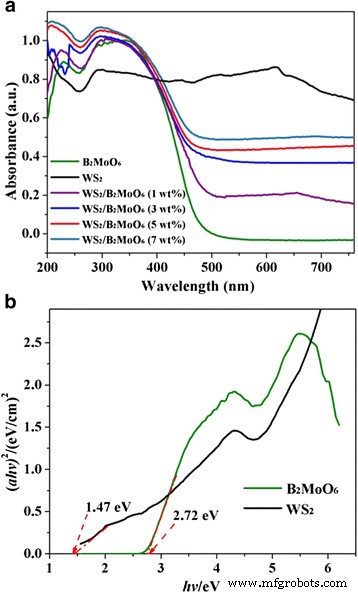
un Spectres de réflectance diffuse UV-vis (UV-Vis-DRS) des échantillons tels que préparés. b Tracé des fonctions de Kubelka-Munk transformées par rapport à l'énergie de la lumière
De plus, les énergies de bande interdite optique (E g ) des échantillons ont été calculés par l'équation suivante [26] :
$$ \alpha h v =A{\gauche( hv-{E}_g\right)}^{n/2} $$où α , hv , A , et E g sont respectivement le coefficient d'absorption, l'énergie photonique, la constante de proportionnalité et la bande interdite. La valeur de n est déterminé par le type de transition (direct (n = 1) ou indirecte (n = 4)) [27, 28]. Une parcelle de (ahv ) 2 versus (hv ) est converti selon l'UV-Vis-DRS. Comme le montre la figure 5b, le E g valeurs de pur WS2 et Bi2 MoO6 ont été estimées à 1,47 et 2,72 eV, respectivement.
Activité photocatalytique
Les activités photocatalytiques des échantillons tels que préparés ont été mesurées en dégradant la rhodamine B (RhB) sous irradiation à la lumière visible. A titre de comparaison, les activités photocatalytiques du Bi2 pur MoO6 et échantillons mélangés mécaniquement (5% WS2 et 95% Bi2 MoO6 ) ont également fait l'objet d'une enquête. Comme le montre la figure 6a, l'effet d'autodégradation de RhB sous irradiation à la lumière visible pourrait être ignoré. On peut clairement voir que le taux de photodégradation de RhB par le pur Bi2 MoO6 n'était que d'environ 39 % après 100 min d'irradiation à la lumière visible. Evidemment, tous les WS2 hiérarchiques /Bi2 MoO6 les composites présentent de meilleures performances photocatalytiques que le Bi2 pur MoO6 . ~48, ~74, ~95 et ~88% de RhB ont été dégradés en utilisant 1% de WS2 /Bi2 MoO6 , 3% WS2 /Bi2 MoO6 , 5% WS2 /Bi2 MoO6 , et 7% WS2 /Bi2 MoO6 , respectivement. Les résultats indiquent que le WS2 optimal contenu dans WS2 /Bi2 MoO6 composite existe lorsque le rapport de masse est de 5%. Pendant ce temps, il a été noté que le WS2 /Bi2 MoO6 Le composite (5 % en poids) présente une activité photocatalytique remarquablement supérieure à celle du WS2 à 5 % mélangé mécaniquement et 95% Bi2 MoO6 . Cela suggère fortement qu'un contact d'interface de nanojonction efficace et de fortes interactions entre WS2 et Bi2 MoO6 sont extrêmement utiles pour améliorer les processus de migration, de transport et de séparation des supports photogénérés. De plus, ces performances photocatalytiques supérieures pourraient être attribuées à la bonne cristallisation et à la surface spécifique élevée des composites et à la faible épaisseur de feuille du WS2 substrat.
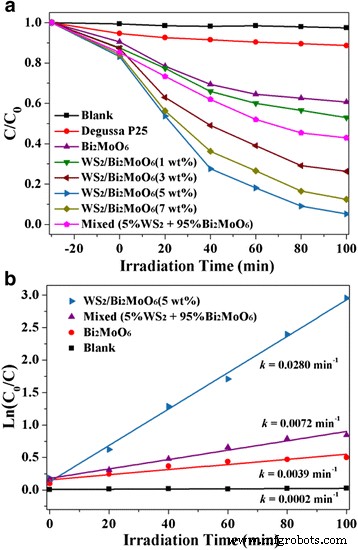
L'activité photocatalytique (a ) et l'ajustement cinétique (b ) des différents photocatalyseurs de la dégradation RhB
De plus, le modèle de cinétique de pseudo-premier ordre a été utilisé pour ajuster les données expérimentales de la dégradation photocatalytique de la solution de RhB, et les résultats sont donnés sur la figure 6b. La constante de vitesse k est de 0,0280 min −1 pour le WS hiérarchique2 /Bi2 MoO6 (5 % en poids), ce qui est 3,8 et 7,1 fois supérieur à celui des WS2 mélangés mécaniquement et Bi2 MoO6 et pur Bi2 MoO6 , respectivement. Ces résultats ont indiqué que RhB pourrait être dégradé plus efficacement par la hiérarchie WS2 /Bi2 MoO6 photocatalyseur composite.
La figure 7 montre les changements de spectre d'adsorption UV-vis de la dégradation de la solution de RhB sur le WS2 /Bi2 MoO6 (5 % en poids) photocatalyseur composite, qui a été réalisée pour étudier plus avant le processus de dégradation photocatalytique de RhB. On peut voir que le pic d'absorption principal de RhB s'est progressivement déplacé de 552 à 537 nm, correspondant à la formation par étapes d'une série de N -intermédiaires déséthylés. Au fur et à mesure que le processus d'irradiation à la lumière visible se poursuit, le pic situé à 537 nm continue de se déplacer et de diminuer, ce qui indique que les molécules de RhB ont été décomposées en fragments moléculaires plus petits et que la structure de RhB a également été détruite à la fin. Les processus de transition en deux étapes pour la photodégradation de RhB ont également été rapportés dans plusieurs études antérieures [29, 30]. Pendant ce temps, la suspension perd progressivement sa couleur au cours de l'expérience, ce qui indique en outre que la structure de RhB a finalement été détruite.
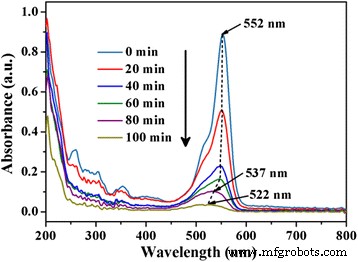
Les changements de spectres d'adsorption optique de la dégradation de la solution de RhB sur le WS2 /Bi2 MoO6 composite (5 % en poids)
Stabilité du catalyseur
La stabilité photocatalytique du WS2 hiérarchique /Bi2 MoO6 composites a été étudié par des expériences de répétabilité pour la dégradation de RhB, comme le montre la figure 8a. On peut constater que l'activité photocatalytique de WS2 /Bi2 MoO6 reste stable dans les premières expériences à deux cycles. Après quatre recyclages, les catalyseurs n'ont pas montré de diminution évidente de l'activité photocatalytique, démontrant que WS2 /Bi2 MoO6 composite a conservé une activité de dégradation relativement élevée pendant le processus de photodégradation. De plus, les échantillons de catalyseur collectés après quatre cycles ont été caractérisés par mesure XRD (Fig. 8b). On peut voir que la structure cristalline et la composition de phase de WS2 /Bi2 MoO6 composite ne change pas après quatre réactions photocatalytiques. Ainsi, la bonne stabilité structurelle assure le WS2 /Bi2 MoO6 photocatalyseurs composites efficaces travaillant sous irradiation de lumière visible.
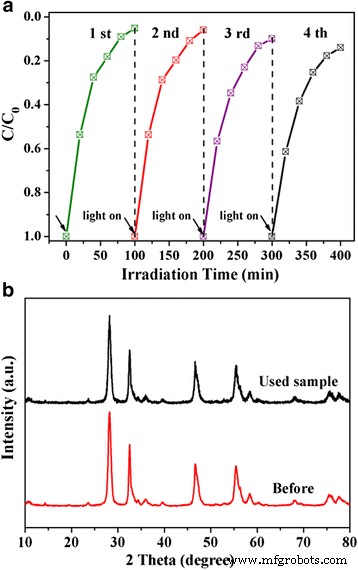
un Des pistes cyclables pour la dégradation de RhB sur le WS2 /Bi2 MoO6 composite (5 % en poids) sous irradiation en lumière visible. b Modèles XRD du WS2 /Bi2 MoO6 échantillon avant et après les expériences à quatre cycles
Mécanisme photocatalytique possible
La figure 9 montre l'expérience de piégeage des principales espèces actives dans le processus photocatalytique du WS2 /Bi2 MoO6 composite. L'isopropanol (IPA), la 1,4-benzoquinone (BQ) et l'acide éthylènediamine tétraacétique disodique (EDTA) ont joué le rôle de piégeurs de ·OH, ·O2 − , et h + , respectivement. On peut observer que l'ajout de 2 mM d'IPA ou de BQ dans la solution de RhB a eu un petit effet sur la constante de vitesse k application , suggérant que ·OH et ·O2 − sont les espèces actives secondaires lors de la réaction photocatalytique, et non les espèces actives principales lors de la réaction photocatalytique. Au contraire, le k application car la dégradation de RhB a manifestement diminué après l'ajout de 2 mM d'EDTA. Par conséquent, il peut être confirmé que h + jouent un rôle clé dans la dégradation de RhB. De plus, N2 a été barboté dans la solution de RhB au débit de 40 mL/min pour s'assurer que la réaction s'est déroulée sans O2 comme extincteur d'électrons. La dégradation de RhB a montré une légère diminution par rapport au cas de la solution équilibrée à l'air et a en outre indiqué que ·O2 − joué un rôle mineur.
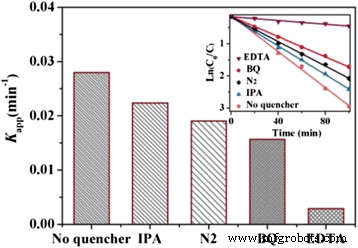
Constante de taux k application du WS2 /Bi2 MoO6 (5 % en poids) composite pour la dégradation de RhB en présence de différents charognards sous irradiation de lumière visible
Expliquer les performances photocatalytiques améliorées, la bande de conduction (CB) et la bande de valence (VB) de WS2 et Bi2 MoO6 les potentiels doivent être calculés. For a semiconductor, the bottom CB and top VB can be estimated by the empirical formula [31]:E CB = X − E 0 − 0.5E g et E VB = E CB + E g , where E CB (E VB ) is the CB (VB) edge potential; X is the electronegativity of the semiconductor; E 0 is the energy of free electrons of the hydrogenscale (~4.5 eV vs NHE); et E g is the band gap energy of the semiconductor obtained from the UV-visible diffuse reflectance absorption. The X values for WS2 and Bi2 MoO6 are calculated to be 5.66 and 5.55 eV, respectively [28, 32, 33]. Thus, E C B et E VB values of WS2 are determined to be +0.43 and +1.9 eV and Bi2 MoO6 are −0.31 and +2.41 eV, respectively.
On the basis of the above results, a possible photocatalytic mechanism scheme of the WS2 /Bi2 MoO6 composite photocatalyst is shown in Fig. 10. It can be found that WS2 and Bi2 MoO6 are excited under visible-light irradiation and generate electrons and holes in their CB and VB, respectively. The electrons on CB of Bi2 MoO6 will easily transfer WS2 due to the CB potential of Bi2 MoO6 (−0.31 eV) is more negative than the CB potential of WS2 (0.43 eV) [29, 30]. The few-layer WS2 nanoslices could act as effective electron collectors, which was favorable to the separation of electron–hole pairs in Bi2 MoO6 . Therefore, this fast electron and hole transfer process can decrease the recombination of charges and prolong the lifetime of holes on VB of Bi2 MoO6 [34]. The CB potential of WS2 (+0.43 eV) is more positive than E0 (O2 /·O2 − ) (−0.046 eV) which suggests that the ·O2 − radicals were not formed through electrons reducing the dissolved O2 [35]. However, a few electrons on the CB of Bi2 MoO6 can react with dissolved O2 to yield ·O2 − radicals because its potential (−0.31 eV) is more negative than E0 (O2 /·O2 − ). Thus, the ·O2 − active species played a minor role. Meanwhile, the photo-induced holes on VB of Bi2 MoO6 could not also directly oxidize the adsorbed H2 O molecules to ·OH radicals because its potential (+2.41 eV) was lower than E0 (·OH/H2 O) (+2.68 V) [36]. Finally, the main active species holes and minor active species ·O2 − act as a strong oxidizing agent to oxidize the organic pollutants (RhB) to CO2 et H2 O. Therefore, the hierarchical WS2 /Bi2 MoO6 composites exhibit improved photocatalytic activity.
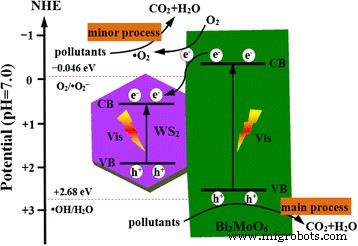
The proposed photocatalytic mechanism scheme of WS2 /Bi2 MoO6 composite under visible light (>420 nm)
Conclusions
In summary, a novel WS2 /Bi2 MoO6 heterostructured photocatalysts were successfully fabricated via a facile solvothermal growth method using pre-exfoliated layered WS2 nanoslices as a substrate. The hierarchical WS2 /Bi2 MoO6 exhibits excellent photocatalytic activity towards the degradation of rhodamine B (RhB) under visible-light irradiation. Based on the results of a series of structure and performance tests, it is believed that there formed a tight nanojunction interface between layered WS2 nanoslices and Bi2 MoO6 nanoflakes, which make the photo-induced electrons be easily transferred to the WS2 substrate. As a result, the recombination of charges was decreased and the lifetime of holes was prolonged. Therefore, the hierarchical WS2 /Bi2 MoO6 composites exhibit much higher visible-light-driven photocatalytic activity than the pure Bi2 MoO6 . Furthermore, the WS2 /Bi2 MoO6 composites are very stable under visible-light irradiation and cycling photocatalytic tests. Thus, the as-prepared WS2 /Bi2 MoO6 photocatalyst has potential application for pollutant abatement.
Nanomatériaux
- Synthèse facile et propriétés optiques de petits nanocristaux et nanotiges de sélénium
- Synthèse facile de nanoparticules SiO2@C ancrées sur MWNT en tant que matériaux anodiques hautes performances pour batteries Li-ion
- Synthèse facile de composite CuSCN coloré et conducteur revêtu de nanoparticules CuS
- Synthèse facile de nanofils d'argent avec différents rapports d'aspect et utilisés comme électrodes transparentes flexibles hautes performances
- Synthèse facile d'oxyde d'étain mésoporeux semblable à un trou de ver via l'auto-assemblage induit par l'évaporation et les propriétés de détection de gaz améliorées
- Synthèse en un seul pot de nanoplaques Cu2ZnSnSe4 et leur activité photocatalytique induite par la lumière visible
- Synthèse écologique et facile de nanofils de Co3O4 et leur application prometteuse avec du graphène dans les batteries lithium-ion
- Synthèse sonochimique en une étape facile et propriétés photocatalytiques des composites graphène/Ag3PO4 Quantum Dots
- Synthèse facile de nanocomposites magnétiques fonctionnalisés en surface pour une adsorption sélective efficace des colorants cationiques



