eau de Javel
Contexte
L'eau de Javel est un composé chimique dérivé de sources naturelles utilisées pour blanchir les tissus. L'eau de Javel fonctionne par le processus d'oxydation, ou l'altération d'un composé par l'introduction de molécules d'oxygène. Une tache est essentiellement un composé chimique, et l'ajout d'eau de Javel décompose les molécules en éléments plus petits afin qu'elle se sépare du tissu. Le détergent et l'agitation de la machine à laver accélèrent le processus de nettoyage. Les propriétés désinfectantes de l'eau de Javel fonctionnent de la même manière :les germes sont détruits et rendus inoffensifs par l'introduction d'oxygène. Dans l'industrie, différentes formes d'eau de Javel sont utilisées pour blanchir des matériaux tels que le papier et le bois, bien que la plupart des agents de blanchiment soient utilisés pour blanchir les textiles.
Historique
Les humains blanchissent les tissus depuis des siècles; les anciens Égyptiens, Grecs et Romains blanchissaient les matériaux. Dès 300
À la fin du XVIIIe siècle, des scientifiques ont découvert un produit chimique qui avait le même effet que le crofting, mais qui donnait des résultats beaucoup plus rapides. En 1774, le chimiste suédois Karl Wilhelm Scheele a découvert l'élément chimique chlore, un halogène gazeux vert-jaunâtre très irritant. En 1785, le scientifique français Claude Berthollet découvrit que le chlore était un excellent agent blanchissant dans les tissus. Certains opérateurs d'usine ont tenté d'exposer leurs tissus au chlore gazeux, mais le processus était si lourd et les fumées si fortes que ces tentatives ont rapidement été abandonnées.
Près de Paris, dans la ville de Javel, Berthollet a commencé une petite usine pour la fabrication d'un nouveau produit appelé "Eau de Javelle". La poudre de blanchiment était constituée de potasse (soude) qui avait absorbé du chlore gazeux. En 1799, une autre poudre décolorante fut inventée par le chimiste écossais Charles Tennant. Dans les premières années de la révolution industrielle, sa poudre de chaux brevetée était largement utilisée pour blanchir une variété de tissus et de produits en papier. Pour fabriquer la poudre de blanchiment, de la chaux éteinte (chaux traitée avec de l'eau) était étalée en couche mince sur le béton ou le sol en plomb d'une grande pièce. Le chlore gazeux était pompé dans la pièce pour être absorbé par la chaux. Bien qu'étant un blanchisseur efficace, la poudre était chimiquement instable. C'était 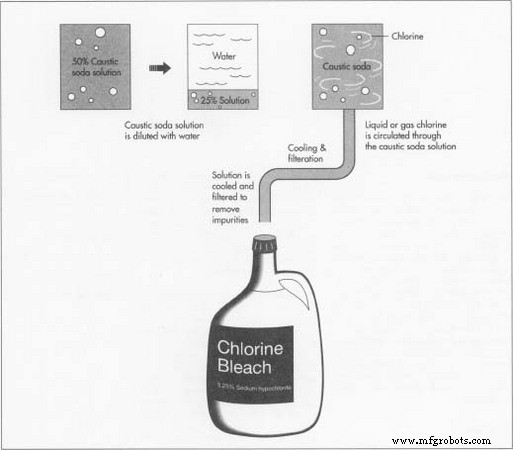 Les matières premières pour la fabrication d'eau de Javel sont le chlore, la soude caustique et l'eau. Le chlore et la soude caustique sont produits en mettant de l'électricité à courant continu dans une solution de sel de chlorure de sodium dans un processus appelé électrolyse. couramment utilisé jusqu'à environ la Première Guerre mondiale, lorsque les solutions de chlore liquide et d'hypochlorite de sodium - les précurseurs de l'eau de Javel domestique moderne - ont été introduites. À peu près à cette époque, les chercheurs ont découvert que l'injection de sel l'eau avec un courant électrique a brisé les molécules de sel (chlorure de sodium) et a produit un composé appelé hypochlorite de sodium. Cette découverte a permis la production de masse d'hypochlorite de sodium, ou chlore, eau de Javel.
Les matières premières pour la fabrication d'eau de Javel sont le chlore, la soude caustique et l'eau. Le chlore et la soude caustique sont produits en mettant de l'électricité à courant continu dans une solution de sel de chlorure de sodium dans un processus appelé électrolyse. couramment utilisé jusqu'à environ la Première Guerre mondiale, lorsque les solutions de chlore liquide et d'hypochlorite de sodium - les précurseurs de l'eau de Javel domestique moderne - ont été introduites. À peu près à cette époque, les chercheurs ont découvert que l'injection de sel l'eau avec un courant électrique a brisé les molécules de sel (chlorure de sodium) et a produit un composé appelé hypochlorite de sodium. Cette découverte a permis la production de masse d'hypochlorite de sodium, ou chlore, eau de Javel.
Types d'eau de Javel
Aujourd'hui, l'eau de Javel se trouve dans presque tous les foyers. Il blanchit les tissus et élimine les taches par une réaction chimique qui décompose la couleur indésirable en particules plus petites qui peuvent être facilement éliminées par lavage. Les deux types d'eau de Javel domestique sont l'eau de Javel et l'eau de Javel au peroxyde. L'eau de Javel au peroxyde a été introduite dans les années 1950. Bien qu'il aide à éliminer les taches, en particulier à des températures de lavage plus élevées, il ne blanchit pas la plupart des matériaux colorés et n'affaiblit pas les tissus, comme le fait l'eau de Javel à l'hypochlorite de sodium. L'eau de Javel au peroxyde ne désinfecte pas et est couramment ajoutée aux détergents à lessive qui sont annoncés comme étant sans danger pour les couleurs. Il a également une durée de conservation plus longue que l'eau de Javel. L'eau de Javel au peroxyde est plus couramment utilisée en Europe, où les machines à laver sont fabriquées avec des serpentins de chauffage internes qui peuvent élever la température de l'eau jusqu'au point d'ébullition.
La forme la plus courante d'eau de Javel domestique aux États-Unis est l'eau de Javel. Il est le plus efficace pour éliminer les taches et désinfecter les tissus. L'eau de Javel est peu coûteuse à fabriquer et efficace à la fois à des températures de lavage chaudes et chaudes. Cependant, il possède de fortes propriétés chimiques qui peuvent fragiliser les fibres textiles.
Les propriétés désinfectantes de l'eau de Javel peuvent également être utiles en dehors du linge. L'eau de Javel désinfecte l'eau potable là où la contamination des eaux souterraines s'est produite, car c'est un puissant germicide. Il a été utilisé pour la première fois pour désinfecter l'eau potable dans le réservoir Croton de New York en 1895 et est approuvé par le gouvernement pour la désinfection des équipements dans l'industrie alimentaire. Ces dernières années, l'eau de Javel a été promue par les activistes de la santé communautaire comme une méthode peu coûteuse pour désinfecter les aiguilles des utilisateurs de drogues par voie intraveineuse.
Matières premières
Les matières premières utilisées pour la fabrication d'eau de Javel sont le chlore, la soude caustique et l'eau. Le chlore et la soude caustique sont produits en mettant de l'électricité à courant continu dans une solution de sel de chlorure de sodium dans un processus appelé électrolyse. Le chlorure de sodium, sel de table commun, provient soit de mines soit de puits souterrains. Le sel est dissous dans de l'eau chaude pour former une solution saline, qui est ensuite traitée contre les impuretés avant de réagir dans la cellule électrolytique.
Le processus de fabrication
La fabrication de l'eau de Javel à l'hypochlorite de sodium nécessite plusieurs étapes. Toutes les étapes peuvent être effectuées dans une grande usine de fabrication, ou le chlore et la soude caustique peuvent être expédiés de différentes usines vers le site du réacteur. Le chlore et la soude caustique sont tous deux des produits chimiques dangereux et sont transportés conformément à des réglementations strictes.
Préparation des composants
- 1 La soude caustique est généralement produite et expédiée sous forme de solution concentrée à 50 %. A destination, cette solution concentrée est diluée avec de l'eau pour former une nouvelle solution à 25 %.
- 2 La chaleur est créée lorsque l'eau dilue la forte solution de soude caustique. La soude caustique diluée est refroidie avant de réagir.
La réaction chimique
- 3 Le chlore et la solution de soude caustique réagissent pour former de l'eau de Javel à l'hypochlorite de sodium. Cette réaction peut avoir lieu dans un lot d'environ 14 000 gallons ou dans un réacteur continu. Pour créer de l'hypochlorite de sodium, du chlore liquide ou gazeux circule dans la solution de soude caustique. La réaction du chlore et de la soude caustique est essentiellement instantanée.
Rafraîchissant et purifiant
- 4 La solution d'eau de Javel est ensuite refroidie pour éviter la décomposition.
- 5 Souvent, cet agent de blanchiment refroidi est déposé ou filtré pour éliminer les impuretés qui peuvent décolorer l'agent de blanchiment ou catalyser sa décomposition.
Livraison
- 6 L'eau de Javel finie à l'hypochlorite de sodium est expédiée à une usine d'embouteillage ou mise en bouteille sur place. L'eau de Javel domestique est généralement constituée d'hypochlorite de sodium à 5,25 % dans une solution aqueuse.
Contrôle qualité
Dans l'usine de fabrication d'eau de Javel, la solution finale d'hypochlorite de sodium est passée à travers une série de filtres pour extraire les impuretés restantes. Il est également testé pour s'assurer qu'il contient exactement 5,25 % d'hypochlorite de sodium. La sécurité est une préoccupation majeure dans les usines de fabrication en raison de la présence de chlore gazeux volatil. Lorsque le chlore est fabriqué à l'extérieur de l'installation du réacteur, il voyage sous forme liquide dans des wagons-citernes spécialement conçus à double paroi qui ne se rompront pas en cas de déraillement. À l'arrivée à l'usine, le chlore liquide est pompé des wagons-citernes dans la cuve de rétention. Par mesure de sécurité, les wagons-citernes sont équipés de vannes d'arrêt qui fonctionnent conjointement avec un système de détection de chlore. En cas de fuite de chlore, le système de détection déclenche un dispositif sur le réservoir qui arrête automatiquement la transmission du liquide en 30 secondes.
À l'intérieur de l'installation, des cuves de chlore sont logées dans un espace clos appelé grange à voitures. Cette pièce fermée est équipée de "laveurs" d'air pour éliminer tout chlore gazeux échappé, nocif pour l'homme et l'environnement. L'épurateur de type vide inhale tout chlore gazeux de la zone fermée et l'injecte avec de la soude caustique. Cela le transforme en eau de Javel, qui est incorporée dans le processus de fabrication. Malgré ces précautions, des exercices de sécurité et d'incendie sont programmés régulièrement pour le personnel de l'usine.
Considérations particulières concernant l'
Emballage
L'eau de Javel domestique à l'hypochlorite de sodium a été présentée aux Américains en 1909 et vendue dans des récipients en acier, puis dans des bouteilles en verre. Au début des années 1960, l'introduction de la cruche en plastique a apporté une alternative d'emballage moins chère, plus légère et incassable. Il réduisait les coûts de transport et protégeait la sécurité des travailleurs impliqués dans son expédition et sa manutention. De plus, le plastique épais ne permettait pas à la lumière ultraviolette d'atteindre l'eau de Javel, ce qui améliorait sa stabilité chimique et son efficacité. Ces dernières années, cependant, les conteneurs en plastique sont devenus une préoccupation environnementale en raison du temps qu'il faut au matériau pour se décomposer dans une décharge. De nombreuses entreprises qui dépendent des emballages en plastique, y compris les fabricants d'eau de Javel, ont commencé à réduire la quantité de plastique dans leurs emballages ou à utiliser des plastiques recyclés. Au début des années 1990, Clorox a introduit des résines post-consommation (PCR) dans ses emballages. Les nouvelles bouteilles sont un mélange de polyéthylène haute densité vierge (PEHD) et de 25 % de plastique recyclé, principalement à partir de bouteilles transparentes de type pot à lait.
Sécurité des consommateurs
L'industrie de la fabrication d'eau de Javel a été critiquée dans les années 1970 lorsque le public s'est inquiété des effets des produits chimiques ménagers sur la santé personnelle. La dioxine, un sous-produit cancérigène de la fabrication de produits chimiques, se trouve souvent dans les produits industriels utilisés pour blanchir le papier et le bois. Dans sa forme finale en bouteille, l'eau de Javel à l'hypochlorite de sodium ne contient pas de dioxines car le chlore doit être à l'état gazeux pour que les dioxines existent. Cependant, du chlore gazeux peut se former lorsque l'eau de Javel entre en contact avec de l'acide, un ingrédient de certains nettoyants pour cuvettes de toilettes, et les étiquettes sur l'eau de Javel domestique contiennent des avertissements spécifiques contre une telle combinaison.
En plus du danger des dioxines, les consommateurs se sont également inquiétés de la toxicité du chlore dans l'eau de Javel à l'hypochlorite de sodium. Cependant, le processus de lessivage désactive le chlore potentiellement toxique et provoque la formation d'eau salée. Une fois que l'eau de rinçage pénètre dans le système d'eau par le drain domestique, les usines de filtration d'eau municipales éliminent les traces restantes de chlore.
Processus de fabrication



