Surrefroidissement de l'eau contrôlé par nanoparticules et ultrasons
Résumé
Nanoparticules, dont Al2 O3 et SiO2 , et les ultrasons ont été adoptés pour améliorer les propriétés de solidification de l'eau. Les effets de la concentration de nanoparticules, de l'angle de contact et de l'intensité des ultrasons sur le degré de surfusion de l'eau ont été étudiés, ainsi que la stabilité de la dispersion des nanoparticules dans l'eau pendant la solidification. Les résultats expérimentaux montrent que le degré de surfusion de l'eau est réduit sous l'effet combiné des ultrasons et des nanoparticules. Par conséquent, la réduction du degré de surfusion augmente avec l'augmentation de l'intensité des ultrasons et de la concentration en nanoparticules et la diminution de l'angle de contact des nanoparticules. De plus, la réduction du degré de surfusion causée par les ultrasons et les nanoparticules ne dépasse pas la somme des réductions du degré de surfusion causées par les ultrasons et les nanoparticules séparément ; la réduction est encore plus faible que celle provoquée par les ultrasons individuellement dans certaines conditions de concentration de nanoparticules et d'angle de contact et d'intensité ultrasonore contrôlés. La stabilité de la dispersion des nanoparticules pendant la solidification ne peut être maintenue que lorsque les nanoparticules et les ultrasons montrent ensemble un effet supérieur sur la réduction du degré de surfusion de l'eau à la seule opération d'ultrasons. Dans le cas contraire, l'agrégation des nanoparticules apparaît dans la solidification de l'eau, ce qui entraîne un échec. Les relations entre la concentration significative de nanoparticules, l'angle de contact et l'intensité ultrasonore, auxquels les exigences de faible surfusion et de stabilité élevée pouvaient être satisfaites, ont été obtenues. Les mécanismes de contrôle de ces phénomènes ont été analysés.
Introduction
La recherche de nouvelles technologies pour éviter les préoccupations croissantes concernant les problèmes environnementaux, la pénurie d'énergie imminente et le coût élevé de l'énergie et des nouvelles centrales électriques a été une préoccupation scientifique au cours des trois dernières décennies. Le principal défi est le manque de stockage de l'énergie excédentaire pour éviter son élimination et combler le fossé entre la production et la consommation d'énergie. Le stockage d'énergie thermique à chaleur latente est une technique particulièrement intéressante car elle permet d'obtenir une densité de stockage d'énergie élevée [1]. L'eau est l'un des matériaux les plus couramment utilisés pour le stockage de la chaleur latente dans la pratique. Il a une densité de stockage thermique volumétrique élevée en raison de sa chaleur latente et de sa conductivité thermique élevées. Cependant, l'un des principaux inconvénients de l'eau, comme l'ont signalé de nombreux chercheurs, a été la surfusion qui se produit pendant les processus de solidification. La surfusion conduit à des températures de refroidissement réduites ; ainsi, la chaleur latente sera libérée à des températures plus basses. En conséquence, une grande différence de température entre la charge et la décharge est nécessaire pour utiliser pleinement la chaleur latente, ce qui n'est pas souhaitable pour les applications de stockage d'énergie thermique efficaces [2]. Ainsi, trouver des méthodes pour réduire le degré de surfusion de l'eau est fondamental pour faire progresser la technologie de stockage d'énergie thermique à chaleur latente.
Au cours de la dernière décennie, l'utilisation de nanoparticules comme agents de nucléation est la méthode la plus répandue et la plus utilisée par les chercheurs pour contrôler les degrés de surfusion de l'eau. Les nanoparticules couramment utilisées sont le métal et l'oxyde métallique, comme le TiO2 , Al2 O3 , Cu et CuO [3,4,5,6]. Ces nanoparticules sont hydrophiles et peuvent faciliter la formation de noyaux de glace en diminuant l'énergie libre de nucléation de Gibbs. D'autres nanoparticules hydrophobes, telles que les nanotubes de carbone et les nanoplaquettes de graphène, ont également été utilisées comme agents de nucléation par certains chercheurs [7,8,9]. La réduction du degré de surfusion de l'eau est attribuée aux surfaces spécifiques élevées des nanoparticules, qui peuvent fournir plus de sites de nucléation et augmenter la probabilité de nucléation à haute température. Selon la littérature, différentes nanoparticules ont des effets de nucléation différents; de plus, les nanoparticules avec des zones spécifiques élevées peuvent éliminer la surfusion de l'eau, alors que les nanoparticules avec hydrophilie ne le sont pas. Par exemple, l'ajout d'une petite quantité de nanoplaquettes de graphène (0,02 % en poids) peut éliminer la surfusion de l'eau [8], alors qu'une réduction de seulement 70,9 % du degré de surfusion peut être obtenue en utilisant TiO2 nanoparticules (1,0 % en poids) [4]. Ainsi, l'augmentation du nombre de sites de nucléation étrangers peut être une meilleure méthode pour contrôler la surfusion de l'eau, par rapport à l'amélioration de l'hydrophilie des agents de nucléation.
L'utilisation de nanoparticules avec des surfaces spécifiques élevées et l'augmentation de la concentration de nanoparticules hydrophiles sont deux façons courantes d'augmenter les sites de nucléation pour la solidification de l'eau. Cependant, le maintien de la dispersion des nanoparticules avec une surface spécifique élevée dans l'eau est extrêmement difficile, et les nanoparticules ont tendance à s'agréger spontanément pour réduire l'énergie libre de surface [10]. Une mauvaise stabilité de dispersion des nanoparticules avec des zones spécifiques élevées entraînera de graves problèmes dans leurs applications, tels que la dégradation des propriétés thermiques lors des cycles thermiques à long terme. Le phénomène d'agrégation ne peut également être évité lorsque la concentration en nanoparticules augmente dans une certaine mesure [11]. Pour les nanoparticules de métal et d'oxyde métallique, la concentration critique estimée est d'environ 1,0 à 2,0 % en poids. Par conséquent, il est nécessaire de trouver d'autres moyens d'augmenter les sites efficaces pour la nucléation de l'eau.
L'application d'ultrasons dans la solidification s'est avérée être une méthode efficace pour réduire le degré de surfusion de l'eau au cours des dernières années [12]. Les ultrasons, lorsqu'ils traversent un milieu liquide, provoquent des vibrations mécaniques du liquide. Si le milieu liquide contient des noyaux gazeux dissous, ce qui sera le cas dans des conditions normales, le milieu liquide peut croître et s'affaisser par l'action des ultrasons. Le phénomène de croissance et d'effondrement de microbulles sous champ ultrasonore est appelé « cavitation acoustique » [13]. On pense généralement que la nucléation de la glace dans l'eau est étroitement liée à la cavitation acoustique. Certains chercheurs considèrent que le changement de pression associé à l'effondrement des bulles de cavitation peut être la raison de l'effet de nucléation des ultrasons [14,15,16,17,18,19,20], tandis que d'autres pensent que le degré de surfusion réduit de l'eau peut être dû aux surfaces de bulles de cavitation fournies, agissant comme des sites de nucléation étrangers [21,22,23]. Des investigations supplémentaires sont donc nécessaires pour mieux comprendre la nucléation de la glace contrôlée par ultrasons.
Récemment, Liu et al. ont mené des expériences sur la solidification de l'eau influencée par les nanoparticules (c'est-à-dire l'oxyde de graphène) et les ultrasons simultanément [24]. Ils ont constaté que le degré de surfusion de l'eau est réduit de manière plus significative sous l'effet combiné des nanoparticules et des ultrasons que celui causé par les nanoparticules ou les ultrasons. Cependant, ce phénomène intéressant n'a pas été bien expliqué dans leur étude et a été généralement attribué à l'effet de cavitation des ultrasons. Nos travaux antérieurs ont démontré que l'introduction de TiO2 les nanoparticules et les ultrasons dans le processus de solidification peuvent réduire le degré de surfusion de l'eau. Plus la puissance des ultrasons est élevée, plus le degré de surfusion est faible [25]. Cependant, nous avons également constaté que le problème d'agrégation susmentionné apparaît dans la solidification de l'eau assistée par ultrasons et TiO2 nanoparticules; c'est-à-dire que les nanoparticules et les bulles ont tendance à être repoussées par l'interface glace-eau qui avance et finalement se regrouper au milieu du récipient, en particulier à des puissances ultrasonores élevées. Cette découverte suggère que la puissance des ultrasons doit être réglée avec soin afin d'obtenir simultanément un faible degré de surfusion et une bonne stabilité des nanoparticules. À ce jour, peu d'études ont été rapportées sur la solidification de l'eau assistée par des nanoparticules et des ultrasons. Ainsi, mener une enquête détaillée pour identifier et élucider l'effet combiné des nanoparticules et des ultrasons est jugé nécessaire.
Dans la présente étude, Al2 O3 et SiO2 des nanoparticules, qui sont hydrophiles et peuvent être dispersées régulièrement dans l'eau, ont été adoptées et des ultrasons ont été introduits dans les processus de solidification des deux suspensions aqueuses. Les effets de la concentration de nanoparticules et de l'intensité des ultrasons sur le degré de surfusion de l'eau ont été étudiés. Cette étude vise principalement à identifier les rôles que les nanoparticules et les ultrasons peuvent jouer dans la solidification de l'eau et à déterminer la méthode de nucléation appropriée et les conditions de contrôle correspondantes pouvant répondre simultanément aux exigences de faible degré de surfusion et de bonne stabilité de la suspension. Le mécanisme de nucléation concernant les bulles de cavitation a également été discuté pour montrer la manière dont les nanoparticules et les ultrasons affectent la solidification de l'eau.
Expérimental
Al hydrophile2 O3 et SiO2 des nanoparticules (Aladdin Chemical Reagent Co. Ltd., Chine) ont été sélectionnées comme agents de nucléation dans cette étude, sur la base de leur forte affinité pour l'eau. L'angle de contact entre les nanoparticules et l'eau a été mesuré en utilisant une méthode de goutte sessile statique avec une goniométrie à angle de contact (DataPhysics OCA40 Micro, Allemagne). Cinq tests ont été effectués pour chaque nanoparticule, et une valeur moyenne a été obtenue à partir de ces tests. Les mesures d'angle de contact étaient reproductibles à moins de 1 % des valeurs moyennes, et les résultats mesurés sont présentés sur la figure 1. , et aucun tensioactif n'a été utilisé. Une sonde à ultrasons (Sonics Vibra Cell, Ningbo Kesheng Ultrasonic Equipment Co. Ltd., Chine) avec une puissance de sortie de 600 W et une fréquence d'alimentation de 20 kHz a été appliquée pour disperser les nanoparticules dans l'eau déminéralisée par vibration pendant 1 h. Les concentrations de nanoparticules ont été fixées à 0,2, 0,4, 0,6, 0,8 et 1,0 % en poids.
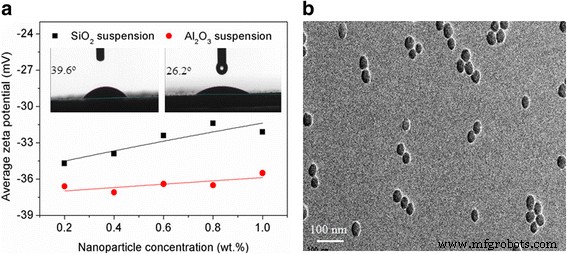
un Potentiels zêta des suspensions aqueuses d'Al2 O3 et SiO2 nanoparticules. b Image MET typique de la suspension aqueuse de SiO2 nanoparticules
Une suspension aqueuse bien dispersée de nanoparticules peut être acquise avec un potentiel zêta élevé pour obtenir une forte force de répulsion électrostatique. Les suspensions de nanoparticules avec des potentiels zêta supérieurs à + 30 mV ou supérieurs à - 30 mV sont normalement considérées comme stables dans la littérature [26]. Ainsi, les potentiels zêta des suspensions aqueuses d'Al2 O3 et SiO2 les nanoparticules à différentes concentrations ont été mesurées à l'aide d'un granulomètre Zetasizer Nano ZS (Malvern Instruments Ltd., Angleterre). Les résultats sont présentés sur la figure 1a. Les mesures ont été répétées trois fois et la reproductibilité des données se situait dans une erreur de 1,5%. Toutes les suspensions de nanoparticules ont un potentiel zêta supérieur à − 30 mV, ce qui suggère que l'Al2 O3 et SiO2 les nanoparticules peuvent être dispersées de façon constante dans l'eau. Une microscopie électronique à transmission (MET, JEM-100CXII, JEOL, Japon) a également été utilisée pour mesurer la distribution des nanoparticules dans l'eau. La figure 1b montre une image MET typique de la suspension aqueuse de SiO2 nanoparticules. De toute évidence, les nanoparticules sont bien réparties. Dans cette étude, la bonne stabilité de dispersion des suspensions aqueuses d'Al2 O3 et SiO2 les nanoparticules ont pu être conservées pendant 4 jours sans montrer de signes de sédimentation.
L'appareil expérimental pour la solidification de l'eau assistée par des nanoparticules et des ultrasons est schématisé sur la Fig. 2a. Les appareils suivants sont les suivants :un système de solidification constitué d'un réservoir de refroidissement conçu et d'un thermostat à basse température (CDC-1, Tianjin Huabei Refrigeration Technology Co. Ltd., Chine) utilisé pour congeler des échantillons ; un système de génération d'ultrasons (un appareil à ultrasons commercial, le sonicateur Sonics Vibra-Cell JY88-IIN, Ningbo Scientz Biotechnology Co. Ltd., Chine) utilisé pour fournir des champs d'ultrasons ; un système d'observation composé d'un enregistreur de données de température (34970A, Agilent Technologies Co. Ltd., USA) ; et un ordinateur utilisé pour surveiller le processus de congélation en temps réel. Pour assurer la distribution uniforme de l'irradiation par ultrasons, la source d'ultrasons a été placée verticalement au centre du réservoir de refroidissement, et le récipient en verre rempli de l'échantillon liquide a été placé à environ 2 pouces de la source d'ultrasons et parallèlement à celle-ci.
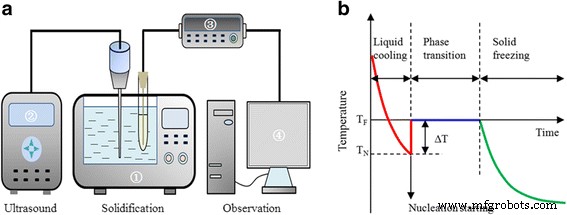
un Schéma de l'appareil expérimental :(1) bain thermostatique, (2) appareil à ultrasons, (3) enregistreur de données de température et (4) ordinateur. b Profil de température typique de la solidification de l'eau :T F , température de congélation ; T N , température de nucléation; et ΔT , degré de surfusion (différence entre T F et T N )
Dans les expériences, les échantillons d'eau mélangés avec et sans nanoparticules d'un volume d'environ 20 mL ont été refroidis à − 20 °C sous différentes intensités ultrasonores allant de 0,14 à 1,27 W cm −2 . Le cycle d'utilisation de l'irradiation par ultrasons a été fixé à 80 %, ce qui représente 8 s activé-2 s désactivé. Le traitement par ultrasons a commencé alors que la température de l'échantillon s'est refroidie à 0 °C et s'est terminé dès que la nucléation de la glace s'est produite dans l'échantillon liquide. Le temps de traitement par ultrasons était très court, moins de 2 min. La variation de la vitesse de refroidissement de l'échantillon liquide due à la chaleur générée par les ultrasons était négligeable en si peu de temps. La figure 2b montre un profil de température typique lors de la solidification. Le processus de solidification peut être divisé en trois étapes ultérieures, à savoir le refroidissement liquide, la transition de phase et la congélation solide. Dans l'étape de refroidissement liquide, la chaleur sensible est retirée de l'échantillon à l'état liquide et sa température est abaissée. Après avoir atteint le point de congélation, la transition de phase n'est généralement pas déclenchée immédiatement mais le refroidissement se poursuit. Ainsi, à la fin de la phase de prérefroidissement, l'échantillon reste dégelé en dessous de son point de congélation; c'est-à-dire que l'échantillon est surfondu. Après un certain degré de surfusion, la nucléation de la glace se produit soudainement. Ensuite, l'échantillon subit la transition de phase. Dans cette étude, un thermocouple de type T cuivre-constante avec une précision de ± 0,2 °C a été utilisé pour mesurer la température. L'expérience de solidification dans des conditions identiques a été répétée au moins 15 fois pour calculer la moyenne des données expérimentales. Les écarts par rapport à la valeur moyenne étaient de ± 1,5 %.
Dans l'analyse de la solidification de l'eau induite par les nanoparticules et les ultrasons, les états des bulles de cavitation à différentes concentrations de nanoparticules et intensités ultrasonores ont été mesurés à l'aide d'une méthode capillaire [27]. La méthode capillaire implique la fixation d'un capillaire qui peut mesurer le changement de volume qui se produit en raison de la formation de grosses bulles inactives formées par la coalescence entre les bulles de cavitation. Les valeurs d'absorbance de la suspension aqueuse de nanoparticules avant et après le cycle de solidification/fusion ont également été mesurées à l'aide d'un spectrophotomètre UV-vis (UV9000S, Shanghai Precision &Scientific Instrument Co., Ltd., Chine) pour analyser la stabilité de la dispersion des nanoparticules étrangères. dans l'eau pendant la solidification. Cinq tests ont été effectués pour chaque échantillon afin de garantir la fiabilité des résultats expérimentaux.
Résultats et discussion
Degré de surfusion de l'eau contrôlé séparément par les nanoparticules et les ultrasons
Les rapports du degré de surfusion requis pour la solidification de l'eau avec des nanoparticules à celui sans nanoparticules (R 1 = ΔT N /ΔT W ) à différentes concentrations de nanoparticules sont indiqués sur la Fig. 3. Le degré de surfusion mesuré de l'eau pure (ΔT W ) est d'environ 11,6 °C. Le rapport de degré de surfusion R 1 est < 1 et diminue avec l'augmentation de la concentration en nanoparticules, ce qui indique que l'Al2 O3 et SiO2 les nanoparticules peuvent favoriser la nucléation de la glace de l'eau comme prévu. L'Al2 O3 les nanoparticules ont un effet de nucléation apparemment plus fort en raison de l'angle de contact plus petit par rapport au SiO2 nanoparticules. Par exemple, une réduction de 28,3 % du degré de surfusion de l'eau est obtenue en ajoutant 0,6 % en poids de SiO2 nanoparticules, alors qu'à même concentration, l'Al2 O3 les nanoparticules peuvent réduire le degré de surfusion de l'eau de 37,4 %. L'effet de nucléation affaibli du SiO2 les nanoparticules causées par un grand angle de contact peuvent être compensées en augmentant la concentration en nanoparticules. Comme le montre la figure 1, une réduction de 37,1 % du degré de surfusion peut également être obtenue en augmentant la concentration de SiO2 nanoparticules à 0,8 % en poids. La figure 1 montre également l'effet des ultrasons sur le degré de surfusion de l'eau. Le rapport du degré de surfusion requis pour la solidification de l'eau avec ultrasons à celui sans ultrasons (R 2 = ΔT U /ΔT W ) est < 1, suggérant que les bulles de cavitation générées par les ultrasons peuvent agir comme agents de nucléation pour favoriser la nucléation de la glace de l'eau. Cet effet de nucléation des ultrasons peut être amélioré en augmentant l'intensité des ultrasons. Dans cette étude, une réduction de 83,1 % du degré de surfusion de l'eau peut être obtenue à une intensité ultrasonore de 1,27 W cm −2 .
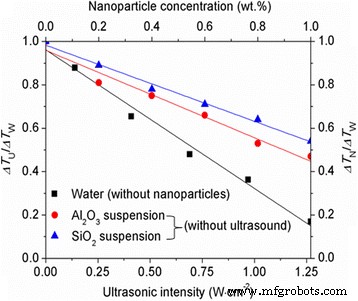
Effets des ultrasons et des nanoparticules sur le degré de surfusion de l'eau. ΔT U /ΔT W représente le rapport du degré de surfusion requis pour la solidification de l'eau avec des ultrasons à celui sans ultrasons. ΔT N /ΔT W représente le rapport du degré de surfusion requis pour la solidification de l'eau avec des nanoparticules à celui sans nanoparticules
Degré de surfusion de l'eau contrôlé mutuellement par les nanoparticules et les ultrasons
La figure 4 montre l'effet combiné des nanoparticules et des ultrasons sur le degré de surfusion de l'eau. Le rapport du degré de surfusion requis pour la solidification de l'eau avec des nanoparticules et des ultrasons à celui sans nanoparticules et des ultrasons (R 3 = ΔT N-U /ΔT W ) est < 1, indiquant que l'utilisation mutuelle des nanoparticules et des ultrasons peut favoriser la nucléation de la glace de l'eau lors de la solidification. Cet effet de nucléation des nanoparticules et des ultrasons est étroitement lié à la concentration de nanoparticules et à l'intensité des ultrasons. Par exemple, une réduction de 63,7% du degré de surfusion de l'eau peut être obtenue à l'Al2 O3 concentration de nanoparticules de 0,2 % en poids lorsque l'intensité des ultrasons augmente de 0,14 à 1,27 W cm −2 . Une réduction de 58,1 % du degré de surfusion de l'eau peut être obtenue à l'intensité des ultrasons de 1,27 W cm −2 lorsque l'Al2 O3 la concentration de nanoparticules augmente de 0,2 à 1,0 % en poids. L'angle de contact des nanoparticules est également un facteur important qui influence l'effet combiné des ultrasons et des nanoparticules. Les degrés de surfusion contrôlés de l'eau par Al2 O3 les nanoparticules sont apparemment plus faibles par rapport à celles contrôlées par SiO2 nanoparticules aux mêmes conditions de concentration de nanoparticules et d'intensité ultrasonore. Par exemple, le degré de surfusion requis pour la solidification de l'eau est réduit de 70,6 % pour l'Al2 O3 nanoparticules à une concentration de 0,6 % en poids et une intensité ultrasonore de 0,69 W cm −2 , alors que seulement une réduction de 56,1% du degré de surfusion est obtenue pour le SiO2 nanoparticules dans les mêmes conditions. Pour obtenir la même réduction de 70,6 % du degré de surfusion, une concentration plus élevée de 1,0 % en poids est requise pour le SiO2 nanoparticules à grand angle de contact. Par conséquent, la nucléation de la glace de l'eau aidée par les nanoparticules et les ultrasons peut être facilitée en augmentant la concentration de nanoparticules et l'intensité des ultrasons et en diminuant l'angle de contact des nanoparticules.
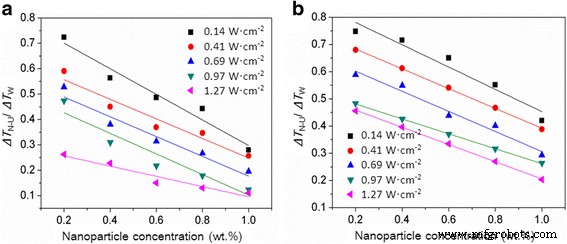
Effet combiné des ultrasons et des nanoparticules sur le degré de surfusion de l'eau [a Al2 O3 nanoparticules, b SiO2 nanoparticules]. ΔT N-U /ΔT W représente le rapport du degré de surfusion requis pour la solidification de l'eau avec nanoparticules et ultrasons à celui sans nanoparticules et ultrasons
Comparaison des degrés de surfusion de l'eau contrôlés par les nanoparticules et les ultrasons séparément et mutuellement
Lorsque les nanoparticules et les ultrasons influencent simultanément la nucléation de la glace de l'eau, l'effet final n'est pas simplement l'addition de tous les effets individuels; c'est-à-dire que la réduction du degré de surfusion de l'eau déterminé par les nanoparticules et les ultrasons ensemble est en fait inférieure à la somme des réductions déterminées par eux séparément. Par exemple, le degré de surfusion de l'eau est réduit de 70,6 % au niveau de l'Al2 O3 concentration en nanoparticules de 0,6 % en poids et intensité des ultrasons de 0,69 W cm −2 (Fig. 4a), ce qui est inférieur à la somme de la réduction de 37,4 % causée par 0,6 % en poids de nanoparticules et de la réduction de 52,1 % causée par 0,69 W cm −2 échographie (Fig. 3). De plus, la réduction du degré de surfusion de l'eau induite par les nanoparticules et les ultrasons est toujours plus importante que celle induite par les nanoparticules individuellement, alors qu'elle peut être supérieure ou inférieure à celle induite par les ultrasons seuls, selon la concentration en nanoparticules et l'intensité des ultrasons. Par exemple, une réduction de 47,2 % du degré de surfusion de l'eau est obtenue à une concentration en nanoparticules de 0,2 % en poids et à une intensité ultrasonore de 0,69 W cm −2 (Fig. 4a), ce qui est supérieur à la réduction de 19,3 % causée par 0,2 % en poids d'Al2 O3 nanoparticules mais plus petites que la réduction de 52,1 % causée par 0,69 W cm −2 échographie (Fig. 3). La figure 5 montre les rapports du degré de surfusion pour la solidification de l'eau avec des nanoparticules et des ultrasons mutuellement à celui avec des ultrasons individuellement (R 4 = ΔT N-U /ΔT U ) à différentes concentrations de nanoparticules et intensités ultrasonores. Ce rapport de degré de surfusion R 4 de l'eau diminue avec l'augmentation de la concentration en nanoparticules et la diminution de l'intensité des ultrasons ; de plus, il est> 1 à de faibles concentrations de nanoparticules et à des intensités ultrasonores élevées et < 1 à des concentrations élevées de nanoparticules et à de faibles intensités ultrasonores.
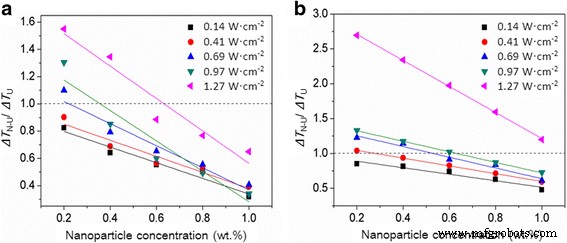
Comparaison des degrés de surfusion de l'eau contrôlés par les ultrasons et les nanoparticules mutuellement et séparément [a Al2 O3 nanoparticules, b SiO2 nanoparticules]. ΔT N-U /ΔT U représente le rapport du degré de surfusion requis pour la solidification de l'eau avec des nanoparticules et des ultrasons à celui avec des ultrasons
Dans cette étude, nous considérons que l'effet combiné des nanoparticules et des ultrasons est positif lorsque le rapport de degré de surfusion R 4 est < 1 et négatif lorsque le rapport de degré de surfusion R 4 est> 1. Les conditions de contrôle correspondantes pour ces deux situations sont affichées sur la figure 6. La figure montre une ligne de séparation rouge sur laquelle tous les rapports de degrés de surfusion R 4 d'eau sont égaux à 1. Dans la zone au-dessus de cette ligne de séparation (zone négative), tous les rapports de degré de surfusion R 4 sont> 1 ; dans la zone en dessous de la ligne de séparation (zone positive), tous les rapports de degrés de surfusion R 4 sont < 1. La concentration en nanoparticules et l'intensité ultrasonore correspondant au rapport de degré de surfusion R 4 de 1 sont définis comme la zone critique et l'intensité critique, respectivement. Apparemment, une correspondance biunivoque existe entre la concentration de nanoparticules et l'intensité des ultrasons ; c'est-à-dire qu'une concentration de nanoparticules plus élevée correspond à une intensité ultrasonore plus élevée sur la ligne de séparation. Lorsque la concentration de nanoparticules est inférieure à la concentration critique à une certaine intensité ultrasonore ou que l'intensité ultrasonore est supérieure à l'intensité critique à une certaine concentration de nanoparticules, le rapport de degré de surfusion R 4 d'eau tombera dans la zone négative, et inversement elle tombera dans la zone positive. De plus, la concentration critique de nanoparticules et l'intensité des ultrasons sont associées à l'angle de contact des nanoparticules. La comparaison de l'Al2 O3 et SiO2 nanoparticules montre que lorsque l'angle de contact des nanoparticules augmente, la ligne de séparation rouge de l'eau se déplace dans le sens d'une concentration élevée en nanoparticules et d'une faible intensité ultrasonore, conduisant à la contraction de la zone positive contrôlée par les nanoparticules et les ultrasons ensemble. Par exemple, le rapport de degré de surfusion contrôlé R 4 d'eau par SiO2 les nanoparticules sont situées dans la zone négative au lieu de la zone positive à la concentration de 0,4 % en poids de nanoparticules et à 0,69 W cm −2 intensité ultrasonore, comparée à celle contrôlée par Al2 O3 nanoparticules.
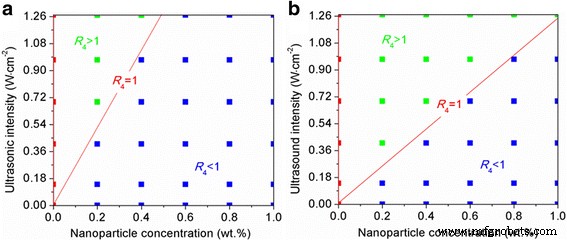
Un diagramme montrant les différents effets des ultrasons et des nanoparticules sur le degré de surfusion de l'eau [a Al2 O3 nanoparticules, b SiO2 nanoparticules]. Les points bleus, rouges et verts représentent que le degré de surfusion requis pour la solidification de l'eau avec des nanoparticules et des ultrasons est inférieur, égal et supérieur à celui des ultrasons individuellement, respectivement
Analyse de la nucléation de l'eau solidifiée sous l'effet combiné des nanoparticules et des ultrasons
Les changements de volume typiques de l'eau et de la suspension de nanoparticules mesurés dans les zones positives et négatives sont illustrés à la Fig. 7. Dans la zone négative, un grand changement de volume est clairement visible, alors qu'il est complètement absent dans la zone positive. A notre connaissance, deux processus, à savoir la diffusion rectifiée et la coalescence des bulles, sont impliqués dans le contrôle de la croissance des bulles de cavitation. La diffusion rectifiée fait référence à la croissance de bulles de cavitation en raison d'un transport de masse inégal à travers la paroi de la bulle pendant les cycles de raréfaction et de compression. Lors de la phase d'expansion de la bulle (raréfaction), les gaz qui se dissolvent dans l'eau diffusent dans la bulle; pendant ce temps, pendant la phase de compression de la bulle (effondrement), les gaz à l'intérieur de la bulle diffusent hors de celle-ci. La coalescence des bulles signifie que certaines bulles de cavitation plus petites fusionnent et forment une bulle plus grande. Contrairement aux bulles de cavitation formées par diffusion rectifiée, les bulles formées par coalescence de bulles ne subissent pas le cycle de cavitation et ne s'effondrent pas [28, 29]. Nous en déduisons donc que les bulles de cavitation dans les zones positives et négatives peuvent être formées par diffusion rectifiée et coalescence de bulles, respectivement. Dans cette étude, les stabilités de dispersion des nanoparticules pendant la solidification de l'eau dans les zones positives et négatives sont également étudiées, et les résultats corroborent l'inférence ci-dessus. Comme le montre la Fig. 7, le rapport d'absorbance (R 5 = A A /Un B ) de la suspension aqueuse d'Al2 O3 nanoparticules n'a pas de changement considérable dans la zone positive, alors que le rapport d'absorbance dans la zone négative est significativement réduit. Le A B et A A sont les valeurs d'absorbance de la suspension de nanoparticules avant et après le cycle de solidification/fusion, respectivement. Cette observation indique que la stabilité de dispersion des nanoparticules dans l'eau peut être maintenue dans la zone positive mais se détériore dans la zone négative. Dans cette étude, de gros agglomérats de nanoparticules apparaissent dans la zone négative, qui se déposeront rapidement lors du processus de fusion ultérieur. La bonne dispersion des nanoparticules dans la zone positive peut être attribuée à l'impact de jets cavitaires qui suivent l'effondrement des bulles de gaz formées par diffusion rectifiée; l'agrégation des nanoparticules dans la zone négative peut être due à l'adsorption des nanoparticules sur les grosses bulles de gaz formées par la coalescence des bulles. L'analyse ci-dessus sur les bulles de cavitation formées dans les zones positives et négatives est illustrée à la figure 8.
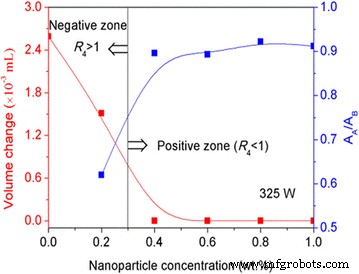
Variations de volume et d'absorbance de l'Al2 O3 suspension de nanoparticules causée par des ultrasons externes à différentes concentrations de nanoparticules
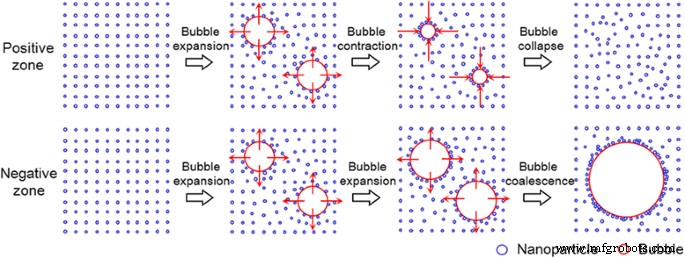
Un diagramme schématique montrant les bulles de cavitation formées dans les zones positives et négatives
Les nanoparticules et les bulles de cavitation peuvent agir comme agents de nucléation pour réduire le degré de surfusion de l'eau comme indiqué ci-dessus. Given that nanoparticles can absorb and scatter the ultrasound energy, the number and size of the bubbles should be decreased. As a result, the nucleating effect of cavitation bubbles possibly weakens in the presence of nanoparticles. Therefore, the superiority of using nanoparticles and ultrasound mutually over using them separately on water solidification depends on whether the nucleating effect of foreign nanoparticles can compensate for the weakened effect of cavitation bubbles. Our experiment results show that in the positive zone (R 4 < 1), the combined effect of nanoparticles and ultrasound is stronger than their respective effects but do not exceed the addition of these respective effects. This result suggests that the weakened effect of cavitation bubbles can be compensated in the positive zone. In the negative zone (R 4 > 1), the cavitation bubbles with large sizes are formed through bubble coalescence pathway, and they have strong adsorption to nanoparticles. Consequently, the combined effect of nanoparticles and bubbles weaken due to the reduction of the total number of the two nucleation sites. This result may be the reason why the required supercooling degree for the nanoparticle- and ultrasound-induced nucleation of water is higher than that induced by ultrasound alone at the same ultrasonic intensity in the negative zone.
Generally, a certain energy barrier has to be overcome to realize the conversion of rectified-diffusion-induced bubbles to bubble-coalescence-induced bubbles. Correspondingly, the rectified-diffusion-induced bubbles can be converted into the bubble-coalescence-induced bubbles by increasing the intensity of ultrasound to some extent. Furthermore, adding nanoparticles with water can favor the formation of rectified-diffusion-induced bubbles by adsorbing and reflecting some energy of ultrasound. In addition, the nanoparticles adjacent to the bubble wall have a shell effect because the cavitation bubbles are generally in the micron range, which is considerably larger than the nanoparticles [30]. The dispersed nanoparticles in water have charged surfaces, and the shell consisting of these nanoparticles should be charged accordingly. As shown in Fig. 1, the nanoparticle suspensions have relatively high zeta potentials. Hence, the coalescence of gas bubbles can be inhibited due to the electrostatic repulsion of the shell, according to the Derjaguin–Landau–Verwey–Overbeek theory [31]. The increase of nanoparticle concentration can certainly strengthen the absorption and shell effects of nanoparticles and thus contributes to the formation of rectified-diffusion-induced bubbles. In short, decreasing the ultrasonic intensity and increasing nanoparticle concentration can facilitate the formation of rectified-diffusion-induced bubbles. Consequently, the critical ultrasonic intensity corresponding to a high nanoparticle concentration, at which the rectified-diffusion-induced bubbles is converted into the bubble-coalescence-induced bubbles, should be higher than that corresponding to a low nanoparticle concentration. Thus, the critical nanoparticle concentration and ultrasonic intensity on the dividing line are positively correlated in this study (Fig. 6). The contact angle of nanoparticles is also proven to be an important factor influencing the ice nucleation of water controlled by nanoparticles and ultrasound. The critical nanoparticle concentration on the dividing line decreases, and the critical ultrasonic intensity increases with the decrease of the contact angle of nanoparticles (Fig. 6). This result may be attributed to the capability of nanoparticles with a small contact angle, which have a strong affinity for water, to be dispersed in the water more steadily and having a stronger shell effect on promoting the formation of rectified-diffusion-induced bubbles, compared with those nanoparticles with a large contact angle.
Conclusions
In this study, the solidification processes of water under the effects of nanoparticles and ultrasound are investigated mutually and separately. The foreign nanoparticles and cavitation bubbles can act as nucleation sites and promote the heterogeneous nucleation of water. Based on the type of cavitation bubbles generated through ultrasound, we divide water solidification into rectified-diffusion-driven and bubble-coalescence-driven solidification. In the rectified-diffusion-driven water solidification, the foreign nanoparticles can be uniformly dispersed in water exposed to an ultrasound field; thus, the water solidification aided by ultrasound and nanoparticles together can occur at a lower supercooling degree compared with that aided by ultrasound or nanoparticles alone due to the increase in the total number of nucleation sites. On the contrary, the adsorption of cavitation bubbles with large sizes for nanoparticles in the bubble-coalescence-driven water solidification leads to a decrease in the number of effective nucleation sites. As a result, a higher supercooling degree is needed for the water solidification assisted by nanoparticles and ultrasound together. In view of the requirements of low supercooling and high stability for the latent heat storage materials, using ultrasound and nanoparticles mutually is a better method of promoting the ice nucleation of water in the rectified-diffusion-driven solidification compared with using them separately, whereas the situation is reversed in the bubble-coalescence-driven water solidification.
The nanoparticle concentration, contact angle, and ultrasonic intensity are three important factors determining the type of the controlled water solidification by ultrasound and nanoparticles. The critical ultrasonic intensity and nanoparticle concentration, at which the required supercooling degrees for the water solidification assisted by nanoparticles and ultrasound mutually and separately are equal, are found to be positively related and affected by the contact angle of nanoparticles; that is, the critical ultrasonic intensity decreases and the critical nanoparticle concentration increases with the increase of the contact angle. The rectified-diffusion-driven water solidification exists in the zone where the ultrasonic intensity is lower and the nanoparticle concentration is higher than their critical values; otherwise, the bubble-coalescence-driven water solidification exists. Reducing the contact angle of nanoparticles can expand and contract the zones of rectified-diffusion-driven and bubble-coalescence-driven water solidification, respectively.
Abréviations
- TEM:
-
Microscope électronique à transmission
Nanomatériaux
- Fonctionnement du capteur de débit d'eau et ses applications
- Aquaponie contrôlée Raspberry Pi
- Nanoparticules pour le traitement du cancer :progrès actuels et défis
- Préparation et propriétés magnétiques des nanoparticules de spinelle FeMn2O4 dopées au cobalt
- Nanotechnologie :du système d'imagerie in Vivo à l'administration contrôlée de médicaments
- Propriétés de synthèse et de luminescence des nanoparticules hydrosolubles α-NaGdF4/β-NaYF4:Yb,Er Core–Shell
- Influence de la rigidité élastique et de l'adhérence de surface sur le rebond des nanoparticules
- Progrès récents dans les méthodes de synthèse et les applications des nanostructures d'argent
- Propriétés des nanoparticules d'oxyde de zinc et leur activité contre les microbes



