Détection photo-électrochimique améliorée de l'acide urique sur une électrode de carbone vitreuse modifiée par nanoparticules d'Au
Résumé
Dans ce travail, une méthode sensible et nouvelle pour la détermination de l'acide urique (UA) a été développée, dans laquelle l'électrode de carbone vitreux (GCE) a été modifiée avec des nanoparticules d'électrodéposition Au et utilisée pour surveiller la concentration d'UA avec l'assistant d'éclairage en lumière visible. . La morphologie des nanoparticules d'Au déposées sur la surface du GCE a été caractérisée par un microscope électronique à balayage (MEB) et les nanoparticules se sont avérées être des sphères bien dispersées avec un diamètre moyen approchant 26,1 nm. Une série de mesures de voltamétrie cyclique (CV) et de voltampérométrie différentielle (DPV) a révélé que l'introduction de lumière visible peut grandement améliorer à la fois la force et la stabilité du courant de réponse en raison de la résonance plasmonique de surface (SPR). Plus précisément, le DPV a montré une relation linéaire entre le courant de crête et la concentration en UA dans la plage de 2,8 à 57,5 μM avec l'équation de I pa (μA) = 0.0121c UA (μM) + 0.3122 (R 2 = 0.9987). Ici, la lumière visible éclairée Au/GCE possède un potentiel pour devenir un capteur électrochimique sensible à l'avenir.
Contexte
L'acide urique (UA) est l'un des produits terminaux du métabolisme des purines et est présent dans les fluides biologiques, tels que le sang et l'urine. Les anomalies des taux d'acide urique suggérant la possibilité de plusieurs maladies, telles que la goutte, les maladies rénales, l'hypertension et les maladies cardiovasculaires, qui sont associées à des taux élevés d'acide urique, alors qu'un taux réduit d'UA provoque des maladies comme la sclérose en plaques, la maladie de Parkinson, la maladie d'Alzheimer , et la névrite optique [1]. Par conséquent, la surveillance de la concentration d'UA dans les fluides corporels humains est cliniquement utile et importante pour la prévention des maladies susmentionnées ou d'autres maladies similaires.
Étant donné que la surveillance de la concentration d'acide urique dans les fluides corporels humains est d'une grande importance, diverses techniques de détection ont été développées selon les rapports précédents, telles que le dosage enzymatique [2, 3], la chromatographie liquide à haute performance (HPLC) [4], spectrométrie de masse [5], électrophorèse capillaire (EC) [6], chimiluminescence [7] et colorimétrie [8, 9]. Cependant, toutes ces méthodes traditionnelles peuvent nécessiter des prétraitements compliqués ou prendre trop de temps. En raison de l'activité électrochimique unique, l'acide urique peut être oxydé de manière irréversible en allantoïne en solution aqueuse, de sorte que de nombreuses recherches se sont concentrées sur la quantification de l'acide urique via des méthodes électrochimiques et les capteurs électrochimiques sont reconnus comme des alternatives prometteuses aux méthodes traditionnelles. Des recherches dans ce domaine ont vu le jour ces dernières années, et de nombreux nouveaux capteurs ont été conçus pour la détection de l'UA, tels que l'électrode modifiée en nanofibres de carbone chargées de nanoparticules de palladium (Pd/CNF-CPE) [10], l'électrode à liquide ionique au carbone (CILE ) [11], électrode modifiée par film hybride PtAu [12], électrode modifiée chitosan-graphène [13], etc. Des méthodes non enzymatiques ont été utilisées pour la détection électrochimique directe de l'UA, et le mécanisme a été démontré comme ci-dessous [14, 15 ] :
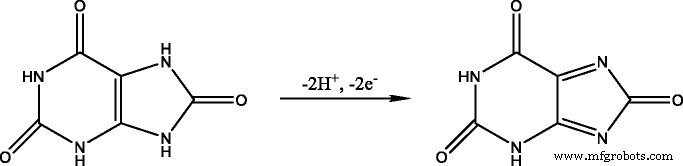
Malgré de nombreux efforts dans la détection de l'UA, les méthodes les plus sensibles, sélectives, stables et faciles doivent encore être explorées jusqu'à présent.
En raison des propriétés supérieures des aspects chimiques et physiques, de nombreux types de nanométaux, tels que l'argent (Ag) [16, 17], l'or (Au) [18, 19], le platine (Pt) [20,21,22, 23], le cuivre (Cu) [24, 25] et le palladium (Pd) [26, 27] ont accéléré de nombreuses recherches dans la fabrication de capteurs électrochimiques pour l'analyse médicale, la surveillance environnementale, le contrôle de la qualité des aliments, etc. [28]. En particulier, les nanoparticules d'or (AuNPs) montrent la supériorité de la conductivité, une grande surface et une bonne biocompatibilité [29] et toutes ces propriétés uniques font des AuNPs un choix approprié pour la détection électrochimique. En outre, l'effet unique de résonance plasmonique de surface (SPR) de l'Au pour la récolte de la lumière visible via l'oscillation cohérente collective des électrons de surface peut être bénéfique pour la grande amélioration de la détection de l'UA [30].
Sur la base des analyses ci-dessus, nous avons démontré ici une méthode d'électrodéposition facile pour fabriquer avec succès des AuNPs en forme de sphère bien dispersés sur la surface de l'électrode de carbone vitreux (GCE). De plus, une série de mesures électrochimiques ont révélé que le fascinant Au/GCE présentait une intensité de courant de réponse considérablement améliorée avec l'aide d'une irradiation de lumière visible. Compte tenu de ceux-ci, nous avons pensé que cette méthode facile assistée par la lumière visible et les nanoparticules d'Au sphériques éclairaient l'application dans la détection plus poussée de l'UA et au-delà.
Méthodes
Appareil
Le microscope électronique à balayage (MEB) (Hitachi SU8010, Japon) a été utilisé pour caractériser la morphologie de l'électrode obtenue. Toutes les études électrochimiques ont été réalisées sur un poste de travail électrochimique CHI760D (Chenhua Instrument Co., Ltd., Shanghai. Chine) avec un système conventionnel à trois électrodes où l'électrode de carbone vitreux modifiée (GCE) a agi comme électrode de travail (surface 0,07 cm 2 ), un fil de platine servait de contre-électrode (diamètre 0,5 mm) et une électrode au calomel saturé (SCE) servait d'électrode de référence, respectivement. La valeur du pH de la solution a été déterminée par un appareil de mesure modèle pHS-2F (Instrument, Shanghai, Chine).
Réactifs
L'acide urique (UA) a été acheté chez Acros Organics (Shanghai, Chine). Acide chloroaurique (HAuCl4 ·H2 O), hydrogénophosphate disodique (Na2 HPO4 ), le dihydrogénophosphate de sodium (NaH2 Bon de commande4 ), ferrocyanure de potassium (K4 [Fe(CN)6 ]), ferricyanure de potassium (K3 [Fe(CN)6 ]) et du chlorure de potassium (KCl) ont été obtenus auprès de Sinopharm Chemicals Reagent Co., Ltd.. De l'eau bidistillée a été utilisée tout au long des expériences. Une solution tampon phosphate (PBS) 0,1 M nouvellement préparée de pH différent a été choisie pour être l'électrolyte. Tous les réactifs ont été utilisés tels quels sans autre purification, et toutes les expériences ont été réalisées à température ambiante.
Préparation des électrodes
Dans ce travail, nous avons choisi une électrode de carbone vitreux de type L pour la commodité d'exposer la surface modifiée avec des nanoparticules d'Au à un éclairage de lumière visible. Le GCE (surface 0,07 cm 2 ) a été soigneusement poli avec une suspension d'alumine de 0,05 μm sur un chiffon de polissage humide, suivi d'une ultrasonication dans de l'éthanol et de l'eau pendant plusieurs minutes pour obtenir une surface semblable à un miroir. Enfin, l'électrode a été rincée abondamment avec de l'eau distillée secondaire et séchée à l'air. Avant le processus électrochimique de suivi, nous avons poli et rincé l'électrode à plusieurs reprises jusqu'à ce que les courbes voltamétriques cycliques (CV) dans 2,5 mM Fe(CN)6 3/4− + 0,1 M de solution de KCl présentent deux pics parfaitement symétriques et la séparation de potentiel de pic (ΔE p ) d'entre eux était inférieur à 100 mV. Des nanoparticules d'Au ont été électrodéposées sur la surface des électrodes prétraitées dans 1 mM H3 Bon de commande4 solution contenant 0,24 mM HAuCl4 à un potentiel constant de -0,2 V. Différentes charges de masse d'AuNP ont été contrôlées en modifiant la quantité électrique au cours du processus de dépôt.
Résultats et discussion
Morphologie et caractérisation de l'électrode
Le microscope électronique à balayage (MEB) a été utilisé pour caractériser la morphologie des nanoparticules d'Au à la surface de GCE. Les nanoparticules d'Au se sont formées à un potentiel constant de -0,2 V avec une certaine quantité électrique de 3 × 10 −3 C, et la densité théorique des particules d'Au sur la surface du GCE a été calculée à 28,9 μg/cm 2 . La figure 1a montre que la surface du GCE est densément recouverte de nanoparticules d'or en forme de points. La figure 1b présente la morphologie de la surface à un grossissement plus élevé et montre que les AuNPs moelleuses et sphériques se dispersent uniformément à la surface de la GCE. L'histogramme de distribution granulométrique représenté dans l'encart de la figure 1b a révélé que les AuNPs bien dispersées ont une distribution granulométrique étroite et que le diamètre moyen calculé était d'environ 26,1 nm. Une observation détaillée peut également nous aider à découvrir que les AuNP tels qu'ils sont obtenus sont presque monodispersés, ce qui montre moins de connexions les unes avec les autres. Dans l'ensemble, ces conditions favorables ont permis d'augmenter considérablement la surface active et, à terme, d'améliorer l'efficacité de la détection.

Images SEM de Au/GCE à plus bas (a ) et un grossissement supérieur (b ). Encart :histogramme de distribution de taille des nanoparticules Au correspondant
Comportements Voltamétriques Cycliques
Après modification par Au, CV en 2,5 mM Fe(CN)6 3/4− + 0,1 M de solution de KCl a été prise pour comparer avec le GCE nu (Fichier supplémentaire 1 :Figure S1). La courbe CV de Au/GCE montre une paire de pics redox symétriques, présentant un courant de réponse plus élevé et une séparation de potentiel de pic plus petite (ΔE p = 63 mV) que celui du GCE nu. D'après les données ci-dessus, nous pouvons conclure que le transfert d'électrons sur Au/GCE était meilleur que celui sur GCE nu.
La figure 2 montre les courbes CV de Au/GCE dans une solution de PBS 0,1 M (pH 7,0) contenant 1,0 mM d'UA avec (a) et sans (b) éclairage en lumière visible pour quatre cercles, respectivement. Nous avons constaté que lorsque la distance entre la lampe au xénon et la surface de l'électrode de travail est fixée à 20 cm, l'intensité lumineuse visible la plus puissante serait présentée. En détail, le courant de crête anodique pour l'UA était de 20 μA sous l'éclairage en lumière visible, tandis que le maximum du courant de crête anodique sans éclairage en lumière visible n'était que de 12 μA. De plus, avec la présence de lumière visible, le courant de crête maintenait une valeur stable; néanmoins, la valeur du courant de crête a montré une déclinaison continue sans éclairage en lumière visible. En outre, le potentiel de pic d'oxydation de Au/GCE sous un éclairage en lumière visible est d'environ 6 mV négatif par rapport à celui sans éclairage en lumière visible. À partir des enquêtes ci-dessus, nous pouvons conclure que la lumière visible peut améliorer les performances photo-électrocatalytiques de Au/GCE vis-à-vis de l'électrooxydation de l'UA.
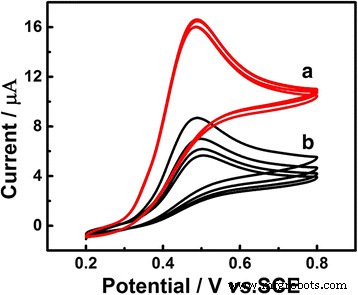
CV de Au/GCE dans une solution de PBS 0,1 M (pH 7,0) contenant 1,0 mM d'UA avec (a) et sans (b) éclairage en lumière visible. Taux de balayage 50 mV s −1
Effet de l'éclairage en lumière visible
L'influence de l'éclairement en lumière visible a été étudiée en ajoutant l'éclairement en lumière visible à un certain moment dans le processus d'une voltamétrie cyclique successive. Comme le montre la figure 3a, la lumière visible a commencé à partir de l'endroit où pointe la flèche. La courbe 1 était le dernier tour des CV sans éclairage en lumière visible. La courbe 2 était le processus de transition, dans lequel l'éclairage de la lumière visible a commencé à partir du potentiel d'environ 0,35 V, où le courant a commencé à augmenter théoriquement selon la Fig. 2. Lorsque l'électrode est exposée à l'éclairage de la lumière visible, le courant a présenté un tendance ascendante, et la courbe CV de la section de balayage inversé chevauche presque la courbe sous l'éclairage de la lumière visible. La courbe CV sous un éclairage complet de la lumière visible a été présentée comme la courbe 3, comme indiqué ci-dessus, le courant s'est toujours maintenu de manière constante. La figure 3b montre la réponse photocourante de Au/GCE sous un éclairage en lumière visible dans une solution de 0,1 M de PBS (pH 7,0) contenant 1,0 mM d'UA au potentiel de 0,48 V, auquel le courant atteint son maximum sur la figure 2. Les photocourants du les électrodes telles que préparées ont été suivies par le courant-temps (I –t ) courbes. Afin de comparer les conditions de lumière et d'absence de lumière pour la détection UA, nous avons interrompu périodiquement l'éclairage de la lampe Xe. On peut constater que pendant que l'éclairage était interrompu, le photocourant a chuté instantanément et le photocourant a augmenté rapidement lorsque l'éclairage a été allumé, puis a atteint la valeur d'équilibre en peu de temps. La périodicité parfaite démontrée dans l'image indiquait que la réponse à l'éclairage de la lumière visible est constante et que le temps requis pour la réponse est égal. L'effet de résonance plasmonique de surface (SPR) des nanoparticules d'Au sous l'éclairage de la lumière visible peut expliquer l'augmentation du photocourant d'Au/GCE d'un côté. La spectroscopie UV-vis des AuNPs telles que préparées a été montrée dans le fichier supplémentaire 1 :Figure S2. Le pic d'absorption était situé à la longueur d'onde de 597 nm, ce qui est approximatif à la longueur d'onde de certains rapports précédents [31, 32]. Dans le détail, les nanoparticules d'Au pourraient récolter l'énergie de la lumière visible [33]. En raison de l'excitation SPR, l'accumulation d'électrons chauds peut occuper de manière transitoire les états vides supérieurs au-dessus du niveau de Fermi, puis un transfert rapide d'électrons de Au à GCE conducteur se produit [34]. Le processus d'oxydation de l'UA a lieu à la surface des nanoparticules d'Au, où la molécule d'UA transfère deux électrons à la nanoparticule d'Au. D'un autre côté, après avoir été modifié avec des nanoparticules d'Au, le taux de transfert d'électrons a été grandement favorisé.
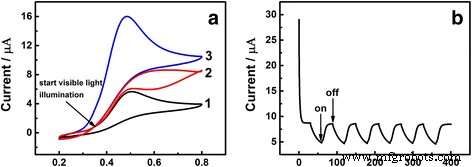
un Potentiel/V vs.SCE. Le CV de Au/GCE dans une solution 0,1 M de PBS (pH 7,0) contenant 1,0 mM d'UA sans (1) et avec (3) éclairage en lumière visible; l'éclairage en lumière visible commence à l'endroit où la flèche pointe (2) . Taux de balayage 50 mV s −1 . b Fois. Réponse photocourante de Au/GCE sous un éclairage en lumière visible dans une solution de 0,1 M de PBS (pH 7,0) contenant 1,0 mM d'UA à 0,48 V. L'éclairage d'une lampe Xe a été interrompu toutes les 30 s
Effet de la quantité d'or
La charge massique d'Au déposé sur la surface de l'électrode a été contrôlée par la quantité électrique, et son influence sur les performances électrochimiques vis-à-vis de l'UA a été évaluée. Comme on peut le voir sur la Fig. 4, lorsque la quantité d'or n'est que de 0,96 μg/cm 2 (Fig. 4e), le courant de crête était presque le même que celui du GCE nu (Fig. 4f), voire une légère baisse. Cependant, comme la quantité d'or passait de 4,8 à 28,9 μg/cm 2 (Fig. 4 (d), (c) et (b)), le courant de crête a augmenté successivement et le potentiel de crête d'oxydation était plus négatif. Continuez à augmenter la quantité d'or à 57,8 μg/cm 2 (Fig. 4a), le courant de crête a manifesté une légère diminution et le potentiel de crête est devenu plus positif. Cela est principalement dû au fait que la qualité de 28,9 μg/cm 2 est la surface la mieux adaptée pour la réaction UA sur Au/GCE. En premier lieu, le GCE nu ou les nanoparticules à faible teneur en Au recouvertes de GCE ne peuvent pas supporter suffisamment de sites d'activité et ont une surface spécifique insuffisante pour la réaction. Pendant ce temps, le GCE, qui est recouvert d'un excès de nanoparticules d'Au, ralentira la vitesse de transfert d'électrons de Au/GCE vers UA. Par conséquent, nous avons choisi l'Au/GCE avec une quantité d'or de 28,9 μg/cm 2 comme électrode de travail dans le processus de détection électrochimique.
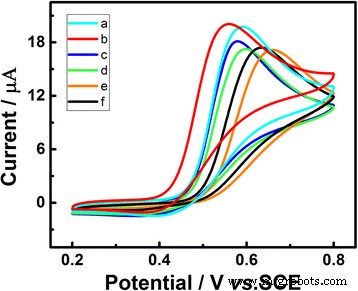
CV d'Au/GCE électrodéposé avec différentes quantités d'or :57,8 (a) , 28,9 (b) , 9.6 (c) , 4.8 (d) , 0,96 μg/cm 2 (e) , et nue GCE (f) dans une solution de PBS 0,1 M (pH 7,0) contenant 1,0 mM d'UA sous un éclairage en lumière visible. Taux de balayage 50 mV s −1 . Potentiel de dépôt -0,2 V
Effet de la valeur du pH
Pour évaluer davantage les conditions optimales pour la détection de l'UA, l'influence de la valeur du pH sur les réponses photo-électrochimiques de 1 mM d'UA sous un éclairage en lumière visible a été étudiée. La figure 5a décrit les CV de Au/GCE dans une solution d'UA 1 mM, et du PBS 0,1 M a été utilisé pour moduler le pH de chaque liquide de test. La figure 5b montre la relation entre la valeur du pH et le courant de crête, à partir de laquelle nous pouvons voir la valeur maximale de I pa est apparu à un pH de 7,0 et a ensuite diminué avec l'augmentation du pH de 7,0 à 9,0, ce qui a prouvé que le pH 7,0 est la valeur de pH optimale pour la détection de l'UA.
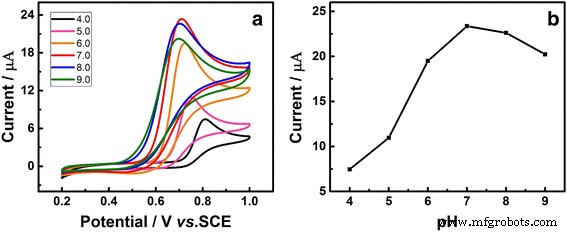
un CV de l'Au/GCE dans 1 mM UA avec différentes solutions de PBS à pH (pH = 4,0, 5,0, 6,0, 7,0, 8,0 et 9,0), vitesse de balayage 50 mV s −1 . b Relation entre le courant de pic d'oxydation et la valeur du pH
Effet du taux de numérisation
Pour étudier comment la vitesse de balayage influence la réponse électrochimique de Au/GCE dans une solution d'UA, les CV ont été exploités sous différentes vitesses de balayage de 20 à 200 mV s −1 avec un intervalle de 20 mV s −1 . Les résultats ont été présentés sur la figure 6, à partir de laquelle nous pouvons voir un décalage positif évident du potentiel de pic d'oxydation en tant qu'accélération de la vitesse de balayage, indiquant que la réaction de l'UA sur la surface de l'électrode est un processus chimique quasi-réversible. En d'autres termes, l'adsorption de l'UA ne s'est pas produite à la surface de l'électrode dans une solution de PBS 0,1 M (pH 7,0). De plus, une corrélation linéaire entre les courants de crête anodiques et la racine carrée des taux de balayage a été facilement trouvée et l'équation d'étalonnage est présente sous la forme I pa (μA) = 1.9254ν 1/2 (mV/s) 1/2 + 9.3766 (R 2 = 0.9702), indiquant que la vitesse de réaction a été déterminée par la diffusion de l'UA [35].
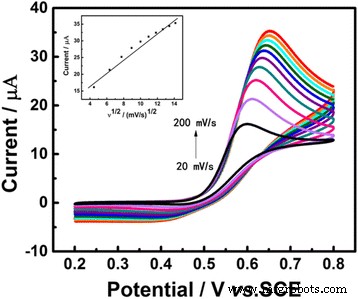
CV de l'Au/GCE dans une solution de 0,1 M de PBS (pH = 7,0) contenant 1 mM d'UA à des vitesses de balayage allant de 20 à 200 mV s −1 . Encart :courbe d'étalonnage du courant de crête en fonction de v 1/2
Détermination de l'UA
La voltamétrie différentielle à impulsions (DPV), avec les caractéristiques d'une meilleure résolution et d'une sensibilité plus élevée que CV, a également été utilisée pour la caractérisation de Au/GCE. Il y avait une relation proportionnelle entre le courant de pic d'oxydation et la concentration en UA dans la plage de 2,8 à 57,5 μM (Fig. 7). L'équation de régression linéaire peut être exprimée sous la forme I pa (μA) = 0.0121c UA (μM) + 0.3122 (R 2 = 0.9987). À titre de comparaison, l'analyse DPV de Au/GCE vers UA sans éclairage par la lumière visible a été présentée dans le fichier supplémentaire 1 :Figure S3, qui présentait une plage linéaire plus étroite de 3 à 21 μM avec l'équation de régression linéaire représentée par I pa (μA) = 0,0112c UA (μM) + 0,2766 (R 2 = 0.9943). Toutes les expériences de cette section ont été menées dans les meilleures conditions obtenues à partir des données expérimentales précédentes. La réutilisabilité de Au/GCE a été estimée en mesurant les réponses CV de huit électrodes dans une solution de PBS 0,1 M (pH 7,0) contenant 1,0 mM d'UA sous un éclairage en lumière visible dans les mêmes conditions. L'écart type relatif des courants de pic d'oxydation est de 7,88 %. La stabilité de Au/GCE sous éclairage visible a également été vérifiée en réalisant l'électrode modifiée qui a été stockée une semaine à 25°C avant l'expérience. Les courants de pointe ont diminué de 9,8 %. Ces résultats ci-dessus indiquent que l'électrode modifiée avec éclairage en lumière visible présente une bonne réutilisabilité et une bonne stabilité. Et cette méthode pourrait tolérer les interférences générales. Dans l'analyse de l'échantillon réel, une récupération de 96,3 % a été obtenue. À partir des recherches ci-dessus, nous pourrions conclure que la lumière visible illuminée Au/GCE montre un potentiel pour être un capteur électrochimique sensible à l'avenir.
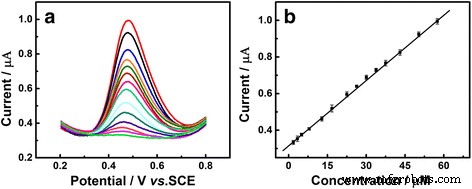
un Courbes DPV de l'Au/GCE dans du PBS 0,1 M (pH 7,0) à différentes concentrations d'UA. b Graphiques des courants de crête anodiques en fonction de la concentration d'UA
Conclusions
En résumé, des nanoparticules d'Au sphériques homogènes ont été simplement modifiées à la surface de GCE avec une électrodéposition à potentiel constant. Les images SEM et l'histogramme de distribution de taille ont révélé que les AuNPs bien dispersées avaient une distribution de taille étroite et que le diamètre moyen était de 26,1 nm. Cela peut être conducteur pour augmenter considérablement la surface active et finalement conduire à l'amélioration de l'efficacité de détection. Les résultats électroanalytiques de l'Au/GCE tel que préparé sous un éclairage en lumière visible ont montré une supériorité évidente par rapport à un éclairage en lumière non visible en raison de la résonance plasma de surface (SPR). De plus, cette étude présente une méthode simple et facile pour détecter la concentration d'acide urique, qui a le potentiel d'être appliquée dans la surveillance d'autres substances biologiques.
Abréviations
- AuNP :
-
Nanoparticules d'or
- CE :
-
Électrophorèse capillaire
- CV :
-
Voltamétrie cyclique
- DPV :
-
Voltamétrie différentielle à impulsions
- GCE :
-
Electrode de carbone vitreux
- HPLC :
-
Chromatographie liquide haute performance
- SEM :
-
Microscope électronique à balayage
- SPR :
-
Résonance plasmonique de surface
- UA :
-
Acide urique
Nanomatériaux
- Les nanotubes de carbone repoussent les limites de l'électronique flexible
- Ocean Carbon imagé à l'échelle atomique
- Les avantages d'une prothèse en fibre de carbone
- Nanodots de carbone comme nanocapteurs bimode pour la détection sélective du peroxyde d'hydrogène
- Formation et propriétés luminescentes de nanocomposites Al2O3:SiOC à base de nanoparticules d'alumine modifiées par le phényltriméthoxysilane
- Biocapteur ultrasensible pour la détection de l'ADN de Vibrio cholerae avec des nanosphères composites polystyrène-acide acrylique
- Stabilité améliorée des nanoparticules magnétiques d'or avec du poly(acide 4-styrènesulfonique-co-acide maléique) :propriétés optiques adaptées pour la détection des protéines
- La préparation de la nanostructure jaune-enveloppe Au@TiO2 et ses applications pour la dégradation et la détection du bleu de méthylène
- Effets synergiques des nanoparticules d'Ag/BiV1-xMoxO4 avec une activité photocatalytique améliorée



