Technologies de capture et de stockage du carbone
Technologies de capture et de stockage du carbone
La capture et le stockage du carbone, également appelés séquestration (CSC), impliquent la capture, le transport, l'injection et le confinement du CO2 (dioxyde de carbone) dans des structures géologiques telles que des réservoirs de pétrole et de gaz épuisés, des aquifères salins terrestres et offshore situés profondément dans la croûte terrestre, des cavernes de sel ou des gisements de charbon inexploitables. Il s'agit à la fois d'une approche pour améliorer la production des opérations pétrolières et gazières existantes et d'un moyen de réduire les émissions de gaz à effet de serre (GES).
Le CSC offre une alternative supplémentaire dans l'utilisation de l'énergie à base de combustibles fossiles, tout en offrant un temps de transition supplémentaire pour que les systèmes énergétiques évoluent vers des combustibles à carbone (C) réduit ou sans C, tels que les énergies renouvelables. Le CSC présente un certain nombre d'avantages économiques et sociaux tels que (i) la réduction des émissions de CO2 dans l'atmosphère, atténuant ainsi potentiellement les changements climatiques dangereux, (ii) l'innovation, l'accès aux technologies de pointe, la création d'emplois et la un développement économique continu et plus durable, (iii) une source de revenus secondaire, car les émissions de GES qui sont captées et stockées peuvent être converties en une marchandise commercialisable qui peut être vendue sur le marché international, (iv) la réduction de la pollution de l'air car les polluants potentiellement nocifs ont à retirer pour permettre le captage du CO2 et la possibilité d'une récupération améliorée du pétrole et du gaz.
Il existe plusieurs défis pour le déploiement du CCS. Certains des défis pour le CSC comprennent (i) la réduction du coût de la capture et l'intensification des processus de capture, (ii) l'identification de l'impact environnemental de la capture, (iii) la détermination des implications de l'accumulation de pression dans une formation de stockage, (iv ) déterminer où l'eau déplacée va dans une injection à grande échelle et quel est le risque pour les eaux souterraines, (v) comment prédire de manière fiable la taille du panache de CO2 et où il migre, (vi) comment gagner en confiance dans la sélection du site, (vii) développer des stratégies de surveillance et des limites de détection rentables, (viii) impliquer les industries de la finance et de l'assurance, (ix) une plus grande certitude réglementaire et politique à tous les niveaux de gouvernement, (x) former une main-d'œuvre pour un déploiement à grande échelle, et (xi) améliorer la sensibilisation et l'acceptation du public.
Les technologies CSC peuvent être appliquées aux processus à émissions à grande échelle, y compris la production d'électricité au charbon et au gaz, le traitement du gaz naturel et la production d'engrais, ainsi que la fabrication de matériaux industriels tels que le fer et l'acier, le ciment et les pâtes et papiers. etc. L'application des technologies CSC à ces processus peut jouer un rôle majeur dans la réduction des émissions de GES. Les technologies de séparation et de capture du carbone sont opérationnelles à grande échelle dans les industries du gaz naturel et des engrais depuis des décennies. Les technologies impliquées dans un système CSC ont quatre composants, à savoir (i) la capture, (ii) le transport, (iii) l'injection et (iv) la surveillance.
Le captage est la séparation du CO2 d'un flux d'effluents et sa compression à un état liquide ou supercritique. Dans la plupart des cas aujourd'hui, la concentration de CO2 qui en résulte est supérieure à 99 %, bien que des concentrations plus faibles puissent être acceptables. Le captage est normalement nécessaire pour pouvoir transporter et stocker le CO2 de manière économique.
Le transport consiste en l'acheminement du CO2 de sa source vers le réservoir de stockage. Le CO2 est séché et généralement comprimé avant d'être transporté vers le stockage. La compression rend le transport du gaz plus efficace. Le CO2 est utilisé commercialement dans un certain nombre d'industries, notamment l'industrie des boissons, et il a été transporté à grande échelle pour être utilisé dans la récupération du pétrole des réservoirs (récupération assistée du pétrole). Bien que le transport par camion, train et bateau soit possible, le transport de grandes quantités de CO2 est le plus économiquement réalisé avec un pipeline. Une infrastructure de pipeline majeure doit être construite pour mettre en œuvre le CSC à grande échelle, et cela présente des défis.
L'injection consiste à déposer du CO2 dans le réservoir de stockage. Les réservoirs souterrains de stockage dépendent des formations géologiques. La sécurité du stockage du CO2 est primordiale. Les risques locaux liés au stockage du CO2 comprennent (i) les fuites de CO2 du lieu de stockage, (ii) l'altération de la chimie du sol et de l'eau potable, et (iii) le déplacement de fluides potentiellement dangereux qui peuvent se trouver dans le réservoir où le CO2 est stocké. Les réservoirs potentiels comprennent l'océan profond, les sédiments océaniques ou la minéralisation (conversion du CO2 en minéraux). Bien qu'une certaine utilisation commerciale du CO2 soit possible, la quantité pouvant être utilisée par rapport à la quantité de CO2 émise est très faible.
Une fois le CO2 injecté, le site de stockage doit être surveillé pour montrer que le CO2 reste dans le réservoir. Le CO2 n'est ni toxique ni inflammable, il ne pose donc qu'un risque minime pour l'environnement, la santé et la sécurité. L'objectif principal de la surveillance est de s'assurer que l'opération de séquestration est efficace, c'est-à-dire que la quasi-totalité du CO2 reste hors de l'atmosphère pendant des siècles. Le programme de surveillance commence avant l'injection pour établir les données de base. La surveillance pendant la phase d'exploitation consiste à enregistrer le comportement dynamique du CO2 lors de son injection et dans le réservoir. Après l'arrêt de l'injection, le programme de surveillance doit être conçu pour s'assurer que le stockage de CO2 répond aux conditions environnementales et de sécurité requises. Un programme de surveillance couvre trois domaines de surveillance, à savoir (i) le domaine souterrain (le réservoir), (ii) le domaine proche de la surface (zones peu profondes et sol) et (iii) le domaine atmosphérique, y compris les puits, les failles et autres caractéristiques géologiques.
Technologies de captage du CO2
Le CO2 peut être capturé à partir de grandes sources d'émission fixes, telles que les installations de production de gaz naturel (où le CO2 est déjà séparé des autres gaz, dans le cadre du processus), les centrales électriques à combustible fossile, les usines sidérurgiques, les cimenteries et certaines usines chimiques. . Contrairement aux deux autres composants du CSC, le transport et le stockage géologique, le premier composant du CSC, à savoir la capture du CO2, dépend presque entièrement de la technologie et est l'étape la plus coûteuse. La technologie permettant de capturer le CO2 de ces sources est en cours d'adaptation de la technologie de séparation du CO2 actuellement utilisée dans des industries telles que l'industrie du gaz naturel et la production d'ammoniac (NH3) ainsi que de la technologie utilisée dans l'industrie de la séparation de l'air. De nouvelles technologies sont également en cours de développement.
Les principales technologies de séparation pour capturer le CO2 sont actuellement (i) l'utilisation d'un solvant liquide pour absorber le CO2 (absorption), (ii) l'utilisation de matériaux solides pour attirer le CO2 à la surface, où il se sépare des autres gaz (adsorption), et (iii) en utilisant des membranes pour séparer le CO2 des autres gaz. D'autres technologies incluent la technologie de boucle chimique (un oxyde métallique réagit avec le carburant, créant des particules métalliques, du CO2 et de la vapeur d'eau), des procédés de séparation à basse température ou cryogéniques (qui reposent sur différentes températures de changement de phase pour divers gaz pour les séparer) et un solide régénérable sec processus.
Les principales technologies concurrentes pour le captage du CO2 provenant de l'utilisation de combustibles fossiles sont (i) le captage post-combustion (PCC) à partir des gaz de combustion des centrales à combustion, (ii) le captage pré-combustion à partir du gaz de synthèse dans les centrales à gazéification, et (iii) le captage oxy combustion par combustion directe du carburant avec de l'oxygène. La plupart des processus de combustion actuels utilisent de l'air et les gaz de combustion qui en résultent contiennent généralement de faibles concentrations de CO2 (moins de 20 %). Ils sont donc plus adaptés aux technologies de captage post-combustion
Technologies de capture post-combustion
Le captage post-combustion peut être considéré comme une forme d'épuration des gaz de combustion. Le processus est ajouté à l'arrière de l'usine, après les autres systèmes de contrôle de la pollution. L'intégration de la chaleur avec l'usine est nécessaire pour qu'elle soit rentable.
L'Electric Power Research Institute (EPRI) a déterminé en 2009 qu'il existe plus de 50 concepts de capture de CO2 post-combustion en cours de développement qui peuvent être regroupés en plusieurs types de processus physiques/chimiques. Ces groupes de types de processus sont (i) absorption chimique, (ii) adsorption, (iii) membranes, (iv) biologique et (v) autres. Chacun de ces différents groupes présente des avantages et des inconvénients différents, ainsi qu'une applicabilité dans différentes situations. Il y a des développements considérables en ce qui concerne les deux premiers groupes.
Procédé d'absorption chimique – Il s'agit d'une ou plusieurs réactions chimiques réversibles entre le CO2 et une solution aqueuse d'un absorbant, tel qu'un solvant à base de mono-éthanol-amine (MEA), et des amines de haute performance (méthyldiéthanolamine activée, aMDEA) etc. Lors du chauffage du produit, la liaison entre l'absorbant et le CO2 peut être rompue, produisant un flux enrichi en CO2. Le processus d'absorption chimique pour séparer le CO2 des gaz de combustion est emprunté à l'industrie de traitement du gaz. Les procédés à base d'amines sont utilisés dans le commerce pour éliminer les impuretés des gaz acides (CO2 et H2S) des flux de gaz de procédé. C'est donc une technologie éprouvée et bien connue.
La formule de la mono-éthanol-amine est H2NCH2CH2OH. L'amine est un groupe de composés organiques, qui peuvent être considérés comme dérivés de l'ammoniac (NH3) par remplacement d'un ou plusieurs atomes H2 par des radicaux organiques. Les groupes de substitution (R) peuvent être alkyle, aryle ou aralykle. Lorsque le (R) est un alkyle, l'amine est appelée alcanolamine. En général, on peut considérer qu'un groupe hydroxyle sert à réduire la pression de vapeur et à augmenter la solubilité dans l'eau, tandis que le groupe amino fournit l'alcalinité nécessaire en solution aqueuse pour absorber les gaz acides. Les akanolamines éliminent le CO2 des flux de gaz résiduaires par une réaction exothermique du CO2 avec la fonctionnalité amine de l'alcanolamine. Les amines d'intérêt commercial pour capter le CO2 sont hydrosolubles.
Les amines sont classées selon le nombre d'atomes H2 de l'ammoniac qui ont été remplacés par des radicaux tels que (i) amine primaire (RNH2) où un atome H2 a été remplacé, (ii) amine secondaire (R2NH) où deux atomes H2 ont été remplacés. remplacé, et (iii) une amine tertiaire (R3N) où les trois atomes H2 ont été remplacés.
Les amines primaires comprennent la monoéthanolamine (MEA) et la diglycolamine (DGA). Le MEA est le solvant traditionnel de choix pour l'absorption du CO2 et l'élimination des gaz acides en général. La MEA est la moins chère des alcanolamines. Sa cinétique de réaction est rapide et il fonctionne bien à basse pression, et à faible concentration en CO2. Cependant, il y a plusieurs inconvénients.
Premièrement, il a une chaleur de réaction élevée avec le CO2, ce qui signifie qu'un niveau élevé d'énergie doit être fourni lors de l'étape de régénération. Deuxièmement, l'absorptivité du MEA avec le CO2 n'est pas élevée. Dans le cas des alcanolamines primaires et secondaires, la formation de carbamate (RNHCOO-) est la réaction principale. L'équation de la réaction est CO2 + 2RNH2 =RNHCOO- + RNH3+. Dans cette réaction, deux moles de MEA doivent être utilisées pour capturer une mole de CO2. Troisièmement, la pleine capacité d'absorption supérieure du MEA n'est pas réalisée en pratique en raison de problèmes de corrosion. L'effet de corrosion est dû au CO2 dissous et varie selon les amines utilisées.
La concentration de MEA dans la phase aqueuse en présence d'O2 est limitée à 20 % en poids. De plus, la MEA a la pression de vapeur la plus élevée de toutes les alcanolamines et un fort transfert de solvant peut se produire lors de l'élimination du CO2 du flux gazeux et lors de l'étape de régénération. Pour réduire les pertes de solvant, un lavage à l'eau du flux gazeux purifié est généralement nécessaire. De plus, le MEA réagit de manière irréversible avec des impuretés mineures telles que le COS et le CS2, entraînant une dégradation du solvant. Le moussage du liquide absorbant MEA dû à l'accumulation d'impuretés peut également être un problème.
Pour les systèmes d'absorption MEA actuels, les taux d'adsorption et de désorption sont raisonnablement élevés, d'où une bonne cinétique de réaction. Cependant, le garnissage dans l'absorbeur (contacteurs, pour faciliter un transfert de masse efficace) représente un coût important, et sa consommation d'énergie est également importante pour le captage du CO2 des fumées. De plus, la température de décapage ne doit pas être trop élevée (autour de 150°C). Sinon, une dimérisation du carbamate peut avoir lieu, détériorant la capacité d'absorption du MEA.
Les amines secondaires comprennent la diéthanolamine (DEA) et la di-isopropylamine (DIPA). Les amines secondaires présentent des avantages par rapport aux amines primaires. Leur chaleur de réaction avec le CO2 est plus faible (360 calories/gramme) contre 455 calories/gramme) pour les amines primaires. Cela signifie que les amines secondaires nécessitent moins de chaleur dans l'étape de régénération que les amines primaires. Cependant, il a tous les autres problèmes des amines primaires.
Les amines tertiaires comprennent la triéthanolamine (TEA) et la méthyl-diéthanolamine (MDEA). Les amines tertiaires réagissent plus lentement avec le CO2 que les amines primaires et secondaires nécessitent donc un taux de circulation de liquide plus élevé pour éliminer le CO2 par rapport aux amines primaires et secondaires. Ceci peut être amélioré par l'utilisation de promoteurs. Un avantage majeur des amines tertiaires est leurs besoins en chaleur plus faibles pour la libération de CO2 à partir du solvant contenant du CO2. Les amines tertiaires ont moins tendance à former des produits de dégradation lors de l'utilisation que les amines primaires et secondaires, et sont plus facilement régénérées. De plus, les amines tertiaires ont des taux de corrosion inférieurs à ceux des amines primaires et secondaires. Le principal inconvénient est sa vitesse de réaction trop lente.
Un organigramme typique du processus d'absorption chimique pour la récupération du CO2 à partir des gaz de combustion est illustré à la figure 1. Au cours de l'opération d'absorption d'amine, le flux de gaz résiduaire et la solution d'amine liquide sont mis en contact à contre-courant dans une tour d'absorption (ou absorbeur).
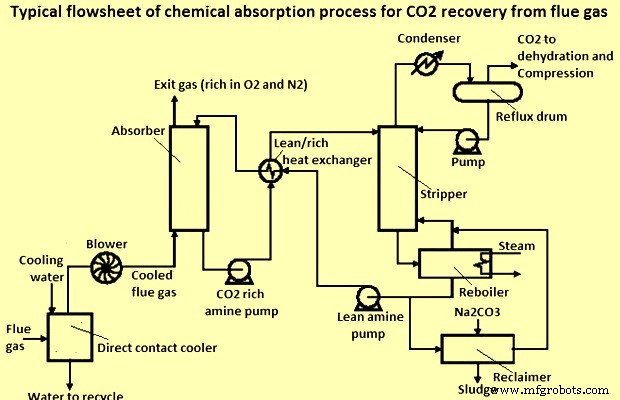
Fig 1 Schéma type d'un processus d'absorption chimique pour la récupération du CO2 des gaz de combustion
Les fumées de combustion sortant de la cheminée sont chaudes (environ 240°C) et à pression atmosphérique. Les gaz de combustion pénétrant dans l'absorbeur à des températures élevées peuvent entraîner une dégradation du solvant et une diminution de l'efficacité d'absorption. Les gaz de combustion doivent être refroidis à un point de rosée de l'eau de 50 degrés C, entrant dans l'absorbeur. L'absorbeur fonctionne généralement à moins de 50 deg C. Ceci est réalisé en pulvérisant de l'eau de refroidissement dans un refroidisseur à contact direct.
Le CO2 dans les gaz de combustion est refroidi avant d'entrer dans l'absorbeur où il réagit avec le carbonate d'ammonium pour former du bicarbonate d'ammonium. Le NH3 est libéré sous forme de gaz à partir de la solution de solvant lorsque le CO2 est absorbé, et la température est maintenue basse pour minimiser cela. Les gaz quittant l'absorbeur passent par un lavage à l'eau pour éliminer l'ammoniac. Le bicarbonate d'ammonium est chauffé dans le régénérateur, séparant le CO2. Le solvant carbonate d'ammonium est renvoyé dans l'absorbeur. L'eau et le NH3 sont éliminés du flux de CO2 quittant la colonne d'extraction.
Un ventilateur est installé pour donner aux gaz de combustion une pression suffisante pour qu'ils traversent le système d'absorption-désorption. Les gaz résiduaires à épurer du CO2 entrent normalement dans l'absorbeur par le bas, remontent et sortent par le haut, tandis que le solvant pénètre par le haut de l'absorbeur, descend (en contact avec le gaz) et ressort par le bas. La dilution de l'amine en circulation avec de l'eau est entreprise pour réduire la viscosité du fluide en circulation. Un fluide à viscosité plus élevée nécessite plus de puissance pour pomper et assurer la circulation. La solution liquide d'amine contenant le gaz absorbé s'écoule ensuite vers une unité de régénération (stripper) où elle est chauffée et les gaz acides libérés. La régénération du solvant peut être effectuée à basse pression pour améliorer la désorption du CO2 du liquide. Une certaine solution d'amine est typiquement transportée dans le courant de gaz acide provenant de l'étape de régénération et la solution d'amine est récupérée à l'aide d'un condenseur, afin d'éviter des pertes excessives de solvant. La solution d'amine pauvre chaude s'écoule ensuite à travers un échangeur de chaleur où elle est mise en contact avec la solution d'amine riche de la tour de contact et de là, la solution d'amine pauvre est renvoyée vers la tour de contact gaz, c'est-à-dire l'absorbeur.
Dans le cas du procédé de lavage aux amines, avec des amines hautes performances (méthyldiéthanolamine activée, aMDEA), le processus complet (amines et compression à une pression de 110 kg/cm²) nécessite environ 1,6 tonne de vapeur basse pression et 160 kWh de puissance par tonne de CO2 capturé.
Les procédés à base d'amines présentent certaines limitations, ce qui a entraîné des avancées technologiques. Dans le passé, la technologie d'épuration aux amines s'est concentrée sur l'élimination du H2S (sulfure d'hydrogène) pour le secteur du gaz naturel. Cependant, les exigences sont différentes pour la récupération du CO2 des gaz de combustion. Un défi est la faible pression des gaz de combustion pour l'absorption du CO2. De plus, les impuretés présentes dans les gaz de combustion, telles que l'O2, les oxydes de soufre (SO2,SO3), les oxydes d'azote et les particules, créent des problèmes particuliers lors du processus de séparation.
En résumé, la récupération du CO2 des gaz de combustion nécessite une quantité importante de traitement de prétraitement afin d'éviter tout encrassement lors de l'étape d'absorption du solvant. Cela augmente le coût du captage du CO2. Cependant, des améliorations significatives peuvent être apportées au procédé d'absorption de solvant en termes d'optimisation des compositions des amines absorbantes et des contacteurs gaz-liquide, afin de gérer cela.
Absorption physique – Pour l'absorption physique, le CO2 est physiquement absorbé dans un solvant selon la loi de Henry. La capacité d'absorption des solvants organiques ou inorganiques pour le CO2 augmente avec l'augmentation de la pression et la diminution des températures. L'absorption de CO2 se produit à des pressions partielles élevées de CO2 et à basse température. Les solvants sont ensuite régénérés soit par chauffage, soit par réduction de pression. L'avantage de cette méthode est qu'elle nécessite relativement peu d'énergie; mais le CO2 doit être à haute pression partielle.
Adsorption physique solide – Un processus d'adsorption comprend deux étapes principales, à savoir (i) l'adsorption et (ii) la désorption. La faisabilité technique d'un procédé est dictée par l'étape d'adsorption, tandis que l'étape de désorption contrôle sa viabilité économique. L'adsorption nécessite une forte affinité entre un adsorbant et le composant à éliminer d'un mélange gazeux (dans ce cas, le CO2). Cependant, plus l'affinité est forte, plus il est difficile de désorber le CO2 et plus l'énergie consommée pour régénérer l'adsorbant pour le réutiliser lors du cycle suivant est élevée. Par conséquent, l'étape de désorption doit être très soigneusement équilibrée par rapport à l'étape d'adsorption pour que le processus global réussisse.
Les procédés d'adsorption sont assez attractifs pour le mécanisme de capture du CO2, malgré leurs inconvénients tels que la faible capacité des adsorbants et l'influence des contaminants comme le SO2 et le H2O sur le processus de séparation. Ce procédé présente également des avantages tels que la disponibilité, la flexibilité, le fonctionnement entièrement automatisé du procédé et la production d'un produit de haute pureté. La séparation peut être effectuée par adsorption modulée en pression (PSA) (Fig 2), adsorption modulée en pression sous vide (VPSA), adsorption modulée en température (TSA), adsorption modulée en pression-température (PTSA) ou adsorption modulée électrique (ESA) processus. Les lits de l'installation sont remplis d'adsorbants solides. La sélectivité dépend de la différence d'équilibre d'adsorption ou des taux d'adsorption et de l'efficacité (concentration et récupération) a une importance sur la configuration du cycle, le temps d'adsorption, la pression d'adsorption et de désorption, la température pendant le processus ainsi que le type d'adsorbant appliqué.
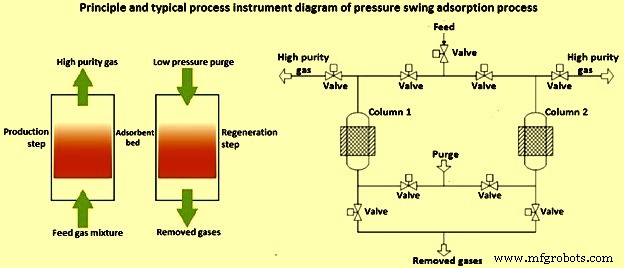
Fig 2 Processus d'adsorption modulée en pression
Le principal avantage de l'adsorption physique par rapport à l'absorption chimique est son fonctionnement et sa régénération simples et économes en énergie, qui peuvent être obtenus avec un cycle d'oscillation de pression ou de température (une oscillation de pression ou de température lorsque le processus passe par un cycle d'absorption-désorption afin pour réaliser la séparation). L'adsorption modulée en pression est un procédé commercial de séparation du H2 des mélanges de H2 et de CO2 dans la production de H2.
Des progrès significatifs ont été réalisés dans le développement d'adsorbants pour l'élimination du CO2 des gaz de combustion. Le principal matériau d'adsorption utilisé a été les zéolithes. Les zéolithes sont plus efficaces pour la séparation du CO2 des espèces moins polaires que le CO2, de sorte que la présence d'eau et de SOx dans les flux de gaz de combustion pose un problème.
De nouveaux adsorbants ont été envisagés et développés tels que les charbons, les silico-aluminates mésoporeux (par exemple les charpentes imidazolates zéolithiques, ZIF) et les charpentes organiques métalliques (MOF). Les adsorbants à base de carbone ont le potentiel d'être régénérés en appliquant une tension électrique (ESA). Les nouveaux matériaux à l'étude comprennent les dérivés d'hydroxydes doubles en couches (LDH et LDO). D'autres avancées incluent la fonctionnalisation des pores du matériau adsorbant en incorporant des amines pour augmenter la charge en CO2. Dans ce cas, le CO2 est séparé par un processus de chimisorption.
De nouveaux procédés sont en cours de développement pour traiter les flux de gaz de combustion à forte humidité et les impuretés. Ceux-ci comprennent des lits adsorbants multicouches. Les lits multicouches permettent d'utiliser des adsorbants à haute sélectivité en CO2 mais ils se dégradent fortement en présence d'eau.
Technologies de captage pré-combustion
Les technologies de captage précombustion consistent à éliminer les polluants et le CO2 lors du traitement en amont des combustibles fossiles avant leur combustion pour la récupération de chaleur (via la vapeur), ou la production d'électricité ou d'H2.
Un inconvénient du captage du C après combustion est la faible concentration de CO2 dans les gaz de combustion, ce qui entraîne une pénalité énergétique relativement élevée et un coût élevé du captage du C. La précombustion s'efforce de réduire ces pénalités en décarbonant le flux de procédé riche en CO2 avant la combustion du combustible riche en H2 restant. Pour réaliser la décarbonisation des carburants hydrocarbonés, ils sont d'abord convertis en gaz de synthèse par la gazéification d'un carburant avec de l'O2 (ou de l'air). Le gaz de synthèse est un mélange de CO (monoxyde de carbone), H2, CO2 et eau, selon le processus de conversion et le combustible et autres composants.
Le gaz de synthèse est un produit intermédiaire, qui peut ensuite être converti pour produire (i) H2, (ii) de l'énergie électrique intégrée, en utilisant la réaction de conversion eau-gaz, ou (iii) une polygénération où une gamme de produits énergétiques peut être présente, y compris électricité, chaleur, H2 et carburants de synthèse et autres produits chimiques. Le processus impliqué avec chacun de ces produits énergétiques finaux est décrit ci-dessous.
Production de H2 par reformage du méthane – La méthode la plus largement utilisée aujourd'hui pour produire du H2 est le reformage catalytique à la vapeur de méthane (CH4). La réaction de reformage consistant à convertir CH4 et H2 O à CO et H2 est endothermique. La réaction est réalisée sur un catalyseur Ni (nickel) à haute température dans un four à chauffage direct alimenté au CH4. Le catalyseur est empoisonné par le S (soufre), donc tout S présent dans la charge doit être éliminé. Le gaz de synthèse passe à son tour dans un convertisseur catalytique de transfert d'eau, où le CO réagit de manière exothermique avec de la vapeur pour produire du H2 et un sous-produit de CO2. Ces sous-produits sont ensuite éliminés du système. Les gaz d'échappement contiennent encore une valeur calorifique importante, ils sont donc brûlés pour produire de la vapeur ou de l'électricité.
Gazéification du charbon – Les technologies de gazéification peuvent produire un flux gazeux à haute teneur en CO2 et à pression modérée. Le charbon d'alimentation est gazéifié en O2 (ou air) pour produire un gaz de synthèse. Le gaz de synthèse est refroidi à 200 °C dans des refroidisseurs de gaz de synthèse générant des vapeurs à haute et basse température. Il est ensuite déplacé davantage dans un réacteur de conversion eau-gaz à basse température. Le réacteur water gas shift est un réacteur catalytique dans lequel le CO réagit avec de la vapeur pour produire plus de H2 et de CO2. Le gaz est ensuite refroidi à 35 degrés C en vue de l'élimination des gaz acides. Environ 99 % de l'H2S est éliminé du gaz de synthèse par absorption physique et converti en soufre élémentaire. Une unité PSA peut être utilisée pour séparer 85 % du H2 du gaz de synthèse sans S. Le H2 laisse environ 60 kg/cm² et une grande pureté (supérieure à 99,99 %). Le CO2 peut être épuré du gaz de synthèse en aval du système de capture de S. Le gaz de purge PSA est comprimé et brûlé dans un cycle combiné de turbine à gaz pour produire de l'énergie électrique.
Les technologies de gazéification sont bien établies pour la production de H2. Des usines commerciales ont été construites et exploitées avec succès pour produire du H2 pour les applications de raffinage et la fabrication de produits chimiques (par exemple, la production de NH3 et de méthanol) à partir d'une gamme de matières premières d'hydrocarbures.
Alimentation électrique intégrée – Le gaz de synthèse à haute teneur en H2 peut être brûlé dans un turbodétendeur pour produire de l'énergie électrique dans un cycle combiné. Si le gaz de synthèse est produit par gazéification, le schéma est appelé cycle combiné de gazéification intégrée (IGCC). L'IGCC permet de produire de l'électricité à haut rendement. Étant donné que le gaz doit être nettoyé pour éviter d'endommager la turbine à gaz, l'IGCC a de très faibles émissions environnementales. De plus, les usines IGCC utilisent moins d'eau. L'IGCC est actuellement utilisé commercialement dans de nombreuses usines du monde entier par gazéification des résidus pétroliers pour fournir de l'électricité, du H2 et de la vapeur.
Les trois principaux types de gazéifieurs de charbon sont (i) le lit mobile, (ii) le lit fluidisé et (iii) le flux entraîné. Cependant, la plupart des gazogènes envisagés pour le captage du CO2 sont actuellement basés sur des gazogènes à flux entraîné. L'application commerciale de l'IGCC à base de charbon a été limitée par ses coûts relativement élevés, la faible disponibilité des centrales et la concurrence des centrales au charbon pulvérisé. Le coût du captage du CO2 dans l'IGCC dépend fortement du type de gazogène.
Comme mentionné ci-dessus, pour permettre la capture du CO2, le gaz combustible doit être acheminé vers un réacteur à changement catalytique où la majeure partie du CO est mise à réagir par la vapeur pour donner du H2 et du CO. Pour le gazéificateur à alimentation en suspension, suffisamment de vapeur est déjà présente dans le gaz combustible provenant de l'évaporation de l'eau bouillie de charbon et du refroidissement par trempe du gaz produit du gazéifieur. Cependant, pour le gazogène à alimentation sèche, la vapeur doit être extraite du cycle de vapeur et ajoutée à l'alimentation en gaz combustible du convertisseur de changement.
Il est à noter que l'IGCC est plus cher pour la production d'électricité que la combustion conventionnelle de charbon pulvérisé, sans captage de CO2 dans les deux cas.
Poly-génération – Le gaz de synthèse est un bon élément de base, car il peut être utilisé pour produire une large gamme de produits énergétiques. La plus grande flexibilité offerte est la polygénération, dans laquelle le "gaz de synthèse" peut produire de la vapeur, de l'électricité, de l'H2 et des produits chimiques (tels que le méthanol, les liquides Fischer-Tropsch) dans un seul complexe d'usine.
Un certain nombre de technologies de séparation différentes, y compris les technologies de solvant, d'adsorbant et de membrane, peuvent être appliquées pour séparer le CO2 des produits de la gazéification.
Absorption – La technologie conventionnelle est l'absorption physique dans un processus en deux étapes qui élimine le H2S puis capture le CO2. Cependant, le gaz doit être refroidi après la réaction de changement de gaz à l'eau, puis réchauffé avant de générer de l'énergie. Cela réduit l'efficacité et augmente les coûts.
Adsorption – Des adsorbants peuvent être utilisés pour séparer le CO2 des flux de gaz de combustion post-combustion en aval de la réaction de conversion gaz-eau. L'adsorption modulée en température (TSA) et l'adsorption modulée sous vide/pression (VSA/PSA) peuvent être utilisées pour récupérer le CO2 de l'adsorbant. Le CO2 est à basse pression lorsqu'il est récupéré via VSA/PSA et doit être compressé pour être stocké.
Membranes – Des systèmes avancés de séparation des gaz à base de membranes sont actuellement en cours de développement pour combiner la réaction de changement de gaz et la séparation de H2 en une seule étape. Les systèmes à base de membranes utilisent un réacteur à membrane de séparation de l'eau et du gaz H2 (HSMR) pour déplacer le gaz de synthèse et extraire le H2. La température maximale d'environ 475 deg C garantit une cinétique chimique rapide et une bonne performance d'équilibre de déplacement des gaz de l'eau est obtenue par l'élimination continue du produit H2.
Il existe trois grandes classes de membranes inorganiques perméables à l'H2, à savoir (i) le tamisage moléculaire céramique, (ii) le transport d'ions céramique dense et (iii) le métal dense.
Avantages et inconvénients de la pré-combustion (décarbonisation) – Les avantages de la pré-combustion (décarbonisation) sont (i) la séparation du CO2 par absorption de solvant ou PSA est prouvée. Les gaz d'échappement arrivent à des pressions élevées et des concentrations élevées de CO2 réduisent considérablement les coûts de capture, (ii) les coûts de compression sont inférieurs à ceux des sources de post-combustion car le CO2 peut être produit à des pressions modérées, (iii) la technologie offre de faibles émissions de SOx et de NOx , (iv) le produit principal est le gaz de synthèse, qui peut être utilisé pour d'autres applications ou produits commerciaux, et (v) une large gamme d'hydrocarbures peut être utilisée comme matière première, comme le gaz, le pétrole, le charbon et le coke de pétrole, etc. Les inconvénients sont (i) le combustible d'alimentation doit d'abord convertir le combustible en gaz de synthèse, (ii) les turbines à gaz, les réchauffeurs, les chaudières doivent être modifiés pour la combustion de H2, (iii) des coûts plus élevés et un plus grand risque technologique, et (iv) il nécessite des modifications majeures des installations existantes pour la modernisation.
Combustion oxycombustible
L'oxycombustion représente une nouvelle approche émergente pour une combustion de combustibles fossiles à émissions quasi nulles et plus propre. Ceci est accompli en brûlant le carburant dans de l'O2 pur au lieu de l'air. En éliminant le N2 (azote) dans le processus de combustion, l'échappement du flux de gaz de combustion est principalement composé d'eau et de CO2, sans aucun N2. Le CO2 de haute pureté peut être récupéré par condensation de l'eau. Cependant, lorsque le combustible est brûlé dans de l'O2 pur, la température de la flamme est beaucoup plus élevée que celle d'un brûleur à soufflage d'air normal et le matériau de construction classique du brûleur n'est pas capable de supporter cette température élevée. Par conséquent, soit le matériau de construction doit être amélioré, soit la température de la flamme doit être abaissée. Le développement de matériaux résistants aux hautes températures a été lent car il s'agit d'une entreprise majeure de R&D (recherche et développement). Il existe un certain nombre de méthodes qui peuvent être utilisées pour modérer la température de la flamme, la plus courante étant le recyclage du CO2. Dans le recyclage du CO2, une partie du flux de gaz de combustion riche en CO2 est recyclée vers le brûleur pour abaisser la température de la flamme de manière similaire à celle d'un brûleur à air soufflé normal. Une autre méthode consiste à utiliser l'injection d'eau plutôt que le recyclage du CO2 pour contrôler la température de la flamme. C'est ce que l'on appelle souvent la combustion d'« hydroxycarburant ». En effet, ces deux options permettent l'utilisation continue d'un matériau réfractaire conventionnel jusqu'à ce qu'un nouveau matériau résistant aux hautes températures puisse être développé.
A primary benefit of oxy-fuel combustion is the very high-purity CO2 stream which is produced during combustion. After trace contaminants are removed, this CO2 stream is more easily purified and removed than post-combustion capture. There are other benefits also such as reduction in NOx formation etc. When burning oil or coal, only two unit operations are needed for the combined removal of all other pollutants namely an electrostatic precipitator (ESP) or bag filter and a condensing heat exchanger (CHX)/reagent system. It is also possible to simplify the reagent system in the CHX to achieve total removal of SO2 with the CO2 stream for geologic storage. This further reduces the cost of unit operations for pollution abatement. The CHX increases the thermal efficiency of the boiler depending on the type of fossil fuel combusted, being the lowest for high rank bituminous coal and highest for natural gas.
Another benefit is the significant reduction in the size and capital cost of all plant equipment compared to conventional air-based combustion systems. This is due to the almost 5-fold decrease in the fire box volume and exit flue gas flow rates as N2 is eliminated in the combustion process.
The major disadvantage of oxy-fuel combustion is the high capital cost (primarily due to O2 requirements) and large electric power requirement inherent in conventional cryogenic air separation units required to generate O2. Oxy-fuel combustion is not currently used in typical large combustion systems because the air separation system is expensive and flue gas recycling is needed to be practiced in order to moderate flame temperature.
Processus de fabrication
- La synergie de l'IoT cellulaire et du Bluetooth LE
- Stockage et manipulation de la courroie
- Fabrication et imagerie de cyclocarbone
- Fibres de carbone :passé, présent et futur
- Braskem s'associe à l'université pour une production de plastique durable utilisant la capture et l'utilisation du CO2
- Hyperconvergence et stockage secondaire :2e partie
- Fabrication du fer par haut fourneau et émissions d'oxyde de carbone
- Revêtement en carbone de type diamant :une innovation dans la fabrication de poinçons et de matrices
- Récupération des bulles, de la bière et du CO2



