Influence des matériaux, de l'hétérostructure et de l'orientation des nanohybrides sur l'activité photocatalytique
Résumé
Dans ce travail, différentes structures à base de nanotiges de ZnO de type n électrodéposées et de Cu2 de type p Les nanostructures O, CuSCN et NiO sont fabriquées pour la dégradation de l'orange de méthyle (MO). L'influence des matériaux, de l'hétérostructure et de l'orientation des nanohybrides sur l'activité photocatalytique est discutée pour la première fois. Les structures à hétérojonction montrent une amélioration remarquable par rapport au semi-conducteur nu. La morphologie de la nanostructure a principalement une influence sur l'activité photocatalytique. NiO a l'activité catalytique la plus élevée parmi les quatre nanostructures semi-conductrices vierges de ZnO, Cu2 O, CuSCN et NiO. La plus grande amélioration de l'activité photocatalytique est obtenue en utilisant une hétérostructure ZnO/NiO (1 min) attribuée à la structure d'hétérojonction et à une surface spécifique extrêmement élevée, qui peut dégrader MO (20 mg/L) en incolore en 20 min avec le photocatalytique le plus rapide vitesse parmi les structures homogènes à hétérojonction. Pendant ce temps, la méthodologie et l'analyse des données décrites ici serviront d'approche efficace pour la conception de nanostructures hybrides pour l'application de l'énergie solaire, et les nanohybrides appropriés auront un potentiel important pour résoudre les problèmes d'environnement et d'énergie.
Contexte
Les nanomatériaux hybrides dotés de propriétés optiques, électroniques et magnétiques exceptionnelles ont suscité beaucoup d'intérêt ces dernières années en raison de leurs applications généralisées dans l'assainissement de l'environnement [1, 2] et la conversion de l'énergie solaire [3, 4]. Ces dernières années, plusieurs variétés de nanohybrides ont été développées, par exemple, les nanocomposites d'oxyde de graphène [5], TiO2 /BiVO4 nanocomposites [6], nanocomposites hydrogel imprimés en 3D [7] et Ru/Li2 O nanocomposites [8]. Parmi les différents types de nanomatériaux, les hétérojonctions basées sur différents nano-semi-conducteurs sont devenues un domaine de recherche important en raison de leurs propriétés photocatalytiques attrayantes [9,10,11] et photovoltaïques [12,13,14]. Récemment, plusieurs travaux de recherche ont été menés sur diverses applications catalytiques de la dégradation des colorants, telles que l'organocatalyseur à membrane nanohybride [15], le catalyseur nanohybride bioinorganique [16] et le catalyseur nanohybride vert [17]. En raison de la toxicité, les colorants organiques dans les eaux usées constituent une menace sérieuse pour la santé humaine [18, 19]. Ainsi, la conversion des colorants organiques en substances inoffensives est essentielle pour la vie humaine et le développement durable. Une variété de matériaux semi-conducteurs inorganiques avec différentes morphologies ont été explorés comme photocatalyseurs pour la purification des eaux usées sous irradiation UV ou à la lumière visible [20,21,22], en particulier l'oxyde de zinc (ZnO) et le dioxyde de titane (TiO2 ) nanomatériaux unidimensionnels (1D). Jusqu'à présent, les nanomatériaux ZnO ont obtenu l'enquête la plus large parmi divers semi-conducteurs, ce qui pourrait être attribué à leurs performances de transfert d'électrons efficaces [23], fournissant des trous photogénérés pour une forte oxydation, une meilleure fonctionnalité respectueuse de l'environnement, une non-toxicité, un faible coût et une bonne stabilité et étant répandu dans la terre [24, 25]. Cependant, l'activité photocatalytique du ZnO est sévèrement limitée par ses défauts internes :réponse de la région UV-visible plus étroite en raison de sa large bande interdite et éventualité élevée de recombinaison des paires électron-trou photogénérées [26, 27]. Afin de surmonter ces limitations, de nombreuses mesures ont été prises, telles que le dopage [28], les métaux nobles composites, tels que l'Au [29, 30] et l'Ag [31]; et la combinaison avec d'autres semi-conducteurs, tels que CdS [32], ZnSe [33], CdSe [34, 35] et PbS [36, 37]. L'obtention d'hétérojonctions à base de ZnO et d'autres semi-conducteurs s'est avérée être un moyen faisable d'améliorer la réponse à la lumière visible et l'efficacité de dégradation des eaux usées. Récemment, plusieurs hétérojonctions basées sur le nanomatériau ZnO et le nano-semi-conducteur de type p sur la dégradation ont été développées. Récemment, le Cu2 Les hétérostructures O-ZnO sur la photocatalyse ont été rapportées par Wang et al. [38] et Yu et al. [39]. Luo et ses collègues ont rapporté l'hétéroarchitecture ZnO/CNF/NiO pour la photocatalyse haute performance [40]. Liu et al. ont rapporté des hétérojonctions de nanofibres électrofilées NiO/ZnO avec une activité photocatalytique améliorée [41]. La structure ZnO/CdS a également une activité photocatalytique plus élevée que les matériaux vierges [42]. Ces rapports indiquent que les hétérostructures possédaient une activité photocatalytique de décomposition de colorant plus élevée que les semi-conducteurs vierges. Cependant, l'efficacité de la dégradation photocatalytique du méthylorange (MO) doit encore être améliorée. En outre, la conception de la structure à hétérojonction doit être approfondie, par exemple, en réduisant les coûts en se débarrassant du métal noble et en utilisant une méthode simple telle que l'électrodéposition et une température de réaction plus basse. Dans cette étude, ZnO, Cu2 Les nanostructures O, CuSCN et NiO sont préparées par une méthode d'électrodéposition simple et peu coûteuse à température ambiante. Des structures d'hétérojonction de différents matériaux et d'orientations différentes sont fabriquées à partir de nanotiges de ZnO de type n et de Cu2 de type p Nanostructures O, CuSCN et NiO. Les hétérostructures présentent de bien meilleures performances photocatalytiques pour la dégradation photocatalytique du MO que le matériau de type n vierge ou le matériau de type p. L'influence sur l'orientation de l'hétérojonction dépend de la qualité cristalline du matériau supérieur de l'hétérojonction. L'influence sur le matériau des différentes conditions de réaction dépend de la morphologie et de la qualité des nanostructures. Parmi les trois matériaux de type p utilisés dans nos travaux, NiO a les performances photocatalytiques les plus excellentes. Le ZnO/NiO (1 min) peut décomposer la solution aqueuse de MO (20 mg/L) de l'orange à l'incolore en 20 min. Il révèle que le matériau et l'orientation peuvent tous deux avoir un effet sur les performances photocatalytiques, ce qui a une grande importance pour la décomposition des polluants organiques; de plus, cette étude est la première étude approfondie de l'influence des matériaux, de l'orientation et de l'hétérostructure sur l'activité photocatalytique et peut favoriser d'autres recherches sur davantage de nanohybrides pour obtenir une efficacité photocatalytique plus élevée.
Méthodes
Matériaux expérimentaux
Verre revêtu d'oxyde d'indium-étain (ITO) (CSG Holding Co., Ltd., 15 Ω/sq), nitrate de zinc (Zn(NO3 )·6H2 O), l'hexaméthylènetétramine (HMT), le sulfate de cuivre (II) pentahydraté, l'hydroxyde de sodium, l'acide lactique, le thiocyanate de potassium, l'acide éthylènediaminetétraacétique, la triéthanolamine et le nitrate de nickel hexahydraté sont tous achetés auprès de Sinopharm Chemical Reagent Co., Ltd. qualité analytique et utilisé tel que reçu sans autre purification.
Préparation de nanostructures
La méthode d'électrodéposition rentable est utilisée dans ce travail pour la préparation de la grande surface de nanostructures en raison du traitement à basse température, des formes de substrat arbitraires et du contrôle précis de la taille des nanostructures [43]. Tous les dépôts sont effectués dans une cellule de verre configurée dans laquelle un substrat ITO, une plaque de platine et une électrode Ag/AgCl en KCl saturé ou une électrode au calomel saturé (SCE) servent d'électrode de travail, de contre-électrode et d'électrode de référence , respectivement. Les conditions de réaction détaillées pour la fabrication de toutes les nanostructures par électrodéposition sont présentées dans le tableau 1. La valeur du pH de Cu2 La solution réactionnelle O est régulée de 10 à 12 par NaOH. La valeur du pH de la solution réactionnelle CuSCN est d'environ 1,5. Enfin, tous les échantillons déposés ci-dessus sont rincés à l'eau déminéralisée pour éliminer l'électrolyte et séchés à l'air naturellement. Aucun recuit post-dépôt n'est utilisé.
Caractérisations
Les diagrammes de diffraction des rayons X (XRD) sont mesurés avec un diffractomètre Rigaku D/Max-2500 utilisant le rayonnement Cu Kα (λ = 1.54 Å) à température ambiante. La vitesse de balayage est de 10°/min. La tension et le courant sont de 40 kV et 40 mA. La surface et la structure en coupe transversale des échantillons sont caractérisées par microscopie électronique à balayage (MEB) à l'aide d'un Philips-FEI XL 30-SFEG à température ambiante sans aucun revêtement de surface. La tension d'accélération est de 10 à 20 kV. Les propriétés optiques des échantillons sont étudiées par spectrométrie de réflectance diffuse UV-vis (UV-vis DRS) à l'aide d'un spectrophotomètre UV-vis Shimadzu UV-3101PC à température ambiante.
Expériences de décomposition photocatalytique
Les activités photocatalytiques des échantillons préparés sont évaluées vis-à-vis de la dégradation de MO en solution aqueuse. Une lampe Xe de 500 W est une source lumineuse de dispositifs de réaction photocatalytique. Dans un processus de photodégradation, l'échantillon est placé dans un réacteur en quartz rempli de 3 mL de solution aqueuse de MO (20 mg/L). Avant irradiation, la solution aqueuse est maintenue à l'obscurité pendant 60 min pour atteindre l'équilibre d'adsorption de MO. Après un temps d'irradiation spécifique, les performances de décomposition photocatalytique sont analysées en mesurant l'absorbance de la solution MO à sa longueur d'onde caractéristique (465 nm) avec un spectrophotomètre UV-vis. Tous les échantillons sont réalisés dans des expériences indépendantes et réalisés à température ambiante.
Résultats et discussion
Préparation de nanostructures et analyse de composition
Tous les ZnO, Cu2 Les nanostructures O, CuSCN et NiO sont synthétisées par la méthode d'électrodéposition rentable à température ambiante. L'électrodéposition est réalisée dans une cellule électrochimique standard à trois électrodes en mode potentiostatique. Les textures cristallines de ZnO, Cu2 Les nanostructures O, CuSCN et NiO sont caractérisées via des profils XRD. Les images XRD de ZnO, Cu2 Les nanostructures O, CuSCN et NiO préparées par la méthode d'électrodéposition sont présentées sur la figure 1. Un ensemble de pics sur la figure 1a apparaît à 2θ d'env. 34,36°, 36,12° et 47,48° pour les nanotiges de ZnO, qui sont respectivement attribuées aux (002), (101) et (102) des cristaux de ZnO. Tous les pics des nanotiges de ZnO peuvent être indexés sur la structure wurtzite hexagonale de ZnO, et aucune autre phase détectable n'existe dans les nanostructures de ZnO, qui sont similaires aux profils XRD de la réf. [39]. De plus, le fort pic de ZnO (002) indique que des nanotiges orientées à haute cristallinité sont obtenues. Trois pics sur la Fig. 1b à 2θ d'env. 29,78°, 36,81° et 42,89° sont observés pour le Cu2 électrodéposé Film O sur substrat ITO, qui sont attribués aux (110), (111) et (200) de Cu2 O cristaux, respectivement, indiquant que Cu2 O a la structure cubique cuivrique pure avec une orientation préférée (111), qui est la même que les profils XRD de la réf. [38]. La diffraction des pics de la Fig. 1c apparaît à 2θ d'environ 16,21°, 27,20° et 32,69° et peuvent être attribués aux plans (003), (101) et (006) des cristaux CuSCN, respectivement, qui peuvent être indexés sur une structure rhomboédrique β -CuSCN [44]. Les modèles XRD de la figure 1d sont attribués aux trois principaux pics NiO à 37,52°, 43,26° et 62,86°, qui font respectivement référence aux plans (111), (200) et (220), aussi similaires que XRD profilés dans Réf. [39]. Tous les modèles XRD révèlent qu'aucune des autres phases n'est détectée et que les nanostructures sont sans impureté. La figure 1e montre les spectres d'absorbance de ZnO, Cu2 Nanostructures O, CuSCN et NiO préparées par la méthode d'électrodéposition. Comme le montre la figure 1e, les nanotiges de ZnO ne peuvent absorber la lumière à haute énergie qu'avec une longueur d'onde inférieure à 370 nm. Un bord de bande d'absorbance à 600 nm peut être observé pour Cu2 O, comme le montre la figure 1e, ce qui est cohérent avec la bande interdite de Cu2 O (2,1 eV). Comme le montre la figure 1e, le CuSCN a une absorption faible et large avec une longueur d'onde supérieure à 350 nm et NiO a une absorption comprise entre 350 et 500 nm mais une faible absorption avec une longueur d'onde supérieure à 500 nm. Toute l'absorption de ZnO, Cu2 Les nanostructures O, CuSCN et NiO sont dans la gamme ultraviolette et visible, ce qui garantira l'absorption de la lumière ultraviolette sous irradiation par lampe Xe dans les expériences de décomposition photocatalytique et la génération conséquente de paires électron-trou.
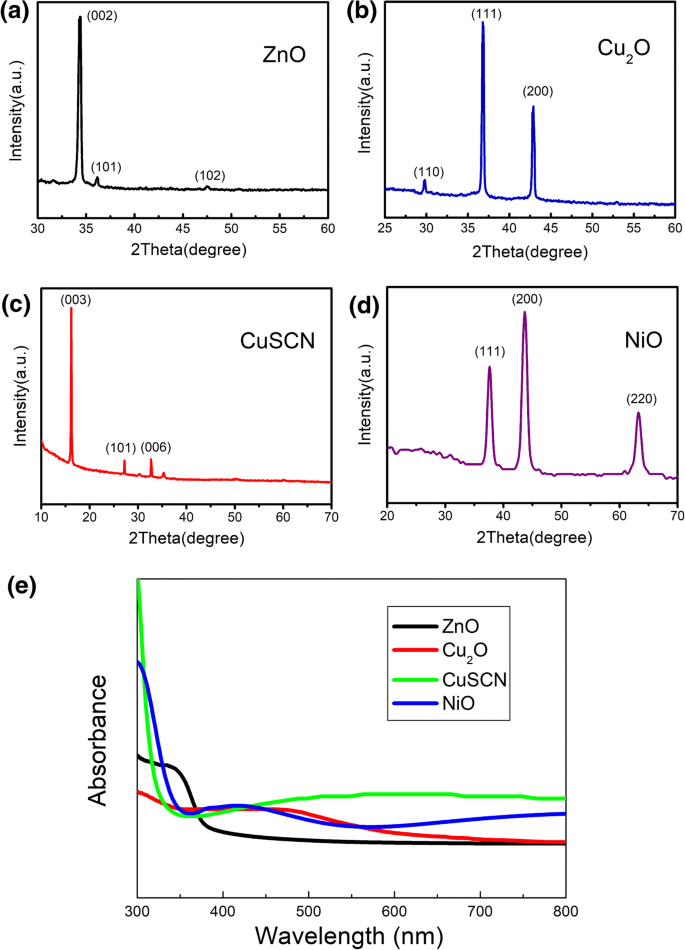
Spectres photoélectroniques aux rayons X de ZnO (a ), Cu2 O (pH 10, 20 min) (b ), CuSCN (3D) (c ), et NiO (1 min) (d ) les nanostructures préparées par la méthode d'électrodéposition et les spectres d'absorbance (e ) de ZnO, Cu2 Nanostructures O (pH 10, 20 min), CuSCN(3D) et NiO(1 min) préparées par la méthode d'électrodéposition
Conception et morphologie des hétérostructures
Différentes hétérojonctions basées sur des nanotiges de ZnO de type n et de Cu2 de type p Des nanostructures O, CuSCN et NiO avec différentes orientations sont fabriquées. Premièrement, le ZnO, Cu2 O, ZnO/Cu2 O, et Cu2 O/ZnO sont préparés pour la dégradation photocatalytique de MO. La figure 2 montre l'image SEM vue de dessus des nanotiges de ZnO (a), ZnO/Cu2 O (pH 12, 20 min) hétérojonction (b), Cu2 O (pH 12, 20 min) (c), et Cu2 Hétérojonction O (pH 12, 20 min)/ZnO (d). Fichier supplémentaire 1 :La figure S1 montre la vue en coupe de ces quatre structures. La figure 3 montre l'image SEM vue de dessus de ZnO/Cu2 O (pH 10, 20 min) hétérojonction (a), ZnO/Cu2 O (pH 10, 40 min) hétérojonction (b), Cu2 Hétérojonction O (pH 10, 20 min)/ZnO (c), Cu2 Hétérojonction O (pH 10, 40 min)/ZnO (d), Cu2 O (pH 10, 20 min) (e), et Cu2 O (pH 10, 40 min) (f). Fichier supplémentaire 1 :La figure S2 montre la vue en coupe de ces six structures. Comme le montre la vue de dessus illustrée à la figure 2a et la vue en coupe transversale dans le fichier supplémentaire 1 :figure S1 (a), les nanotiges de ZnO obtenues par la méthode d'électrodéposition ont presque la structure d'un prisme hexagonal. Le diamètre et la longueur des nanotiges sont respectivement de l'ordre de 200 à 300 nm et de 800 à 1 200 nm. Comme le montrent les Fig. 2c et 3e et f, on peut noter que le Cu2 Les cristaux d'O croissent de cubes en octaèdres lorsque la valeur du pH de la solution d'électrodéposition passe de 10 à 12. Les cristaux obtenus à pH ~ 10 avec un temps de réaction de 20 et 40 min ne sont pas tous des cubes parfaits en raison de la dissolution différente du cristal dans la solution réactionnelle [45]. On voit aussi clairement que le Cu2 Les cristaux d'O deviennent plus gros et plus denses au fil du temps, et le Cu2 Les cristaux d'O se rassembleront et s'agrégeront lorsque le temps de réaction sera plus long. Dans le processus d'agrégation, le Cu2 Les cristaux d'O seront entassés en raison de la grande densité. Comme le montrent les Fig. 2b et 3a et b, on peut conclure que Cu2 Les cristaux d'O cultivés sur les nanotiges de ZnO sont aussi compacts que le Cu2 Cristaux d'O cultivés sur le substrat de verre ITO nu et certains sont plus petits que le Cu2 Cristaux d'O cultivés sur du verre ITO en raison du point de nucléation différent. Lorsque le pH de la solution réactionnelle est de 10, les nanotiges de ZnO poussent sur le Cu2 Les cristaux d'O sont plus compacts que les nanotiges de ZnO cultivées sur du verre ITO, et le diamètre et la longueur des nanotiges de ZnO cultivées sur le Cu2 Les cristaux d'O sont presque identiques aux nanotiges de ZnO cultivées sur du verre ITO, comme le montrent les Fig. 3c et d. Les nanotiges de ZnO cultivées sur le Cu2 Les cristaux d'O (pH 10, 40 min) sont un peu plus denses que les nanotiges de ZnO cultivées sur le Cu2 Des cristaux d'O (pH 10, 20 min) et des tiges de ZnO beaucoup plus grosses apparaîtront sur la couche des nanotiges de ZnO. Comme le montre la Fig. 2d, les nanotiges de ZnO cultivées sur le Cu2 Les cristaux d'O (pH 12, 20 min) sont beaucoup plus clairsemés que les nanotiges de ZnO cultivées sur le verre ITO. Le diamètre et la longueur des nanotiges de ZnO cultivées sur le Cu2 Les cristaux d'O (pH 12, 20 min) ne sont pas homogènes dans une large gamme.

L'image SEM vue de dessus des nanotiges de ZnO (a ), ZnO/Cu2 O (pH 12, 20 min) hétérojonction (b ), Cu2 O (pH 12, 20 min) (c ), et Cu2 Hétérojonction O (pH 12, 20 min)/ZnO (d )

L'image SEM vue de dessus de ZnO/Cu2 O (pH 10, 20 min) hétérojonction (a ), ZnO/Cu2 O (pH 10, 40 min) hétérojonction (b ), Cu2 Hétérojonction O (pH 10, 20 min)/ZnO (c ), Cu2 Hétérojonction O (pH 10, 40 min)/ZnO (d ), Cu2 O (pH 10, 20 min) (e ), et Cu2 O (pH 10, 40 min) (f )
Deuxièmement, ZnO, CuSCN, ZnO/CuSCN et CuSCN/ZnO sont préparés pour la dégradation photocatalytique de MO. Deux nanostructures CuSCN différentes, des structures de type prisme hexagonal (3D) et des nanofils (NW), sont préparées par la méthode d'électrodéposition. La figure 4 montre l'image SEM vue de dessus de l'hétérojonction ZnO/CuSCN (3D) (a), de l'hétérojonction ZnO/CuSCN (NWs) (b), de l'hétérojonction CuSCN (3D)/ZnO (c), de l'hétérojonction CuSCN (NWs)/ZnO ( d), CuSCN (3D) (e) et CuSCN (NWs) (f). Fichier supplémentaire 1 :La figure S3 montre la vue en coupe de ces six structures. Les structures CuSCN (3D) et CuSCN (NWs) électrodéposées sur des nanotiges de ZnO sont plus denses que celles sur verre ITO, comme le montrent les Fig. 4a et b. Les nanotiges de ZnO sous les structures CuSCN (3D) sont partiellement gravées par la solution de réaction CuSCN avec un pH érosif de 1,5, comme le montrent la figure 4a et le fichier 1 supplémentaire :figure S3(a). Les nanotiges de ZnO sous les structures CuSCN (NWs) sont principalement gravées par la solution réactionnelle CuSCN avec un pH de 1,5, mais le contour des nanotiges de ZnO est maintenu après l'électrodéposition des structures CuSCN (NWs), comme le montre la Fig. 4b et le fichier supplémentaire 1 :Figure S3(b). Le CuSCN (3D) sur les nanotiges de ZnO est beaucoup plus intensif que les structures CuSCN (NWs) sur les nanotiges de ZnO, et les nanotiges de ZnO sous les structures CuSCN (NWs) disparaissent presque en ne restant que le vestige du prisme hexagonal de ZnO. Les nanotiges de ZnO préparées sur la couche de CuSCN sont plus compactes que les nanotiges de ZnO cultivées sur du verre ITO, et le diamètre et la longueur des nanotiges de ZnO cultivées sur CuSCN sont plus petites que les nanotiges de ZnO cultivées sur du verre ITO en raison du point de nucléation différent , comme le montrent les Fig. 4c et d. Les structures CuSCN (3D) et CuSCN (NWs) préparées par la méthode d'électrodéposition sur verre ITO sont orientées avec une densité élevée et presque verticale par rapport au substrat avec un diamètre d'environ 100 nm et 80 nm, respectivement, comme le montrent les Fig. 4e et f.

L'image SEM vue de dessus de l'hétérojonction ZnO/CuSCN (3D) (a ), l'hétérojonction ZnO/ CuSCN (NWs) (b ), hétérojonction CuSCN (3D)/ZnO (c ), hétérojonction CuSCN (NWs)/ZnO (d ), CuSCN (3D) (e ) et CuSCN (NWs) (f )
Enfin, le ZnO, NiO, ZnO/NiO et NiO/ZnO sont préparés pour la dégradation photocatalytique du MO. La figure 5 montre l'image SEM vue de dessus de l'hétérojonction ZnO/NiO (1 min) (a), de l'hétérojonction ZnO/NiO (10 min) (b), de l'hétérojonction NiO (1 min)/ZnO (c), NiO (10 min) /Hétérojonction ZnO (d), NiO (1 min) (e) et NiO (10 min) (f). Fichier supplémentaire 1 :La figure S4 montre la vue en coupe de ces six structures. La nanostructure de NiO électrodéposée sur des nanotiges de ZnO pendant 1 min est un maillage entrecoupé de nanotiges de ZnO, comme indiqué sur la figure 5a et le fichier supplémentaire 1 :figure S4(a). Les nanotiges de ZnO électrodéposées sur la nanostructure NiO (1 min) sont partiellement exposées en grandissant à travers le maillage de NiO (1 min), et la partie restante des nanotiges de ZnO est restée dans le maillage qui ne peut pas être vu dans les images SEM de la vue de dessus, comme le montre la figure 5c et le fichier 1 supplémentaire :figure S4(c). La nanostructure NiO électrodéposée sur du verre ITO pendant 1 min est le maillage intercalé multicouche uniformément réparti sur le verre ITO avec une surface spécifique élevée, comme indiqué sur la figure 5e et le fichier supplémentaire 1 :figure S4(e). La nanostructure de NiO électrodéposée sur des nanotiges de ZnO pendant 10 min est constituée de fleurs composées de nombreuses particules, comme le montre la figure 5b et le fichier supplémentaire 1 :figure S4(b). La nanostructure NiO électrodéposée sur du verre ITO pendant 10 min est composée de nombreuses particules de NiO qui peuvent former une couche compacte sur le verre ITO et une couche de particules sur la couche compacte, comme indiqué sur la figure 5f et le fichier 1 supplémentaire :figure S4(f ). D'après la vue en coupe transversale du MEB dans le fichier supplémentaire 1 :Figure S4 (f), certaines fissures peuvent être trouvées dans la couche compacte sur le verre ITO en raison de la force d'extrusion générée par les particules de NiO. Lorsque ZnO est électrodéposé sur NiO (10 min), les plus petites nanotiges de ZnO (par rapport à celles du verre ITO) se développent sur la couche de particules de NiO, et la forme des particules de NiO disparaît, ne restant que la morphologie des nanotiges de ZnO, comme illustré à la figure 5d et au fichier 1 supplémentaire :figure S4(d). Les fissures dans la couche compacte de NiO sur le verre ITO peuvent également être vues dans le fichier supplémentaire 1 :Figure S4(d), et certaines fissures dans la structure des nanotiges de ZnO sont générées par les fissures dans la couche compacte.

L'image SEM vue de dessus de l'hétérojonction ZnO/NiO (1 min) (a ), l'hétérojonction ZnO/NiO (10 min) (b ), l'hétérojonction NiO (1 min)/ZnO (c ), l'hétérojonction NiO (10 min)/ZnO (d ), NiO (1 min) (e ), et NiO (10 min) (f )
Activité photocatalytique
Les propriétés photocatalytiques sont étudiées via la dégradation du MO, un polluant organique courant [46, 47]. Trois systèmes de ZnO/Cu2 O, ZnO/CuSCN et ZnO/NiO sont discutés, y compris le ZnO vierge, le Cu2 vierge O (ou CuSCN ou NiO), ZnO/Cu2 O (ou CuSCN ou NiO), et Cu2 O (ou CuSCN ou NiO) avec quatre structures dans chaque système. Bien que la méthode d'électrodéposition utilisée dans ce travail pour la préparation des nanostructures soit écologique et environnementale, la méthode de préparation peut nécessiter une quantité considérable de produits chimiques indésirables, ce qui compromet le caractère écologique des méthodes. Le problème tel que la récupération durable des produits chimiques par membrane peut être résolu par un processus hybride continu comprenant un réacteur à flux et une unité de nanofiltration ultérieure pour le recyclage in situ du solvant et du réactif qui a été développé par Szekely et al. [48]. Fichier supplémentaire 1 : les figures S5 et S6 présentent les changements de concentration de MO en l'absence et en présence de différents photocatalyseurs. De toute évidence, la teneur en MO a peu changé en l'absence du catalyseur par rapport à l'ajout du catalyseur. Sous irradiation à la lumière visible, seulement 15 % de MO sont décomposés après 40 min en l'absence de catalyseur, comme indiqué dans le fichier supplémentaire 1 :Figure S5 (a). Les nanotiges vierges de ZnO présentent un certain degré d'activité photocatalytique pour la décomposition de MO. Cependant, en raison des limitations des défauts internes (large bande interdite et recombinaison facile des paires électron-trou) et de la surface spécifique, les performances photocatalytiques sont toujours médiocres, comme le montre le fichier supplémentaire 1 :Figure S6(a), Figure S6( b) et la figure S6(c). La comparaison de la surface spécifique des nanostructures est conjecturée à partir de la taille et de la densité de la surface par image SEM [49,50,51]. Les changements de concentration de MO avec ZnO, Cu2 O (pH 10, 20 min), Cu2 O (pH 10, 40 min), Cu2 O (pH 12, 20 min), ZnO/Cu2 O (pH 10, 20 min), ZnO/Cu2 O (pH 10, 40 min), ZnO/Cu2 O (pH 12, 20 min), Cu2 O (pH 10, 20 min)/ZnO, Cu2 O(pH 10, 40 min)/ZnO et Cu2 O (pH 12, 20 min)/ZnO car les catalyseurs sont indiqués dans le fichier supplémentaire 1 :Figure S6(a). L'intensité du pic d'absorption est progressivement diminuée et décalée vers le bleu à mesure que le temps d'irradiation augmente de 0 à 40 min. Le décalage vers le bleu peut être attribué à la désalkylation [52]. Les performances photocatalytiques de trois Cu2 différents O, Cu2 O (pH 10, 20 min), Cu2 O (pH 10, 40 min) et Cu2 O (pH 12, 20 min), est similaire en raison de la morphologie et de la surface spécifique similaires, comme le montrent les Fig. 2c et 3a et b. Les performances photocatalytiques du Cu2 vierge O est plus pauvre que celui des nanotiges de ZnO vierges en raison d'une plus grande frontière cristalline, d'une mobilité des porteurs plus faible, d'une surface spécifique plus petite et d'une recombinaison plus facile des électrons et des trous. Les performances photocatalytiques du ZnO/Cu2 O (pH 10, 20 min), ZnO/Cu2 O (pH 10, 40 min) et ZnO/Cu2 O (pH 12, 20 min) est presque le même en raison de la morphologie similaire et de la surface spécifique de la couche supérieure Cu2 O, comme le montrent les Fig. 2b et 3e et f. Les performances photocatalytiques de trois hétérojonctions de ZnO/Cu2 O est inférieur à celui des nanotiges de ZnO vierges en raison de la plus petite surface spécifique de la couche supérieure Cu2 O en tant que connexion directe à la solution MO mais est supérieur à celui de Cu2 vierge O dû à l'effet d'hétérojonction de ZnO et Cu2 O. Les performances photocatalytiques du Cu2 L'architecture O/ZnO est la plus élevée dans le ZnO/Cu2 système O en raison de leur structure à hétérojonction et de la plus grande surface spécifique de la couche supérieure ZnO. Par rapport aux nanotiges clairsemées de ZnO sur Cu2 O (pH 12, 20 min) et trop de gros nanotiges de ZnO sur Cu2 O (pH 10, 40 min), Cu2 O (pH 10, 20 min)/ZnO a la meilleure performance photocatalytique parmi trois Cu2 Architectures O/ZnO résultant de nanostructures parfaites de ZnO cultivées sur Cu2 O (pH 10, 20 min), comme le montrent les Fig. 2d et 3c et d. L'influence sur le pH de la réaction, le temps de réaction et l'orientation de l'hétérojonction est discutée, et en conclusion, le temps de réaction a peu d'effet sur les performances photocatalytiques dans le ZnO/Cu2 système. En résumé, dans le ZnO/Cu2 Système O, Cu2 O (pH 10, 20 min)/ZnO a les meilleures performances photocatalytiques.
Les changements de concentration de MO avec ZnO, CuSCN (3D), CuSCN (NWs), ZnO/CuSCN (3D), ZnO/CuSCN (NWs), CuSCN (3D)/ZnO et CuSCN (NWs)/ZnO comme catalyseurs sont illustré dans le fichier supplémentaire 1 :Figure S6(b). Les performances photocatalytiques du CuSCN vierge sont inférieures à celles des nanotiges de ZnO vierges en raison d'une surface spécifique plus petite, d'une mobilité des porteurs plus faible et d'une recombinaison plus facile des électrons et des trous. Les performances photocatalytiques du CuSCN (NWs) sont meilleures que celles du CuSCN (3D) en raison de la plus grande surface spécifique des nanostructures CuSCN, comme le montrent les Fig. 4e et f. Les performances photocatalytiques du CuSCN (3D)/ZnO et du CuSCN (NWs)/ZnO sont meilleures que celles du ZnO en raison de leur structure à hétérojonction et de leur plus grande surface spécifique. CuSCN (NWs)/ZnO a les meilleures performances photocatalytiques que CuSCN (3D)/ZnO en raison des nanotiges de ZnO plus petites et mieux réparties cultivées sur la nanostructure CuSCN et de la plus grande surface spécifique qui en résulte. Dans le système ZnO/CuSCN, l'architecture ZnO/CuSCN a les meilleures performances photocatalytiques parmi ZnO, CuSCN, ZnO/CuSCN et CuSCN/ZnO en raison de la structure à hétérojonction, de la plus grande surface spécifique du matériau supérieur de l'hétérojonction, et la plus grande surface de contact avec la solution MO. Les nanotiges de ZnO sous structures CuSCN (3D) sont partiellement gravées par la solution réactionnelle CuSCN avec un pH érosif, et les nanotiges ZnO sous structures CuSCN (NWs) sont principalement gravées par la solution réactionnelle CuSCN avec un pH de 1,5 ne maintenant que le contour et quelques restes de nanotiges de ZnO, comme indiqué sur les figures 4a et b et le fichier supplémentaire 1 : figure S3 (a, b). Bien que les nanotiges de ZnO sous les structures CuSCN (3D) soient partiellement gravées, l'espace entre les nanotiges devient plus grand que celui parmi les nanotiges de ZnO vierges avec la plus grande surface spécifique qui en résulte et est plus clair et plus net que les nanotiges de ZnO sous les structures CuSCN (NWs) avec gravure presque complète. Ainsi, les performances photocatalytiques du ZnO/CuSCN (3D) sont meilleures que celles du ZnO/CuSCN (NWs). L'influence sur la morphologie de la nanostructure et l'orientation de l'hétérojonction sont discutées, et les deux peuvent affecter les performances photocatalytiques dans le système ZnO/CuSCN. En résumé, le ZnO/CuSCN (3D) a les meilleures performances photocatalytiques dans le système ZnO/CuSCN.
Fichier supplémentaire 1 : La figure S6(c) montre les changements de concentration de MO avec ZnO, NiO (1 min), NiO (10 min), ZnO/NiO (1 min), ZnO/NiO (10 min), NiO (1 min )/ZnO, et NiO (10 min)/ZnO comme catalyseur. Les performances photocatalytiques du NiO vierge (10 min) sont inférieures à celles des nanotiges de ZnO vierges en raison de la plus grande nanostructure, de la surface spécifique plus petite qui en résulte, de la mobilité des porteurs plus faible et de la recombinaison plus facile des électrons et des trous. Les performances photocatalytiques de NiO (1 min) sont meilleures que NiO (10 min) et ZnO en raison de la surface spécifique beaucoup plus grande des nanostructures NiO, comme le montrent les Fig. 5e et f. Les performances photocatalytiques du NiO (10 min)/ZnO sont inférieures à celles du ZnO en raison de la nanostructure encore plus grande de la couche supérieure NiO (10 min) et de la plus petite surface spécifique. As shown in Fig. 5c, ZnO nanorods are partially exposed growing through the meshwork of NiO (1 min) and the remnant part of the ZnO nanorods are remained in the meshwork. NiO (1 min) nanostructures are the multi-layer interspersed meshwork uniformly distributed on the ITO glass with much higher specific surface area, as shown in Fig. 5e. So, NiO (1 min)/ZnO has a little better photocatalytic performance than ZnO and a lower photocatalytic action than NiO (1 min). The photocatalytic performance of ZnO/NiO (1 min) and ZnO/NiO (10 min) is better than others due to their heterojunction structure and larger specific surface area. ZnO/NiO(1 min) architecture has the best photocatalytic performance in the ZnO/NiO system as a result of the heterojunction structure, extremely higher specific surface area of the upper material in the heterojunction, and the consequent larger contact area with the MO solution. The influence on reaction time and orientation of the heterojunction are discussed and both will give an effect on the photocatalytic performance in the ZnO/NiO system. In summary, ZnO/NiO (1 min) has the best photocatalytic performance in the ZnO/NiO system.
Figure 6a and b show the concentration changes of MO and the UV-vis absorption spectra of MO aqueous solution with ZnO, Cu2 O (pH 10, 20 min), CuSCN (3D), NiO (1 min), Cu2 O (pH 10, 20 min)/ZnO, ZnO/CuSCN (3D), and ZnO/NiO (1 min) as the catalysts. Among the four semiconductor nanostructures ZnO, Cu2 O (pH 10, 20 min), CuSCN (3D), and NiO (1 min), NiO has the most excellent photocatalytic performance owing to the multi-layer interspersed meshwork uniformly distributed and the consequent extremely higher specific surface area. ZnO has the bigger mobility and bigger specific surface area than Cu2 O and CuSCN so that ZnO has the better photocatalytic performance. Cu2 O has the better photocatalytic performance than CuSCN due to the bigger specific surface area. ZnO/NiO (1 min) heterostructure has the most excellent photocatalytic performance among all the heterostructures based on n-type ZnO and p-type Cu2 O, CuSCN, and NiO. It is owing to more charge transfer caused by heterojunction structure, more photo-generated carrier as a result of higher specific surface area caused by the meshwork nanostructure of the upper NiO directly contacting to MO, and less carrier recombination caused by more compact contact of NiO/ZnO than Cu2 O/ZnO and CuSCN/ZnO, as shown in Additional file 1:Figure S2(c), Figure S3(a), and Figure S4(a). In summary, NiO is the most suitable material for photocatalytic degradation of MO among the four semiconductor nanostructures of ZnO, Cu2 O, CuSCN, and NiO. The photocatalytic performance of the semiconductor can be affected both by the mobility and the specific surface caused by the nanostructure. ZnO/NiO (1 min) heterostructure has the most excellent photocatalytic performance among all the architectures based on ZnO, Cu2 O, CuSCN, and NiO. Influencing factor on the photocatalytic performance of all these architectures can be summarized as the inherent mobility of the material, the heterojunction architecture, and the morphology of nanostructure. The scheme of the photocatalysis mechanism using heterostructure photocatalyst is shown in Additional file 1:Figure S7. The mechanisms for improved photocatalytic properties are demonstrated in Additional file 1. To further assess the photocatalytic activity, we have compared the degradation ability of our best heterojunction in every system with other nanohybrids in Table 2. Compared with other catalysts, ZnO/NiO (1 min) demonstrated the best photocatalytic performance.
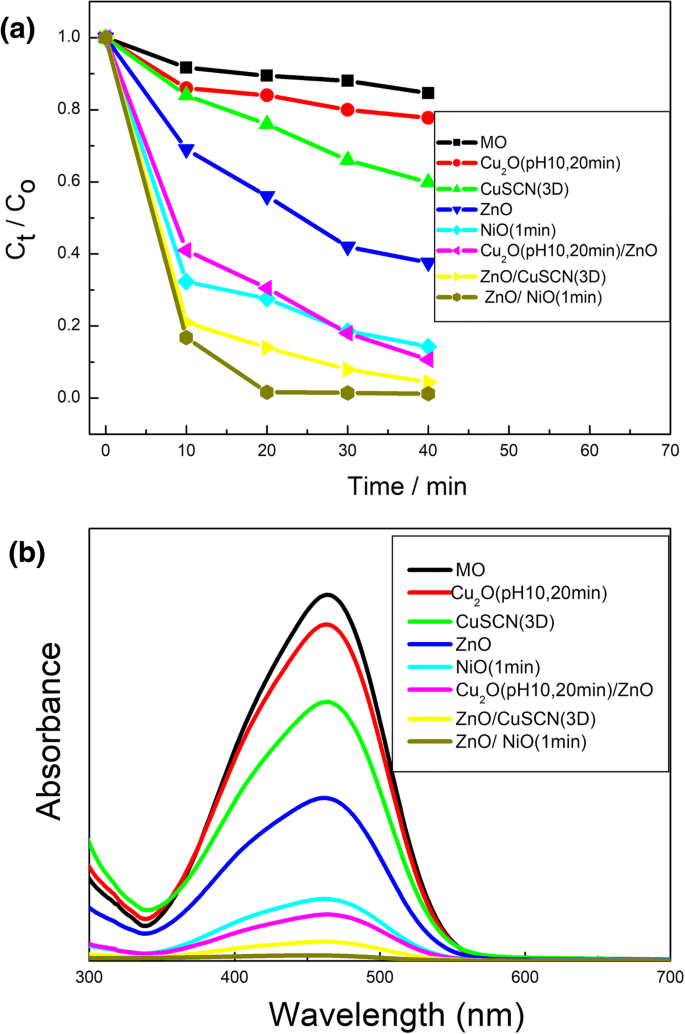
un The relative concentration (Ct /C0 ) of MO versus time under light irradiation in the absence and presence of various photocatalysts:ZnO, Cu2 O (pH 10, 20 min), CuSCN (3D), NiO (1 min), Cu2 O (pH 10, 20 min)/ZnO, ZnO/CuSCN (3D), and ZnO/NiO(1 min); b The UV-vis absorption spectra of MO aqueous solution with different photocatalysts:ZnO, Cu2 O (pH 10, 20 min), CuSCN (3D), NiO (1 min), Cu2 O (pH 10, 20 min)/ZnO, ZnO/CuSCN (3D), and ZnO/NiO(1 min)
Conclusions
In summary, different heterojunctions based on n-type ZnO nanorods and p-type Cu2 O, CuSCN, and NiO nanostructures with different orientations are fabricated. All these structures exhibit certain photocatalytic activity for the degradation of MO. Several conclusions can be summarized with analysis of these photocatalytic data as follows:the morphology of nanostructure has significant influence on photocatalytic activity; the photocatalytic activity of heterojunction structure is better than pristine semiconductor except consideration of the influence of the nanostructure morphology; the orientation of the heterojunction has no remarkable influence on photocatalytic activity; NiO has the best photocatalytic activity among the four pristine semiconductor nanostructures ZnO, Cu2 O, CuSCN, and NiO; and ZnO/NiO (1 min) heterostructure has the most excellent photocatalytic performance among all the architectures. The great enhancement of the photocatalytic activity is obtained using ZnO/NiO (1 min) heterostructure attributed to the heterojunction structure and extremely higher specific surface area. The study on the influence of materials, nanostructure morphology, and orientation in heterostructure on photocatalytic activity can provide a theoretical direction for the photocatalyst research with application in the energy and environment fields, and it can be concluded with a perspective on the future photocatalyst and a bright prospect of these controllable nanohybrid materials.
Abréviations
- 1D :
-
Unidimensionnel
- EDTA :
-
Ethylenediaminetetraacetic acid
- HMT:
-
Hexamethylenetetramine
- MO:
-
Methyl orange
- NW:
-
Nanowire
- SCE :
-
Électrode au calomel saturé
- SEM :
-
Microscopie électronique à balayage
- UV-vis DRS:
-
UV-vis diffuse reflectance spectrometry
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- L'évolution du SLS :nouvelles technologies, matériaux et applications
- La formule parfaite pour aligner les opérations et la maintenance
- Les meilleurs matériaux d'impression 3D en métal pour la fabrication additive
- Dévoilement de la structure atomique et électronique des nanofibres de carbone empilées
- Matériaux et conception de PCB pour haute tension
- Les meilleurs matériaux pour des prototypes de qualité alimentaire
- Les meilleurs matériaux pour vos prototypes médicaux
- Une méthode évolutive pour l'intégration à grande surface de matériaux 2D
- Freins, embrayages et matériaux de friction pour l'industrie pétrolière et gazière



