Comprendre l'activité antibactérienne photocatalytique dépendante de la structure :une étude de cas de la BiVO4 modifiée par Ag
Résumé
Dans ce travail, Ag/BiVO4 des photocatalyseurs hétérostructuraux ont été développés afin de révéler une cinétique exceptionnelle de migration de charge photo-induite dépendante de la structure ainsi que le processus dynamique antibactérien photocatalytique sous-jacent. L'interface dépendante de la structure de BiVO4 et des nanoparticules d'Ag ont été construites avec succès pour améliorer l'efficacité de transfert de charge d'interface photoinduite et la corrélation d'interface. Le calcul DFT a indiqué qu'une charge nette d'environ 0,33 e entre Ag et tz-BiVO4 a été obtenu par un transfert de charge d'interface extraordinaire, étant bien plus important que celui entre Ag et ms-BiVO4 . Une charge nette plus élevée a des conséquences sur la mobilité des porteurs de charge de tz-BiVO4 qui peut augmenter la migration et la séparation des porteurs de charge pour Ag/tz-BiVO4 hétérojonction. Contact interfacial fin entre Ag et tz-BiVO4 a conduit à des performances photocatalytiques optimisées vers E. coli inactivation, étant majoritairement supérieure à celle de tz-BiVO4 , ms-BiVO4 , et Ag/ms-BiVO4 catalyseurs. Outre l'activité photocatalytique, l'activité d'inactivation thermocatalytique de Ag/tz-BiVO4 présentait également un facteur d'environ 7,2 et 3,1 fois supérieur à celui du tz-BiVO4 et Ag/ms-BiVO4 . Les mesures de piégeage et d'EPR ont suggéré que l'activité photocatalytique dépendante de la structure de Ag/BiVO4 provient principalement de la variation prononcée de la capacité à produire H2 O2 espèces actives, où la capacité de générer H2 O2 sur Ag/tz-BiVO4 est fortement accéléré. De plus, on ne peut ignorer que cette étude constitue un candidat idéal pour de nombreux aspects, tels que la pollution de l'environnement et de l'eau causée par des micro-organismes pathogènes et la désinfection du matériel médical, des emballages alimentaires, des matériaux ménagers et des lieux publics, etc.
Contexte
L'utilisation de la lumière solaire et des semi-conducteurs à des fins photocatalytiques est toujours un point chaud de la recherche, qui trouve de nombreuses applications dans la conversion d'énergie et l'assainissement de l'environnement [1, 2]. Les nano-hétérojonctions ont également reçu une attention qui doit être prise au sérieux, car elles peuvent être appliquées à divers aspects et ont obtenu des résultats extraordinaires dans de nombreuses applications potentielles [3,4,5,6,7,8]. De plus, en raison de ses avantages d'énergie à haut rendement, respectueuse de l'environnement et renouvelable, la technologie antibactérienne photocatalytique a un rôle irremplaçable dans la gouvernance environnementale et la stérilisation [9, 10]. Récemment, BiVO4 émerge un excellent candidat en raison de sa structure cristalline accordable et de sa structure électronique appropriée [11, 12]. Cependant, malgré les caractéristiques structurelles favorables de BiVO4 , une transmission inefficace des porteurs de charge et une courte durée de diffusion des porteurs entravent son application dans la pratique. Du point de vue de la physique du solide, on pense que les performances photocatalytiques sont principalement régulées par la distorsion de la microstructure. Le zircon tétragonal (tz-) BiVO4 synthétisé par voie colloïdale éthylène-glycol contrôlable à température ambiante induit une activité photocatalytique fortement améliorée par rapport à la scheelite monoclinique (ms-) BiVO4 , pourtant le mécanisme sous-jacent reste ambigu [13]. Par conséquent, la modification de BiVO4 ne se limite pas à l'amélioration de l'activité photocatalytique; il est aussi absolument nécessaire d'expliquer la cinétique de transfert de charge photoinduite à partir de la microstructure.
Fréquemment, les localisations de porteurs de charge en excès comme les soi-disant polarons localisés accompagnées d'une régulation microstructurale et interfaciale ont un impact émotionnel intense sur la mobilité des porteurs de charge des semi-conducteurs oxydes. Polarons localisés dans BiVO4 soit inhibent la cinétique de mobilité des charges, soit influencent l'activité photocatalytique au niveau des surfaces [14, 15]. La reconstruction de structures de surface ou d'interface peut entraîner la variation de l'extension du polaron qui affecte la mobilité des porteurs de charge ainsi que les performances photocatalytiques. Les métaux nobles, comme Ag, Au et et al., peuvent agir comme photosensibilisateurs pour absorber la lumière visible et réguler la génération de porteurs de charge par transfert direct d'électrons ou connexion de couplage dipôle-dipôle [16, 17]. La jonction du métal noble avec le semi-conducteur pour établir le transfert de charge interfacial fournit une approche efficace pour influencer l'extension du polaron ainsi que la mobilité des porteurs de charge qui peut augmenter la migration et la séparation des porteurs de charge. Par exemple, la nanosphère Au décorée Mo:BiVO4 la photoanode affiche une intensité de photocourant augmentée d'environ 2,2 fois par rapport au Mo:BiVO4 [18]. Enquêtes récentes sur Ag/BiVO4 les nanostructures démontrent des performances photocatalytiques hautement améliorées vis-à-vis de l'oxydation de l'eau, de la dégradation des colorants organiques, etc. [19, 20]. La plupart des rapports se sont très souvent concentrés uniquement sur la caractérisation fine de la réponse photocatalytique, mais ne se sont pas concentrés sur les analyses microstructurales qui régissaient profondément les performances photophysiques et photochimiques natives des semi-conducteurs. Considérant la découverte des propriétés natives dépendantes de la structure, l'identification expérimentale de la structure de phase ainsi que la caractéristique de surface/interface de Ag/BiVO4 la nanostructure est essentielle et avantageuse pour réguler les propriétés natives et fournit quelques indications sur divers semi-conducteurs à structure liée.
Ici, ce travail vise à fournir une preuve en contrôlant rationnellement la structure de phase de BiVO4 et l'assemblage de nanoparticules d'Ag à des fins antibactériennes photocatalytiques afin de révéler la migration de charge photo-induite dépendante de la structure ainsi que le processus dynamique antibactérien photocatalytique sous-jacent.
Méthodes/Expérimental
Produits chimiques
Nitrate de bismuth (Bi(NO3 )3 • 5H2 O) (pureté 99%), nitrate d'argent (AgNO3 ) (pureté 99,8 %) et l'éthanol absolu (pureté 99,7 %) ont été obtenus auprès de Wind Ship à Tianjin Chemical Reagent Co. Ltd (Tianjin, Chine). Métavanadate d'ammonium (NH4 VO 3 ) (pureté 99,9 %) a été acheté auprès d'Adamas Reagent Co. Ltd (Shanghai, Chine). De l'eau distillée était également nécessaire. Tous les réactifs ont été utilisés sans autre purification.
Synthèse de BiVO4 et BiVO Ag-Loaded4
Synthèse de BiVO4
BiVO4 les échantillons ont été préparés par la méthode hydrothermale. Une millimole de Bi(NO3 )3 a été ajouté dans 20 mL d'eau distillée sous agitation douce, et une suspension blanche s'est formée pendant 30 min. Une millimole de NH4 VO 3 a été ajouté dans 40 mL d'eau distillée pour former une suspension blanche sous agitation pendant 30 min. Ensuite, NH4 VO 3 suspension a été goutte à goutte dans le Bi(NO3 )3 solution pour former une suspension orange. Le pH de la suspension orange est de 0,59. Une solution d'hydroxyde de sodium a été adoptée pour ajuster la valeur du pH de 0 à 12 pour la suspension ci-dessus. Et la suspension a été chargée dans un autoclave 100 % revêtu de Téflon. L'autoclave a été scellé et chauffé dans un four à 180 °C pendant 12 h. La valeur du pH de la suspension après la réaction a été maintenue. L'autoclave a ensuite été naturellement refroidi à température ambiante, où la poudre jaune obtenue a été collectée et lavée avec de l'eau distillée et de l'éthanol plusieurs fois pour éliminer les ions et les restes éventuels jusqu'à la valeur de pH proche de la neutralité et séchée sous vide pour une caractérisation ultérieure.
Synthèse de BiVO Ag-Loaded4
Un ensemble de cinq solutions identiques a été préparée, chacune contenant 1 g de BiVO4 mélangé dans 40 mL d'éthanol et soniqué pendant 10 min. Un autre ensemble de solutions contenant une quantité appropriée d'AgNO3 a été obtenu. Ensuite, AgNO3 solution aqueuse a été soigneusement versée dans BiVO4 solution et maintenu dans l'obscurité pendant 1 h sous agitation constante. Après cela, le mélange d'AgNO3 et BiVO4 a été exposé à la lumière UV pendant 2 h sous agitation de manière à ce que des nanoparticules d'Ag chargées BiVO4 échantillons. Les échantillons ont ensuite été séchés pendant une nuit à 60°C. La teneur initiale en charge d'Ag a été fixée à 1 % en poids, 3 % en poids, 5 % en poids, 7 % en poids et 10 % en poids.
Préparation des bactéries
La poudre lyophilisée a été dissoute et 1 mL de la suspension bactérienne a été collé à la plaque de culture solide avec un cure-dent stérilisé à chaud. La plaque de culture solide inoculée a été inversée et placée dans un incubateur à 37 °C pendant 12 h. Ensuite, la sélection de la colonie unique et l'expansion de la culture sont effectuées. La densité cellulaire finale a été ajustée à environ 1 × 10 7 –1 × 10 9 unité formant colonie (UFC) mL −1 .
Inactivation bactérienne photocatalytique
L'inactivation photocatalytique VLD d'Escherichia coli (E. coli ATCC 8099, bactéries Gram-négatives) et Staphylococcus aureus (S. aureus ATCC 25923, bactéries Gram-positives) par Ag/tz-BiVO4 a été réalisée sous irradiation de tubes fluorescents (PCX50C Discover). Une suspension (40 mL) contenant les cellules bactériennes et le photocatalyseur (40 mg). Ensuite, la solution a été allumée pour démarrer les expériences d'inactivation photocatalytique. À différents intervalles de temps, des aliquotes des échantillons ont été recueillies et diluées en série avec une solution aqueuse stérilisée. Ensuite, 1 mL des échantillons dilués a été immédiatement étalé sur des plaques de Nutrient Agar et incubé à 37 °C pendant 12 h pour déterminer le nombre de cellules de survie. S. aureus cultivé à 54°C pendant 24h. Pour la comparaison, un contrôle lumineux (cellules bactériennes et lumière sans photocatalyseur) et un contrôle sombre (photocatalyseur et cellules bactériennes sans lumière) ont également été effectués dans l'étude.
La performance de dégradation photocatalytique des échantillons préparés a été évaluée par photodégradation de la solution de colorant MB (bleu de méthylène) (5 mg/L, 30 mL) sous irradiation de lumière visible. Une lampe au xénon de 300 W équipée d'un filtre de coupure de 420 nm a été utilisée comme source lumineuse. Dans l'expérience de photodégradation, 15 mg de photocatalyseurs ont été dispersés dans 30 mL de la solution de colorant MB. Pour assurer l'équilibre d'adsorption et de désorption, le tube de quartz contenant la solution a été maintenu à l'obscurité pendant 1 h avant irradiation. À des intervalles de temps spécifiques, 4 mL de la suspension ont été collectés et analysés par spectromètre à réflectance diffuse UV-visible. Les pics d'absorption à 672 nm ont été utilisés pour déterminer la concentration de la solution de MB résiduelle.
Pour identifier les espèces réactives dominantes responsables de l'inactivation bactérienne photocatalytique, des composés spécifiques (c. Toutes les expériences ci-dessus ont été répétées en triple. Dans le même temps, l'expérience de capture de la dégradation photocatalytique de la solution de MB a également été réalisée.
Procédure de préparation pour l'observation SEM des bactéries
Les mélanges de photocatalyseur E. coli avant et après l'inactivation ont d'abord été prélevés et centrifugés et lavé la solution bactérienne deux fois avec du PBS (phosphate buffer saline). Après cela, les cellules récoltées ont été préfixées dans du glutaraldéhyde à 2,5 % pendant 12 h. Après avoir été lavés avec du PBS 0,1 M, les échantillons ont été déshydratés dans une série graduée d'éthanol (20 % pour une fois, 50 % pour une fois, 80 % pour une fois, 100 % pour une fois) chacun pendant 10 min puis laver les côtés avec t-butanol. Enfin, déposez-le sur une plaquette de silicium propre pour l'observation SEM.
Caractérisations de la morphologie, de la structure et des propriétés optiques
La pureté de phase de tous les échantillons a été caractérisée par diffraction des rayons X (XRD) sur le diffractomètre à rayons X Rigaku DMAX2500 en utilisant une cible en cuivre (λ =0,15406 nm). La vitesse de balayage était de 1° par minute, le pas de balayage était de 0,05° et la plage de balayage était réglée sur 5 à 80°. La morphologie des échantillons a été déterminée en utilisant la microscopie électronique à balayage (SEM) sur un appareil S4800 fonctionnant à 10 kV et la microscopie électronique à transmission (MET) sur un appareil DHG-9240B FEI avec une tension d'accélération de 200 kV. Une quantité appropriée de catalyseur à tester a été dispersée dans de l'éthanol absolu par dispersion ultrasonique. Dans le test SEM, l'échantillon dispersé a été déposé sur une plaquette de silicium propre, et dans le test TEM, il a été déposé sur une maille de cuivre supportée par un film de carbone. Des mesures de spectroscopie photoélectronique aux rayons X (XPS) ont été effectuées sur un Thermo ESCALAB 250 avec une raie Al Ka (1486,6 eV) à 150 W. Pour compenser les effets des charges de surface, les énergies de liaison ont été calibrées en utilisant le pic C 1 s à 284,60 eV comme le référence; le programme casaXPS a été utilisé pour réaliser la quantification des éléments. Les spectres diffus UV-visible des échantillons ont été mesurés à l'aide d'un spectromètre UV/vis Lambda 750 s. Le sulfate de baryum a été choisi comme substrat de référence et la plage de test de balayage a été fixée à 200 ~ 800 nm. Le spectre de tension de surface (SPV) a été obtenu par un système d'auto-assemblage composé d'une chambre d'échantillon, d'un amplificateur de verrouillage avec un hacheur de lumière et d'une lampe au xénon de 300 W comme source lumineuse. Les performances photoélectrochimiques des échantillons ont été enregistrées sur une station de travail électrochimique AUT302N (Metrohm) avec une cellule standard à trois électrodes. Parmi eux, les électrodes de l'échantillon de catalyseur, de l'Ag/AgCl standard et du platine ont été définies comme l'électrode de travail, de référence et de compteur, respectivement. La solution électrolytique était du sulfate de sodium (Na2 SO4 ) solution avec la concentration de 0,2 M, et la source lumineuse était une lumière LED. L'analyse des spectres de photoluminescence a été réalisée sur un spectrofluorimètre Edinburgh Instruments FLS920. Les spectres de résonance paramagnétique électronique (RPE) pour les radicaux hydroxyles (échantillon, 4 mg; DMPO, 0,22 M; volume de solution aqueuse, 2,0 mL) et les radicaux superoxyde (échantillon, 4 mg; DMPO, 0,22 M; volume de solution de méthanol, 2,0 mL) ont été fourni à la fois dans l'irradiation de lumière sombre et visible à 3186 G et 9056,895 MHz par un spectromètre à résonance de spin électronique ER200-SRC (Bruker, Allemagne). L'intensité du champ magnétique, l'intensité des micro-ondes et la largeur de balayage ont été fixées à 0,2 µmT, 1 µmW et 250 µmT, respectivement. L'échantillon à tester a été placé à l'intérieur du tube RMN, et le test a été réalisé dans l'air à température ambiante. Toutes les optimisations structurelles et les calculs de propriétés ont été effectués à l'aide du progiciel CASTEP basé sur la théorie de la fonctionnelle de la densité (DFT) dans Materials Studio 2017 R2. Le Perdew Burke Ernzerh (PBE) d'approximation de gradient généralisé (GGA) a été sélectionné pour la corrélation d'échange de l'interaction entre les électrons. L'énergie de coupure cinétique de 380 eV a été fixée. La fonction d'onde plane a été utilisée comme ensembles de base. Les calculs de l'état électronique et de la densité d'état ont été effectués sur la base de la structure cristalline optimisée.
Résultats et discussion
Les données XRD impliquent qu'une variation de la structure de phase de la scheelite monoclinique (ms-) à la structure tétragonale du zircon (tz-) de BiVO4 peut être atteint (Fig. S1). La jonction des nanoparticules d'Ag n'a conduit à aucune altération évidente des pics de diffraction de BiVO4 (Fig. 1a et Fig. S2). Cependant, à partir des résultats raffinés de Rietveld, il est noté que soit Ag/tz-BiVO4 ou Ag/ms-BiVO4 a montré une expansion de réseau apparente par rapport au tz-BiVO4 vierge et ms-BiVO4 échantillons, qui est résumé dans le tableau S1. Variation de réseau de BiVO4 matrice a promis un contact interfacial fin entre Ag et BiVO4 nanoparticules, ce qui est également prouvé par des observations MET. Les images TEM et HRTEM ont été données sur la figure 1b. Apparemment, soit ms-BiVO4 ou tz-BiVO4 peut servir de support pour lier des nanoparticules d'Ag hautement dispersées, où la teneur en nanoparticules d'Ag est proche de la valeur initiale telle que vérifiée par les données EDS (Fig. S3) [21, 22]. L'espacement d de 0,239 nm correspond au plan (111) de Ag (JCPDS n°87-0597), tandis que les franges adjacentes du réseau de 0,308 nm et 0,484 nm sont étroitement liées au plan (112) de ms-BiVO
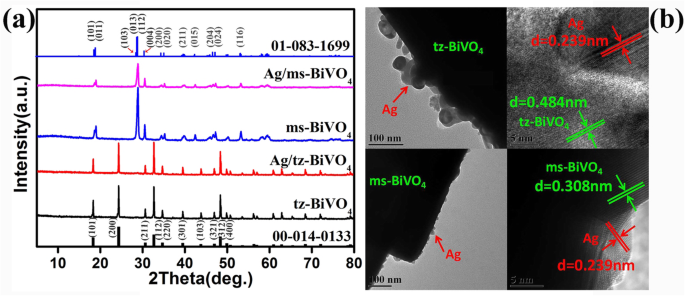
un Modèles XRD de tz-BiVO vierge4 , Ag/tz-BiVO4 échantillon, vierge ms-BiVO4 , et Ag/ms-BiVO4 goûter. b Image MET de Ag/tz-BiVO4 , HRTEM de Ag/tz-BiVO4 , image MET de Ag/ms-BiVO4 , et HRTEM de Ag/ms-BiVO4
Pour acquérir la composition chimique de surface et les états d'oxydation des échantillons tels que préparés, la technique XPS a été adoptée. Les résultats XPS peuvent pleinement vérifier que l'Ag/BiVO4 catalyseur a été préparé avec succès par les analyses des énergies de liaison sur les éléments Bi, V, O et Ag, comme illustré sur les Fig. 2 et Fig. S4. De la Fig. 2a, on voit que l'orbitale Bi 4f de tz-BiVO4 peut être bien reproduit à deux pics avec des énergies de liaison de 164,1 eV et 158,8 eV, qui peuvent être attribués au Bi 4f5/2 et Bi 4f7/2 orbitales, étant proche de la valeur rapportée précédente [23, 24]. Comme pour Ag/tz-BiVO4 , une énergie de liaison légère vers la baisse d'environ 0,3 eV a été observée pour l'orbitale Bi 4f. La figure 2b montre les données XPS haute résolution de l'élément V. Il est clair que les énergies de liaison de V 2p1/2 et V 2p3/2 localiser à ~ 524,2 eV et 516,6 eV pour un tz-BiVO4 vierge . Semblable à celle de l'orbitale Bi 4f, l'orbitale V 2p a également donné un décalage vers le rouge des énergies de liaison pour Ag/tz-BiVO4 hétérojonction. De plus, l'analyse XPS de O 1 s a également été illustrée sur la figure 2c. Trois énergies de liaison typiques de l'orbitale O 1 s pour tz-BiVO4 apparaît à 529,6 eV, 531,6 eV et 533 eV, respectivement, qui peuvent être attribués à l'oxygène du réseau, à l'oxygène de l'hydratation de surface ainsi qu'à l'O2 moléculaire absorbé chimiquement , respectivement [25]. Comme pour Ag/tz-BiVO4 , un décalage vers le rouge de ~ 0,2 eV a été observé pour l'oxygène du réseau par rapport au tz-BiVO4 vierge . Un tel comportement est supposé être lié à l'expansion du réseau ainsi qu'à l'interaction interfaciale entre Ag et tz-BiVO4 . Très souvent, l'expansion du réseau s'accompagne de liaisons de réseau moyennes allongées et d'une force affaiblie de ces liaisons, ce qui conduit à la diminution des énergies de liaison [26]. D'autre part, la variation des énergies de liaison reflète le réarrangement de la densité électronique à proximité des atomes, qui peut être influencé par la modification de surface. La diminution des énergies de liaison implique également le contact interfacial fin entre Ag et tz-BiVO4 , prédisant un transfert interfacial peut se produire, ce qui a entraîné la variation de la densité électronique [27]. Cette suspension peut être vérifiée par les résultats théoriques suivants. De plus, les données XPS ont également confirmé la caractéristique métallique des nanoparticules d'Ag, et aucune preuve d'Ag + a été observée dans Ag/tz-BiVO4 hétérojonction (Fig. 2d) [28]. Par contre, les résultats XPS de Ag/ms-BiVO4 ont également été donnés sur la figure S4. Similaire à celui de Ag/tz-BiVO4 hétérojonction, les énergies de liaison des orbitales Bi 4f, V 2p et O 1 s dans Ag/ms-BiVO4 présentait également un minuscule décalage vers le rouge d'environ 0,1 ~ 0,2 eV. La légère variation du décalage d'énergie de liaison dans Ag/tz-BiVO4 et Ag/ms-BiVO4 est probablement attribuable à la caractéristique interfaciale dépendante de la structure de BiVO4 et des nanoparticules d'Ag.
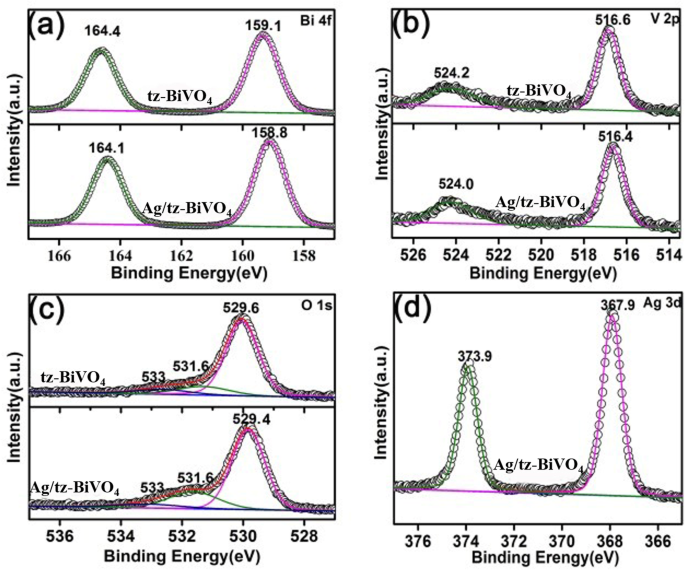
Spectres XPS de tz-BiVO4 et Ag/tz-BiVO4 échantillons :(a ) Bi 4f, (b ) V 2p, (c ) O 1 s, et (d ) Ag orbitale 3d
Depuis l'expansion du réseau de BiVO4 s'est produite après la modification de Ag, la structure électronique peut également être influencée, ce qui peut être vérifié par des calculs de la théorie fonctionnelle de la densité (DFT). En raison d'une grande disparité de réseau entre Ag et BiVO4 , la convergence et l'optimisation structurelle d'Ag/BiVO4 est inaccessible. Ainsi, un modèle cluster/surface a été établi pour révéler les corrélations interfaciales entre Ag et BiVO4 (Fig. S5 et Fig. S6). L'énergie de bande interdite de tz-BiVO4 a été estimée à 2,59 eV, ce qui est supérieur à celui de 2,17 eV pour ms-BiVO4 (Fig. S7), étant conforme aux résultats rapportés précédemment [13, 29]. L'ancrage du cluster Ag sur BiVO4 surfaces n'a pas de conséquences évidentes sur les transitions électroniques typiques de l'orbitale O 2p à V 3d, comme illustré par les spectres de réflectance diffuse UV-visible des échantillons tels que préparés (Fig. 3a). D'après la figure 3a, on voit que les deux ms-BiVO4 et tz-BiVO4 a montré une réponse à la lumière visible. Selon la théorie de Kubelka-Munk, l'énergie de la bande interdite des échantillons peut être calculée à partir de la relation entre l'absorption lumineuse et la bande interdite.
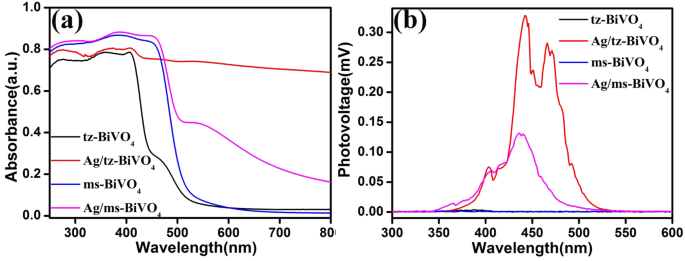
Spectres de réflectance diffuse UV-visible (a ) et les spectres de tension de surface (b ) des échantillons tels que préparés
(αhν ) 2 =A (hν − E g )
où α , h , ν , E g , et A taux d'absorption moyen, constante de Planck, fréquence, bande interdite et constante, respectivement. L'énergie de bande interdite de ms-BiVO4 et tz-BiVO4 a été estimée à 2,40 eV et 2,69 eV, respectivement (Fig. S8), ce qui est proche des résultats de la DFT. On note la modification des nanoparticules d'Ag sur BiVO4 surfaces ont conduit à une extension de l'absorption de la lumière visible (Fig. S9). L'absorption élargie devrait provenir des effets SPR des nanoparticules d'Ag. Outre la capacité d'absorption de la lumière visible, la modification de la nanoparticule d'Ag sur BiVO4 peut également avoir un impact important sur la cinétique des porteurs de charge photoinduits.
Comme illustré par les signaux de tension de surface (SPV) sur la figure 3b, le signal SPV maximal de tz-BiVO4 a été atteint à 0,33 mV après modification de l'Ag, ce qui est environ 91,7 fois supérieur à celui du tz-BiVO4 vierge . De plus, il est à noter que l'intensité du signal SPV pour Ag/tz-BiVO4 est également beaucoup plus élevé que celui d'Ag/ms-BiVO4 . Fréquemment, le signal SPV ne dérive que du processus de génération et de séparation de charge photoinduite, de sorte que l'intensité du signal SPV reflète l'efficacité de la séparation des porteurs de charge [30, 31]. Des signaux plus élevés prédisent souvent une efficacité de séparation de charge améliorée, ce qui suggère qu'une interaction plus forte entre Ag et tz-BiVO4 existe que pour Ag et ms-BiVO4 , étant encore clarifié par les calculs DFT. L'analyse de la population atomique suggère que tz-BiVO4 a acquis une charge nette d'environ 0,33 e après modification du cluster Ag. Tandis que pour ms-BiVO4 , seule une petite charge nette de ~ 0,04 e se produit lorsqu'elle est ancrée avec un cluster Ag (tableau S2). Puisque le transfert de charge interfacial dépend fortement des niveaux de Fermi ainsi que des structures électroniques. Pour confirmer la population atomique et l'isolement de charge entre Ag et BiVO4 , les fonctions de travail de BiVO4 et Ag/BiVO4 ont été donnés dans la Fig. 4. Comme illustré dans les Fig. 4 a et b, les fonctions de travail pour tz-BiVO4 et ms-BiVO4 ont été calculés à 4,569 eV et 5,621 eV en alignant le niveau de Fermi sur le niveau d'énergie du vide (EVL). Sur la base de la relation entre l'EVL et l'électrode à hydrogène normale (NHE) [32], les niveaux de Fermi de tz-BiVO4 et ms-BiVO4 ont été déterminés à 0,069 V et 1,121 V, respectivement. Compte tenu de la physique du solide, les électrons peuvent circuler entre les hétéro-interfaces, étant fortement dépendants de l'emplacement des niveaux de Fermi. Étant donné que le niveau de Fermi d'Ag se situe à 0,4 V vs NHE, ce qui est supérieur à celui de tz-BiVO4 pour que les électrons soient transférés de tz-BiVO4 surfaces à Ag. Par conséquent, Ag est chargé négativement et tz-BiVO4 est chargé positivement, étant conforme aux résultats DFT. Ce résultat prédit un champ électrique interne dirigé de Ag vers tz-BiVO4 , suggérant une injection efficace d'électrons photoinduits à partir de la bande de conduction de tz-BiVO4 à Ag se produirait. Comme pour ms-BiVO4 , son niveau de Fermi inférieur s'attend à un processus de transfert d'électrons inverse de Ag à ms-BiVO4 . Cependant, l'analyse de la population atomique a démontré qu'aucune migration d'électrons apparente entre Ag et ms-BiVO4 a été observé. Ce résultat peut impliquer une faible efficacité de séparation des porteurs de charge photoinduite pour Ag/ms-BiVO4 hétérocatalyseur.
La fonction de travail du tz-BiVO4 vierge (un ) et le ms-BiVO4 immaculé (b )
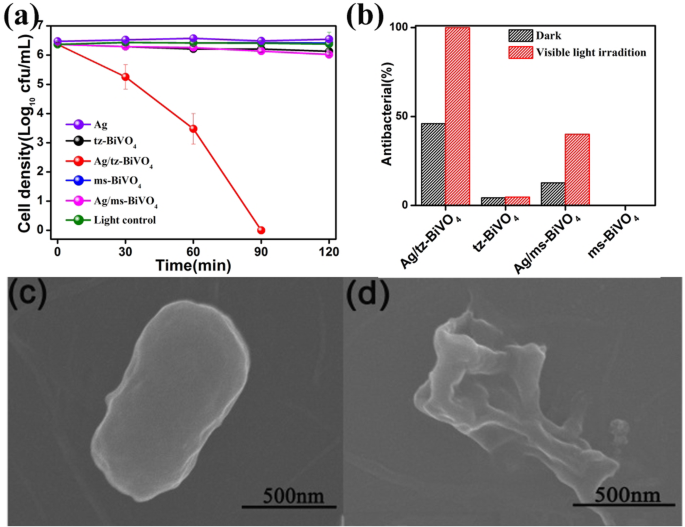
Compte tenu des résultats mentionnés ci-dessus, Ag/BiVO4 Les hétérostructures afficheraient des performances photocatalytiques dépendantes de la structure. Une bactérie sauvage, E. coli , a été choisie comme bactérie modèle pour étudier l'activité d'inactivation photocatalytique de Ag/tz-BiVO4 et Ag/ms-BiVO4 , respectivement. Parce que E. coli est une bactérie Gram-négative, une étude auxiliaire a également été réalisée en utilisant un représentant de bactéries Gram-positives avec S. aureus (Fig. S10). Une étude comparative a d'abord été menée pour vérifier l'inactivité de la lumière visible vers le E. coli inactivation. Comme le montre la figure 5a, les expériences d'inactivation de E. coli par tz-BiVO4 , Ag/tz-BiVO4 , ms-BiVO4 , et Ag/ms-BiVO4 ont été réalisées sous irradiation en lumière visible. On peut voir sur la figure 5a que les performances d'inactivation pour E. coli sur un tz-BiVO vierge4 et ms-BiVO4 photocatalyseur était simplement détectable. Cependant, l'ancrage des nanoparticules d'Ag peut moduler les performances d'inactivation photocatalytique de BiVO4 (Fig. S11). Pendant ce temps, une performance photocatalytique dépendante de la structure a été observée. Lorsque le rapport pondéral d'Ag atteint 7%, Ag/tz-BiVO4 a présenté une efficacité d'inactivation photocatalytique optimisée par rapport à E. coli par rapport à certains matériaux des rapports précédents (tableau S3). En 90 min, l'efficacité d'inactivation bactérienne atteint 100%, alors que Ag/ms-BiVO4 l'hétérophotocatalyseur présentait une activité photocatalytique minuscule envers E. coli inactivation sous irradiation LV (Fig. S11). Comme indiqué précédemment, les nanoparticules d'Ag ont montré une activité antibactérienne. Ainsi, une expérience contrôlée a été réalisée dans une chambre noire pour témoigner de la synergie de l'effet photocatalytique de l'Ag/BiVO4 hétérostructures pour l'inactivation de E. coli . Comme le montre la figure 5b, le processus d'inactivation a été mené en moins de 2 h sous irradiation VL ou dans l'obscurité pour comparer l'effet de stérilisation photocatalytique et thermocatalytique des catalyseurs tels que préparés. On constate que ms-BiVO4 était inerte à l'inactivation de E. coli , tandis que tz-BiVO4 présentait une faible activité sous irradiation VL ou dans l'obscurité. Après modification des nanoparticules d'Ag, l'activité thermocatalytique a été grandement améliorée. Par exemple, l'activité d'inactivation thermocatalytique de Ag/tz-BiVO4 amélioré un facteur d'environ 7,2 et 3,1 fois supérieur à celui de tz-BiVO4 et Ag/ms-BiVO4 . De plus, avec l'irradiation VL, l'activité catalytique des deux Ag/tz-BiVO4 et Ag/ms-BiVO4 a été majoritairement amélioré. Des résultats similaires peuvent être obtenus dans la dégradation photocatalytique de la solution de colorant MB (Fig. S12a). Après 7 h d'irradiation à la lumière visible, le taux de dégradation photocatalytique de la solution de colorant MB par 7Ag/tz-BiVO4 peut atteindre environ 85 %. Afin de connaître le processus de destruction de E. coli par Ag/tz-BiVO4 , l'observation SEM a été menée pour examiner les changements de morphologie au cours du processus d'inactivation photocatalytique, comme illustré sur les Fig. 5 c et d. Comme le montre la figure 5c, lorsque la bactérie n'était pas en contact avec le catalyseur, E. coli présentait une forme de bâtonnet bien conservée et une structure cellulaire intacte. Après 2hh de réaction d'irradiation, des structures membranaires désorganisées sont observées (Fig. 5d), ce qui démontre que la cellule est complètement décomposée. Cela correspond bien aux études précédentes selon lesquelles le traitement photocatalytique peut induire un trouble significatif de la perméabilité membranaire des cellules bactériennes.

L'inactivation photocatalytique de E. coli par Ag/tz-BiVO4 et Ag/ms-BiVO4 photocatalyseurs sous irradiation LV (a ). Etude comparative de l'effet de stérilisation photocatalytique et thermocatalytique (b ). Les images SEM d'individus E. coli cellule étant photocatalytiquement inactivée par Ag/tz-BiVO4 pour 0 h (c ) et 2 h (d )
Pour obtenir de plus amples informations sur le processus photocatalytique ainsi que sur les espèces oxygénées radicalaires qui déterminent le processus d'inactivation de E. coli , plusieurs types de piégeurs d'espèces radicalaires ont été soigneusement introduits en répétant le processus photocatalytique de E. coli inactivation. Comme le montre la figure 6a, l'oxalate de sodium, l'isopropanol, le Cr(VI), le Fe(II)-EDTA et la tétraméthylpipéridine (TEMPOL) ont été pris comme capteurs de trous (h + ), radicaux hydroxyles (•OH), électrons (e − ), H2 O2 , et les radicaux superoxydes (•O2 − ) [33, 34]. Avant que l'expérience sur les charognards ne soit réalisée, les concentrations de différents charognards ont été optimisées dans des recherches antérieures. When no scavenger was added, 10 6 cfu mL −1 of E. coli could be completely inactivated within 90 min. The bacterial inactivation is virtually suppressed with the addition of TEMPOL and Fe(II)-EDTA as the scavenger of •O2 − et H2 O2 , suggesting that •O2 − et H2 O2 played critical roles in the photocatalytic inactivation process. After the addition of sodium oxalate and isopropanol, it can be observed that the bactericidal inactivation efficiency over Ag/tz-BiVO4 were partially inhibited, suggesting that h + and •OH could directly destroy the E. coli cells with a powerful oxidation capability, whereas photoinduced electrons exhibited unobservable impact on the inactivation process of E. coli . And the capture experiment of photocatalytic degradation of MB dye solution was also carried out under visible light irradiation. In Fig. S12b, t-BuOH, silver nitrate (AgNO3 ), ethylenediaminetetraacetic acid (EDTA), and Fe(II)-EDTA were taken as the scavengers for •OH, e − , h + , et H2 O2 , respectivement. The results indicate that H2 O2 is the main active species in the experiment of photocatalytic degradation of MB dye solution. The active species •OH, e − , et h + also have different effects on the photocatalytic degradation process, which is different from the role of active species in the photocatalytic sterilization capture experiment caused by errors in the plate counting method.
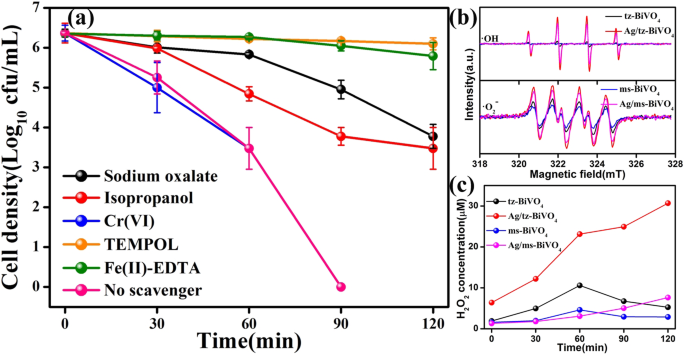
Photocatalytic inactivation efficiencies with respective scavengers in the presence of Ag/tz-BiVO4 (un ). EPR spectra of •OH and DMPO-•O2 − in the presence of pristine tz-BiVO4 , Ag/tz-BiVO4 , pristine ms-BiVO4 , and Ag/ms-BiVO4 under VL irradiation (b ). Relative concentration of H2 O2 by pristine tz-BiVO4 , Ag/tz-BiVO4 , pristine ms-BiVO4 , and Ag/ms-BiVO4 (the pH of the suspension was adjusted to 9 using NaOH and took 3.5 mL; 50 μL of 0.7 mM lucigenin solution was added) (c )
To acquire further information of the active species, electron paramagnetic resonance (EPR) measurement was used. In brief, DMPO acted as a spin trapper to testify the existence of •O2 − and •OH species [35, 36]. As displayed in Fig. 6b, very weak characteristic EPR signal of DMPO-•OH species was observed by prolonging VL irradiation time (Fig. S13). After Ag nanoparticles modification, the intensity of EPR signal of DMPO-•OH was drastically improved for both tz-BiVO4 and ms-BiVO4 , suggesting that the capability to generate •OH for BiVO4 was greatly enhanced with Ag nanoparticles anchoring, being originated from the enhancement of charge carrier separation efficiency. Moreover, it is noted in Fig. 6c that the typical EPR signal of DMPO-•O2 − was also detected for all as-prepared samples (Fig. S14). Similar result to the EPR signal of DMPO-•OH is that the intensity of DMPO-•O2 − was also improved for Ag/tz-BiVO4 and Ag/ms-BiVO4 heterostructures. Interestingly, the EPR signal intensity of either DMPO-•OH or DMPO-•O2 − for Ag/tz-BiVO4 is higher than that for Ag/ms-BiVO4 . For photocatalytic process, the electronic band potential always plays dominate roles in modulating the active species as well as the photocatalytic activity. On the basis of Mulliken electronegativity and band gap energy [37], the conduction band potentials of tz-BiVO4 and ms-BiVO4 were calculated to be about 0.21 V and 0.30 V versus NHE (S15). Thereby, the valence band potentials tz-BiVO4 and ms-BiVO4 were determined to be 2.90 V and 2.70 V versus NHE. According to previous literatures, the redox potential of •OH/H2 O locate at 2.38 V versus NHE [38], suggesting the participation of •OH in the photocatalytic process for the inactivation of E. coli . However, it is seen that the redox potential of •O2 − /O2 (− 0.33 V versus NHE) is more negative than the conduction potential of tz-BiVO4 and ms-BiVO4 , indicating both tz-BiVO4 and ms-BiVO4 are not capable to generate •O2 − reactive species. This result seems to be contrary to the trapping experiments. Then, it is necessary to specify the origination of the •O2 − reactive species. In aqueous solution, a photoinduced hole can oxidize H2 O2 to produce one •O2 − via the following equation:H2 O2 + h + → •O2 − + 2H + [39]. Moreover, the generation •O2 − can also be achieved by reaction of H2 O2 with •OH by the following equation:H2 O2 + •OH → •O2 − + H2 O + H + [40]. From this point, the capability for the generation of H2 O2 over the as-prepared BiVO4 samples should be investigated. The concentration of H2 O2 as a function of VL irradiation time was given in Fig. 5c. Clearly, H2 O2 can be generated for all as-prepared samples under VL irradiation. Predominantly, H2 O2 concentration gradually increased from 6.40 to 30.69 μM in initial 120 min under VL irradiation for Ag/tz-BiVO4 heterostructure, which is much higher than the other samples. Consequently, junction of Ag and tz-BiVO4 can greatly improve the capability of the photocatalysts to generate H2 O2 due to the fine interfacial contact, which resulted in highly improved photocatalytic activity toward E. coli inactivation as well as the phase dependent photocatalytic activity of Ag modified BiVO4 heterostructures.
As a result, a plausible explanation for the inactivation of E. coli over Ag/tz-BiVO4 was proposed. As the CB edge potential of tz-BiVO4 is higher than that of the metallic Ag nanoparticles, the electrons in the CB of tz-BiVO4 can quickly transfer toward to Ag nanoparticles, inhibiting the recombination of electron–hole pairs between the VB and CB of BiVO4 . The photogenerated holes migrate to the surface of the semiconductor and then directly contact with bacteria, or even produce H2 O2 and •OH with H2 O molecules. Simultaneously, the enrichment of electrons on the Ag nanoparticles may be subsequently scavenged by H2 O2 to produce •OH active species. The free radicals can react with the organic matter that constitutes the microbial organism and directly oxidize the organic matter into inorganic substances such as CO2 et H2 O. This process will change the original state and properties of the microbial organism, thereby directly hindering the proliferation of microbial cells and preventing bacteria.
Conclusions
In summary, Ag/BiVO4 heterostructural photocatalysts were developed with the aim to deliver a proof by rationally controlling the phase structure of BiVO4 and assembling Ag nanoparticles for photocatalytic antibacterial purpose in order to reveal structural-dependent photoinduced charge migration as well as the underlying photocatalytic antibacterial dynamic process. DFT theoretical calculation indicates an interfacial charge transfer between Ag and tz-BiVO4 with a net charge of about 0.33 e, which is far larger than that between Ag and ms-BiVO4 , predicting fine interfacial contact and improved charge separation efficiency of Ag/tz-BiVO4 . Relying on further experimental characterization, the optimized photocatalytic performance toward E. coli inactivation of Ag/tz-BiVO4 is predominately higher than that of tz-BiVO4 , ms-BiVO4 , and Ag/ms-BiVO4 catalyseurs. Besides photocatalytic activity, the thermocatalytic inactivation activity of Ag/tz-BiVO4 also exhibited a factor of about 7.2 and 3.1 times higher than that of tz-BiVO4 and Ag/ms-BiVO4 . In combination with trapping experiment and EPR measurement, •O2 − , •OH, and H2 O2 active species played critical roles in the photocatalytic inactivation process. Moreover, detailed investigation suggested that the structural-dependent photocatalytic activity of Ag/BiVO4 mainly originated from the pronounced variation of the capability to produce H2 O2 active species, where the capability of generating H2 O2 over Ag/tz-BiVO4 is highly accelerated. This work provides hints for regulating the native properties of various structural-linked semiconductors.
Disponibilité des données et des matériaux
Les ensembles de données soutenant les conclusions de cet article sont inclus dans l'article.
Abréviations
- SEM:
-
Microscopie électronique à balayage
- TEM :
-
Microscopie électronique à transmission
- XRD :
-
X-ray power diffraction
- XPS :
-
Spectroscopie photoélectronique aux rayons X
- EPR :
-
Electron paramagnetic resonance
- SPV :
-
Surface photovoltage spectrum
- DFT :
-
Théorie fonctionnelle de la densité
Nanomatériaux
- Comprendre l'UART
- Comprendre les avantages de la maintenance prédictive
- Comprendre les bases de la fraiseuse
- Comprendre la valeur de l'automatisation dans la fabrication
- Comprendre le fonctionnement de l'amortisseur
- Comprendre le terme couplage
- Comprendre la flexibilité d'un matériau
- Comprendre les applications du moteur diesel
- Comprendre le fonctionnement d'un radiateur de chauffage



