Mécanisme de formation de la structure chimique du noyau cutané dans les monofilaments de polyacrylonitrile stabilisés
Résumé
Bien qu'il y ait un demi-siècle depuis que les fibres de carbone à base de polyacrylonitrile (PAN) ont été développées pour la première fois, le mécanisme exact de formation de la structure peau-noyau des fibres de carbone à base de PAN, en particulier les fibres de PAN stabilisées, n'était toujours pas bien clarifié du point de vue de la structure chimique. Afin de relever ce défi susmentionné, un outil puissant avec une résolution à l'échelle nanométrique nommé microscopie à force photo-induite a été appliqué pour cartographier la distribution des groupes chimiques dans la section transversale des fibres PAN stabilisées et révéler le mécanisme d'évolution de la structure du noyau de la peau tout au long de la stabilisation. traiter. Les résultats ont indiqué que la formation de la structure peau-cœur de la fibre PAN stabilisée était attribuée aux réactions chimiques complexes et superposées causées par le gradient d'oxygène le long de la direction radiale et la formation d'une couche cristalline dense à l'interface entre la peau et la partie centrale. Enfin, la couche cristalline a été détruite et les monofilaments avaient tendance à être homogènes avec une oxydation supplémentaire.
Introduction
La fibre de carbone à base de PAN (CF) est un matériau de pointe avec une résistance à la traction et un module de Young élevés, ainsi qu'une excellente résistance à la chaleur. En raison de ses propriétés supérieures, il a été largement appliqué comme matériau structurel renforcé dans l'aviation, l'aérospatiale et d'autres nouveaux domaines industriels [1,2,3]. Actuellement, les fibres de carbone les plus résistantes disponibles dans le commerce possèdent une résistance à la traction de ~ 7 GPa. Cependant, sur la base des calculs de force de liaison –C–C avec un modèle de graphite idéal, la résistance théorique des fibres de carbone est d'environ 180 GPa [4]. L'énorme écart entre la résistance à la traction réelle et théorique est principalement attribué à la structure hétérogène peau-noyau de la fibre de carbone. Cette hétérogénéité structurelle entraîne une répartition inégale des contraintes dans le monofilament en fibre de carbone. La destruction a tendance à se produire dans la zone, qui subit un stress plus élevé, entraînant ainsi la rupture de la fibre de carbone [5,6,7]. Par conséquent, il est très important de comprendre le mécanisme de formation de ce défaut structurel et de minimiser son effet sur les propriétés des fibres de carbone résultantes.
La fabrication des fibres de carbone implique trois étapes, dont le filage des précurseurs de PAN, la stabilisation thermique et la carbonisation. Parmi celles-ci, la stabilisation thermique est l'étape la plus complexe qui implique des réactions telles que la cyclisation, la déshydrogénation et l'oxydation. La réaction de cyclisation conduit à la génération de structures cyclisées et à la conversion de -C≡N en -C=N. La réaction de déshydrogénation est associée à la formation de –C=C. Les groupes carbonyle sont introduits après que les fibres précurseurs aient subi une réaction d'oxydation [2, 8]. Le processus de stabilisation contribue à la transformation des chaînes PAN linéaires en une structure en échelle infusible et résistante à la chaleur, ce qui est nécessaire pour le processus de carbonisation [9,10,11]. La préparation de la fibre de carbone à base de PAN est un processus continu, pour le dire autrement, et la structure finale hétérogène peau-noyau en fibre de carbone est principalement héritée de la fibre PAN stabilisée. Par conséquent, révéler le mécanisme de formation de la structure peau-noyau du monofilament PAN stabilisé, en particulier la distribution structurelle chimique, est bénéfique pour minimiser l'hétérogénéité structurelle au sein de la fibre de carbone.
De nombreuses études ont porté sur la stabilisation des fibres PAN. Cependant, les recherches sur la structure peau-noyau des fibres PAN stabilisées sont très limitées. Lv et al. [12] ont rapporté que la diffusion hétérogène de l'oxygène de la peau au noyau entraîne la formation d'une région cutanée dense, qui retarde la diffusion ultérieure de l'oxygène et conduit à la formation d'une structure peau-noyau. Nunna et al. [13] ont utilisé la spectroscopie Raman et l'analyse élémentaire pour révéler la structure du noyau cutané des fibres stabilisées. Ces travaux élégants ont grandement contribué à l'étude de la structure peau-cœur des fibres de PAN stabilisées. Cependant, ils se concentrent principalement sur la propriété mécanique radiale des fibres de stabilisation PAN plutôt que sur la structure chimique, les informations structurelles détaillées ne sont toujours pas très claires. Par conséquent, l'équipement à haute résolution spatiale est nécessaire pour l'étude de la structure chimique peau-noyau des fibres PAN stabilisées à différentes étapes du processus de stabilisation.
Dans cette étude, la microscopie à force photo-induite (PiFM) a été appliquée pour analyser le mécanisme de formation de la structure chimique de la peau au sein des monofilaments PAN stabilisés à différentes températures. Comme le montre la Fig. 1, PiFM est une technique de microscopie à sonde à balayage de pointe qui combine une pointe de microscopie à force atomique (AFM) avec un laser infrarouge accordable pour induire un dipôle pour l'imagerie chimique. Il peut offrir une résolution latérale de ~ 10 nm. Il y a un pouls à f m = f 1 − f 0 , où f 0 et f 1 sont les première et deuxième résonances mécaniques du mode propre du porte-à-faux. La topographie et le signal PiFM de l'échantillon sont enregistrés simultanément par le système de rétroaction AFM à f 1 et f 0 , respectivement [14].
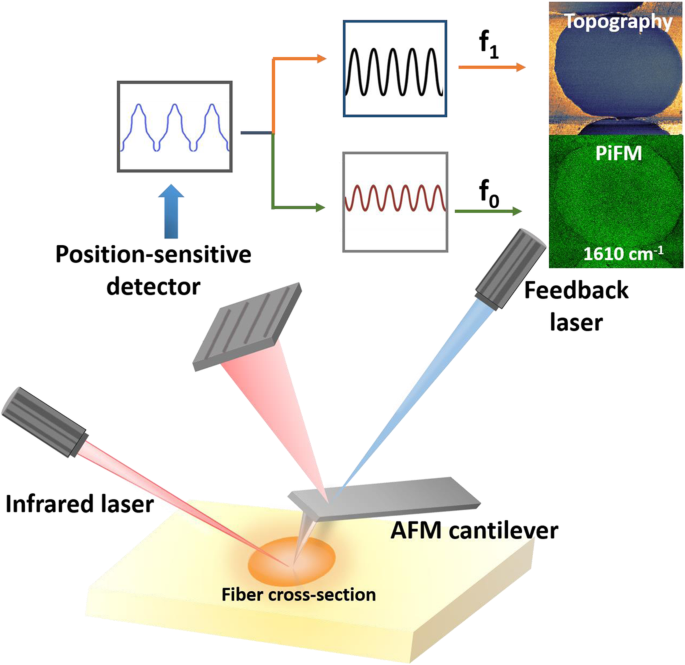
Schéma simplifié de la configuration de la microscopie à force photo-induite (PiFM)
Méthodes
Préparation de l'échantillon
Des échantillons de différents stades de stabilisation sous différentes températures ambiantes ont été collectés. Les fibres PAN utilisées dans cette étude sont les fibres précurseurs 6 K de HENGSHEN T700 (HENGSHEN Co. Jiangsu, CHINE). Les fibres précurseurs passaient en continu dans cinq fours avec des températures progressivement croissantes (210 °C, 220 °C, 230 °C, 240 °C, 250 °C). Les échantillons ont été notés de 01 à 05 de manière séquentielle. Le temps de stabilisation dans chaque four était de 8 min et la vitesse de déplacement du câble était de 30 m/h.
La procédure de préparation des échantillons pour les mesures PiFM est la suivante :tout d'abord, un câble de fibre est attaché directement au bas du modèle pour s'assurer que l'axe de la fibre est parallèle et proche de la surface du bloc époxy, puis noyé dans la résine époxy. Pour acquérir la section transversale, la surface perpendiculaire à l'axe de la fibre a été meulée et polie mécaniquement par une machine à polir (Struers Inc.).
Caractérisation
Des mesures PiFM (Molcular Vista, USA) ont été effectuées pour étudier les changements de groupes fonctionnels dans différentes positions radiales du monofilament pendant la stabilisation et ont été opérées sans contact pour éviter que les échantillons les plus mous ne soient endommagés et obtenir une résolution spatiale plus élevée que la topographie AFM.
La spectroscopie Raman a été réalisée avec un objectif × 100 en utilisant le laser 532 nm de la spectroscopie confocale Raman (RM2000, Renishaw, Royaume-Uni).
Résultats et discussions
La figure 2b présente les spectres PiFM typiques dans 1400–1900 cm −1 région à différentes positions le long de la direction radiale. La bande d'absorption autour de 1580 cm −1 est due à la combinaison des vibrations des modes d'étirement –C=C et –C=N [15]. La bande d'absorption autour de 1720 cm −1 est attribué au ν C=O . On a pu observer que l'intensité de ces deux bandes changeait avec les positions. Ce phénomène était dû aux diverses structures chimiques formées par les différentes réactions le long de la direction radiale lors de la stabilisation. Cependant, l'évolution de la structure chimique peau-noyau dans les monofilaments n'a pas pu être révélée visuellement. Par conséquent, la cartographie PiFM a été réalisée dans les deux modes de vibration avec une spécificité à l'échelle nanométrique.
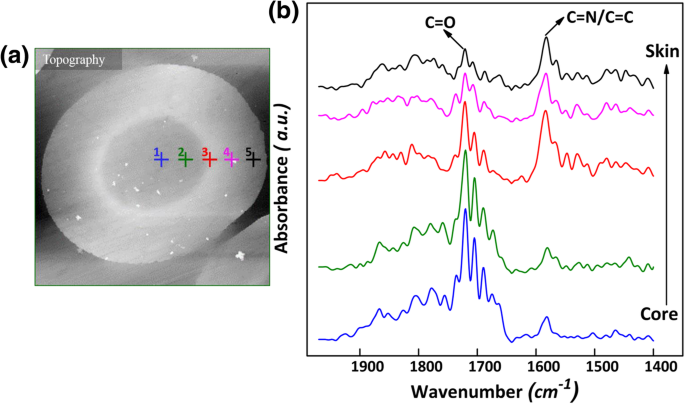
un Image topographique de l'échantillon 03 ; b Les spectres en 1400–1900 cm −1 de différents points le long de la direction radiale
La figure 3 montre la topographie et la cartographie PiFM de l'intensité d'absorbance à 1600 et 1730 cm −1 des échantillons 01–05. L'intensité de ν –C=C et ν –C=N à 1600 cm −1 du noyau était évidemment plus petit que celui de la peau. Cela a été attribué aux différentes réactions chimiques causées par la distribution du gradient de concentration en oxygène dans la section transversale. Les schémas de réaction chimique proposés du PAN traité thermiquement sont illustrés dans le schéma 1, la déshydrogénation est principalement entraînée par l'oxygène, tandis que la condition anoxique est plus propice à l'apparition de la cyclisation [16]. Au stade initial, plus d'oxygène était concentré dans la partie de la peau, donc cette partie avait tendance à se produire par réaction de déshydrogénation et à générer plus de liaisons insaturées. Les liaisons insaturées formées dans la partie de la peau ont amélioré l'intensité globale à 1600 cm −1 . De plus, un anneau brillant apparaissait à l'interface entre la peau et le noyau des échantillons 02 et 03, ce qui peut être attribué à la formation d'une couche cristalline à l'interface. Nunna et al. [17] ont prouvé que les propriétés mécaniques de la peau et de l'âme sont différentes, et que le module réduit de la peau est supérieur à celui de l'âme. Bien que la peau et le noyau subissent une même contrainte en fonction de la force d'étirement pendant la stabilisation, la capacité de résistance à la déformation des chaînes moléculaires dans la peau était supérieure à celle du noyau en raison d'un module plus élevé. Par conséquent, il y avait une force de cisaillement émergeant à l'interface entre la peau et la partie centrale. Dans ce cas, les chaînes moléculaires dans la région d'interface s'empileraient plus efficacement et régulièrement sous la force de cisaillement, générant ainsi une densité plus élevée de groupes fonctionnels -C=N et -C=C. Selon la loi de Lambert-Beer, il devrait y avoir une augmentation de l'intensité d'absorption infrarouge, entraînant l'apparition de l'anneau brillant. De plus, la couche cristalline fine et dense retarde davantage la diffusion de l'oxygène vers le cœur. Par conséquent, la différence peau-noyau de l'échantillon 03 a été encore agrandie. Cependant, au fur et à mesure du processus de stabilisation, l'anneau brillant a progressivement disparu et les monofilaments ont eu tendance à être homogènes, comme le montre la figure 3 04-05. C'est parce que la poursuite de l'oxydation conduit à la destruction de la couche barrière cristalline, ce qui a été bénéfique pour la diffusion de l'oxygène et la déshydrogénation dans la partie centrale. Ceci est également en bon accord avec le phénomène que la cristallinité de la fibre PAN stabilisée présente augmentant initialement, puis montre une diminution continue avec l'augmentation de la température [18].

Topographie des échantillons 01-05 ; Cartographie PiFM de l'intensité d'absorbance à 1600 et 1730 \( {\mathsf{cm}}^{-\mathsf{1}} \) pour les échantillons 01-05
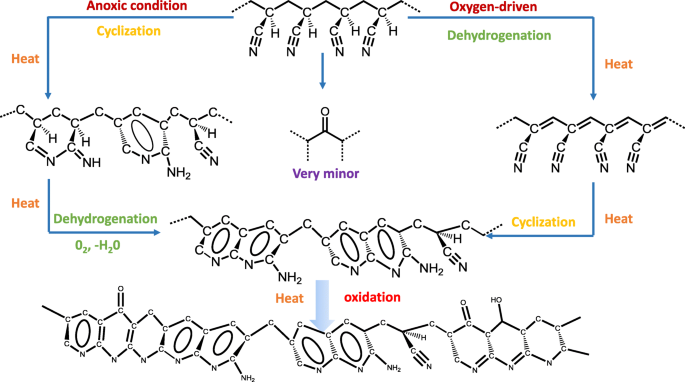
Modifications structurelles proposées pendant la stabilisation
D'autre part, bien que l'intensité globale à 1730 cm −1 n'a montré presque aucune augmentation jusqu'à l'échantillon 04, une différence évidente de peau-noyau a été observée dans les échantillons 02 et 03. C'est parce que le PAN a été obtenu par la copolymérisation d'acrylonitrile et d'acide itaconique qui contient un groupe carbonyle. Au stade initial, la réaction de déshydrogénation avait tendance à se produire dans la partie de la peau, de sorte que le groupe carbonyle a été éliminé sous forme de H2 O. Par conséquent, la partie centrale a une concentration plus élevée de groupe carbonyle. Avec la stabilisation supplémentaire, la température plus élevée et l'uniformité améliorée de la teneur en oxygène le long de la direction radiale ont favorisé l'oxydation dans la peau et la déshydrogénation dans le noyau simultanément dans les échantillons 04 et 05. L'oxydation impliquait non seulement la formation de liaisons -C=O, mais a également amélioré la déshydrogénation en éliminant l'hydrogène sous forme de H2 O [19]. Comme le montre la Fig. 3, il est clair d'observer que les structures conjuguées et oxydées ont tendance à être homogènes dans les échantillons 04 et 05 en termes d'intensités d'absorbance à 1600 et 1730 cm −1 .
Comme le montre la figure 3, les échantillons étaient principalement riches en -C=O dans la région centrale et riches en -C=N/−C=C dans la région de la peau. La figure 4 montre le mappage PiFM des échantillons 01 à 03. Pour la quantification, le rapport de I–C=O /I–C=N/−C=C a été calculé et présenté dans le tableau 1, qui a été considéré comme le rapport de la structure oxydée à la structure conjuguée. Il y avait une nette diminution des échantillons 01 à 03, montrant que la concentration plus élevée de doubles liaisons carbone-carbone était générée après une réaction de déshydrogénation supplémentaire dans la région de la peau.
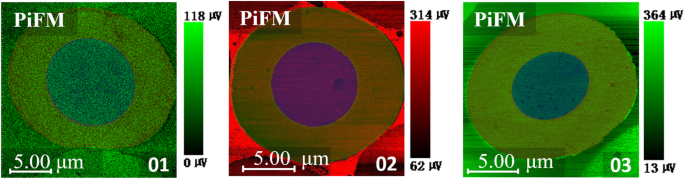
Analyse micro-zone sur l'image
Des mesures Raman pour la section transversale des fibres ont été effectuées pour prouver davantage que les domaines de réaction de déshydrogénation dans la région de la peau. Le rapport d'aire intégrale de la bande D à G A D /Un G la valeur est considérée comme le sp 2 /sp 3 –Rapport C [20]. La figure 5 montre le A D /Un G valeur dans la peau et les régions centrales des fibres par rapport à la température de traitement de 220 °C à 250 °C (il n'y avait presque pas de signal de bande D et G de l'échantillon 01, ce qui est dû au faible degré de réaction de déshydrogénation et au fort effet de fluorescence causé par substance organique). Une différence significative existait entre la peau et le noyau, la partie de la peau ayant une concentration plus élevée de sp 2 atomes de carbone hybrides. Cela a été attribué à un degré plus élevé de réaction de déshydrogénation dans la partie de la peau, ce qui conduit à la formation de -C=C. Au fur et à mesure du processus de stabilisation, le A D /Un G valeur légèrement diminué, indiquant le degré plus élevé de graphitisation. Ceci est en bon accord avec les résultats de la cartographie PiFM.
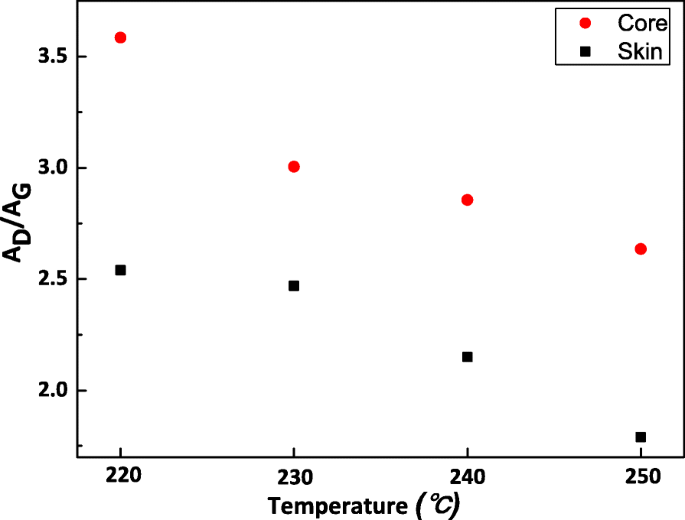
Le A D /Un G valeur dans la peau et les régions centrales des fibres par rapport à la température de traitement de 220 °C à 250 °C
Afin de décrire schématiquement la formation de la structure chimique du noyau de la peau de la fibre stabilisée par PAN, un schéma global du mécanisme de formation le plus probable est dessiné sur la figure 6. Les différentes réactions sont étiquetées par la couleur correspondante, le bleu représente la déshydrogénation, le jaune représente cyclisation, et le rouge marque l'oxydation. La formation de la structure chimique peau-noyau a été causée par le domaine de cyclisation dans la région du noyau tandis que la partie de la peau a subi le domaine de déshydrogénation entraînée par l'oxygène. Cela peut être attribué à la distribution hétérogène de l'oxygène dans la peau et la partie centrale. En outre, l'hétérogénéité structurelle a également été augmentée par la couche cristalline formée à l'interface entre la peau et le noyau. Avec le développement du processus de stabilisation, la couche cristalline a été détruite par oxydation. Séquentiellement, le degré accru d'oxydation dans l'ensemble du monofilament pourrait favoriser l'homogénéité apparente de la fibre.
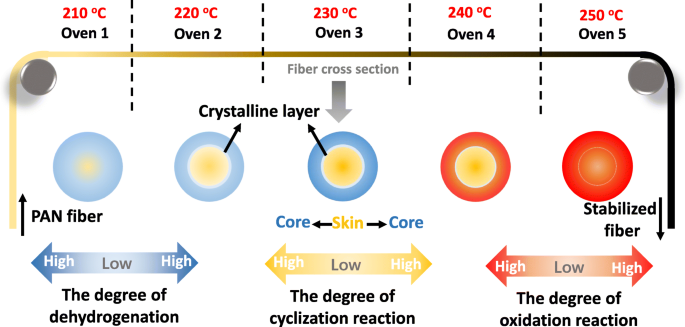
Mécanisme de formation de la structure skin-core des fibres PAN stabilisées
Conclusions
Cette étude montre que la structure peau-cœur des fibres de PAN stabilisées initialement formées par cyclisation s'est produite dans une région centrale tandis que la partie de la peau a subi le domaine de déshydrogénation entraînée par l'oxygène. Ensuite, avec le degré d'oxydation plus élevé, les filaments pourraient avoir tendance à être homogènes.
Abréviations
- AFM :
-
Microscopie à force atomique
- PAN :
-
Polyacrylonitrile
- PiFM :
-
Microscopie à force photo-induite
Nanomatériaux
- Feutre
- Spandex
- Fil
- Corde
- Mécanisme de formation de super-réseaux de nanoparticules bien ordonnés et denses déposés à partir de la phase gazeuse sur des surfaces sans gabarit
- Dévoilement de la structure atomique et électronique des nanofibres de carbone empilées
- Structure et propriétés électroniques de la nanoargile de kaolinite dopée par un métal de transition
- Influence des conditions de formation de nanomatériaux Pd/SnO2 sur les propriétés des capteurs d'hydrogène
- C - Structure du programme



