Élimination des antibiotiques de l'eau avec une membrane de nanofiltration 3D 100 % carbone
Résumé
Les récents développements industriels et l'augmentation de la demande énergétique ont entraîné une augmentation significative des niveaux de polluants environnementaux, qui sont devenus un grave problème mondial. Ici, nous proposons une nouvelle membrane de nanofiltration (NF) tout carbone qui se compose de nanotubes de carbone multi-parois (MWCNT) interposés entre des nanofeuillets d'oxyde de graphène (GO) pour former une structure tridimensionnelle (3D). La membrane telle que préparée contient de nombreux nanocanaux bidimensionnels (2D) capables de tamiser physiquement les molécules d'antibiotiques par interaction électrostatique. En conséquence, la membrane préparée, d'une épaisseur de 4,26 μm, présente à la fois une forte adsorption de 99,23 % pour le chlorhydrate de tétracycline (TCH) et une forte perméation à l'eau de 16,12 L m − 2 h − 1 barre − 1 . De plus, le colorant cationique bleu de méthylène (MB) a également été éliminé à hauteur de 83,88 %, ce qui indique de larges applications de la membrane préparée.
Contexte
Récemment, les composés pharmaceutiques, en particulier les antibiotiques, ont attiré une attention croissante dans le monde parce que leur présence dans l'eau naturelle constitue une menace pour les écosystèmes et la santé publique, même à de faibles concentrations [1, 2]. À ce jour, diverses technologies ont été développées dans le but d'éliminer les antibiotiques du milieu aquatique, tels que les processus d'oxydation et d'adsorption [3, 4]. Les processus d'oxydation, tels que la photocatalyse, la sonolyse et la réaction de Fenton, impliquent des procédures complexes, tandis que les séparations membranaires sont potentiellement plus simples [5]. Cependant, de nombreuses membranes actuellement disponibles pour l'élimination de molécules d'antibiotiques plus petites sont moins efficaces car elles fonctionnent simplement par un effet d'exclusion de taille [6].
Ces dernières années, des matériaux à base de carbone ont été utilisés comme adsorbants pour l'élimination des antibiotiques [7, 8]. En particulier, le graphène a également été largement appliqué pour éliminer les polluants de l'eau en raison de sa nature d'un atome d'épaisseur, de ses surfaces spécifiques élevées et de ses structures poreuses [9,10,11]. L'oxyde de graphène (GO) a des caractéristiques structurelles distinctives [12], une excellente hydrophilie, de fortes propriétés antisalissures [13] et une résistance mécanique élevée. Ces propriétés le rendent adapté aux applications de purification et de dessalement de l'eau. De plus, GO peut être produit à grande échelle, contrairement au graphène vierge [14]. Cependant, en raison de la tendance à l'empilement des nanofeuilles GO, des matériaux polymères ou de grandes nanoparticules doivent être intercalés entre eux pour augmenter l'espacement intercouche [15, 16]. Les nanotubes de carbone (CNT), en tant que matériaux unidimensionnels (1D) avec d'excellentes propriétés et compatibilités, se sont avérés être des « nano-coins » idéaux pour la régulation de l'espacement intercouche de GO [17]. Par rapport aux nanotubes de carbone à paroi unique (SWCNT), les nanotubes de carbone à parois multiples (MWCNT) offrent une plus grande stabilité dans des conditions d'écoulement hydrodynamique [18]. De plus, il a été prouvé que l'espacement intercalaire accru par intercalation de nanofeuillets GO avec des MWCNT améliore le flux d'eau. Cependant, l'agrégation indésirable de CNT en solution aqueuse entrave souvent l'application de membranes à base de CNT/GO. A l'inverse, divers polyélectrolytes ont été utilisés pour améliorer la dispersion des NTC par fonctionnalisation [19, 20].
Dans ce travail, nous proposons une nouvelle membrane de nanofiltration (NF) tout carbone qui se compose de MWCNT interposés entre des nanofeuillets GO. Du chlorure de poly diallyldiméthylammonium (PDDA), en tant que polyélectrolyte cationique, a été greffé sur les MWCNT pour assurer leur cationisation, conférant de fortes propriétés antifouling en raison de l'excellente dispersité. En raison des groupes fonctionnels contenant de l'oxygène ajoutés à la fois de manière irrégulière le long des bords et sur les surfaces des feuilles GO, GO peut être considéré comme un polyélectrolyte anionique. Ainsi, la réaction entre les PDDA-MWCNT et GO était principalement le résultat d'une interaction de charge. La membrane NF préparée a été systématiquement caractérisée et utilisée comme absorbant pour l'élimination du chlorhydrate de tétracycline (TCH) et du bleu de méthylène (MB) comme polluants organiques modèles. Les concentrations des solutions filtrées de TCH et de MB ont été déterminées par spectrophotométrie UV/Vis.
Résultats et discussion
L'hybride MWCNTs/GO a été utilisé pour produire une membrane autonome et flexible basée sur une simple méthode de filtration sous vide. Comme illustré sur la figure 1a, le PDDA, le polyélectrolyte cationique, pourrait être facilement ajouté à la surface des MWCNT, conférant une charge positive. GO, en tant que polyélectrolyte anionique, pourrait alors réagir avec les MWCNT chargés positivement par interaction électrostatique. Enfin, une membrane ultrafine a été préparée par filtration sous vide de la dispersion ci-dessus.
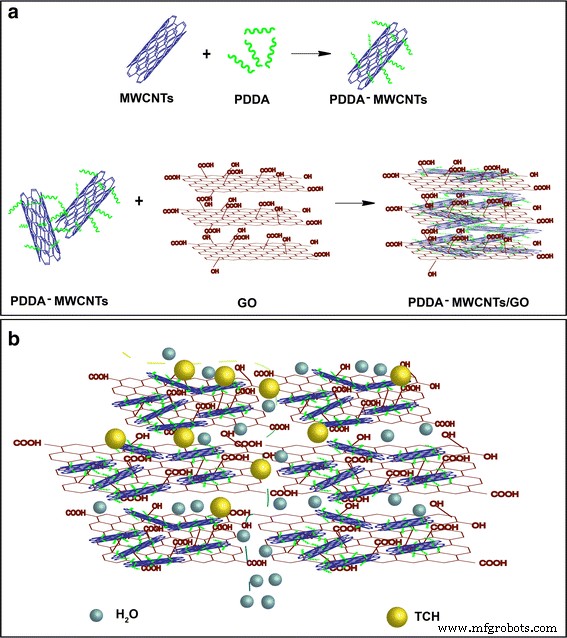
un Le processus construit pour la membrane PDDA-MWCNTs/GO. b Le schéma d'adsorption des antibiotiques par membrane PDDA-MWCNTs/GO
Le processus d'adsorption possible est illustré à la Fig. 1b. L'introduction de MWCNT entre les nanofeuillets GO a ouvert des canaux à l'échelle nanométrique, ce qui a permis d'améliorer l'écoulement des molécules d'eau [21]. Les molécules de TCH ont été interceptées dans les canaux nanométriques en raison de l'encombrement stérique et de leur interaction covalente avec les groupes fonctionnels de la membrane tout en carbone préparée.
Une image optique d'une membrane PDDA-MWCNTs/GO est présentée sur la figure 2a. La membrane tout en carbone préparée ressemblait à du tissu et présentait une excellente flexibilité mécanique (Fig. 2b). La membrane telle que préparée s'est avérée hydrophile par une mesure de l'angle de contact avec l'eau (Fichier supplémentaire 1 :Figure S1) [22, 23]. Néanmoins, il s'est avéré stable lorsqu'il est trempé dans l'eau (Fig. 2c). De plus, la membrane pouvait être réutilisée plus de sept fois sans développer de fissures évidentes (Fig. 2d).

Images optiques de la membrane PDDA-MWCNTs/GO (a ), la souplesse de la membrane (b ), et la stabilité de la membrane dans l'eau (c ). Membrane ayant été filtrée pendant plus de 8 cycles (d ). e Images SEM de coupes transversales de la membrane PDDA-MWCNTs/GO (épaisseur 4,26 μm). L'encart montre une image à plus fort grossissement de la membrane PDDA-MWCNTs/GO. f Images MET de la membrane;PDDA-MWCNTs/GO
Une image SEM d'une coupe transversale de la membrane préparée est illustrée à la Fig. 2e. L'épaisseur de la membrane a été estimée à 4,26 μm, et les MWCNT se sont avérés être uniformément insérés entre les feuilles de GO. De plus, des rides à la surface de la membrane préparée étaient apparentes à partir d'une image AFM (Fichier supplémentaire 1 :Figure S2A), conduisant à une plus grande zone de contact avec les contaminants. Les images MET de la membrane tout en carbone ont révélé que les MWCNT modifiés étaient bien dispersés dans le GO, conformément aux résultats SEM.
Comme le montre la figure 3a, par rapport à la membrane GO, la membrane PDDA-MWCNTs/GO présentait une structure plus poreuse. La variation de la concentration de PDDA a influencé la dispersion des MWCNT dans le GO (Fig. 3b-e). En raison de la forte propriété adhésive du PDDA [24], une concentration élevée de celui-ci (20 % en poids) a entraîné l'agglomération des MWCNT (Fig. 3e). Cependant, comme le montrent les figures 3a–d, des concentrations de PDDA de 0, 2, 5 ou 8 % en poids étaient insuffisantes pour disperser 4 mg de MWCNT, et l'épaisseur de la membrane a été affectée. Les raisons possibles sont les suivantes. Premièrement, les membranes étaient épaisses en partie parce que les MWCNT étaient facilement agglomérés à de faibles concentrations de PDDA. Deuxièmement, une interaction non covalente entre une concentration appropriée de feuilles de PDDA et de GO peut conduire à une membrane ultrafine. Troisièmement, étant donné que les MWCNT sont presque enveloppés de PDDA à longue chaîne à des concentrations excessivement élevées, de grandes structures poreuses se forment. Cependant, le mécanisme de cette formation de pores est encore inconnu. Il a été conclu qu'une concentration de PDDA de 10 % en poids donnait la dispersion optimale des MWCNT dans GO (Fig. 2e). La caractérisation morphologique, y compris SEM et MET, est présentée dans le fichier supplémentaire 1 :Figure S3. On peut observer que le PDDA est modifié avec succès dans la surface des NTC et que l'épaisseur du PDDA est d'environ 5,2 nm [25]. Des isothermes d'adsorption-désorption d'azote ont été utilisés pour caractériser les porosités des membranes MWCNTs/GO et PDDA-MWCNTs/GO (Fig. 4). Les PDDA-MWCNTs/GO ont montré une capacité d'adsorption-désorption accrue par rapport à la membrane MWCNTs/GO. La membrane PDDA-MWCNTs/GO NF avait une surface spécifique plus élevée (402,96 m 2 g −1 ) que la membrane MWCNTs/GO (378,45 m 2 g −1 ). De plus, une isotherme d'azote typique de type IV avec des boucles d'hystérésis pour la membrane NF préparée a corroboré ses propriétés mésoporeuses [26]. L'image en médaillon montre la distribution de la taille des pores correspondante calculée par le modèle Barrett-Joyner-Halenda (BJH), qui indique que les pores des deux membranes avaient un diamètre d'environ 3 à 10 nm, ce qui correspond au N2 isotherme.
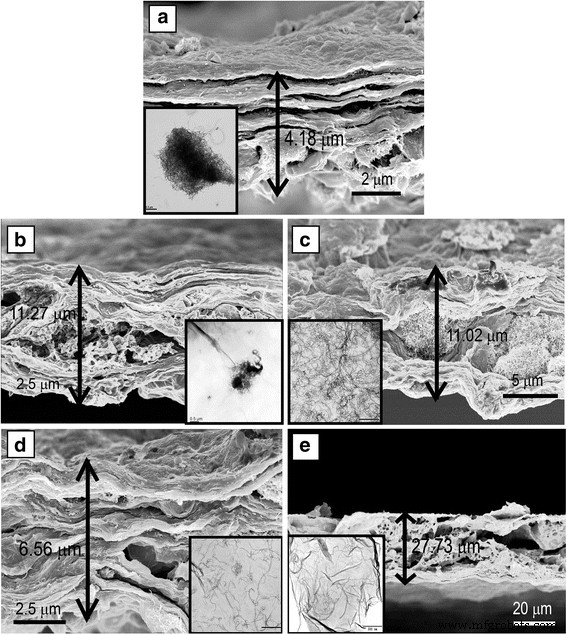
un Images SEM de coupes transversales de la membrane MWCNTs/GO. b –e Images SEM des coupes transversales de la membrane MWCNTs/GO ; l'encart montre des images TEM. La concentration de PDDA est de 0, 2, 5, 8 et 20 % en poids, respectivement
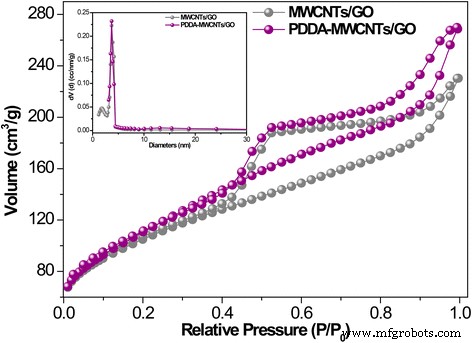
N2 isothermes d'adsorption-désorption des membranes MWCNTs/GO et PDDA-MWCNTs/GO. L'encart montre la distribution de la taille des pores des membranes MWCNTs/GO et PDDA-MWCNTs/GO
Comme le montre la Fig. 5a, un pic de diffraction caractéristique pour l'échantillon GO a été observé à 11,02° (001), indiquant une distance entre les nanofeuillets de 0,80 nm [27], alors que pour les MWCNTs, des pics ont été observés à 26,96° (002) et 44,89° [28], conformément aux précédents rapports de la littérature. Après l'incorporation des MWCNTs dans GO, les pics de diffraction caractéristiques des deux composants ont significativement diminué en raison de l'inhibition du réempilement des nanofeuillets GO et de l'agrégation des MWCNTs, reflétant la faible propension à la cristallisation de la membrane NF hiérarchique. De plus, le pic de diffraction des nanofeuillets GO s'est légèrement déplacé de 11,02° à 10,63°, correspondant à une augmentation de l'espacement intercouche de 0,81 à 0,87 nm. Les bandes dans les spectres XPS à balayage large des membranes respectives ont confirmé l'augmentation de la teneur en N 1 s dans la membrane PDDA-MWCNTs/GO.
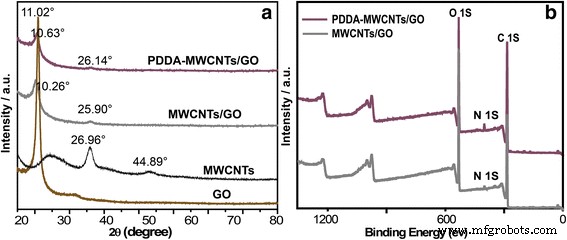
un Les modèles XRD de GO, MWCNTs, MWCNTs/GO et PDDA-MWCNTs/GO. b Spectres XPS des membranes MWCNTs/GO et PDDA-MWCNTs/GO
La figure 6a montre les spectres d'absorption UV/Vis de la solution initiale de TCH (20 mL, 500 μm) et des filtrats obtenus après passage sur les membranes MWCNTs/GO et PDDA-MWCNTs/GO. Après filtration à travers les membranes entièrement en carbone, la solution a montré une intensité d'absorption plus faible dans la région jusqu'à 420 nm. Combiné avec l'image en médaillon, les concentrations restantes de TCH après filtration à travers les membranes MWCNTs/GO et PDDA-MWCNTs/GO étaient de 18,78 et 6,74 μM, respectivement. Les capacités d'adsorption ont pu être converties en pourcentages d'adsorption, qui ont été évalués à 95,04 % pour les MWCNTs/GO et 99,23 % pour les PDDA-MWCNTs/GO, après une seule filtration à travers chaque membrane. Ainsi, par rapport à la membrane MWCNTs/GO, la membrane PDDA-MWCNTs/GO a provoqué une diminution plus prononcée de l'intensité d'absorption. A partir de ces résultats, nous pouvons conclure que la filtration du TCH implique à la fois les groupes fonctionnels interfaciaux et un effet synergique. De plus, le flux de perméation d'eau pour la membrane PDDA-MWCNTs/GO a été évalué à 16,12 L m − 2 h − 1 barre − 1 après fonctionnalisation, environ le double de celle de la membrane MWCNTs/GO. La membrane PDDA-MWCNTs/GO a clairement démontré les meilleurs résultats en termes de capacité d'adsorption élevée et de flux de perméation de l'eau. La figure 6b montre l'adsorption statique du TCH. Dans cette expérience, la masse de la membrane PDDA-MWCNTs/GO était de 1 mg. Après adsorption statique, la quantité adsorbée sur la membrane PDDA-MWCNTs/GO était de 436,13 mg g −1 , confirmant sa grande capacité d'élimination du TCH de l'eau.
un Spectres d'absorption UV/Vis de la solution initiale de TCH et des solutions résiduelles obtenues par filtration à l'aide de membranes MWCNTs/GO et PDDA-MWCNTs/GO. L'image d'insertion est la courbe standard de concentration de TCH (10 μM, 20 μM, 40 μM, 50 μM, 100 μM, 250 μM, 500 μM). b L'adsorption statique du TCH
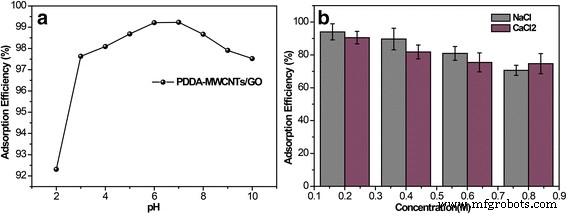
La stabilité est importante pour l'application pratique des membranes NF. Ici, nous avons mené des expériences d'adsorption dans des environnements difficiles, à savoir des conditions basiques, acides [29] et ioniques (Fig. 7). Nous avons anticipé que le pH affecterait l'interaction électrostatique en régulant les charges sur le TCH et la membrane. On constate que le potentiel zêta de la membrane est d'environ - 45 mV, tandis que le TCH a une charge positive et négative dans les conditions acides et alcalines, respectivement [30]. Lorsque le pH augmentait de 2 à 4 ou de 8 à 10, l'adsorption de TCH était légèrement diminuée (Fig. 7a). Cela peut être dû au gonflement de la membrane ou à la répulsion électrostatique [31]. Le pH neutre s'est avéré optimal, et toutes les autres expériences rapportées ici ont été menées à pH 7. Comme nous avons pu le voir, pour la membrane PDDA-MWCNTs/GO, le comportement d'adsorption n'a été que légèrement influencé. De là, on pourrait supposer que le principal mécanisme d'adsorption est la capture de molécules dans les nanocanaux. Comme le montre la figure 7b, l'adsorption du TCH diminue avec l'augmentation de la concentration en sel. Les effets de gonflement et de relargage membranaire induits par le sel peuvent avoir influencé de manière synergique les performances d'adsorption [32]. Néanmoins, la membrane préparée a montré une tolérance modérée aux ions salins.

un Effet de l'adsorption du TCH à différents pH. b Effet de l'adsorption du TCH en solution saline
Nous avons utilisé un colorant MB comme molécule chargée positivement pour étudier plus avant le mécanisme d'adsorption. Nous avons conclu qu'un effet synergique était actif, impliquant le tamisage moléculaire dans les nanocanaux, l'hydrophobie des nanocanaux non oxydes dans la membrane et l'interaction de charge entre le soluté et la membrane [33]. Le potentiel ζ de la membrane PDDA-MWCNTs/GO NF est d'environ pH 7, indiquant une bonne stabilisation, et il a montré une plus grande adsorption du TCH zwitterionique (99,23 %) que celle du colorant MB chargé positivement (88,23 %). Nous attribuons cela au fait que l'exclusion de taille est le principal facteur dans les canaux contrôlés à l'échelle nanométrique [34, 35], cohérent avec les résultats des expériences de pH.
Conclusions
En résumé, nous avons proposé une nouvelle membrane NF 3D tout carbone dotée de propriétés extraordinaires, à savoir des nanofeuilles ultrafines à haute adsorption, une stabilisation avec des propriétés antisalissure extraordinaires et une perméation rapide de l'eau. La synthèse est rapide et respectueuse de l'environnement, ce qui en fait une méthode prometteuse pour la fabrication de membranes NF. La membrane fonctionnalisée PDDA-MWCNTs/GO NF présentait des propriétés supérieures par rapport à la membrane MWCNTs/GO NF en raison de la forte dispersion des MWCNTs et de l'interaction de charge entre les composants. Les performances d'adsorption élevées peuvent être attribuées à un effet synergique entre le tamisage moléculaire, l'hydrophobie des nanocanaux non oxydes dans la membrane et l'interaction de charge entre le soluté et la membrane. Le processus de préparation simple combiné aux nombreuses propriétés extraordinaires font de cette membrane MWCNTs/GO NF fonctionnalisée un candidat prometteur pour les applications de séparation chimique.
Méthodes/Expérimental
Matériaux
La dispersion GO (2 mg/mL) a été achetée auprès de Nanjing XFNANO Materials Tech Co. (Nanjing, Chine). Des MWCNT purs d'un diamètre moyen de 20 à 30 nm et d'une longueur approximative de 10 à 30 μm ont été achetés auprès de Beijing Boyu High-tech Novel Materials Technology Co. (Pékin, Chine). PDDA (200 000 ≤ MW ≤ 350 000, 20 % en poids dans H2 O), poudre de TCH (étalon analytique), solide de chlorure de sodium (NaCl, S), solide de chlorure de calcium (CaCl2 , S), l'acide chlorhydrique (HCl) et l'éthanol anhydre (CH3 CH2 OH) ont été achetés chez Aladdin Chemical Co. (Shanghai, Chine). Eau déminéralisée (18 M Ω cm −1 ) utilisé tout au long des expériences a été produit par un système de purification d'eau (Billerica, MA, USA).
Appareil
Des images au microscope électronique à balayage (MEB) de la membrane tout en carbone préparée ont été acquises avec un microscope électronique à balayage à émission de champ (FESEM, Ultra 55, Carl Zeiss, Allemagne). Des suspensions d'oxyde de graphène et de MWCNT ont été déposées sur des grilles de cuivre recouvertes de carbone et les substances volatiles ont été évaporées dans des conditions ambiantes. La microscopie électronique à transmission (MET) a été réalisée à l'aide d'un microscope électronique Hitachi H-800 (Japon) fonctionnant à une tension d'accélération de 200 kV. Les spectres UV/Vis ont été enregistrés sur un spectromètre Lambda-25 (Perkin-Elmer Inc. USA). Les mesures de Brunauer-Emmett-Teller (BET) ont été effectuées à 77 K sur un analyseur Autosorb-iQ-C (Quantachrome Instruments, USA). Les diagrammes de diffraction des rayons X (XRD) ont été obtenus avec un diffractomètre Shimadzu XD-3A (Japon), utilisant le rayonnement CuKα, λ = 0.15418 nm. Divers éléments dans les échantillons ont été déterminés par spectroscopie photoélectronique aux rayons X (XPS, PHI 5000 Versa Probe, Japon). Les mesures statiques de l'angle de contact avec l'eau ont été effectuées à 25°C à l'aide d'un mesureur d'angle de contact (Rame-Hart-100, États-Unis) utilisant des gouttes d'eau pure désionisée. Les potentiels zêta des membranes ont été testés au moyen d'un analyseur électrocinétique SurPASS (Autriche) avec une cellule de serrage à 300 mbar. Un microscope à force atomique Bruker Multimode 8 (AFM, Allemagne) a été utilisé pour caractériser les nanomatériaux préparés, qui avaient été enduits sur un substrat de mica.
Synthèse de MWCNT fonctionnalisés PDDA
Des MWCNT fonctionnalisés par PDDA ont été préparés comme décrit précédemment [36]. Les MWCNT (4,0 mg) ont d'abord été dispersés dans de l'eau déminéralisée (1 mL) à l'aide d'ultrasons, et du PDDA (10 % en poids) dans de l'eau a été ajouté goutte à goutte. Le produit centrifugé a ensuite été lavé plusieurs fois avec de l'eau déminéralisée et séché dans une étuve sous vide à 70 °C pendant 24 h.
Assemblage de la membrane MWCNT-Interposed GO (MWCNTs/GO)
Les MWCNT (4,0 mg) ont été ajoutés à une suspension aqueuse de GO (24 mL, 0,5 mg mL −1 ) sous agitation et sonication. La dispersion homogène a ensuite été filtrée sous vide sur une membrane poreuse en fluorure de polyvinylidène avec une taille de pores de 0,22 µm. Enfin, la membrane a été séchée dans une étuve à vide à 60 °C pendant 3 min et a pu être facilement décollée de la membrane en fluorure de polyvinylidène après trempage dans de l'éthanol anhydre.
Expériences d'adsorption d'antibiotiques utilisant la membrane tout carbone
Afin d'évaluer les performances d'adsorption vis-à-vis des antibiotiques, la solution de TCH (20 mL, 500 μM) a été filtrée sous vide à 0,9 bar à travers la membrane préparée. La concentration du filtrat a été déterminée par spectrophotométrie UV/Vis. Selon la concentration déterminée, les taux de rejet des molécules de TCH pourraient être calculés à l'aide de l'équation suivante :
$$ R=\left(1-{C}_{\mathrm{p}}/{C}_{\mathrm{o}}\right)\times 100\% $$où C o représente la concentration de TCH dans la solution originale et C p est la concentration de TCH dans la solution de perméat. Toutes les données ont été calculées sur la base des résultats d'au moins trois expériences.
Expériences de stabilité avec les membranes tout carbone
Les solides de TCH ont été dissous dans différentes solutions de pH (pH = 2, 3, 4, 5, 6, 7, 8, 9 et 10) en utilisant HCl (1,0 M) ou NaOH (1,0 M). La solution de TCH telle que préparée (20 mL, 500 μM) a été filtrée à travers la membrane tout en carbone pour évaluer sa tolérance aux conditions difficiles. Pour explorer la stabilité de la membrane tout carbone en solution saline, différentes concentrations de NaCl et CaCl2 (0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8 et 0,9 M) ont également été préparés. Ensuite, le TCH a été dissous dans la solution saline ci-dessus. De même, les solutions de TCH (20 mL, 500 μM) ont été filtrées à travers la membrane tout en carbone. Les concentrations de tous les filtrats ont été déterminées par spectrophotométrie UV/Vis.
Abréviations
- AFM :
-
Microscope à force atomique
- PARI :
-
Brunauer–Emmett–Teller
- MWCNT :
-
Nanotubes de carbone multi-parois
- PDDA :
-
Chlorure de polydiméthylammonium
- SEM :
-
Microscopie électronique à balayage
- SWCNT :
-
Nanotubes de carbone monoparoi
- TCH :
-
Chlorhydrate de tétracycline
- TEM :
-
Microscopie électronique à transmission
- XPS :
-
Spectroscopie photoélectronique aux rayons X
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- Avertisseur d'eau Raspberry Pi 2 avec t cobbler plus
- Arrosage automatisé des plantes Raspberry Pi avec site Web
- Entretien avec Craig Trevor de Persuasion Inc.
- Élimination des colorants cationiques photocatalytiquement améliorée avec des hydroxydes doubles en couches de Zn-Al
- 5 avantages à tirer des compteurs d'eau intelligents IoT
- Célébrer la Journée mondiale de l'eau avec des initiatives pour l'eau propre
- Atlas Copco s'associe à la brasserie Widmer Brothers
- Comment éliminer l'humidité de l'air comprimé
- Il fait froid avec les refroidisseurs industriels



