La préparation de la nanostructure jaune-enveloppe Au@TiO2 et ses applications pour la dégradation et la détection du bleu de méthylène
Résumé
Cet article rapporte la synthèse d'un nouveau type de Au@TiO2 nanostructures jaune-enveloppe en intégrant la méthode de pulvérisation ionique avec la technique de dépôt de couche atomique (ALD) et ses applications en tant que photocatalyseur à lumière visible et substrat de spectroscopie Raman à surface améliorée (SERS). La taille et la quantité de nanoparticules d'or confinées dans TiO2 les nanotubes pourraient être facilement contrôlés en ajustant correctement le temps de pulvérisation. La structure et la morphologie uniques de l'Au@TiO2 résultant les échantillons ont été étudiés en utilisant diverses techniques spectroscopiques et microscopiques en détail. Il a été constaté que tous les échantillons testés peuvent absorber la lumière visible avec une absorption maximale aux longueurs d'onde de résonance plasmonique de surface localisée (LSPR) (550 à 590 nm) qui sont déterminées par la taille des nanoparticules d'or. L'Au@TiO2 des composites jaune-coquille ont été utilisés comme photocatalyseur pour la dégradation du bleu de méthylène (MB). Par rapport au TiO2 pur nanotubes, Au@TiO2 Les composites présentent des propriétés photocatalytiques améliorées vis-à-vis de la dégradation du MB. L'effet SERS de Au@TiO2 Des composites jaune-coquille ont également été réalisés pour étudier la sensibilité de détection de MB.
Contexte
Les nanocomposites hétérogènes de métaux/semi-conducteurs ont suscité un intérêt considérable pour la recherche en raison de leurs propriétés physico-chimiques uniques et de leurs applications potentielles dans la conversion de l'énergie solaire [1], la biomédecine [2], la diffusion Raman à surface améliorée [3], les diodes électroluminescentes [4 ] et l'assainissement de l'environnement [5]. Motivés par leurs diverses applications, un grand nombre d'efforts ont été déployés pour concevoir et moduler les compositions, les nanostructures et les dimensions de tels matériaux [6,7,8]. Par exemple, Yin et al. [9] ont synthétisé des nanostructures hybrides ZnO/Ag et ZnO/Pd et ont découvert que le dépôt d'Ag ou de Pd sur ZnO améliorait considérablement l'activité photocatalytique du ZnO. Sun et al. [10] a démontré que Au-Fe3 O4 nanoparticules avec interactions nanométriques entre Au et Fe3 O4 présentait une riche variété de propriétés magnétiques, physiques et chimiques.
Ces dernières années, des progrès significatifs dans la synthèse contrôlée de métaux/semi-conducteurs appliqués à la photocatalyse ont été réalisés en raison des problèmes environnementaux de plus en plus graves tels que la pollution de l'air [11, 12] et les applications techniques potentielles dans la conversion d'énergie [13]. Parmi les différents composites métal/semi-conducteurs qui ont été proposés, ceux impliquant TiO2 et nano Au sont les plus pratiques car une telle hétérostructure a une forte résonance plasmonique de surface localisée (LSPR) dans la gamme du spectre visible et en fait un nouveau type de photocatalyseur à réponse large [14,15,16]. Une autre fonction avantageuse de Au/TiO2 nanocomposites est que les nanoparticules d'Au fonctionnent comme un stockage d'électrons, réduisant efficacement la recombinaison des paires électron-trou photoexcitées et augmentant finalement le rendement quantique de la photocatalyse [17, 18]. Quelques investigations innovantes basées sur Au/TiO2 système composite appliqué dans la dégradation des colorants organiques, la séparation de l'eau solaire et la conversion des composés organiques ont démontré leurs caractéristiques photocatalytiques efficaces à la lumière visible, indiquant un rôle crucial des effets plasmoniques de l'Au joué dans Au/TiO2 système [17, 19, 20].
Cependant, l'une des principales limitations pour Au/TiO2 nanocomposites traduit en applications pratiques est la mauvaise stabilité des catalyseurs d'or supportés. Les propriétés exceptionnelles présentées dans les nanoparticules d'origine peuvent s'affaiblir car elles ont tendance à s'agglomérer et à se développer en particules plus grosses dans diverses conditions de réaction [21, 22]. Et dans certains autres cas, il a été prouvé que des nanoparticules d'Au se déposaient sur les surfaces de TiO2 sont susceptibles de subir une corrosion ou une dissolution au cours d'une réaction catalytique [23]. La conception et la construction de composites structurés cœur-coquille et jaune-coquille sont considérées comme une méthode efficace pour résoudre ces problèmes. Gong et al. [24] ont rapporté la fabrication d'or nanorod@TiO2 catalyseurs jaune-coquille avec différents rapports d'aspect de nanotige d'or grâce à une méthode à médiation par les semences. Les nanocomposites hybrides à plusieurs composants présentent également les activités photocatalytiques améliorées dans la réaction d'oxydation de l'alcool benzylique. Zaera et ses collaborateurs [21] ont rendu compte de la synthèse et de la caractérisation d'un nouveau Au@TiO2 catalyseur nanostructuré jaune-coquille, montrant une activité de promotion comparable à celles observées avec Au/TiO2 plus conventionnel catalyseurs mais une stabilité améliorée contre le frittage. Kim et al. [25] synthétisé des nanostructures plasmoniques core-shell constituées d'Au-TiO2 pris en charge sur SiO2 sphères dans des cellules solaires à colorant (DSSC), qui présentaient des rendements de conversion de puissance sensiblement améliorés d'environ 14 %. Malgré d'énormes efforts de recherche ont été faits, la synthèse facile de Au@TiO2 composites avec une structure cœur-coquille/jaune-coquille bien définie reste un défi pour une application de masse.
Récemment, de nombreuses études ont confirmé qu'une chiralité contrôlée à l'échelle nanométrique pourrait induire un effet LSPR plus important car une nanostructure chirale multihélicoïdale peut donner lieu à une biréfringence induite à l'échelle microscopique et générer l'effet Kerr causé par un champ électrique induit à l'échelle macroscopique [26, 27,28]. Dans cette étude, l'Au@TiO2 Des nanocomposites jaune-coquille avec une structure semblable à une fibre hélicoïdale ont été synthétisés avec succès par une stratégie contrôlable et facile. Les nanoparticules d'or chargées à la surface des nanobobines de carbone (CNC) ont été produites par pulvérisation ionique. Le TiO2 des films d'épaisseur très uniforme et contrôlée pourraient être intégrés de manière stable à la surface de nanoparticules d'or par une technologie de dépôt de couche atomique (ALD). Suivi d'une étape de recuit, l'Au@TiO2 des nanocomposites ont été obtenus. La méthode développée ci-dessus peut également être étendue pour fabriquer d'autres métaux (Pt, Ag)@TiO2 nanocomposites jaune-coquille avec une nanostructure hélicoïdale. En tant que photocatalyseur représentatif, les activités photocatalytiques de Au@TiO2 obtenu les nanocomposites ont été évalués par dégradation du bleu de méthylène (MB) sous irradiation de lumière visible. De plus, les activités de spectroscopie Raman améliorée en surface (SERS) de Au@TiO2 des nanocomposites ont également été étudiés grâce à la détection de MB.
Expérimental
Synthèse de Au@TiO2
Les CNC utilisées comme modèles ont été préparées par la méthode de dépôt chimique en phase vapeur, comme indiqué précédemment. En bref, des nanoparticules d'acétylène et de cuivre ont été utilisées comme source de carbone et comme catalyseurs appropriés, respectivement. La croissance des CNC a été réalisée à pression atmosphérique dans un tube de quartz horizontal. Une plaque en céramique contenant les catalyseurs au cuivre a été placée dans le réacteur. Après avoir chauffé le tube à 250 °C sous vide, de l'acétylène a été introduit dans le réacteur [29,30,31]. Une fois l'appareil refroidi à température ambiante, les CNC préparées ont été obtenues.
Les CNC obtenus ont été dispersés dans de l'éthanol sous agitation ultrasonique puis barbouillés uniformément sur la surface d'une lame de verre. Après avoir été séchée à l'air ambiant, la couche d'Au a été déposée par un instrument de pulvérisation ionique (Hitachi, E-1010). La taille et l'épaisseur des films d'Au ont été déterminées par le courant de décharge et le temps de pulvérisation. Dans cette étape, le courant de décharge était de 10 mA et le temps de pulvérisation variait de 30 à 120 s. Les échantillons obtenus ont été marqués comme CNCs@Au-x , dans laquelle x se réfère au temps de pulvérisation (secondes). Par la suite, les échantillons ont été dispersés dans de l'éthanol par agitation aux ultrasons puis étalés sur une plaquette de quartz pour être recouverts de TiO2 par le procédé ALD. L'ALD est une sorte de technique de préparation de revêtement en phase vapeur et peut obtenir un contrôle précis de l'épaisseur et une excellente uniformité des films [32,33,34,35,36]. Le procédé ALD a été réalisé dans un réacteur ALD à paroi chaude de type flux à 145 °C avec du tétraisopropanolate de titane (TTIP) et de l'H2 désionisé O utilisé comme précurseurs de titane et d'oxygène, respectivement. Enfin, après le procédé ALD, les nanobobines revêtues ci-dessus ont été calcinées à 450 °C pendant 2 h dans l'air sous pression ambiante pour éliminer les noyaux de carbone et le TiO2 hélicoïdal. Des structures jaune-coquille d'or recouvertes d'Au ont été obtenues. A titre de comparaison, le TiO2 pur tube hélicoïdal a également été collecté par TiO2 calciné - CNC revêtus sans pulvérisation cathodique Au et est noté TiO2 dans la discussion suivante.
Caractérisation des matériaux
Les diagrammes de diffraction des rayons X (XRD) ont été enregistrés sur un diffractomètre Bruker D8 Advance avec du cuivre Kα (λ = 0,154056 nm) source de rayonnement. Les images de microscopie électronique à balayage (MEB) ont été acquises avec un microscope Hitachi S-4800. Des images de microscopie électronique à transmission (MET), de diffraction électronique à zone sélectionnée (SAED) et de MET haute résolution (HRTEM) ont été obtenues à l'aide d'un instrument de microscope JEOL JEM-2100 fonctionnant à 200 kV. Les données de spectroscopie photoélectronique à rayons X (XPS) ont été acquises à l'aide d'un spectromètre PHI5000 Versaprobe-II avec une source monochromatique Al Kα (1486,6 eV). Les spectres d'absorption optique ont été enregistrés à l'aide d'un spectrophotomètre d'absorption UV-Vis-NIR PerkinElmer Lambda 750s. Les spectres de diffusion Raman ont été enregistrés sur un spectromètre Renishaw Invia Reflex Laser Raman. La longueur d'onde d'excitation était de 514 nm à partir d'un laser à ions argon refroidi par air avec une puissance effective de 2 mW.
Évaluation des activités photocatalytiques
Les activités photocatalytiques des catalyseurs ont été étudiées par la photodégradation des colorants MB dans des solutions aqueuses en utilisant la procédure décrite ci-dessous. Deux milligrammes de catalyseur ont été répartis uniformément dans un photoréacteur de 100 ml équipé de conduites d'eau de refroidissement en circulation. Ensuite, 20 mL de 0,01 mg/mL de solutions de MB ont été ajoutés dans le photoréacteur. Avant la photoirradiation, le système a été mélangé par ultrasons pendant 2 minutes et agité magnétiquement bidirectionnel pendant 30 minutes à la fois dans l'obscurité afin d'équilibrer l'adsorption-désorption entre les photocatalyseurs et MB. Le photoréacteur de 100 ml ci-dessus contenant la suspension a ensuite été irradié sous une lampe au xénon de 300 W (Beijing Perfectlight Technology Co. Ltd., PLS-SXE300C) avec des filtres de coupure de sorte que les longueurs d'onde de la lumière entre 420 et 780 nm atteignent les solutions. Au cours du processus de réaction photocatalytique, l'intensité d'irradiation était de ~ 154 mW cm −2 et l'eau de refroidissement a été maintenue en circulation pour dissiper l'effet thermique du système. À des intervalles de temps toutes les 10 min pour une durée totale de 90 min, une partie (1 mL) des suspensions a été pipetée et immédiatement diluée à 3 mL, et 2 mL de surnageant ont été collectés après séparation centrifuge. Finalement, la concentration résiduelle de MB dans le surnageant a été analysée en utilisant un spectrophotomètre UV-Vis-NIR à la longueur d'onde caractéristique de la solution (λ Mo = 664 nm).
Résultats et discussion
Analyse de la morphologie et de la structure des phases
La figure 1a affiche un flux de préparation schématique de Au@TiO2 hétérostructure vitellin-shell, y compris la pulvérisation cathodique Au, TiO2 procédés d'enrobage et de calcination. La figure 1b-e montre des images MET typiques correspondant à chaque procédure ci-dessus. Les CNC utilisées comme modèle de départ dans ce travail ont un diamètre de fibre, un diamètre de bobine et un pas de bobine uniformes, et le diamètre moyen de la fibre est d'environ 80 nm (Fichier supplémentaire 1 :Figure S1). Après le traitement de pulvérisation cathodique d'Au, la couche externe des CNC a été recouverte de nombreuses nanoparticules d'Au uniformes, comme le montre la figure 1c. Comme on le voit sur l'image TEM montrée sur la Fig.1d, en appliquant 200 cycles ALD pour TiO2 dépôt, un TiO2 uniforme un revêtement d'une épaisseur d'environ 8 nm est appliqué à la surface des Au/CNC. Généralement, la phase anatase de TiO2 a des performances photocatalytiques bien meilleures que celles du rutile [37, 38]. Pour cette raison, nous avons choisi 450 °C comme température de calcination appropriée pour éliminer les noyaux de carbone et obtenir le Au@TiO2 final. structure jaune-coquille. Comme le montre la Fig.1e, le TiO2 des nanotubes avec des nanoparticules d'Au encapsulées et de l'espace libre ont été formés. Après toutes les étapes de traitement, la morphologie hélicoïdale élégante des CNC de départ peut être bien conservée.
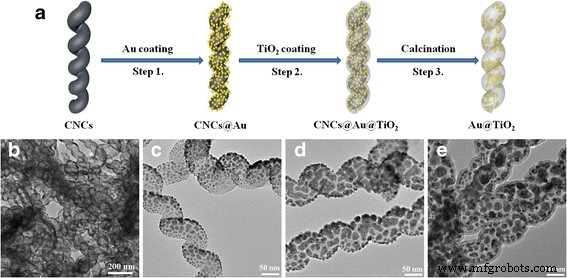
un Illustration schématique du processus de synthèse de Au-x@TiO2 . b –e Les images MET révèlent l'évolution morphologique
La cristallinité et les structures de tous les échantillons ont été mesurées par XRD. Comme observé sur la figure 2a, les pics de diffraction pour le TiO2 pur l'échantillon peut être attribué à une phase anatase bien cristallisée (JCPDS 21-1272), sans pics d'impuretés supplémentaires. Pour Au/TiO2 , les pics de diffraction supplémentaires de la Fig. 2b–e peuvent être bien indexés à l'Au cubique à faces centrées (FCC) (JCPDS 01-1174), qui a conformé le revêtement réussi de nanoparticules d'Au sur la surface des CNC par pulvérisation cathodique ionique. Le TiO2 (004) à 38,2° chevauche largement le pic Au (111) à 38,3°. Il est intéressant de noter qu'un pic faible situé à 35,5 degrés sur la figure 2b–e peut être indexé sur le plan (020) de γ -Ti3 O5 , indiquant que le rapport atomique Ti/O n'est pas exactement 1/2 pour Au/TiO2 . Dans le présent travail, la forte action réductrice de la fibre de carbone et des nanoparticules d'Au à haute température induit probablement la production de lacunes d'oxygène et d'états d'oxydation inférieurs du titane. De plus, en raison de la diminution du contenu relatif pour TiO2 , on peut observer que tous les TiO2 les pics de diffraction s'affaiblissent avec l'augmentation du temps de pulvérisation de 30 à 120 s.
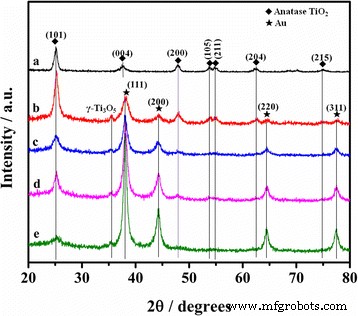
modèles XRD. un TiO2 . b Au-30@TiO2 . c Au-50@TiO2 . d Au-80@TiO2 . e Au-120@TiO2
La figure 3 montre les images MET de TiO2 et Au-x@TiO2 avec un temps de pulvérisation Au différent (x signifie le temps de pulvérisation, x = 30, 50, 80, 120). Pour TiO2 , on peut observer que l'échantillon présente une structure tubulaire hélicoïdale similaire à celle des gabarits CNC. Aucun effondrement des matériaux de la coque ne s'est produit pendant le processus de recuit pour éliminer les noyaux de carbone. Le TiO2 la coque a une épaisseur d'environ 8 nm après 200 cycles. En raison d'un plus grand numéro atomique de Au par rapport à celui de Ti dans Au@TiO2 , les nanoparticules d'Au montrent un contraste plus sombre résultant en une morphologie jaune-coquille clairement visible. Le diamètre moyen des nanoparticules d'Au augmente clairement avec l'augmentation du temps de pulvérisation. Il s'élève à environ 4,5, 5,5, 10,5 et 20,5 nm correspondant au temps de pulvérisation de 30, 50, 80 et 120 s, respectivement (Fichier supplémentaire 1 :Figure S2, a2-d2). Comme le montre la Fig. 3b–d, le TiO2 homogène un film mince d'environ 8 nm d'épaisseur est également obtenu pour Au-30@TiO2 , Au-50@TiO2, et Au-80@TiO2 nanocomposites avec le même ALD TiO2 déposition. Cependant, l'épaisseur de TiO2 shell pour Au-120@TiO2 diminue jusqu'à environ 5 nm (Fig. 3e), ce qui peut être attribué à l'influence de la grande taille et des agglomérations importantes de nanoparticules d'Au.
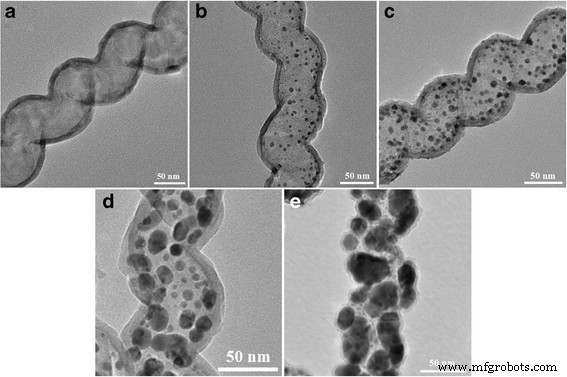
images TEM. un TiO2 . b Au-30@TiO2 . c Au-50@TiO2 . d Au-80@TiO2 . e Au-120@TiO2
Les structures microscopiques détaillées du TiO2 et Au-30@TiO2 les nanocompositions ont été étudiées plus avant par HRTEM. Comme observé dans la Fig. 4a–b, les deux TiO2 les coquilles et les nanoparticules d'Au sont bien cristallisées attribuées à l'anatase TiO2 (101) (0,3565 et 0,3501 nm) et Au (111) (0,2399 nm) des réseaux cristallins, respectivement. A noter que l'interface en Au/TiO2 Les nanostructures jaune-coquille sont clairement visibles (Fig. 4b) en raison du contraste différent. Une telle interface riche est importante pour l'application de photocatalyse suivante car elle peut fournir l'accès pour le transport d'électrons chauds des nanoparticules d'Au au TiO2 sur excitation LSPR [20]. L'encart de la figure 4b affiche le modèle SAED enregistré sur Au-30@TiO2 nanostructure. Les anneaux de diffraction clairs peuvent être attribués aux plans cristallins (101) et (211) de l'anatase TiO2 et (220) et (111) plans cristallins de Au, respectivement, en accord avec les résultats XRD. Afin d'analyser l'état chimique de l'Au et d'acquérir des informations fondamentales approfondies sur l'interaction de l'Au avec TiO2 , Au-30@TiO2 nanocomposite a été étudié plus en détail par des mesures XPS. Les spectres à haute résolution de Ti 2p et Au 4f sont présentés respectivement sur les figures 4c et d. Comme le montre la figure 4c, deux pics avec une énergie de liaison à environ 458,4 et 464,2 eV peuvent être attribués à Ti 2p3/2 et Ti 2p1/2 composantes spin-orbite de Ti 4+ , respectivement [39]. La figure 4d montre le spectre Au 4f XPS avec deux pics apparus à 83,6 et 87,4 eV pour Au 4f7/2 et Au 4f5/2 niveaux, respectivement, suggérant que les espèces Au existent à l'état métallique. Le décalage négatif relatif (0,4 eV) de Au 4f7/2 pic en comparaison de l'Au en vrac (4f7/2 à 84,0 eV) peut être attribué au transfert d'électrons à partir des lacunes d'oxygène du TiO2 à Au, ce qui confirme le fort Au/TiO2 interaction [40, 41].
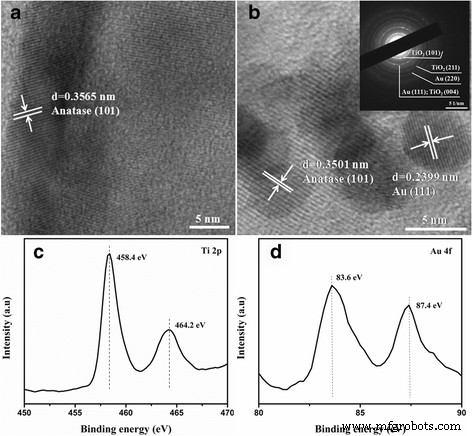
Images HRTEM de a TiO2 et b Au-30@TiO2 , dans laquelle l'encart en haut à droite dans b montre les modèles SAED de Au-30@TiO2 nanostructure. XPS haute résolution de c Ti 2p et d Au 4f de Au-30@TiO2
La figure 5 montre les spectres de réflexion diffuse UV-Vis du TiO2 et Au-x@TiO2 nanostructures. Une bande d'absorption intense inférieure à 400 nm est observée pour tous ces échantillons, ce qui peut être dû à la large bande interdite de l'anatase TiO2 [42]. Par rapport au TiO2 , on peut constater que le Au-x@TiO2 a non seulement une absorption similaire en dessous de 400 nm, mais également une plage d'absorption améliorée de 400 à 800 nm avec un large pic d'absorption à environ 580 nm résultant de l'effet LSPR des nanoparticules d'Au [43]. Ces résultats indiquent qu'une meilleure activité photocatalytique pour Au-x@TiO2 peut être attendu sous irradiation de lumière visible, en particulier pour le Au-80@TiO2 avec une intensité d'absorption plus forte. Le léger décalage de l'absorption LSPR pour Au@TiO2 des nanostructures avec des temps de pulvérisation différents sont également raisonnables car la nanoparticule d'Au est sensible à sa taille et à l'environnement environnant [24, 42]. Ces observations déclarent que le Au-x@TiO2 les photocatalyseurs peuvent posséder une plage de récolte de lumière réglable en ajustant la forme, le diamètre et la morphologie des nanoparticules d'Au [44].
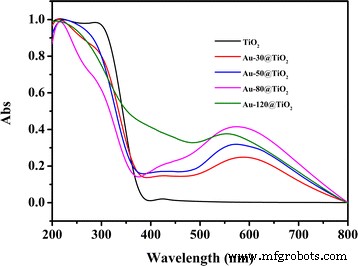
Spectres d'absorption UV-Vis du TiO2 et Au-x@TiO2
Activité photocatalytique
L'élimination des polluants organiques des eaux usées produites par l'industrie et les ménages a attiré beaucoup d'attention [45,46,47,48]. Le MB est fréquemment utilisé comme polluant ciblé pour évaluer l'efficacité catalytique dans les réactions photocatalytiques, car la couleur bleue du MB provenant de l'absorption à 664 nm s'estomperait progressivement avec le processus de dégradation [49, 50] et peut être facilement surveillée par des spectres d'absorption UV-Vis . Les activités photocatalytiques du TiO2 et Au-x@TiO2 les composites ont été évalués en surveillant l'absorbance du colorant MB à 664 nm pour détecter le taux de dégradation sous irradiation à la lumière visible (420 à 780 nm). Les changements de concentration relative de MB en fonction du temps d'irradiation sur les différents catalyseurs sont présentés sur la figure 6a. A titre de comparaison, l'activité photocatalytique du TiO2 pur nanotubes a d'abord été examiné. On peut constater qu'environ 60% du MB a été dégradé avec TiO2 comme photocatalyseur sous irradiation de lumière visible pendant 90 min. L'efficacité photocatalytique relativement faible du TiO2 est due à sa faible capacité d'absorption de la lumière visible. Par rapport à l'expérience à blanc ci-dessus, le Au-x@TiO2 les photocatalyseurs présentent une efficacité de dégradation plus élevée et l'efficacité de dégradation pour Au-80@TiO2 s'élève à environ 90 % dans les mêmes conditions expérimentales. Les propriétés photocatalytiques favorisantes peuvent être attribuées à une augmentation du taux de génération d'électrons-trous en raison de la présence d'hétéro-interface et de l'absorption de lumière correspondante améliorée par le plasmon [51, 52]. On sait que le plan à haute énergie (200) de l'Au et l'épaisseur de TiO2 les coquilles sont des paramètres importants affectant l'activité [24, 53]. Parmi Au-x@TiO2 photocatalyseurs, avec l'augmentation du temps de pulvérisation, le pic Au (200) présente plus de plans à haute énergie, comme le montre l'intensité du pic XRD correspondant. De plus, Au-120@TiO2 avec un diluant TiO2 shell (5 nm) est incapable de fournir suffisamment de sites de réaction pour la consommation d'électrons. Ainsi, sur la base de l'épaisseur appropriée et similaire de TiO2 shell sur différents Au-x@TiO2 , Au-80@TiO2 montre l'activité la plus élevée.
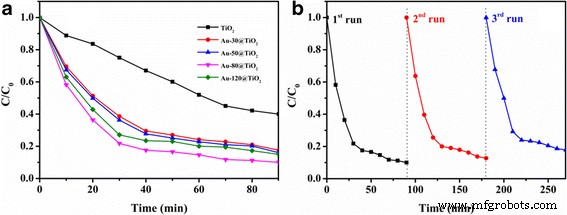
un Évaluation de la concentration de MB en fonction du temps de réaction dans différentes conditions. b Recyclabilité de la dégradation photocatalytique de la solution aqueuse de MB en utilisant Au-80@TiO2 avec trois cycles
En tant que catalyseurs hétérogènes, la réutilisation du catalyseur est également très importante dans l'application pratique. Nous avons effectué trois opérations consécutives pour étudier la réutilisabilité de l'Au-80@TiO2 . Comme le montre la figure 6b, aucune désactivation notable n'est observée, indiquant une excellente durabilité de Au-80@TiO2 . Image MET de Au-80@TiO2 (Fichier supplémentaire 1 :Figure S3) après recyclage trois fois révèle que les structures hélicoïdales jaune-enveloppe des catalyseurs sont bien maintenues, ce qui confirme en outre que l'effet confiné de TiO2 les nanotubes peuvent empêcher la perte d'Au et améliorent ainsi la stabilité des catalyseurs.
Sur la base des résultats ci-dessus, nous proposons un processus photocatalytique pour la dégradation du MB en utilisant Au@TiO2 hélicoïdal nanostructures (Fig. 7). Sous irradiation de lumière visible, des électrons chauds sont produits par l'effet LSPR de la nanoparticule Au à l'intérieur du TiO2 nanotube. Les électrons suivants seraient transférés de Au à la bande de conduction de TiO2 . La dégradation du MB adsorbé partirait des trous (•Au + ) parce que les trous peuvent piéger l'eau adsorbée en surface, générant des espèces radicalaires hydroxyle hautement réactives [24, 51, 54]. Simultanément, l'électron injecté dans la bande de conduction de TiO2 peut être piégé par les molécules d'oxygène pour former des radicaux superoxyde réactifs •O2 − . Ensuite, il peut encore réagir avec H + pour rapporter actif •HO2 − et • les radicaux OH. Enfin, les polluants organiques peuvent être détruits par ces radicaux en formation. Dans ce travail, on pense que la lumière polarisée est tournée par le chiral hélicoïdal Au@TiO2 La structure peut accélérer l'excitation du LSPR, ce qui améliore encore l'activité photocatalytique de l'hélice Au@TiO2 . De plus, la molécule MB adsorbée peut être excitée et transfère un électron à la bande de conduction de TiO2 comme le TiO2 pur les nanotubes montrent une petite activité photocatalytique sous irradiation de lumière visible. Ainsi, l'effet de photosensibilisation du MB devrait également conduire à une petite partie de la décomposition du MB.
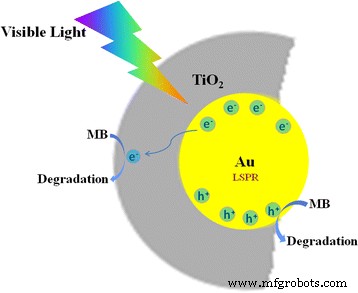
Représentation schématique du mécanisme de dégradation photocatalytique du MB sur Au@TiO2
Activité SERS
Pour exploiter l'application multifonctionnelle de tels catalyseurs, nous avons effectué des expériences supplémentaires en utilisant Au-x@TiO2 comme substrats SERS pour détecter les molécules MB adsorbées à la surface des nanoparticules d'or. Comme nous pouvons le voir sur la Fig. 8a, lors d'un sondage avec 1,0 × 10 −5 Solution M MB, l'activité SERS du substrat tel que préparé diminue avec l'augmentation du temps de pulvérisation d'Au de 30 à 120 s. Ce résultat indique que Au-30@TiO2 a les performances SERS les plus excellentes, ce qui implique que les nanoparticules d'Au en contact avec TiO2 les nanoparticules peuvent former un grand nombre de points chauds, ce qui peut faciliter une amélioration efficace du SERS [55]. Explorer l'influence de différentes concentrations de solution de MB sur la capacité de détection de Au-30@TiO2 , une mesure Raman a également été effectuée. Comme le montre la figure 8b, l'intensité du signal Raman diminue avec la diminution des concentrations de MB allant de 10 à 4 à 10 −6 M. Le signal Raman discernable de 10 −6 M MB avec bande Raman variant de 900 à 1500 cm −1 , indiquant que Au-30@TiO2 a agi comme substrat SERS, peut détecter des concentrations de MB aussi faibles que 10 −6 M, qui montre des applications potentielles pour la détection de polluants [56].
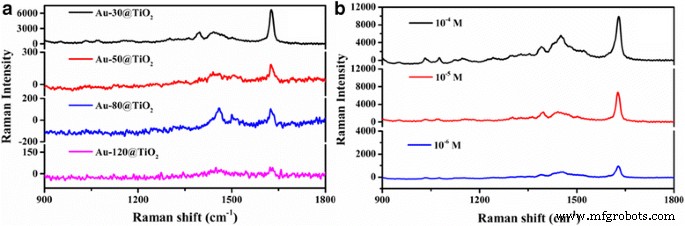
un Les spectres SERS de 1,0 × 10 −5 Solution M MB collectée sur les substrats avec différents Au-x@TiO2 . b Les spectres SERS du MB avec différentes concentrations collectés sur l'Au-30@TiO2 substrat
Conclusions
Dans cette étude, nous avons réussi à synthétiser Au@TiO2 nanocomposites hétérogènes jaune-coquille avec une morphologie en forme de bobine hélicoïdale et ont étudié leur utilisation multifonctionnelle, y compris la photocatalyse et l'effet SERS. La dégradation visible de la photocatalyse du MB montre que l'Au-x@TiO2 obtenu Le composite avec le temps de pulvérisation des nanoparticules d'Au de 80 s montre les performances photocatalytiques les plus élevées en raison de l'absorption accrue de la lumière et de la restriction de la recombinaison des paires électron-trou photoexcitées par l'effet LSPR des nanoparticules d'Au. Les mesures Raman suggèrent que le Au-x@TiO2 peuvent être utilisés comme substrats actifs SERS efficaces. Compte tenu de ses propriétés et de ses caractéristiques fascinantes, le nouveau nanocomposite hétérogène peut être une source d'inspiration dans divers domaines, notamment le fractionnement de l'eau et les cellules solaires. De plus, le jaune-coquille hélicoïdal Au@TiO2 Le système modèle étudié ici peut être étendu à la conception d'autres hétérostructures, telles que Ag@TiO2 , Au@ZnO et Au@NiO, pour une application dans la conversion solaire.
Nanomatériaux
- Apprentissage automatique et vision intelligente pour la périphérie industrielle
- Nanoparticules d'or multifonctionnelles pour des applications diagnostiques et thérapeutiques améliorées :une revue
- Nanoparticules pour le traitement du cancer :progrès actuels et défis
- Préparation et propriétés magnétiques des nanoparticules de spinelle FeMn2O4 dopées au cobalt
- Préparation de nanoparticules mPEG-ICA chargées en ICA et leur application dans le traitement des dommages cellulaires H9c2 induits par le LPS
- Fabrication, caractérisation et cytotoxicité de nanoparticules de carbonate de calcium dérivées de coquilles d'or conjuguées de forme sphérique pour des applications biomédicales
- A Resumable Fluorescent Probe BHN-Fe3O4@SiO2 Hybrid Nanostructure for Fe3+ and its Application in Bioimaging
- Saponines de Platycodon de Platycodi Radix (Platycodon grandiflorum) pour la synthèse verte de nanoparticules d'or et d'argent
- Génération d'espèces réactives de l'oxygène dans des solutions aqueuses contenant des nanoparticules GdVO4:Eu3+ et leurs complexes avec le bleu de méthylène



