Amélioration de la conductivité de l'électrolyte polymère solide par reformage du grain
Résumé
L'électrolyte polymère solide (SPE) à base d'oxyde de polyéthylène (PEO) est considéré comme ayant de grandes perspectives d'application dans les batteries Li-ion tout-solides. Cependant, l'application des SPE à base de PEO est entravée par la conductivité ionique relativement faible, qui dépend fortement de sa cristallinité et de la densité des joints de grains. Dans ce travail, une méthode de laminage-presse simple et efficace est appliquée pour réduire la cristallinité des SPE à base de PEO pour la première fois. Avec le SPE enroulé à base de PEO, le LiFePO4 La batterie li-ion tout solide /SPE/Li offre une capacité spécifique rechargeable supérieure de 162,6 mAh g −1 avec un écart de tension de décharge-charge de 60 mV à une densité de courant de 0,2 C avec un taux de décroissance de capacité beaucoup plus faible. L'amélioration des propriétés électrochimiques peut être attribuée à la méthode de laminage-presse, conduisant à une conductivité double et à une énergie d'activation réduite par rapport à celle de l'électrolyte préparé par la méthode de coulée traditionnelle. Le présent travail fournit une méthode de reformage des grains efficace et facile à utiliser pour SPE, digne d'une application future.
Introduction
En raison de leur haute densité énergétique et de leurs excellentes performances de sécurité, les batteries li-ion à semi-conducteurs sont largement considérées comme des systèmes prometteurs pour le stockage d'énergie électrochimique rechargeable de nouvelle génération [1,2,3,4]. Pour obtenir une batterie Li-ion entièrement à semi-conducteurs hautes performances, les électrolytes à semi-conducteurs doivent avoir une conductivité ionique élevée satisfaisante, une bonne stabilité mécanique/électrochimique et une interface électrode-électrolyte adéquate [2,3,4].
L'électrolyte polymère solide (SPE) à base d'oxyde de polyéthylène (PEO) a de grandes perspectives d'application en raison de sa bonne flexibilité, sa bonne compatibilité avec les métaux lithium, son processus facile et son faible coût [5]. En plus de la batterie li-ion solide, la SPE à base de PEO a également une large perspective d'application dans de nombreux domaines tels que la batterie Mg-ion et la batterie Li-S [6,7,8]. Cependant, la faible conductivité a grandement entravé l'application des SPE à base de PEO :les électrolytes de PEO présentent une conductivité qui varie de 10 à 8 à 10 −6 S cm −1 à température ambiante, et la faible conductivité augmentera la polarisation interne de la batterie et diminuera la capacité de décharge-charge et l'efficacité énergétique [9,10,11,12]. Dans les SPE à base de PEO, le li-ion forme une liaison de coordination avec l'oxygène dans le PEO et migre par coordination et dissociation continue avec les atomes d'oxygène. Par conséquent, la mobilité du li-ion dépend principalement du mouvement des segments de chaîne polymère au niveau du joint de grain et de la région de phase amorphe, et la conductivité ionique à travers le joint de grain et la région de phase amorphe est beaucoup plus élevée que celle à travers les lamelles cristallines [10] .
Pour diminuer la cristallinité du PEO et améliorer la conductivité des SPE, différentes approches ont été développées et appliquées, telles que le remplissage et le greffage. Les charges de taille nanométrique ont été largement utilisées dans les SPE à base de PEO, y compris l'Al2 de taille nanométrique O3 , TiO2 , SiO2 , Li0.3 3La0,557 TiO3 , et Li6.4 La3 Zr1.4 Ta0.6 O12 [12,13,14,15,16,17]. Ces charges de taille nanométrique peuvent inhiber la cristallisation du PEO et favoriser la formation de joints de grains et de régions amorphes. En outre, certaines charges à haute conductivité ionique peuvent également fournir une voie de transport ionique supplémentaire pour le transport li-ion [13,14,15]. Le greffage réduit également la cristallinité de la SPE à base de PEO. A titre d'exemple, le PEO a été greffé sur un squelette poly(hydroxylstyrène) ainsi que des copolymères blocs avec du polystyrène. Le macromoléculaire obtenu supprime considérablement la propension des chaînes PEO à la formation de cristaux complexes et améliore ainsi la conductivité ionique des SEP [18].
Le laminage à la presse est une technique de reformage normale pour le traitement des métaux [19,20,21]. En appliquant une force externe sur la surface du métal, le laminage à la presse peut écraser et affiner les grains, ainsi qu'augmenter la proportion des joints de grains et la dureté du métal [22, 23]. En raison de son processus simple, de son faible coût, de son efficacité élevée et de son effet évident de raffinement du grain, la méthode de laminage par pression est largement utilisée pour la fabrication d'échantillons de grandes feuilles ou plaques en vrac. Étant donné que le laminage à la presse peut casser les grains et augmenter les limites des grains et la phase amorphe, il a le potentiel d'être appliqué aux SPE à base de PEO pour réduire la cristallinité des électrolytes et améliorer la conductivité. Dans ce travail, nous rapportons une voie de laminage à la presse simple et facile pour préparer un électrolyte à l'état solide à base de PEO avec une conductivité ionique élevée pour les batteries li-ion à l'état solide. Cette nouvelle méthode présente les caractéristiques suivantes :(i) après le laminage, les sphérolites d'électrolyte polymère sont broyées et reformées, entraînant une diminution de la cristallinité et une double augmentation de la conductivité et (ii) avec la faible cristallinité, les SPE à base de PEO peut fournir plus de voies de transport pour la distribution du courant li-ion à l'équilibre sur la surface du lithium afin d'empêcher la croissance des dendrites. En outre, la méthode de pressage-laminage pour former les SPE à base de PEO proposée dans ce travail est très simple.
Méthode et caractérisation
Préparation d'électrolyte polymère solide
Oxyde de polyéthylène chimique de qualité analytique (PEO, Mw =600 000), oxyde d'aluminium de taille nanométrique (Al2 O3 , d ≤ 20 nm), le sel de lithium bis(trifluorométhane)sulfonimide (LiTFSI) et l'acétonitrile sont achetés auprès d'Aladdin, Chine, et utilisés tels quels.
L'électrolyte polymère solide d'origine a été préparé par une méthode de coulée simple :le PEO, Al2 O3, et LiTFSI ont été mélangés dans de l'acétonitrile pendant 24 h avec un rapport moléculaire EO/Li de 16/1 et PEO/Al2 O3 rapport pondéral de 90/10, puis la suspension blanche obtenue a été coulée dans un moule en polytétrafluoroéthylène et séchée dans du N2 sec débit à température ambiante pendant 24 h. L'électrolyte transparent résultant est nommé PAL-C, puis transféré dans un séchoir pour être conservé. Pour préparer l'électrolyte PAL-R, un électrolyte polymère solide PAL-C tel que préparé a été laminé à froid dans une presse à rouleaux sous la charge de ligne de 150 N mm −1 . Afin d'éliminer l'influence de l'épaisseur de l'électrolyte sur les performances, les épaisseurs de chaque électrolyte ont été contrôlées à ~ 135 μm.
Préparation des électrodes
L'électrode positive a été préparée par la méthode conventionnelle de la racle avec le LiFePO4 (LFP, BTR New Energy Material Ltd., Chine), noir d'acétylène (AB), PEO et rapport massique LiTFSI de 7:1:1,4:0,6. Le PEO et le LiTFSI ont d'abord été complètement dissous dans de l'acétonitrile, puis le LFP et l'AB ont été ajoutés à la solution transparente obtenue. Une suspension uniforme a été obtenue après agitation magnétique du mélange pendant 24 h, puis enduite sur une feuille d'aluminium par la méthode conventionnelle de la racle. L'électrode a ensuite été séchée à 80°C pendant 12µh et a finalement été découpée en disques circulaires de diamètre 12µmm. La charge de masse de matière active de l'électrode LFP telle que préparée est contrôlée pour être de ~ 1,5 mg cm −2 .
Caractérisations électrolytiques
Les morphologies des grains de l'électrolyte PAL-C et PAL-R ont été obtenues par microscopie électronique à balayage (MEB, JEOL-7500F). La cristallinité a été analysée avec un système de diffraction des rayons X (XRD, modèle PW1825) utilisant une source Cu-Kα fonctionnant à 40 keV. Les mesures de calorimétrie différentielle à balayage (DSC) ont été testées sur un instrument TA (Q5000IR) avec une vitesse de chauffe de 5 °C min-1 de -70 à 10 °C sous N2 atmosphère. Le rapport contrainte/déformation a été évalué par les courbes contrainte-déformation et la résistance à la traction a été prise sur une machine d'essai de traction (CMT6104, Chine) comme valeur de contrainte au maximum des courbes.
Performance électrochimique de l'électrolyte solide polymère à base de PEO
L'électrolyte solide polymère tel que synthétisé a été découpé en un disque d'un diamètre de 16,5 µm pour un test de performance électrochimique. Les conductivités ioniques des électrolytes polymères solides ont été mesurées dans des cellules CR2032 en prenant en sandwich l'électrolyte solide entre deux feuilles d'acier inoxydable (SS) poli (d =14,0 mm). La conductivité ionique a été obtenue sur cellule SS/SPE/SS par spectroscopie d'impédance électrochimique (EIS) sur la station électrochimique CHI660E avec une gamme de fréquence de 1 à 100 mHz à une température de 25 à 65°C. L'effet inhibiteur de la SPE à base de PEO sur la croissance des dendrites de lithium a été mené dans la cellule de symétrie Li/SPE/Li sur le système de test Neware (Neware, Chine) sous les densités de courant de décharge-charge de 0,1, 0,2 et 0,3 mA cm −2 à 60°C, respectivement. Le numéro de transfert li-ion (t Li+ ) de différents électrolytes a été évalué par une mesure combinée de l'impédance alternative et de la polarisation continue en utilisant la méthode décrite par Evans et al. [21]. Les courants de polarisation pour une cellule Li/SPE/Li symétrique (y compris le (I o ) et en régime permanent (I s ) des valeurs de courant) sous un petit potentiel de polarisation (ΔV) à 10 mV ont été enregistrées. Pendant ce temps, les valeurs initiales et stationnaires des résistances interfaciales Li/électrolyte (R 0 et R s ) ont été examinés avec des mesures d'impédance avant et après la polarisation DC. Le t Li+ a été calculé avec l'équation de Bruce-Vincent-Evans :
$$ {t}_{{\mathrm{Li}}^{+}}=\frac{I_{\mathrm{s}}\left(\Delta \mathrm{V}-{I}_0{R}_0 \right)}{I_0\left(\Delta \mathrm{V}-{I}_{\mathrm{s}}{R}_{\mathrm{s}}\right)} $$ (1)Les performances de la batterie des électrolytes polymères solides ont été testées dans la batterie li-ion tout solide avec une cathode LFP telle que préparée, une SPE à base de PEO et une anode en métal Li. Les batteries ont été assemblées dans une boîte à gants remplie d'argon (DELLIX, Chine, eau et oxygène ≤ 0,1 ppm) sans aucun autre électrolyte liquide. Les tests de décharge galvanostatique ont été effectués sur un système de cyclage de batterie à une densité de courant de 0,1 C (1 C =170 mA g −1 ) avec une plage de tension de 2,0 à 3,75 V. Avant le processus de charge-décharge, les résistances de transfert de charge ont été mesurées par des spectres d'impédance électrochimique (EIS) fonctionnant avec une plage de fréquences de 100 kHz à 0,1 Hz et une amplitude de tension alternative de 5 mV. La vitesse et les performances cyclistes ont été obtenues à partir de 0,1 C à 1 C et 0,5 C , respectivement. Tous les tests de performance de batterie mentionnés ci-dessus ont été effectués à 60 °C sur le système de test Neware (Neware, Chine).
Résultats et discussion
Les images SEM des électrolytes obtenus révèlent directement la taille des grains et la distribution des joints de grains de l'électrolyte tel que préparé (PAL-C) et de l'électrolyte laminé (PAL-R). L'électrolyte PAL-C présente une structure polycristalline de sphérolite compacte avec un diamètre de sphérolite de 50 µm (Fig. 1a et S1a). Pour les SPE à base de PEO, on pense que les ions li sont principalement transportés à travers les joints de grains et la phase amorphe. Par conséquent, le PAL-C SPE à gros grains obtenu par coulée est défavorable au transport des li-ions et limite la conductivité des électrolytes. Le traitement par laminage peut casser le grain d'électrolyte, ce qui peut réduire considérablement la cristallinité et augmenter la voie de transport des li-ions. Après laminage à la presse, la grosse sphérolite a disparu et l'électrolyte a montré une structure relativement homogène pour PAL-R (Fig. 1b et S1b). Cette structure homogène uniforme est considérée comme ayant des avantages évidents pour améliorer la conductivité des SPE.
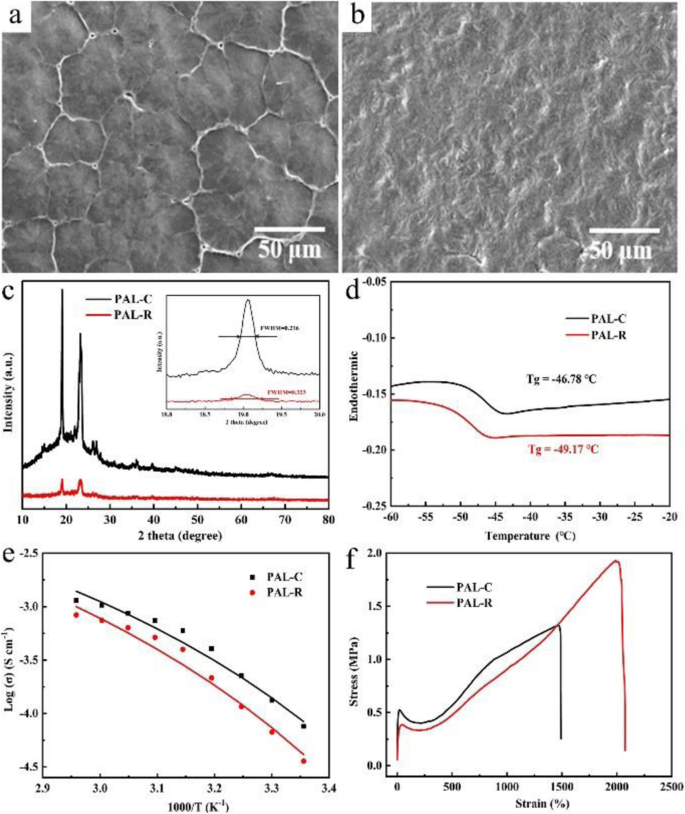
Caractérisation matérielle des différents SPES :a , b Images SEM du grain PEO dans SPE avant (a ) et après (b ) laminage à la presse ; c Modèles XRD pour différentes SPE (en médaillon :les pics XRD agrandis à 19,0 °) ; d profils DSC ; e conductivité ionique; et f courbes contrainte-déformation des SPE PAL-C et PAL-R
Afin d'analyser plus en détail le changement de cristallinité avant et après laminage, un test XRD a été effectué et les résultats sont présentés sur la figure 1c. Les pics de diffraction de l'électrolyte PAL-C à 19,0° et 23,2° sont nets et intenses, indiquant la nature hautement cristalline [22, 23]. À titre de comparaison, le diagramme de diffraction du PAL-R présente plusieurs pics larges et faibles, ce qui suggère que la cristallinité du PAL-R est considérablement réduite après le laminage à la presse. En outre, les principaux pics XRD de PEO à 19,0° sont également caractérisés par des changements significatifs de la pleine largeur à mi-hauteur (0,216 pour PAL-C et 0,323 pour PAL-R), ce qui implique que la phase amorphe dans l'électrolyte a augmenté. On pense que la diminution de la cristallinité a un effet significatif sur l'amélioration de la conductivité.
Les profils DSC des électrolytes PAL-C et PAL-R ont été testés et présentés sur la figure 1d, qui révèle la température de transition vitreuse (T g ) différences entre les deux électrolytes. Les résultats suggèrent que le T g de PAL-R est de −49,17 °C, ce qui est inférieur à celui de PAL-C (−46,78 °C). Ce résultat montre que dans l'électrolyte PAL-R, le mouvement des segments polymères peut se produire à plus basse température, ce qui conduit à une conductivité ionique plus élevée que celle de l'électrolyte PAL-C.
La conductivité ionique σ de PAL-C et PAL-R SPE est calculée avec l'équation suivante :
$$ \sigma =L/ RS $$ (2)où S , L , et R représentent la zone géométrique des électrodes de blocage en acier inoxydable, l'épaisseur des électrolytes et la résistance apparente de l'échantillon obtenus à partir des tracés d'impédance, respectivement. Les spectres d'impédance des électrolytes polymères solides PAL-C et PAL-R à différentes températures sont testés et illustrés sur la figure S2. La figure 1c montre la dépendance à la température de la conductivité ionique calculée des électrolytes PAL-C et PAL-R. L'électrolyte PAL-R tel que préparé atteint une conductivité ionique de 7,58 × 10 −5 S cm −1 à 25 °C et 1,03 × 10 −3 S cm −1 à 60 °C, ce qui est deux fois supérieur à celui de l'électrolyte PAL-C (3,58 × 10 −5 S cm −1 à 25°C et 7,43 × 10 −4 S cm −1 à 60 °C) et meilleure que celle de la SPE à base de PEO préparée par d'autres méthodes [14, 24, 25]. L'amélioration de la conductivité li-ion est attribuée à la réduction de la cristallinité de la SPE à base de PEO après le processus de laminage par pression et devrait conduire à de bonnes performances de la batterie. La relation entre le journal σ et 1000/T des SPE PAL-C et PAL-R révèle que la dépendance à la température de la conductivité suit l'équation empirique de Vogel-Tammann-Fulcher (VTF) [10, 16, 26, 27] :
$$ \sigma ={\sigma}_0{T}^{-1/2}\exp \left(-{E}_a/ RT\right) $$ (3)où σ , E un , σ 0 , T , et R représentent respectivement la conductivité ionique, l'énergie d'activation, le facteur pré-exponentiel, un facteur de température et la constante des gaz parfaits. Le E un de PAL-C et PAL-R a été calculé à l'aide de l'équation VTF (Fig. 1e), et les résultats montrent la valeur d'ajustement de E un pour PAL-R est de 5,0 × 10 −2 eV, ce qui est bien inférieur à celui du PAL-C (5,8 × 10 −2 eV). Le E inférieur un démontre que le mouvement li-ion dans l'électrolyte PAL-R nécessite moins d'énergie que celui des électrolytes PAL-C, indiquant une conductivité plus élevée.
La propriété mécanique de la SPE est directement liée à son effet barrière à la dendrite de lithium. La figure 1f montre les résultats des tests de contrainte-déformation des SPE PAL-C et PAL-R. La ductilité du PAL-R SPE atteint 1990%, ce qui est bien supérieur à celui du PAL-C SPE (1470%). Cette ductilité renforcée du PAL-R SPE améliorerait considérablement la tolérance à la pénétration des dendrites et inhiberait les courts-circuits dans les batteries. Les fenêtres électrochimiques de deux électrolytes polymères solides différents ont été testées avec la méthode de voltamétrie à balayage linéaire et les résultats sont présentés sur la figure S2. Les tensions de décomposition des deux électrolytes ont été testées pour atteindre 5,8 µV, ce qui suggère que la stabilité de l'électrolyte polymère solide n'a pas changé après le laminage à la presse. Les densités réelles des deux électrolytes sont obtenues en utilisant la méthode de drainage d'Archimède avec du kérosène comme milieu, et les densités de PAL-C et PAL-R sont calculées pour être toutes les deux de 1,38 ± 0,02 g cm −3 . Les résultats montrent que la différence de conductivité obtenue de ces deux électrolytes provient de la différence de joint de grain plutôt que du changement de densité.
L'effet inhibiteur des deux SPE sur la croissance des dendrites de lithium est testé avec une cellule symétrique Li/SPE/Li. Avant le début du test, une spectroscopie d'impédance électrochimique (EIS) est effectuée pour analyser les propriétés d'interface Li-SPE de différentes cellules et les résultats sont présentés sur la figure 2a. Les tracés EIS sont équipés d'un mode simple qui consiste en une résistance ohmique (R Ω ), résistance d'interface (R f ), résistance de transfert de charge (R ct ), éléments à phase constante (CPE1 et 2), et résistance à la diffusion de Warburg (Wo) [28, 29]. Les résultats simulés de R Ω , R f , et R ct dans la batterie utilisant l'électrolyte PAL-R sont calculés à 19,12, 5,72 et 17,65 Ω, respectivement, ce qui est plus petit que ceux utilisant des électrolytes PLA-C (21,83, 5,99 et 21,77 Ω). La diminution de la résistance de la solution (R Ω ) et la résistance interfaciale (R f ) peut être attribué à deux raisons :(i) après laminage, davantage de joints de grains sont créés dans l'électrolyte PAL-R, ce qui entraîne une conductivité plus élevée et une résistance de solution plus faible. (ii) La surface de l'électrolyte relativement lisse et les joints de grains accrus sont bénéfiques pour améliorer le contact de surface entre l'électrolyte et le lithium métal, conduisant à une résistance de solution et une résistance interfaciale inférieures. Les résistances de solution diminuées et la connexion interfaciale améliorée fournissent plus de voies de transport li-ion et d'interfaces de réaction pour la réaction électrochimique, conduisant finalement à la réduction de la résistance de transfert de charge (R ct ). Après le test EIS initial, une tension de 10 mV DC a été appliquée aux cellules symétriques Li/SPE/Li pour étudier le nombre de transfert li-ion dans différents SPE [30, 31]. Sur la base de la courbe courant-temps (Fig. 2b), impédance avant et après polarisation (Fig. 2a et S3), le nombre de transfert li-ion pour PAL-R SPE est calculé à 0,24, ce qui est supérieur à la valeur de PAL-C SPE (0,16). Cette amélioration peut être attribuée à la réduction de la phase de cristallinité, qui libère plus de li-ions pour le transport des ions. Après le test EIS, les cellules symétriques Li/PAL-C/Li et Li/PAL-R/Li ont été chargées et déchargées à 60°C pendant 30 min sous des densités de courant de 0,1, 0,2 et 0,3 mA cm − 2 , respectivement (Fig. 2c). A partir de ce résultat, nous pouvons constater que la tension de la cellule Li/PAL-R/Li peut être stabilisée à 33 mV et 67 mV à des densités de courant de 0,1 et 0,2 mA cm −2 , respectivement, qui sont beaucoup plus petites que celle de Li/PAL-C/Li (56 et 126 mV). Pour une densité de courant plus élevée (0,3 mA cm −2 ), PAL-R SEP peut cycler de manière stable pendant 200 cycles, mais la pénétration des dendrites se produit après seulement quelques cycles de PAL-C SPE sous la même densité de courant. Les morphologies de surface de l'électrode au lithium avec différentes SPE après 200 cycles à 0,2 mA cm −2 ont été testés et représentés sur les Fig. 2c, d. Il existe des dendrites de lithium irrégulières massives avec le PAL-C SPE, mais une surface de lithium relativement lisse avec le PAL-R SPE a pu être trouvée. Ce résultat peut être attribué à la conductivité ionique élevée et à la voie de transport uniforme des ions de PAL-R SPE, qui conduiront au dépôt uniforme de lithium pour éviter le court-circuit interne causé par la croissance des dendrites de lithium.
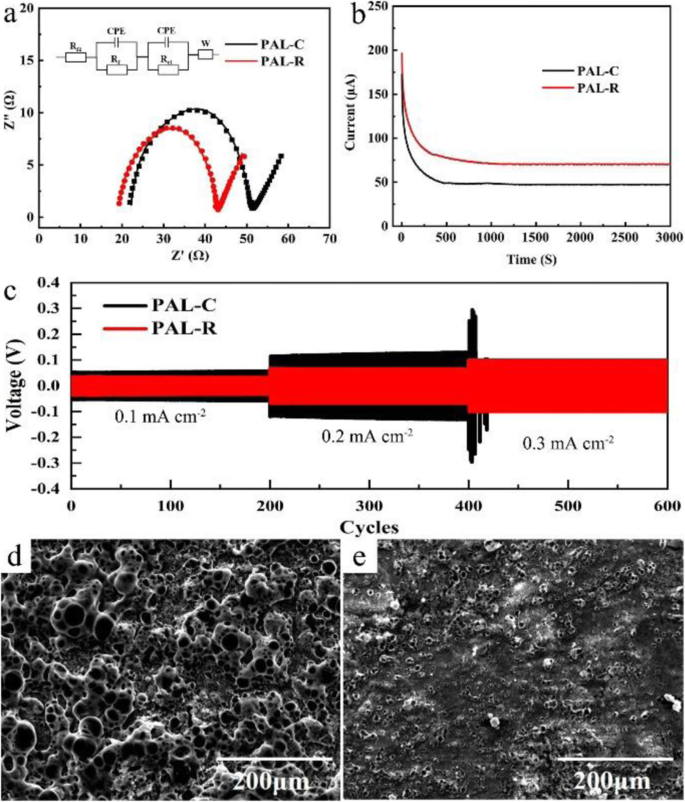
un Tracés EIS (encart :le modèle de circuit équivalent). b Courbe de polarisation DC et c performances de cyclage des cellules symétriques Li/SPE/Li avec différentes SPE. d et e La morphologie du métal Li après 200 cycles en cellule symétrique Li/SPE/Li avec PAL-C et PAL-R SPE, respectivement
Performances de charge-décharge galvanostatique des batteries li-ion tout solides contenant du LiFePO4 La cathode (LFP), l'anode Li avec différentes SPE sont testées et les résultats sont présentés sur la Fig. 3. Avant le test de charge-décharge galvanostatique, l'impédance de chaque batterie a été testée et équipée d'un modèle de circuit équivalent (encadré de la Fig. 3a) . Dans ce modèle, R Ω correspond à la résistance ohmique; R ct représente la résistance de transfert de charge pour les réactions électrochimiques ; CPE est l'élément à angle de phase constant lié à la capacité à double couche de la cathode poreuse, et Z w est la contribution de Warburg de longueur finie. On constate que R Ω diminue de 17,1 à 14,4 et R ct diminue de 47,5 à 33,1 pour la batterie avec PAL-C et PAL-R SPE, respectivement, comme le montre la figure 3a. Le R diminué Ω et R ct peut être attribué à la cristallinité inférieure de PAL-R SPE, qui peut fournir plus de voies de transport li-ion pour améliorer la conductivité de l'électrolyte et faciliter la réaction redox dans l'électrode LFP simultanément. La figure 3b montre les capacités de charge-décharge des batteries li-ion tout solide avec différentes SPE à 60 °C sous une densité de courant de 0,2 C . La batterie avec électrolyte PAL-R offre une capacité de décharge de 162,6 mAh g −1 avec un écart de tension de décharge-charge de 60 mV, tandis que la batterie avec électrolyte PAL-C offre une capacité de décharge de 156,7 mAh g −1 avec l'écart de tension de décharge-charge de 82 mV. L'augmentation de la capacité de décharge et la diminution de l'écart de tension peuvent être attribuées à la conductivité plus élevée et aux résistances plus faibles de l'électrolyte PAL-R par rapport à l'électrolyte PAL-C. La performance de taux de batteries li-ion tout solide avec différentes SPE a été réalisée sous des densités de courant de 0,1 C , 0,2 C , 0,5 C , 1 C , et 0,2 C (Fig. 3c, d et S4), respectivement. Les résultats indiquent que la batterie avec PAL-R peut fournir une capacité de 164,3, 162,6, 161,8, 157,8 et 161,2 mAh g −1 , respectivement. Cette performance est bien meilleure que la batterie à électrolyte PAL-C, qui ne délivre que des capacités de 161,5, 156,7, 148,7, 142,1 et 151,8 mAh g −1 , respectivement. Ce résultat a illustré que l'électrolyte PAL-R pouvait permettre le fonctionnement à haut débit en raison de la conductivité plus élevée.
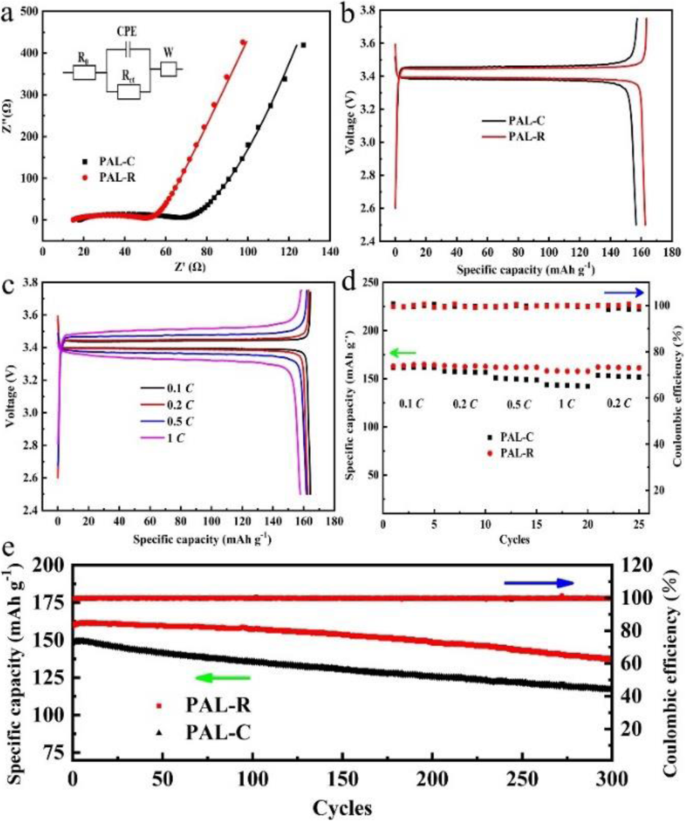
un Tracés EIS et résultats simulés pour les batteries LFP/SPE/Li avec différents SPE (encart :le modèle de circuit équivalent), b performances de décharge-charge des batteries LFP/SPE/Li avec différents SPE à 0,2 C , c courbes de décharge-charge de la batterie LFP/SPE/Li avec PAL-R SPE à différentes densités de courant, d taux de performance ; et e performances à long cycle des batteries LFP/SPE/Li avec différents SPE
Les performances de cycle de la batterie avec différents SPE ont été testées sous la densité de courant de 0,5 C (Fig. 3e). Pour la cellule LFP/PAL-C/Li, la capacité de décharge maintient 117,1 mAh g −1 après 300 cycles avec un taux de décroissance de capacité de 0,071% par cycle. A titre de comparaison, la cellule LFP/PAL-R/Li maintient une capacité de décharge de 136,8 mAh g −1 avec un taux de décroissance de capacité de 0,048% par cycle dans les mêmes conditions. Dans la batterie LFP/PEO-SPE/Li li-ion tout solide existante, la baisse de capacité provient principalement de deux aspects :(i) la génération et la croissance continues de dendrites de lithium sur l'anode dilue le contact entre l'électrode Li et l'électrolyte , ce qui entraîne une augmentation de la résistance de l'anode. (ii) Bien que le PEO ait une bonne stabilité, il se décompose toujours pendant la plage de tension de charge-décharge [14, 29]. Les produits de décomposition accumulés augmenteront progressivement la résistance de réaction de l'électrode cathodique. Dans la batterie tout solide avec électrolyte PAL-R, l'augmentation de la résistance de l'anode est inhibée en raison des bonnes performances d'inhibition des dendrites. Cependant, la réaction de décomposition continue dans l'électrode cathodique provoque une augmentation de la résistance de la batterie et devient progressivement la principale raison de la diminution de la capacité de la batterie après 100 cycles. En revanche, la batterie tout solide avec électrolyte PAL-C surfe à la fois de la résistance croissante de l'anode et de la résistance cathodique, entraînant une baisse continue de la capacité pendant 300 cycles. Les résultats montrent que le traitement de laminage peut améliorer les performances électrochimiques de l'électrolyte et qu'un électrolyte à l'état solide plus stable devrait être développé pour une application future.
Conclusion
Dans ce travail, nous avons appliqué une technologie simple de laminage-presse pour améliorer les performances des SPE à base de PEO pour les batteries li-ion tout-solides. Le SPE laminé à base de PEO présente une cristallinité réduite et une phase amorphe accrue, ce qui devrait être bénéfique pour le transport des li-ions. Après traitement, la SPE à base de PEO offre une conductivité à température ambiante doublée et une énergie d'activation réduite. Il est montré expérimentalement le LiFePO4 /SPE/Li batterie li-ion tout solide avec le SPE enroulé à base de PEO présente une capacité spécifique rechargeable de 162,6 mAh g −1 avec un écart de tension de décharge-charge de 60 mV à une densité de courant de 0,2 C , ce qui est bien meilleur que celui du SPE coulé à base de PEO (156,7 mAh g −1 et 82 µmV). De plus, le taux de décroissance de la capacité a été réduit à 0,0048 % par cycle après 300 cycles à 0,5 C . Tous les résultats montrent que la technologie de reformage des grains est une technologie prometteuse pour améliorer les performances des SPE à base de PEO.
Disponibilité des données et des matériaux
Toutes les données générées ou analysées au cours de cette étude sont incluses dans cet article publié et ses fichiers d'informations supplémentaires.
Abréviations
- PEO :
-
Oxyde de polyéthylène
- LFP :
-
LiFePO4
- SPE :
-
Electrolyte polymère solide
- AB :
-
Noir d'acétylène
- LiTFSI :
-
Sel de lithium bis(trifluorométhane)sulfonimide
- SEM :
-
Microscopie électronique à balayage
- XRD :
-
Diffraction des rayons X
- DSC :
-
Calorimétrie différentielle à balayage
- EIS :
-
Spectroscopie d'impédance électrochimique
- SS :
-
Acier inoxydable
Nanomatériaux
- Impression 3D polymère :Exploration de 6 exemples innovants de la technologie en action
- Le rôle de l'imbrication dans l'impression 3D polymère
- Blog :Les meilleurs OEM de consommables polymères en Chine
- Blog :Comprendre le processus de fabrication du PDMS
- Amélioration de l'expérience client :au-delà du résultat de l'enquête
- Amélioration des niveaux de service client en rayon
- Thermoplastique vs plastique thermodurcissable :quelle est la différence ?
- Améliorer l'usinabilité de l'aluminium
- Le rôle de la technologie de l'IA dans l'amélioration du secteur des énergies renouvelables



