Application de nanofeuillets de nitrure de bore chimiquement exfoliés dopés au Co pour éliminer rapidement les polluants organiques de l'eau textile
Résumé
Les matériaux stratifiés bidimensionnels dopés avec des métaux de transition présentent une magnétisation améliorée et une stabilité catalytique améliorée pendant le traitement de l'eau, conduisant à des applications environnementales potentielles dans plusieurs secteurs industriels. Dans la présente étude, des nanofeuillets de nitrure de bore dopé au cobalt (Co) (BN-NS) ont été explorés pour une telle application. Un processus d'exfoliation chimique a été utilisé pour exfolier le BN-NS et la voie hydrothermale a été adoptée pour incorporer le dopant Co à diverses concentrations (par exemple, 2,5, 5, 7,5 et 10 % en poids). Une étude par diffraction des rayons X (XRD) a indiqué que la cristallinité s'améliorait lors du dopage avec la formation d'une phase hexagonale du matériau synthétisé. La diffraction électronique à zone sélectionnée (SAED) a confirmé une cristallinité améliorée, ce qui corrobore les résultats de la DRX. L'espacement entre les couches a été évalué à l'aide d'un microscope électronique à transmission à haute résolution (HR-TEM) équipé du logiciel de micrographie numérique Gatan. L'analyse de la composition et des groupes fonctionnels a été réalisée avec la spectroscopie à rayons X à dispersion d'énergie (EDS) et la spectroscopie infrarouge à transformée de Fourier (FTIR), respectivement. Un microscope électronique à balayage à émission de champ (FE-SEM) et HR-TEM ont été utilisés pour sonder les morphologies de surface des échantillons préparés. Les modes de liaison dans l'échantillon ont été identifiés par analyse Raman. Les propriétés optiques ont été examinées par spectroscopie UV-vis. Des spectres de photoluminescence ont été acquis pour estimer la séparation et la recombinaison des excitons. Les propriétés magnétiques ont été étudiées au moyen d'une boucle d'hystérésis acquise à l'aide de mesures VSM. Le colorant bleu de méthylène a été dégradé avec l'hôte tel que préparé et des nanofeuilles dopées utilisées comme catalyseurs et étudiés à travers des spectres d'absorption allant de 250 à 800 nm. Les résultats expérimentaux de cette étude indiquent que le BN-NS co-dopé a montré des propriétés magnétiques améliorées et peut être utilisé pour dégrader les colorants présents sous forme d'effluent dans les eaux usées industrielles.
Introduction
Récemment, le nitrure de bore (BN), un matériau stratifié bidimensionnel prometteur similaire au graphène, le disulfure de tungstène (WS2 ), et le bisulfure de molybdène (MoS2 ), a beaucoup retenu l'attention. Le nitrure de bore existe généralement sous sa forme cristallographique la plus stable, c'est-à-dire le nitrure de bore hexagonal (h-BN). De plus, il se présente sous forme de nitrure de bore cubique (c-BN) qui est structurellement analogue au diamant, de nitrure de bore rhomboédrique (r-BN) et d'une phase amorphe [1]. L'espacement intercouche entre les couches de h-BN est de 3,30 ~ 3,34 tandis que le graphite présente un espacement de 3,33 ~ 3,35 . De plus, le h-BN est un bon isolant qui possède une bande interdite de ~ 5,9 eV [2, 3]. La structure cristalline du h-BN ressemble à celle du graphène, raison pour laquelle il est parfois appelé « graphène blanc » et est désigné comme le « matériau jumeau » du graphène. Fait intéressant, les atomes de bore et d'azote sont liés de manière covalente et disposés selon un motif en nid d'abeille [2, 4]. De plus, le h-BN offre d'excellentes propriétés physiques, chimiques, thermiques, électriques, optiques et diélectriques, ce qui le rend attrayant pour une utilisation dans diverses applications [5,6,7]. Des études ont été menées pour modifier les caractéristiques d'isolation du BN via le réglage de la bande interdite et les propriétés structurelles [3, 8]. Les nanofeuillets de nitrure de bore (BN-NS) ont été initialement préparés en 2004 en exfoliant un matériau en vrac en raison de son indisponibilité dans la nature. À ce jour, diverses méthodes ont été adoptées pour produire des nanofeuilles, notamment l'exfoliation chimique [9], le broyage à billes [10], l'irradiation par faisceau d'électrons [11] et la technique de vapeur chimique [12]. Diverses autres voies d'exfoliation sont également décrites dans la littérature [13,14,15].
Les applications potentielles du BN-NS incluent l'utilisation dans les dispositifs optoélectroniques et les dispositifs de gestion thermique. Il est particulièrement adapté à une utilisation comme photocatalyseur et catalyseur dans le traitement des eaux usées [3, 16, 17]. L'eau joue un rôle vital dans la survie et le développement de toutes les espèces vivantes sur terre, y compris l'humanité. Un approvisionnement adéquat en eau de bonne qualité en toutes saisons a un impact majeur sur l'environnement et la croissance économique d'une région [18, 19]. De plus, l'industrie alimentaire mondiale dépend fortement d'un approvisionnement constant en eau propre [20]. La disponibilité d'eau pure et douce est influencée par de nombreux facteurs, notamment le taux élevé de croissance démographique. On estime qu'environ 2,7 milliards de personnes dans de nombreux pays sont confrontées à une pénurie d'eau potable [18, 21].
Selon la littérature, un grand nombre de colorants, dont le rouge Congo, le jaune Martius, l'orange de méthyle, le rouge de méthyle et le bleu de méthyle sont utilisés dans divers secteurs industriels tels que le cuir, la construction, le papier, la fabrication de métaux et l'impression [22,23 ,24]. Les ions métalliques nocifs (Pb, Cr, Hg, Cu, etc.) produits en raison de l'utilisation de ces colorants ont des effets délétères sur la vie humaine et aquatique. L'exposition à des colorants non traités et à des ions métalliques toxiques peut entraîner des maladies graves telles que l'anémie, le cancer, l'encéphalopathie et l'affaiblissement du système immunitaire [20, 25]. De plus, la matière organique naturelle superflue peut augmenter le niveau de toxicité et nuire aux systèmes de purification de l'eau [26].
Le sel et d'autres impuretés mineures peuvent être éliminés de l'eau au moyen de techniques largement disponibles; cependant, l'élimination des colorants nocifs et des ions de métaux toxiques est plus difficile. Diverses voies ont été utilisées pour purifier l'eau de ces contaminants, notamment la photocatalyse [16], l'assistance magnétique [27], l'élimination de l'huile [28] et la filtration et la coagulation [29]. Parmi ces techniques, la catalyse tient une place importante puisqu'elle est considérée comme respectueuse de l'environnement, rentable et économe en énergie. De plus, la grande surface spécifique et les propriétés chimiques et physiques supérieures du BN-NS le rendent approprié pour une utilisation comme catalyseur dans le traitement des eaux usées [17].
Dans la présente étude, les propriétés magnétiques des échantillons synthétisés sont également étudiées en raison de leur impact potentiel sur le processus de traitement des eaux usées. Classiquement, les métaux de transition qui contiennent des électrons dans les couches 3d ou 4f sont responsables de l'origine du magnétisme. La littérature indique que l'aimantation spontanée est également observée dans les éléments légers sans métal qui contiennent des électrons en s et p orbitaire [30, 31]. De plus, l'origine du ferromagnétisme dans les semi-conducteurs ou oxydes magnétiques dilués (DMS(O)s) est fortement débattue [32, 33]. L'analyse théorique suggère que les défauts périodiques dans les nanomatériaux à base de graphène (2D), en particulier le h-BN, induisent un ordre magnétique (ferromagnétisme, ferrimagnétisme et anti-ferromagnétisme) [34]. De plus, ces défauts du h-BN agissent favorablement pour altérer son comportement diamagnétique vis-à-vis du ferromagnétisme [35]. Les métaux de transition (par exemple, Ni, Fe, Cu, Zn et Co) présentent des propriétés magnétiques satisfaisantes ; par conséquent, le dopage de ces espèces dans les nanofeuillets de BN augure des résultats prometteurs. En conséquence, le dopage du métal de transition (Co) dans le h-BN donne lieu à des défauts extrinsèques qui, avec les défauts intrinsèques, servent à améliorer ses propriétés magnétiques [36].
Dans la présente étude, une technique hydrothermale simple a été utilisée pour préparer des nanofeuillets de BN co-dopé avec une activité catalytique et un comportement magnétique améliorés. L'effet du dopage a été étudié en évaluant les propriétés structurelles, morphologiques, optiques et magnétiques du BN-NS.
Méthodes
L'étude actuelle visait à synthétiser diverses concentrations de Co dans des nanofeuillets de h-BN par voie hydrothermale pour éliminer les polluants organiques de l'eau textile et le comportement magnétique.
Matériaux
Poudre de BN en vrac (98 %), diméthylformamide (DMF), bleu de méthylène (MB) et borohydrure de sodium (NaBH4 ) ont été achetés auprès de Sigma-Aldrich Co. (Allemagne). Nitrate de cobalt (II) hexahydraté (CoH12 N2 O12 ) (98 %) a été acheté auprès de VWR Chemicals (Royaume-Uni). Tous les produits chimiques acquis pour cette étude ont été utilisés sans purification supplémentaire.
Exfoliation et synthèse de BN co-dopé
La voie d'exfoliation chimique a été utilisée pour synthétiser le BN-NS. Tout d'abord, 5 g de poudre de BN en vrac ont été dissous dans 200 mL de DMF et agités pendant 20 min pour obtenir la solution mère. Ceci a été suivi d'une sonication vigoureuse pendant 12 h. Après sonication, des feuilles de BN flottées ont été recueillies à partir de la solution mère. Le dopage a été réalisé via une approche hydrothermale. Dans cette méthode, du nitrate de cobalt (II) hexahydraté a été utilisé comme dopant au cobalt. Divers rapports pondéraux de nitrate de cobalt (II) hexahydrate (2,5, 5, 7,5 et 10 % en poids) ont été dopés sur les nanofeuillets de BN collectés. Ensuite, du BN-NS sélectionné et de l'hexahydrate de nitrate de cobalt (II) avec divers rapports (1:0,25, 1:0,05, 1:0,075, 1:0,1) ont été dispersés dans 100 mL d'eau déminéralisée sous agitation continue pendant 15 min. La suspension a été versée dans un autoclave en acier inoxydable, placé dans une étuve sous vide à 200°C pendant 10 h comme présenté schématiquement sur la figure 1. Enfin, l'autoclave a été retiré du four et refroidi à température ambiante. Le précurseur a été séché sur une plaque chauffante à 100-120°C.
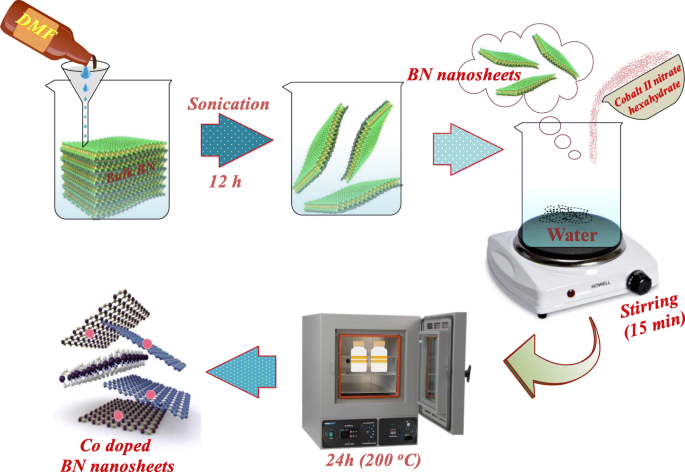
Illustration schématique de l'exfoliation et de la synthèse de BN-NS co-dopé
Activité catalytique
L'activité catalytique du BN-NS pur et co-dopé a été mesurée pour déterminer le degré de dégradation du colorant. Cela a été entrepris en surveillant la dégradation du MB dans une solution aqueuse de NaBH4 qui sert d'agent réducteur. MB et NaBH4 ont été fraîchement préparés pour assurer l'intégrité des données expérimentales. Habituellement, MB est l'indicateur redox le plus couramment utilisé en chimie analytique pour réguler l'activité catalytique lors d'un test de dégradation de colorant. De plus, le MB reste bleu sous forme oxydée alors qu'il apparaît neutre lorsqu'il est réduit [37]. Deux expériences catalytiques ont été réalisées, la première avec 500 μL de NaBH4 et 2 mg de catalyseur et le second avec 1000 μL de NaBH4 et 4 mg de catalyseur. En général, la concentration d'un catalyseur utilisé dans une expérience est le facteur le plus important qui affecte la réaction chimique. Un catalyseur abaisse l'énergie d'activation (E un ) d'une réaction servant ainsi à améliorer sa stabilité et sa vitesse de réaction. Le MB est avant tout un colorant toxique dangereux pour l'environnement. Il peut être réduit de NaBH4 qui le convertit en une espèce non toxique et incolore. Cependant, le processus de réduction est relativement lent en présence de NaBH4 . Les BN-NS non dopés et co-dopés présentent une grande surface spécifique qui, combinée à une augmentation de la réactivité de la réaction, sert à accélérer l'efficacité de réduction du colorant. L'incorporation d'un catalyseur dans le MB en présence d'un agent réducteur provoque une adsorption. De plus, une couche de réducteur dispersée sur les catalyseurs peut également accélérer l'adsorption en raison de la réaction d'oxydoréduction entre le catalyseur et le MB. La réaction de réduction par un catalyseur se produit en transférant e − du contenu des donateurs BH4 − (par exemple, de NaBH4 ) au contenu accepteur MB facilité par le BN-NS pur et dopé. Cela se traduit par la diminution de E un qui sert à stabiliser la réaction. L'activité catalytique a été évaluée en prenant 500 ou 1000 μL de NaBH4 dilué dans 10 mL de solution MB dans une cellule de quartz. Ensuite, un catalyseur (2 ou 4 mg) a été ajouté pour étudier la dégradation du MB. La dégradation du colorant a été évaluée par spectrophotométrie comme illustré schématiquement sur la figure 2. De plus, des spectres d'absorption allant de 200 à 800 nm obtenus avec MB ont été utilisés comme référence à température ambiante. La dégradation du colorant en présence de catalyseur pur et dopé a confirmé une activité catalytique accrue, tandis que NaBH4 n'a pas réussi à dégrader MB.

Illustration schématique du montage expérimental utilisé pour évaluer l'activité catalytique
Caractérisation des matériaux
Les échantillons préparés ont été analysés à l'aide de diverses techniques. La constitution de la phase et le degré de cristallinité ont été évalués à l'aide du diffractomètre à rayons X (XRD) analytique PAN X-pert PRO avec un rayonnement Cu-Kα (λ =1,5418 Å) et 2θ allant de 5° à 80°. La spectroscopie infrarouge à transformée de Fourier (FTIR) a été réalisée à l'aide d'un spectromètre Perkin Elmer pour confirmer la présence de groupes fonctionnels. Les spectres d'émission ont été obtenus à partir d'un spectroscope à photoluminescence (PL) en utilisant le spectrofluoromètre JASCO FP-8200. Les spectres Raman ont été obtenus avec un microscope DXR Raman (Thermo scientifique) ayant une diode Laser à 532 nm. L'examen morphologique a été réalisé à l'aide d'un microscope électronique à balayage à émission de champ JSM-6460LV (FE-SEM) et d'un microscope électronique à transmission haute résolution Philips CM30 et JEOL JEM 2100F (HR-TEM). Les propriétés optiques ont été enregistrées à l'aide d'un spectrophotomètre UV-visible Genesys 10S. La spectroscopie à rayons X à dispersion d'énergie (EDS) a été utilisée pour tracer la composition élémentaire. Les propriétés magnétiques ont été mesurées avec un magnétomètre à échantillon vibrant (VSM).
Résultats et discussion
XRD a été utilisé pour analyser la phase et la structure cristalline des échantillons préparés, comme illustré sur la figure 3a. Des pics de diffraction ont été observés à 26,8°, 41,6°, 43,52° et 50,2° qui ont été indexés comme plans (002), (100), (101) et (102), respectivement. Les réflexions observées confirment la présence d'une phase hexagonale de BN et concordent bien avec JCPDS 00-034-0421 [38, 39]. Il convient de noter que l'intensité de pic caractéristique de l'échantillon pur à l'échantillon dopé augmente, ce qui suggère que la cristallinité a été améliorée avec l'incorporation de Co. De plus, les motifs XRD indiquent un décalage de pic vers un angle de diffraction plus élevé, qui est attribué à la présence de dopant dans les spécimens [40]. Espacement intercalaire d 002 calculé à l'aide de la loi de Bragg (nλ = 2dsinθ) était de ~ 0,34 nm, ce qui est cohérent avec les résultats HR-TEM [41].
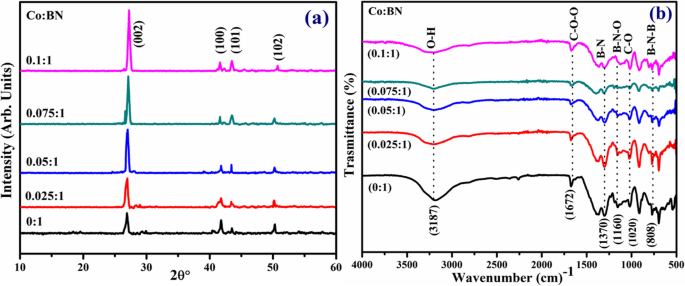
un Modèles XRD de concentrations vierges et diverses (2,5, 5, 7,5 et 10 % en poids) de BN-NS co-dopé. b Spectres FTIR
La FTIR a été réalisée pour identifier les empreintes digitales IR dans les nanofeuilles de contrôle et dopées, comme illustré sur la figure 3d. Les spectres ont été observés à ~ 808, 1020, 1160, 1370, 1672 et 3187 cm −1 . Deux pics centraux ont été identifiés à 808 et 1370 cm −1 qui sont supposés être associés à B–N–B (vibrations de flexion) et B–N (vibrations d'étirement). Ce dernier pic est associé à la vibration de flexion A2u mode (hors plan) tandis que le premier pic coïncide bien avec la vibration d'étirement E1u mode (dans le plan) [42, 43]. De plus, des pics à 1020, 1160 et 1672 cm −1 étaient cohérents avec les liaisons C–O, B–N–O et C=O, respectivement [44]. Un autre pic centré à 3187 cm −1 correspond à la liaison B–OH [45, 46].
L'identification des empreintes structurelles a été réalisée par spectres Raman, comme illustré sur la figure 4a. Les spectres montrent une bande Raman caractéristique centrée à 1370 cm −1 qui est attribué à E2g mode phonon actif du h-BN et corrélé au pic G du graphène [47]. Le BN-NS exfolié présente des pics mineurs à 550 et 880 cm −1 qui est attribué au fond fluorescent [48]. De plus, il est rapporté dans la littérature que le monocristal h-BN de haute qualité présente E2g mode phonon actif à 1367 cm −1 [40]. Dans cette étude, E2g décalé vers le rouge le mode phonon actif se produit à la suite d'une faible interaction entre les couches intermédiaires de BN. De plus, les spectres Raman décalés vers le rouge montrent la présence de quelques nanofeuillets en couches, ce qui provoque un léger allongement au sein des liaisons bore et azote (B-N) [49, 50]. Par conséquent, cet allongement de la liaison B-N est dû au ramollissement des phonons et est en bon accord avec les résultats précédemment cités. De plus, le dopage élémentaire, l'ordre des couches empilées, la taille du domaine et la porosité pourraient entraîner un élargissement et un déplacement des pics [51].
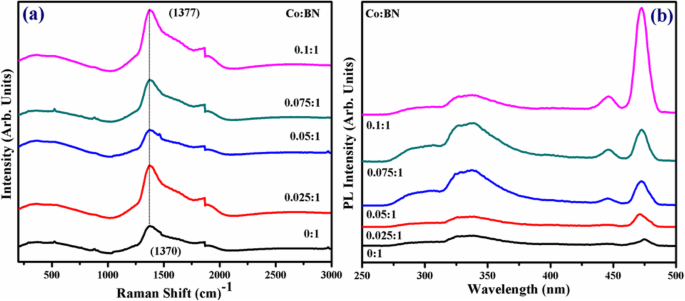
un Spectres de contrôle Raman et BN-NS dopés. b Spectres PL
La spectroscopie PL a été réalisée pour comprendre la migration excitonique et la recombinaison des paires électron-trou, comme le montre la figure 4b. Les spectres ont été observés avec une longueur d'onde d'excitation et d'émission de λ ex =220 nm et λ les =310 nm, respectivement. La bande caractéristique observée à ~ 322–342 nm correspond à la transition électron-trou due au niveau d'impureté [52, 53]. Il est à noter que la bande excitonique augmente mais ne montre pas de décalage de longueur d'onde lors du dopage. Les pics caractéristiques à ~ 446 nm et ~ 471 nm indiquent que l'intensité PL montre une forte augmentation des échantillons purs aux échantillons dopés. Pendant ce temps, le BN-NS dopé à 10 % en poids a une intensité PL maximale parmi tous les échantillons, ce qui indique une recombinaison électron-trou maximale. L'intensité diminue progressivement en raison de la concentration de dopage indiquant une séparation des charges photo-générées [54]. Les spectres d'émission ont révélé un comportement PL dépendant de l'excitation qui est cohérent avec les résultats précédemment rapportés [55].
La spectroscopie UV-vis a été utilisée pour étudier les spectres d'absorption et la bande interdite des produits tels que préparés, comme le montre la figure 5a. Le pic d'absorption caractéristique de l'hôte BN-NS était à un seuil de ~ 205 nm dans la région ultraviolette profonde (DUV) se référant à la bande interdite de ~ 5.7 eV comme présenté sur la figure 5b. Il convient de mentionner que le BN en vrac induit une bande interdite de 5,2 à 5,4 eV tandis qu'une monocouche expose une bande interdite de ~ 6,07 eV qui coïncide bien avec les calculs théoriques (par exemple, 6,0 eV). Dans le cas des bi/multicouches, la valeur de la bande interdite va de 5,56 à 5,92 eV [43]. Étant cohérents avec une large bande interdite sur la figure 5b et le comportement de luminescence DUV sur la figure 5a, les nanofeuillets h-BN peuvent être considérés comme un nouveau candidat pour une variété d'applications dans l'émission de photons, le laser UV et les détecteurs DUV [56] . De plus, le bord d'absorption s'est déplacé vers des longueurs d'onde plus longues avec des concentrations de dopage croissantes (2,5 à 10 % en poids) démontrant un décalage vers le rouge (Fig. 5b) [57].
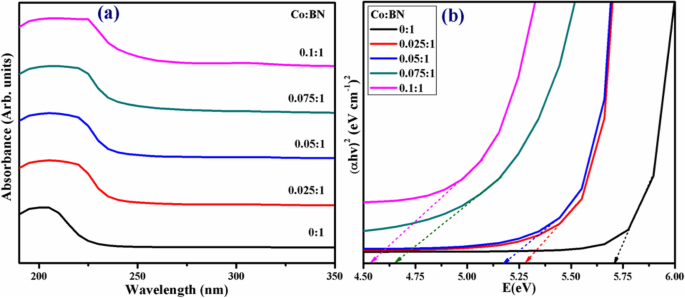
un Spectres UV-vis de BN-NS nu et co-dopé. b Tauc-plot pour bandgap
La morphologie et la composition du contrôle et du BN-NS dopé ont été analysées avec FE-SEM comme le montre la figure 6a. Les micrographies indiquent que les particules obtenues possédaient une structure de nanofeuillet agrégé avec une surface lisse et des bords incurvés. La figure 6 b–d montre des nanofeuillets de BN recouverts de cobalt. Une agglomération a été observée dans tous les échantillons. Les micrographies FE-SEM révèlent que les nanofeuilles sont pliées avec une structure en couches compacte et possèdent une forme et une dimension latérale non uniformes. La configuration et les dimensions des nanofeuillets sont une conséquence de l'exfoliation de la poudre de BN en vrac. La morphologie du produit obtenu a été en outre confirmée par une analyse HR-TEM. À partir des micrographies HR-TEM présentées sur les figures 6a–d, une morphologie en forme de feuille des produits tels que préparés a été observée. De plus, des surfaces rugueuses compactes de nanofeuilles ont été observées avec des caractéristiques légèrement poreuses qui se traduisent par une activité catalytique améliorée. Des taches sphériques sombres ont été observées indiquant l'incorporation réussie du dopage. Un empilement minutieux et des bords recourbés de nanofeuillets ont été enregistrés, comme le montre l'analyse SEM sur la figure 6a–d. Les résultats expérimentaux suggèrent que les analyses FE-SEM et HR-TEM indiquent une exfoliation réussie des nanofeuillets de BN à partir de BN en vrac.

un , a' Images FE-SEM et HR-TEM de BN-NS pur. b –d FE-SEM de (2,5, 7,5 et 10 % en poids) dopé BN-NS. b' –d’ HR-TEM de (2,5, 7,5 et 10 % en poids) dopé BN-NS (encart 50 nm)
Des mesures d'espacement intercouches d'échantillons nus et dopés ont été effectuées avec IFFT (voir encadré) induite au moyen d'images FFT de HR-TEM examinées par le logiciel de micrographie numérique Gatan pour distinguer les franges du réseau. d observé -la valeur d'espacement pour le BN-NS vierge et dopé à 2,5 % en poids est de 0,34 nm et 0,21 nm, ce qui correspond à d 002 et d 100 plans, respectivement, comme illustré sur les Fig. 7a, c. Ces résultats concordent bien avec l'analyse XRD et les données standard [58]. De plus, les profils SAED sont illustrés à la Fig. 7b, d qui signifient des anneaux de diffraction de points lumineux. Ces anneaux de diffraction ont été indexés comme provenant des plans (002), (100), (101) et (102) qui concordent bien avec les résultats de la DRX. Les motifs SAED suggèrent que tous les anneaux appartiennent au BN hexagonal et valident la nature hautement cristalline des nanofeuillets [58].
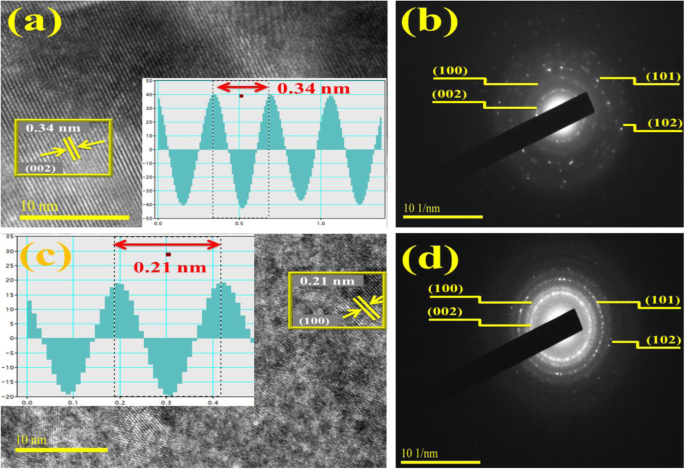
un , c d -analyse de l'espacement de l'hôte et du BN-NS dopé à 2,5 % en poids. b , d Modèles de contrôle SAED et BN-NS dopé à 2,5 % en poids
La composition élémentaire de surface du BN-NS dopé a été étudiée par analyse EDS, comme le montrent les figures 8a–d, respectivement. Les micrographies obtenues présentent de forts pics de bore (B) et d'azote (N), tandis qu'un signal mineur pour le cobalt (Co) a également été observé dans le spectre EDS (Fig. 8a). Deux pics modérés de Co à 0,5 et 7 keV ont été observés dans des échantillons dopés au Co, ce qui confirme l'incorporation réussie du dopant. De plus, le signal de carbone inférieur à 1 keV provient des languettes de carbone utilisées pour maintenir l'échantillon pendant l'analyse et/ou est dû à des comptages de fond élevés dans le détecteur SEM-EDS. Sinon, il n'y avait pas de carbone dans l'échantillon [59].

un –d Analyse EDS de diverses concentrations (2,5, 5, 7,5 et 10 % en poids) de BN-NS co-dopé
Les propriétés magnétiques du BN-NS co-dopé ont été évaluées avec la courbe M–H en utilisant des mesures VSM. Dans le graphique présenté sur la figure 9, l'aspect sigmoïde des boucles M–H démontre que le BN-NS co-dopé est caractérisé par un moment magnétique. L'étude de la littérature révèle que le BN vierge montre un comportement diamagnétique avec une susceptibilité (χ ≈ − 8,6 × 10 −7 émeu/g) [31, 35]. En revanche, le BN-NS co-dopé présente un ferromagnétisme à température ambiante (RT-FM) résultant de l'interaction d'échange entre Co +2 ions et dipôles non appariés qui ont tendance à s'aligner le long du champ magnétique appliqué. On peut voir que la boucle d'hystérésis apparaît plus précise ainsi que la concentration de dopage augmente, ce qui affirme la pureté et l'incorporation réussie du dopant. La coercivité, la rémanence et l'aimantation à saturation du BN-NS co-dopé prédisent la douceur et la dureté du matériau magnétique. Le codopage dans le BN-NS entraîne la formation d'un matériau magnétique doux. Les valeurs de rémanence (M r ), magnétisation à saturation (M s ), et la coercitivité (H C ) pour diverses concentrations de dopage (2,5, 5 et 7,5 % en poids) ont été calculés par la courbe M–H, comme le montre le tableau 1.
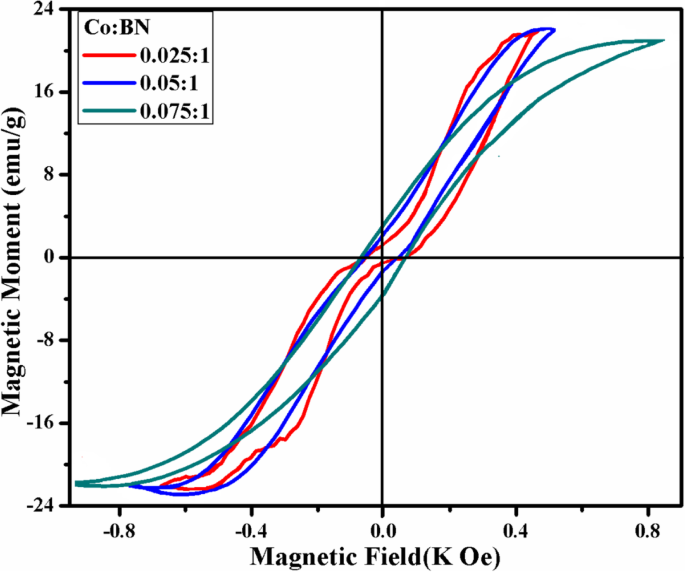
Courbe M–H de diverses concentrations (2,5, 5 et 7,5 % en poids) de BN-NS co-dopé
L'activité catalytique du BN-NS vierge et co-dopé qui fonctionne comme catalyseur a été exprimée par la dégradation du MB et étudiée par des spectres d'absorption surveillés avec un spectrophotomètre UV-vis. La figure 10 a–h montre les résultats de l'activité catalytique en utilisant 500 μL de NaBH4 et 2 mg de catalyseur. D'après la figure 10a, on peut voir que NaBH4 ne parvient pas à dégrader MB avec succès, car il ne dégrade que 8% du colorant après 40 min. Incorporation de BN-NS pur dans MB en présence de NaBH4 a entraîné une dégradation de 45 % en 30 min (Fig. 10b). De plus, la capacité de dégradation du BN-NS co-dopé (voir Fig. 10b–e) était significativement plus élevée. Diverses concentrations (2,5, 5, 7,5 et 10 % en poids) de catalyseur dopé démontrent une dégradation de 58, 77, 90 et 97 % en 13, 8, 3 et 2 min, respectivement. Fait intéressant, les nanofeuilles dopées à 10 % en poids produisent une activité catalytique supérieure et dégradent 97 % du colorant en seulement 2 min, ce qui est supérieur aux concentrations dopées (7,5, 5 et 2,5 % en poids) et une intensité de pic caractéristique est observée à ~ 290 et 665 nm. Cette augmentation de la dégradation du colorant est probablement due à l'amélioration de l'adsorption disponible ainsi que des sites catalytiques sur les catalyseurs. Dans ce mécanisme, l'état 3d de Co interagit bien avec l'état 2p des sites B ou N correspondants disponibles dans BN-NS. Cette forte interaction entre les états 3d Co et 2p B ou N augmente l'activité catalytique et entraîne une dégradation rapide du colorant, ce qui soutient favorablement nos résultats [60].
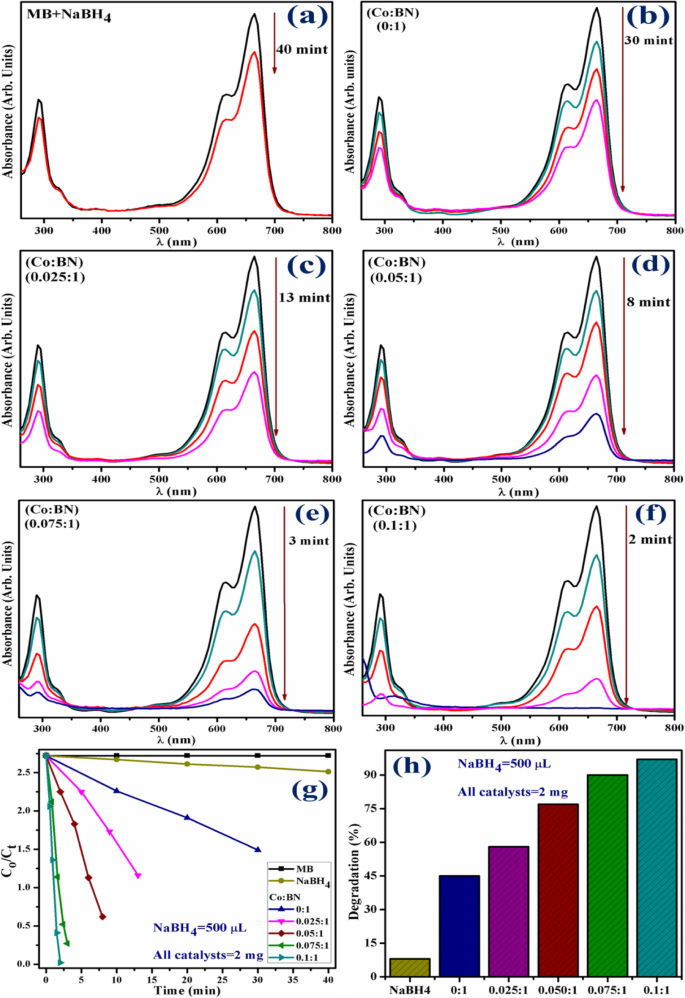
un Spectres UV-vis dépendant du temps de NaBH4 . b BN-NS vierge. c –f Diverses concentrations (2,5, 5, 7,5 et 10 % en poids) de BN-NS co-dopé. g Parcelles de C t /C o en fonction du temps. h Comparaison du pourcentage de dégradation sur différentes concentrations de BN-NS
L'expérience catalytique a été répétée en utilisant 1000 μL de NaBH4 et 4 mg de catalyseur. En augmentant la concentration du catalyseur, la réaction se déroule plus rapidement par rapport à l'expérience mentionnée précédemment. Cette observation est en bon accord avec la littérature. Dans la présente expérience, NaBH4 n'a toujours pas réussi à dégrader le MB tandis que le BN-NS vierge et diverses concentrations (2,5, 5, 7,5 et 10 % en poids) de catalyseur dopé se sont dégradés à 51, 65, 82, 95 et 99 % dans 27, 10, 6, 2 et 1 min, respectivement, tel qu'évalué avec un spectrophotomètre. Les résultats expérimentaux mesurant l'activité catalytique sont illustrés sur les Fig. 11a, b.
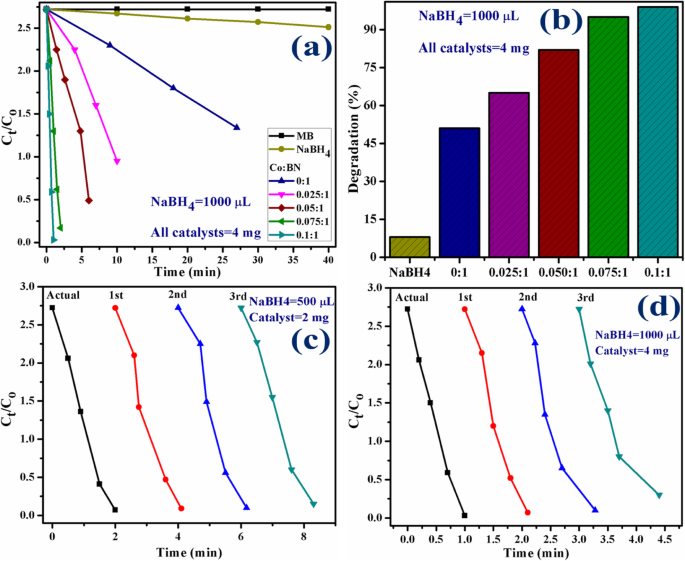
un Parcelles de C t /C o en fonction du temps en utilisant NaBH4 =1000 μL et catalyseurs =4 mg. b Comparaison du pourcentage de dégradation sur différentes concentrations. c Parcelles de C t /C o en fonction du temps pour la réutilisation du BN-NS co-dopé à 10 % en poids. d Parcelles de C t /C o en fonction du temps pour la réutilisation du BN-NS co-dopé à 10 % en poids
Selon la loi de Beer-Lambert, le rapport de la concentration de MB à un instant donné (C t ) et la concentration initiale de MB (C o ), dénommé C t /C o , peut être estimée par le rapport d'absorbance parallèle (A t /Un o ). Les figures 10f et 11a illustrent l'évolution dans le temps de C t /C o utilisé pour tous les catalyseurs tandis que les figures 10 g et 11 b indiquent le pourcentage de dégradation de tous les catalyseurs. Le pourcentage de dégradation a été évalué par l'Eq. 1.
$$ \mathrm{Dégradation}\ \left(\%\right)=\frac{Co- Ct}{Co}\times 100 $$ (1)De plus, la valeur du pH est une variable opérationnelle vitale dans le traitement de dégradation des colorants. De plus, le pH joue un rôle important dans le traitement des eaux usées textiles et dans les mécanismes de réaction qui contribuent à la dégradation des colorants. Il convient de mentionner que le pourcentage de dégradation dépend dans une large mesure de la valeur du pH. Dans la présente expérience, la valeur du pH a été fixée à 8,5. De manière significative, la dégradation du colorant due à l'activité catalytique a démontré les meilleurs résultats dans un environnement alcalin qui soutient favorablement nos résultats expérimentaux. Plusieurs rapports révèlent que la plus forte dégradation de colorant par activité catalytique a été observée dans un environnement alcalin [61].
La stabilité et la réutilisation (capacité de recyclage) des catalyseurs est une caractéristique importante pour évaluer un catalyseur utilisé pour la dégradation des colorants. Dans la présente étude, la stabilité des catalyseurs a été évaluée en permettant à l'expérience réalisée de rester pendant 48 h. Après 48 h, les résultats étaient les mêmes que ceux obtenus initialement, c'est-à-dire que la dégradation était toujours dans son état précédent. La réutilisation du catalyseur a été étudiée en recyclant 10 % en poids de catalyseur dopé au Co qui a servi de catalyseur supérieur dans la présente étude pendant trois cycles. Les spectres extraits de l'activité catalytique recyclée ont été évalués comme le montre la figure 11c, d.
De plus, la charge du catalyseur avant et après trois fois le processus de recyclage a été examinée. Dans la première et la deuxième activité, une perte de poids mineure de catalyseur allant de 2 mg et 4 mg (avant) à 1,7 mg et 3,6 mg (après trois cycles) a été détectée en considérant ~ 5% de déviation de détection dans la présente expérience. Ces résultats indiquent que le BN-NS co-dopé présente une stabilité exceptionnelle tout en servant de catalyseur. Enfin, cette étude suggère que le BN-NS co-dopé présente un comportement catalytique efficace et exceptionnel vis-à-vis de la dégradation des colorants dans le traitement des eaux usées industrielles.
Conclusion
Dans cette étude, des nanofeuillets de nitrure de bore (BN-NS) ont été synthétisés par exfoliation chimique de poudre de BN en vrac. Diverses concentrations (2,5, 5, 7,5 et 10 % en poids) de Co ont été incorporées avec succès via l'approche hydrothermale. As prepared, pure and doped BN-NS were characterized by a variety of techniques to evaluate the effect of doping. XRD patterns confirm the presence of the hexagonal phase of BN with improved crystallinity from pure to doped samples. Furthermore, the peak shift indicates the successful incorporation of doping. FTIR spectra indicate sp 2 bonded B–N stretching vibrations consistent with E1g mode (in-plane) as well as B–N–B bending vibration associated with A2u mode (out plane). Raman spectroscopy affirmed E2g active phonon mode of h-BN while photoluminescence spectroscopy revealed emission spectra that were attributed to exciton migration and recombination. Host and Co-doped BN-NS displayed absorbance in the DUV region along with a redshift that causes a decrease in bandgap energy suggesting it to be a suitable material for degradation of dye from industrial wastewater and organic pollutants. Sheet-like morphology of obtained product was studied by means of FE-SEM and HR-TEM. Slightly porous features result in high catalytic activity due to available adsorption sites. EDS analysis showed the purity of the sample and confirmed the incorporation of dopant in nanosheets. The magnetic behavior of Co-doped BN-NS was investigated through VSM measurements that display strong ferromagnetic behavior while pristine BN-NS show diamagnetic behavior. Significantly, the sigmoidal appearance of the hysteresis loop becomes more precise from lower to a higher concentration of Co-doped BN-NS, which point toward the formation of a soft magnetic material. Lastly, pure and Co-doped BN-NS was utilized as a catalyst in dye degradation. The catalytic activity provides efficient results for most samples but 10 wt% Co-doped catalyst showed significant outcome with the highest dye degradation (99%) in 1 min, making it a novel catalyst in this study. Extracted results from pure and doped BN-NS can be used as a guideline to modify and enhance magnetic properties in order to improve reliability in modern optoelectronic technology. Finally, the synthesized material has the potential to be used as a stable, reusable, and superior nano-catalyst to replace conventional wastewater treatment methods.
Disponibilité des données et des matériaux
Toutes les données sont entièrement disponibles sans restriction.
Abréviations
- BN-NS:
-
Boron nitride nanosheets
- Co:
-
Cobalt
- UV-vis :
-
Spectroscopie visible ultra-violet
- XRD :
-
Diffraction des rayons X
- DUV:
-
Deep ultraviolet region
- FTIR :
-
Spectroscopie infrarouge à transformée de Fourier
- PL :
-
Photoluminescence
- DMF :
-
Diméthylformamide
- Mo :
-
Bleu de méthylène
- NaBH4 :
-
Sodium borohydride
- EDS :
-
Spectroscopie à rayons X à dispersion d'énergie
- FE-SEM :
-
Microscopie électronique à balayage à émission de champ
- HR-TEM :
-
Microscopie électronique à transmission haute résolution
- JCPDS :
-
Joint committee on powder diffraction standards,
- VSM:
-
Vibrating sample magnetometer measurements
Nanomatériaux
- Python supprime les doublons d'une liste
- États électroniques de nanocristaux dopés à l'oxygène et émission visible sur silicium noir préparés par ns-Laser
- Nouveaux nanocomposites de polystyrène avec polyaniline dopé à l'acide lauryl sulfurique
- Vers des chaînes à un seul atome avec du tellure exfolié
- Microsphères de carbone magnétique comme adsorbant réutilisable pour l'élimination des sulfamides de l'eau
- Réponse photovoltaïque prononcée du phototransistor MoTe2 multicouche avec formulaire de contact asymétrique
- Exfoliation liquide à haute efficacité de nanofeuillets de nitrure de bore à l'aide d'une solution aqueuse d'alcanolamine
- Synthèse écologique et facile de nanofils de Co3O4 et leur application prometteuse avec du graphène dans les batteries lithium-ion
- Comment éliminer l'humidité de l'air comprimé



