Le diagramme de phase fer-carbone
Le diagramme de phase fer-carbone
Les diagrammes de phase sont des outils très importants dans l'étude des alliages pour résoudre de nombreux problèmes pratiques en métallurgie. Ces diagrammes définissent les régions de stabilité d'une phase qui peuvent exister dans un système d'alliage sous la condition d'une pression atmosphérique constante. Pour un système binaire, les coordonnées de ces diagrammes sont la température et la composition. Les interrelations entre les phases, la température et la composition dans un système d'alliage sont normalement présentées par diagramme de phase uniquement dans des conditions d'équilibre. De telles conditions se produisent lors de faibles vitesses de chauffage et de refroidissement des alliages, lorsque la cinétique des transformations ne joue pas un rôle important.
Dans leur forme la plus simple, le fer et les aciers sont des alliages de fer (Fe) et de carbone (C). Il existe trois types d'alliages ferreux. Ces alliages sont constitués (i) de fer ayant une teneur en C inférieure à 0,0008 % à température ambiante, (ii) d'aciers ayant une teneur en C allant de 0,008 % à 2,14 % (normalement moins de 1 %) et ayant une microstructure composée de ferrite et de cémentite ), et (iii) fonte avec une teneur en C allant de 2,14 , L'étude de la constitution et de la structure du fer et des aciers commence par le diagramme de phase fer-carbone (Fe-C) (Fig 1). Le diagramme de phase Fe-C est également utilisé comme base pour la compréhension des procédés de traitement thermique.
De nombreuses caractéristiques de base du système Fe-C influencent le comportement des alliages de fer et d'acier les plus complexes. Par exemple, les phases trouvées dans le système binaire simple Fe-C persistent dans les aciers complexes, mais il est nécessaire d'examiner les effets des éléments d'alliage sur la formation et les propriétés de ces phases. Le diagramme Fe-C fournit une base précieuse sur laquelle la connaissance des aciers au carbone et des aciers alliés peut être construite.
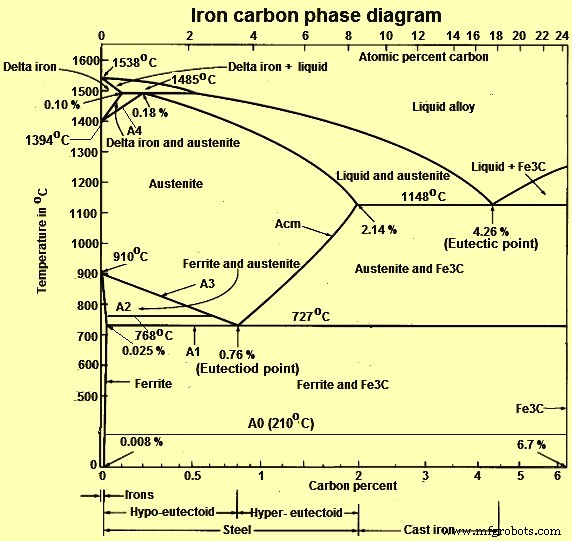
Fig 1 Diagramme de phase fer-carbone
C est une impureté interstitielle dans Fe. Il forme une solution solide avec les phases alpha, gamma et delta de fer. La solubilité maximale du C dans le fer alpha est de 0,025 % à 727 deg C. Le fer cubique centré (BCC) a des positions interstitielles relativement petites. La solubilité maximale du C dans le fer gamma cubique à faces centrées (FCC) est de 2,14 % à 1 148 deg C. Le fer FCC a des positions interstitielles plus grandes. Les propriétés mécaniques des alliages fer-carbone (fer et aciers) dépendent de leur microstructure, c'est-à-dire de la manière dont les différentes phases sont mélangées.
Le diagramme de phase fer-carbone de la figure 2 montre en fait deux diagrammes, à savoir (i) le diagramme fer-graphite stable (lignes rouges), (ii) et le diagramme métastable Fe-Fe3C. La cémentite est métastable, et le véritable équilibre se situe entre le fer et le graphite (C). Bien que le graphite soit largement présent dans les fontes, il est généralement difficile d'obtenir cette phase d'équilibre dans les aciers. La condition stable prend généralement très longtemps à se développer, en particulier dans la plage des basses températures et des faibles émissions de carbone. Ainsi, le diagramme d'équilibre normal généralement utilisé est le diagramme métastable Fe-Fe3C car il est pertinent pour le comportement de la plupart des aciers en pratique.
Les détails des diagrammes de phase stables et métastables du système Fe-C, en particulier du côté riche en Fe, sont bien mieux connus que tout autre système binaire de complexité similaire. Cependant, il existe encore des domaines importants où le diagramme de phase n'a pas été bien établi, comme dans les plages de température, de composition et de pression qui ne sont pas directement liées à la fabrication du fer et de l'acier.
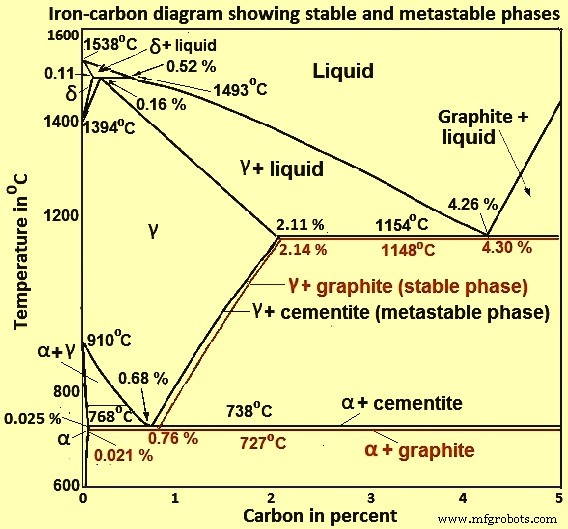
Fig 2 Diagramme fer-carbone montrant les phases stables et métastables
Il existe des phases métallurgiques et des microconstituants importants dans le système fer-carbone. Dans le système Fe-Fe3C, le carbone est une impureté interstitielle dans Fe. Il forme une solution solide avec des phases alpha (ferrite alpha), gamma (austénite) et delta (ferrite delta) de fer. Ce sont des phases importantes dans le diagramme de phase Fe - Fe3C. Entre les champs monophasiques, on trouve des régions avec des mélanges de deux phases, telles que la ferrite et la cémentite, l'austénite et la cémentite, et la ferrite et l'austénite. Aux températures les plus élevées, le champ de phase liquide peut être trouvé et en dessous se trouvent les champs à deux phases liquide et austénite, liquide et cémentite, et liquide et ferrite. Dans le traitement thermique des aciers, la phase liquide est toujours évitée. Au point eutectique (4,26 % C), l'alliage liquide lors du refroidissement est directement converti en austénite et en cémentite sans champ diphasique. De même, au point eutectoïde (0,76 % C), la phase austénitique lors du refroidissement est directement convertie en ferrite et en cémentite sans aucun champ biphasé. Certaines limites importantes des champs monophasés ont reçu des noms spéciaux qui facilitent la compréhension du diagramme.
Les phases principales du fer et des aciers en équilibre sont les phases suivantes.
- Ferrite ou phase de fer alpha – C'est une forme stable de fer à température ambiante. C'est une phase relativement douce à basse température et une phase d'équilibre stable. Il se transforme en austénite FCC (phase gamma) à 910 deg C. La ferrite est un constituant courant des aciers et a une structure BCC, qui est moins dense que la structure FCC. Il est doux et assez ductile. Il est magnétique en dessous de 768 degrés C. Il a une faible résistance et une bonne ténacité.
- Austénite ou phase de fer gamma :l'austénite est une phase à haute température. C'est une solution solide de C dans le fer FCC. Par conséquent, il a une structure FCC, qui est une structure compacte. C'est une phase non magnétique et ductile. Il se transforme en ferrite delta BCC à 1394 deg C. Il n'est pas stable en dessous de la température eutectique (727 deg C) à moins d'être refroidi rapidement. L'austénite a une bonne résistance et ténacité.
- Phase de ferrite delta – Il s'agit d'une solution solide de C dans BCC fer. Il n'est stable qu'à une température supérieure à 1 394 degrés C. Il fond à 1 538 degrés C. Il possède des propriétés paramagnétiques.
- Cémentite - C'est du Fe3C ou du carbure de fer. C'est un composé intermétallique de Fe et C. Il a une structure orthorhombique complexe et est une phase métastable. C'est une phase dure et cassante. Il a une faible résistance à la traction, une bonne résistance à la compression et une faible ténacité. Il se décompose (très lentement, en plusieurs années) en ferrite alpha et C (graphite) à la plage de température de 650 deg C à 700 deg C.
En comparant l'austénite à la ferrite, la solubilité du carbone est plus dans l'austénite avec une valeur maximale de 2,14 % à 1148 deg C. Cette solubilité élevée du carbone dans l'austénite est extrêmement importante dans le traitement thermique, lorsque le traitement de mise en solution dans l'austénite suivi d'une trempe rapide à température ambiante permet la formation d'une solution solide sursaturée de carbone dans le fer. La phase de ferrite est restreinte avec une solubilité maximale du carbone de 0,025 % à 727 °C. Étant donné que la plage de carbone disponible dans les aciers courants est de 0,05 % à 1,5 %, la ferrite est normalement associée à la cémentite sous l'une ou l'autre forme. De même, la phase delta est très restreinte et se situe dans la plage de température comprise entre 1394 deg C et 1538 deg C/ Elle disparaît complètement lorsque la teneur en carbone atteint 0,5 %.
L'alliage de composition eutectoïde (0,76 % C) lorsqu'il est refroidi lentement, forme la perlite, qui est une structure en couches de deux phases, à savoir l'alpha‐ferrite et la cémentite. La perlite est le mélange de phases ferrite-cémentite. Il a un aspect caractéristique et peut être traité comme une entité micro structurelle ou un micro constituant. C'est un agrégat de lamelles alternées de ferrite et de cémentite qui dégénère (sphéroidise ou grossit) en particules de cémentite dispersées avec une matrice de ferrite après un maintien prolongé en dessous de 727 ° C. C'est un eutectoïde et a une structure BCC. C'est une solution partiellement soluble de Fe et de C. Mécaniquement, la perlite a des propriétés intermédiaires à la ferrite douce et ductile et à la cémentite dure et cassante. Il a une résistance élevée et une faible ténacité.
Les alliages hypo-eutectoïdes contiennent de la ferrite pro-eutectoïde (formée au-dessus de la température eutectoïde) ainsi que la perlite eutectoïde qui contient de la ferrite eutectoïde et de la cémentite. Les alliages hyper-eutectoïdes contiennent de la cémentite pro-eutectoïde (formée au-dessus de la température eutectoïde avec de la perlite qui contient de la ferrite eutectoïde et de la cémentite.
En cas de solidification hors équilibre du système Fe-C, un type supplémentaire de microstructures peut également être formé. Certaines de ces microstructures sont données ci-dessous.
- Bainite - C'est une phase entre la perlite et la martensite. C'est un microconstituant métastable dur et se compose d'un mélange non lamellaire de ferrite et de cémentite à une échelle extrêmement fine. La bainite supérieure se forme à des températures plus élevées et a un aspect plumeux. La bainite inférieure se forme à des températures plus basses et a un aspect aciculaire. La dureté de la bainite augmente avec la diminution de la température de sa formation. Il a une bonne résistance et ténacité.
- Martensite - C'est une forme très dure de structure cristalline en acier. Il porte le nom du métallurgiste allemand Adolf Martens. Il se forme par refroidissement rapide et est dur et cassant. Il s'agit d'une forme de fer tétragonale centrée sur le corps (BCT) dans laquelle une partie du carbone est dissoute. Il se forme pendant la trempe, lorsque le réseau cubique d'austénite centré sur la face est déformé dans la structure tétragonale centrée sur le corps sans la perte de ses atomes de carbone contenus dans la cémentite et la ferrite. C'est une solution super saturée d'atomes de carbone dans la ferrite. C'est une phase métastable dure. Il a une morphologie en lattes lorsque C est inférieur à 0,6 %, une morphologie en plaques lorsque C est supérieur à 1 % et un mélange de ceux entre les deux. Il a une résistance et une dureté élevées et une faible ténacité.
- Sorbite/troostite – Les structures de l'étage inférieur de perlite avec de très fins flocons sont appelées sorbite et troostite. Ce sont les structures de transformation de l'étape perlitique qui correspondent aux vitesses de refroidissement croissantes. Cependant, cela modifie le rapport de structure et la formation de perlite en ce qui concerne la distance des flocons. La structure ne peut pas être vue au microscope optique.
- Ferrite de Widmanstatten - Elle est obtenue lorsque l'acier au carbone ordinaire hypo-eutectoïde est refroidi rapidement à une température supérieure à la température A3. En raison du refroidissement rapide, les cristaux de ferrite disposent de peu de temps pour nucléer non seulement à la limite des grains, mais également à l'intérieur des gros grains d'austénite. Ils se développent rapidement dans une direction cristalline préférée à l'intérieur du grain et deviennent ainsi longs. La structure se présente sous la forme d'aiguilles (lattes) ou de plaques qui ont tendance à s'aligner dans la même direction dans un grain.
Il existe de nombreuses températures et points critiques dans le diagramme Fer-C qui sont importants à la fois du point de vue de base et du point de vue pratique. Ce sont les températures auxquelles lors du refroidissement, ou du chauffage, les transformations de phase aussi bien magnétiques s'y produisent. Les températures auxquelles les transformations se produisent à l'état solide sont appelées températures critiques ou points critiques. Les températures principales et les points critiques sont indiqués ci-dessous.
- Température A0 - C'est la température de Curie lorsque le changement magnétique à non magnétique de la cémentite se produit lors du chauffage. La structure peut développer des défauts tels que des dislocations, des failles et des lacunes. La cémentite est métallique et ferromagnétique avec une température de Curie d'environ 210 deg C. Lorsqu'ils sont alliés, les solutés métalliques se substituent aux sites de fer ; des atomes plus petits tels que le bore remplacent le carbone sur les sites interstitiels.
- Température A1 - C'est la température (727 deg C) à laquelle se produit la transformation eutectoïde. A cette température, la perlite se transforme en austénite lors du chauffage et vice versa
- Température A2 - C'est ce qu'on appelle la température de Curie de la ferrite (768 deg C), où la ferrite ferromagnétique lors du chauffage se transforme en paramagnétique. A cette température aucun changement de microstructure n'est impliqué
- Température A3 - Il s'agit de la température à laquelle la ferrite commence juste à se former à partir de l'austénite, lors du refroidissement de l'acier hypo-eutectoïde ou des dernières traces de ferrite libre se transformant en austénite, lors du chauffage. Ainsi, il s'agit de la température correspondant à la limite de phase gamma + alpha / gamma pour l'acier hypo-eutectoïde et est fonction de la teneur en carbone de l'acier, car elle diminue de 910 deg C à 0 % C à 727 deg C à 0,76 % C Elle est aussi appelée température critique supérieure des aciers hypo-eutectoïdes. L'intervalle de température entre les températures A1 et A3 est appelé la plage critique dans laquelle l'austénite existe en équilibre avec la ferrite.
- Température Acm - C'est la température, dans un acier hyper-eutectoïde, à laquelle la cémentite pro-eutectoïde commence juste à se former (en refroidissant) à partir de l'austénite. Il représente la température de la limite de phase gamma/gamma + Fe3C et est fonction du carbone. La ligne Acm illustre que la solubilité solide du carbone dans l'austénite diminue très rapidement d'un maximum de 2,14 % à 1148 °C à un maximum de 0,76 % à 727 °C, en raison d'une plus grande stabilité de la cémentite à des températures plus basses. Le carbone supplémentaire précipite à partir de l'austénite sous forme de cémentite pro-eutectoïde dans les aciers hyper eutectoïdes (également appelée cémentite secondaire dans les fontes). La séparation de la cémentite de l'austénite (lors du refroidissement) s'accompagne également d'un dégagement de chaleur.
- Température A4 - C'est la température à laquelle l'austénite se transforme en fer delta. La valeur la plus basse pour cette température est de 1394 degrés Celsius, ce qui correspond au cas du fer pur. Cette température augmente à mesure que le pourcentage de carbone augmente.
- Température Ms - C'est la température à laquelle la transformation de l'austénite en martensite commence pendant le refroidissement.
- Température Mf - C'est la température à laquelle la formation de martensite se termine pendant le refroidissement. Tous les changements, à l'exception de la formation de martensite, se produisent à des températures plus basses pendant le refroidissement que pendant le chauffage et dépendent du taux de changement de température.
Transformation austénite-ferrite – Dans des conditions d'équilibre, la ferrite proeutectoïde se forme dans les alliages fer-carbone contenant jusqu'à 0,76 % de carbone. La réaction se produit à 910 degrés C dans le fer pur, mais a lieu entre 910 degrés C et 727 degrés C dans les alliages fer-carbone. Cependant, en passant de l'état austénitique à des températures inférieures à la température eutectoïde, la ferrite peut se former jusqu'à des températures aussi basses que 600 °C. et des phases hypereutectoïdes, bien que dans chaque cas il y ait des variations dues à la cristallographie précise des phases impliquées. Par exemple, les mêmes principes s'appliquent à la formation de cémentite à partir d'austénite, mais il n'est pas difficile de distinguer morphologiquement la ferrite de la cémentite.
Transformation austénite-cémentite – Il existe différentes morphologies de cémentite qui se forment à des températures de transformation de plus en plus basses. Le développement initial des allotriomorphes aux joints de grains est très similaire à celui de la ferrite et la croissance des plaques latérales ou de la cémentite de Widmanstatten suit le même schéma. L'allotriomorphe a une forme qui ne reflète pas sa symétrie cristalline interne. En effet, il a tendance à nucléer à la surface des grains d'austénite, formant ainsi des couches qui suivent les contours des joints de grains. Les plaques de cémentite ont une forme cristallographique plus rigoureuse, malgré le fait que la relation d'orientation avec l'austénite est plus complexe. Comme dans le cas de la ferrite, la plupart des plaques latérales proviennent d'allotriomorphes aux joints de grains, mais dans la réaction de la cémentite, davantage de plaques latérales nucléent aux joints jumeaux dans l'austénite.
Réaction austénite-perlite – La perlite est la microstructure la plus familière dans le diagramme de phase fer-carbone. Il a été découvert par Sorby il y a plus d'un siècle, qui a supposé à juste titre qu'il s'agissait d'un mélange lamellaire de fer et de carbure de fer. C'est un constituant très courant d'une grande variété d'aciers, où il apporte une contribution substantielle à la résistance. Les structures eutectoïdes lamellaires de ce type sont largement répandues dans la métallurgie des aciers. Ces structures ont beaucoup en commun avec les réactions de précipitation cellulaire. Les deux types de réaction se produisent par nucléation et croissance et sont donc contrôlés par diffusion. Les noyaux de perlite apparaissent sur les joints de grains d'austénite, mais il est clair qu'ils peuvent également être associés à la fois à la ferrite pro-eutectoïde et à la cémentite. Dans les aciers commerciaux, les nodules de perlite peuvent nucléer sur les inclusions.
Processus de fabrication
- Fer contre acier :quelle est la différence ?
- Que sont les métaux ferreux ? Obtenez les faits
- Fer à repasser
- Comment la 5G va orienter la prochaine phase de l'industrie 4.0
- Qu'est-ce que le diagramme de phase fer-carbone ?
- Comment choisir la bonne qualité de fonte ductile
- Les grandes entreprises de fonderie de fer
- Pourquoi la fonte grise est-elle le matériau de forgeage le plus populaire ?
- Les nombreux avantages de la fonte grise



