Introduction sélective d'impureté Cu dans du ZnS finement dispersé obtenu lors du processus de synthèse en une étape
Résumé
Le ZnS:Cu fin, obtenu par la méthode d'auto-propagation de la synthèse à haute température, a été étudié. Comme flux dans le mélange NaCl a été utilisé, Zn et S ont été pris dans le rapport stoechiométrique; La concentration en Cu en charge était d'environ 1,5 % en poids. À l'aide des données SEM, il a été établi que le ZnS:Cu obtenu se compose de deux fractions :la première avec des particules de taille ~10 μm et plus, et l'autre avec des tailles de 50 à 500 nm. Il a été établi que la composition des fractions ZnS:Cu était essentiellement différente. Selon les données de l'EDS, la concentration de Cu dans les particules d'une fraction de 50 à 500 nm est d'environ 2 % en poids, et dans les particules d'une taille d'environ 10 μm et plus, la présence de Cu n'a pas été détectée. Les raisons qui conduisent au dopage sélectif des particules en fonction de leur taille ainsi que le rôle du NaCl dans les processus en cours lors de la synthèse du matériau sont discutés.
Contexte
À l'heure actuelle, une attention considérable est consacrée au développement de différentes nouvelles méthodes technologiques de fabrication de structures semi-conductrices complexes. À cet égard, les recherches concernant l'optimisation des méthodes de synthèse de matériaux semi-conducteurs axées sur la fabrication de structures semi-conductrices de haute qualité (stœchiométriques, sans impuretés, etc.) ou complexes (solutions solides, matériaux nanostructurés) dans un cycle technologique sont particulièrement intéressantes. De telles investigations ont également une importance pour les connaissances fondamentales car elles permettent de mieux comprendre l'interconnexion entre la structure, la composition et les propriétés du matériau produit et les régimes technologiques de sa synthèse. Les études de régularité de l'interconnexion mentionnée ci-dessus sont importantes également en ce qui concerne les possibilités d'application, la compréhension des régularités dans la séquence «composition – structure – propriétés» permet de contrôler ou de modifier la structure et les propriétés des matériaux.
Une place particulière dans les enquêtes sur l'influence du régime de fabrication sur la structure et les propriétés des matériaux a le cas lorsque des agents de fusion sont utilisés dans la synthèse de matériaux. S'il est nécessaire d'obtenir la substance sous forme de cristaux bien formés, les fondants sont souvent utilisés comme minéralisateurs. C'est particulièrement utile dans les conditions de température élevée, lorsque la mobilité élevée des atomes qui forment le réseau peut conduire à la formation d'une grande quantité de défauts [1].
À cet égard, il est intéressant d'étudier les particularités de la possibilité de fabrication du ZnS obtenu par la méthode d'auto-propagation de la synthèse à haute température (SHS) en utilisant comme matériau de flux avec liaison ionique. Les possibilités technologiques SHS sont larges et permettent de réaliser le dopage du matériau par différents éléments et composés au cours du processus de synthèse. La variation des méthodes de processus de combustion dans l'onde SHS offre la possibilité de fabriquer un produit ciblé sous forme d'échantillon coulé avec des tailles prédéfinies ainsi que sous forme de poudre avec la dispersion de taille nécessaire.
Il faut noter que l'utilisation de fondants permet de contrôler la température du processus de combustion et de modifier les conditions de solubilité des dopants dans le matériau synthétisé. En particulier, pour fournir des conditions pour ce qu'on appelle la « solubilité rétrograde » [2], lorsqu'une impureté introduite n'entre que dans des zones particulières du matériau ou n'entre pas du tout. Une telle situation est réalisée lorsque le niveau de Fermi coupe le sommet de la bande d'états d'impuretés localisés.
La variation des méthodes de processus de combustion dans l'onde SHS offre la possibilité de fabriquer un produit ciblé sous forme d'échantillon coulé avec des tailles prédéfinies ainsi que sous forme de poudre avec la dispersion de taille nécessaire.
Ce phénomène sera plus prononcé dans les matériaux avec des bandes d'états d'impuretés localisées localisées à proximité maximale du niveau de Fermi. De tels matériaux s'équilibrent sur le bord de stabilité des complexes covalents du métal introduit et principal [3].
Ce travail a été consacré à la clarification de l'influence du NaCl introduit dans le mélange en tant qu'agent de fusion, sur la concentration de Cu dans des particules de ZnS:Cu finement dispersées de différentes tailles, obtenues par la méthode SHS [4, 5].
Méthodes
Dans le présent travail, des recherches sur le ZnS:Cu fin obtenu par la méthode SHS (ZnS:Cu–SHS) ont été effectuées. Pour la fabrication de ZnS:Cu–SHS, Zn et S ont été pris dans le rapport stoechiométrique. Le dopage par mélange de cuivre a été réalisé à partir de chlorure de cuivre CuCl directement pendant le processus de synthèse. La concentration de Cu en charge était d'environ 1,5 % en poids. ZnS:Cu a été obtenu à des températures qui ont fourni un processus d'interaction du soufre et du zinc. Une partie de la libération au cours de la réaction d'interaction de S et de Zn a été absorbée par le flux (NaCl), ce qui permet de diminuer la température de synthèse du matériau. La quantité de NaCl dans le mélange était de 5 % en poids.
Les spectres de photoluminescence (PL) et les spectres d'excitation luminescente (PLE) ont été enregistrés à température ambiante à l'aide d'une installation SDL-2. Pendant l'enregistrement PLE, l'excitation a été réalisée en utilisant le rayonnement d'une lampe au xénon et d'un monochromateur MDR-12.
Des études de morphologie et de taille des particules ont été réalisées à l'aide du microscope électronique à balayage JAMP-9500F (Jeol).
Les mesures de la composition des éléments des particules ont été effectuées en utilisant la méthode de spectroscopie à rayons X à dispersion d'énergie (EDS) et le spectromètre INCA PentaFETx3 (Oxford Instruments).
Résultats et discussion
Des images SEM typiques pour les fractions fines après rinçage à l'eau distillée sont présentées sur la Fig. 1. Comme le montrent les images SEM, la fraction fine synthétisée représente elle-même un mélange de particules de différentes tailles, dans lesquelles des nanoparticules sont présentes ainsi que des particules de tailles micro et submicroniques. .

Images SEM de ZnS:Cu fin, obtenues par la méthode SHS. un Vue générale. b Mélange de particules de différentes tailles
Sur la figure 2, les spectres PL et PLE de ZnS-SHS sont présentés. Comme le montre la figure 2, le spectre PL de ZnS-SHS représente lui-même une large bande avec un maximum dans la région de 505 à 525 nm. Il est bien connu que la bande PL de ZnS:Cu dans la région bleu-vert est complexe et, comme d'habitude, représente elle-même la superposition de plusieurs bandes, qui sont déterminées par le mélange de cuivre et aussi par les défauts intrinsèques du ZnS. La nature des centres de luminescence, qui déterminent les bandes bleues et vertes de Cu dans le ZnS, est décrite en détail dans [6,7,8]. Les auteurs de [6, 7, 9,10,11,12,13] ont montré, ce centre, qui est responsable de l'apparition de la bande verte de Cu avec λmax ~ 505÷530 nm, est un ion cuivre isolé, qui remplace l'ion zinc dans le réseau ZnS.
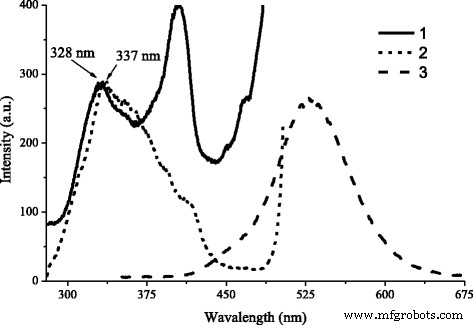
Spectres PLE de ZnS:Cu synthétisé par SHS, normalisés sur la bande d'absorption fondamentale d'intensité. 1 – initial ZnS:Cu – SHS, 2 – ZnS:Cu – SHS après lavage à l'eau distillée. 3 – Spectre PL de ZnS:Cu – SHS initial
Bande bleue avec λmax ~440÷465 nm se connectent avec la formation d'associés similaires au type de paire DA Cui -CuZn [6, 7, 13] ou CuZn - CuZn [11, 12]. Dans la région spectrale donnée, les bandes sont également présentes qui sont causées par les centres d'oxygène [6, 10, 14], et les bandes de rayonnement auto-activé de [6, 7, 11, 12].
Le PLE de ZnS:Cu–SHS (Fig. 2, courbe 1) comprend des bandes correspondant aux transitions d'excitation de bande à bande dans le ZnS en vrac et de taille quantique. Cela indique la présence dans le matériau de grosses particules avec des tailles supérieures à des centaines de nm et ainsi des particules avec des tailles inférieures à 5 nm (c'est-à-dire du rayon de l'exciton de Bohr dans le ZnS). D'après [14], Eg La valeur pour le ZnS est d'environ 3,65 eV, ce qui correspond à la bande d'absorption de 340 nm. Le décalage du maximum de la bande d'absorption fondamentale sur 10 nm, indique la présence dans la matière des particules de tailles correspondant à la manifestation de l'effet quantique [15].
Après lavage du matériau initial dans de l'eau distillée, le maximum d'absorption fondamentale s'est déplacé du côté des ondes longues (Fig. 2, courbe 2). Cela témoigne que le lavage à l'eau distillée a conduit non seulement à l'érosion du matériel de NaCl qui restait après la synthèse, mais aussi et des particules avec des tailles inférieures à 5 nm.
D'après les données de la microscopie électronique à balayage (voir Fig. 1), la majeure partie du matériau obtenu est constituée de deux fractions isolées. La première fraction est constituée de particules individuelles d'une taille d'environ 10 μm (Fig. 1a). La deuxième partie est représentée par des particules de tailles allant de quelques centaines de nanomètres à plusieurs microns (Fig. 1b).
Ainsi, la composition de charge choisie et les régimes de synthèse ont permis d'obtenir simultanément, c'est-à-dire au cours d'une synthèse, les particules de nano-, méso-et micro-taille.
Les enquêtes sur la composition des éléments par EDS ont montré que dans le ZnS:Cu obtenu dans différentes particules, la violation de la stoechiométrie peut aller jusqu'à 4 at. % (Tableau 1).
Dans le même temps, selon les données de ces investigations, la présence de dopant au cuivre dans les particules avec des tailles de l'ordre de centaines de nm est de l'ordre de ~ 2 % en poids (Figs. 3a, 2), et dans les grosses particules avec des tailles ~ 10 μm, la présence de Cu n'a pas été détectée (Figs. 3a, 1). Dans le tableau 1, la composition en éléments (en % at.) des particules dans les conglomérats et des grosses particules séparées illustrées à la figure 1a est présentée.
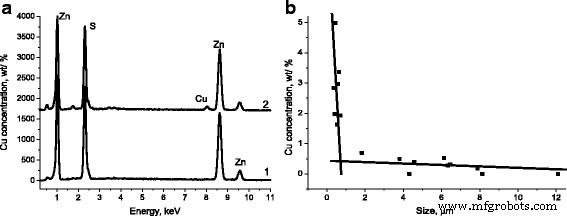
un Spectres EDS de particules ZnS-SHS avec des tailles :1–27 μm, 2–0,3 μm. b Concentration de Cu en fonction de la taille des particules de ZnS-SHS
Sur la figure 3b, la concentration en Cu en fonction de la taille des particules de ZnS-SHS est indiquée. Comme le montre la figure 3b pour les particules avec des tailles de ~ 300 à ~ 700 nm, une forte concentration de dopant au cuivre est observée, avec une valeur de ~ 5 % en poids pour des particules de 370 nm. Dans le même temps, pour les particules d'une taille comprise entre ~2 et 12 μm, la concentration en cuivre ne dépasse pas 0,7 % en poids, et dans certaines particules (de taille ~8 μm, ~12 μm), le dopant au cuivre n'est pas enregistré par la méthode EDS, c'est-à-dire qu'il est pratiquement absent. Il est nécessaire de noter ici que la concentration en cuivre en charge était d'environ 1,5 % en poids. Ainsi, comme en témoignent les données mentionnées ci-dessus, le dopage par le cuivre des particules de ZnS, qui se forment au cours du processus de synthèse, est réalisé de manière différente en fonction de leurs tailles.
Considérons les raisons qui peuvent expliquer un si faible niveau de dopage caractéristique pour les grosses particules (2÷12) et un niveau de dopage extrêmement élevé pour les petites (<2 μm) ZnS:Cu – particules SHS.
Dans notre cas, la formation de ZnS (matériaux avec liaison ion-covalente, pourcentage de liaison ionique ~40% [15]) est réalisée avec un voisinage immédiat avec NaCl (matériau ionique [16]. L'apparition de la phase ZnS pendant le processus de synthèse subit avec le dégagement de chaleur , qui dans son cas conduit à la décomposition du CuCl sur les composants et à la fusion du NaCl. Température de fusion du NaCl - 800 °C, température d'ébullition - 1465 °C [17]. La décomposition du CuCl sur les composants subit en raison d'une réaction de dismutation, ce qui conduit à la formation de CuCl2 avec dégagement de Cu à 500 °C [18], et à une augmentation de température supérieure à 500 °C, CuCl2 dans son cas est décomposé en CuCl et Cl avec volatilisation ultérieure de Cl. C'est-à-dire que la cristallisation du ZnS se produit à partir du mélange fondu de NaCl et de ZnS. De tels processus de type pendant le transport dans les systèmes solide-liquide sont appelés minéralisation [1, 19].
Ainsi, la formation de particules de ZnS de différentes tailles se déroule en parallèle. Les grosses particules de ZnS se forment dans la masse fondue ou dans le NaCl environnant. Le transport du cuivre à travers la phase liquide du NaCl est difficile en raison de sa faible solubilité [20], en plus de cela, la décomposition du CuCl ne se produit pas en une seule fois, et cela réduit également le taux d'introduction de Cu dans le ZnS.
La formation de particules de petite taille, très probablement, est réalisée en phase gazeuse de Zn et S. Dans ce cas, l'apparition de la phase CuS a une faible probabilité, car pour sa formation une plus grande quantité si de la chaleur est nécessaire [20]. Après formation, les petites particules sont au voisinage de Cu et de grosses particules de ZnS. Étant donné que la taille des petites particules devient proportionnelle à la taille de la région de charge d'espace (SCR) dans le ZnS, les particules se trouvent alors dans la région d'épuisement des porteurs de charge. Cela est dû au fait que lorsque la taille des particules diminue jusqu'à la valeur inférieure au double de la valeur de la profondeur de criblage (L ) l'imposition se produit de SCR localisée le long d'une surface de particule sur la SCR de la surface opposée. Le chevauchement mutuel des surfaces SCR entraîne une diminution de la largeur entre le niveau de Fermi E F et haut de la bande de valence E V [21]. Par conséquent, la concentration des principaux porteurs de charge dans les particules de taille r < 2 L s'avère faible, ou en d'autres termes, la particule s'avère dans la zone d'épuisement. Dans ce cas, comme mentionné dans [3], lorsque la bande d'impuretés est remplie à plus de la moitié de la transition de phase du premier ordre, accompagnée d'un changement brusque de la valeur du potentiel chimique et d'autres paramètres thermodynamiques du matériau, est thermodynamiquement favorable. Dans le cas contraire la transition s'accompagne de l'augmentation du niveau de Fermi lors du chauffage, ce qui correspond à l'entropie négative du processus, c'est-à-dire que la décomposition du matériau homogène doit être observée dans les régions enrichies en porteurs à une concentration assurant le remplissage de la bande d'impuretés pas moins de la moitié et sur les régions épuisées par les transporteurs. Autrement dit, l'abaissement du niveau de Fermi et son entrée dans la zone des niveaux d'impuretés entraînent leur vidange, c'est-à-dire thermodynamiquement défavorable au matériau. Par conséquent, l'introduction de cuivre comme impureté donneuse dans le ZnS, où le cuivre occupe une position interstitielle, devient thermodynamiquement favorable pour le matériau. Cela a peut-être conduit à une concentration aussi élevée de cuivre dans les particules de petite fraction. Aussi, pour une interprétation plus univoque des résultats obtenus, des investigations complémentaires sont nécessaires.
Ainsi, les résultats présentés montrent que la méthode SHS permet d'obtenir des matériaux avec des tailles de particules de ZnS dans une large gamme - de la taille micro à la taille nanométrique. Par ailleurs, le choix des régimes de synthèse, du matériau de fondant et de sa quantité en mélange permet de doper sélectivement les particules en fonction de leurs tailles.
Conclusions
Les investigations menées sur le ZnS:Cu obtenu par la méthode SHS avec ajout de NaCl en charge comme flux ont montré que l'introduction de NaCl permet d'augmenter la quantité de fraction fine (50-500 nm) dans le matériau. Les données EDS ont montré que la concentration de Cu dans les fractions est différente. La concentration de Cu dans les fractions avec des tailles de particules comprises entre 50 et 500 nm se compose d'environ 2 % en poids, et dans les particules d'une taille d'environ 10 μm et plus, la présence de Cu n'a pas été détectée. Ainsi, la sélection des régimes de synthèse, du matériau de flux et de sa quantité en charge permet lors de l'utilisation de la méthode SHS de réaliser un dopage sélectif des particules en fonction de leur taille. Les résultats obtenus sont bien expliqués dans le cadre du modèle d'impureté « solubilité rétrograde » dans les matériaux multi-composants.
Abréviations
- CuCl :
-
Chlorure de cuivre
- NaCl :
-
Chlorure de sodium
- SHS :
-
Synthèse autopropageante à haute température
- ZnS :
-
Cou ZnS dopé par Cu
- ZnS :
-
Cu–SHS -ZnS:Cu obtenu par la méthode SHS
- ZnS :
-
Sulfure de zinc
Nanomatériaux
- Une introduction aux parties d'un boulon
- Dans le domaine des usines de traitement avec Ethernet
- Une introduction au processus d'infusion de résine
- Comment fonctionne le processus CMC
- En quoi consiste le processus de fabrication ?
- Regard sur le processus d'évaluation des équipements d'occasion :comment cela fonctionne
- Qu'est-ce que le processus de fabrication du savon ?
- Introduction au procédé de moulage de précision en acier inoxydable
- Rationalisation du processus



