Détection de peroxyde d'hydrogène basée sur la modification des surfaces internes de nanopores à l'état solide
Résumé
Il existe de nombreuses techniques de détection de molécules. Mais la détection de molécules à travers des nanopores à l'état solide dans une solution est l'une des technologies prometteuses, à haut débit et à faible coût utilisées de nos jours. Dans la présente enquête, une plate-forme de nanopores à l'état solide a été fabriquée pour la détection du peroxyde d'hydrogène (H2 O2 ), qui n'est pas seulement un produit sans étiquette, mais aussi un participant important dans la réaction redox. Nous avons réussi à fabriquer du nitrure de silicium (Si3 N4 ) nanopores d'un diamètre d'environ 50 nm en utilisant un faisceau d'ions Ga focalisé, la surface interne du nanopore a été modifiée avec de la peroxydase de raifort (HRP) en utilisant la chimie de couplage carbodiimide. Les enzymes HRP immobilisées ont la capacité d'induire des réactions d'oxydoréduction dans un seul canal nanopore. De plus, un seul ABTS agrégé en temps réel •+ les événements de translocation moléculaire ont été surveillés et étudiés. Le biocapteur à nanopores à l'état solide conçu est réversible et peut être appliqué pour détecter H2 O2 plusieurs fois.
Contexte
La technologie de détection des nanopores provient du compteur Coulter [1] et du canal ionique cellulaire [2]. Nanopore détecte les molécules chargées présentes dans une solution qui la traverse. L'apparition des molécules dans le nanopore peut modifier la conductance du pore apparemment, par conséquent une modification du signal de courant. Le changement de courant fournit des informations sur les tailles et la concentration des molécules à l'intérieur du pore, pour révéler le processus dynamique des comportements de translocation des molécules [3]. Certains objets nanométriques peuvent être détectés à l'aide d'un nanopore, tels que les nanoparticules [4,5,6], les virus [7,8,9], les molécules de protéines [10,11,12,13] et les séquences d'ADN [14,15,16 ,17]. Les nanopores sont de deux types. Biologie nanopore et nanopore à l'état solide. Le nanopore biologique a un rapport signal sur bruit (SNR) plus faible et une résolution plus élevée. Les protéines petites et dépliées peuvent être détectées en utilisant des nanopores biologiques [18,19,20,21,22,23]. Le nanopore à l'état solide est de taille réglable et a une plus grande stabilité. Le nanopore à l'état solide est normalement percé sur un film, ce film divise la cellule fluidique en deux parties [24]. Une tension polarisée est appliquée à travers une fine membrane contenant un nanopore, entraînant un courant ionique d'une cellule à l'autre [25]. Les molécules de protéines, y compris les structures repliées et dépliées, sont détectées et analysées par des nanopores à l'état solide [26,27,28,29]. L'interaction des protéines peut également être détectée à l'aide de nanopores à l'état solide [30, 31]. De plus, il a la capacité de détecter la cinétique des protéines [32, 33]. Afin de résoudre les limites de la plage de détection, des nanopores à l'état solide modifiés chimiquement ont été largement appliqués [34,35,36,37,38,39], des nanopores à l'état solide modifiés chimiquement ont été appliqués pour détecter l'ADN simple brin [40] et des protéines [41].
De nombreuses méthodes quantitatives ont déjà été appliquées pour la détection de H2 O2 , la plupart d'entre eux sont basés sur la spectrométrie [42,43,44,45], la chimioluminescence [46,47,48,49], l'ampérométrie [50,51,52,53] et l'électrochimie [54,55,56,57] . Les méthodes conventionnelles de spectrométrie et de chimioluminescence sont généralement longues et coûteuses. Le capteur nanopore à l'état solide a une faible consommation et une structure simple, et peut être utilisé pour détecter de petites molécules.
Ici, nous présentons un type de nanopore à l'état solide qui a été modifié avec de la peroxydase de raifort (HRP). Les HRP ont été immobilisés sur la surface interne du nanopore à l'état solide, les HRP immobilisés sont restés actifs dans la réaction redox qui s'est produite à l'intérieur d'un seul canal de nanopore en présence de H2 O2 [58]. L'ABTS •+ produit dans la réaction d'oxydoréduction s'agrégerait, puis l'ABTS agrégé •+ passé à travers les nanopores. Les événements de translocation peuvent être détectés. Pour la détection du peroxyde d'hydrogène, la structure de l'état solide est simple, et il peut détecter l'ABTS agrégé •+ en utilisant une faible consommation de réactifs. Ce nanopore à l'état solide de modification des enzymes de la peroxydase de raifort (HRP) peut accomplir le peroxyde d'hydrogène (H2 O2 ) détectant indirectement, via l'ABTS agrégé •+ détection. Il a une signification instructive pour la détection de molécules uniques et l'assemblage de molécules nanopore interne à l'état solide.
Méthodes
Produits chimiques et matériaux
La molécule de peroxydase de raifort (HRP) (1mg mL -1 , Enzyme Commission n°.1.11.1.7, 44 kDa) a été acheté auprès de Xiya Reagent (Chengdu, Chine). L'échantillon (HRP) a été dissous dans du PBS 0,1 M filtré à 0,02 µm, stocké à 4 °C et utilisé dans les deux jours suivant la préparation. Chlorure de potassium (KCl), N-(3-diméthylaminopropyl)-N'-éthylcarbodiimide (EDC), N-hydroxysuccinimide (NHS) et 2,2'-Azino-bis (3-éthylbenzothiazoline-6-sulfonique acide) ((ABTS ), 98%) ont été achetés auprès de DiBo Chemical Technology co., LTD (Shanghai, Chine). Peroxyde d'hydrogène (H2 O2 , 30%) a été acheté chez Sinopharm Chemical Reagent Co., Ltd. Le (3-aminopropyl)triéthoxysilane (3-APTES) a été acheté chez Sigma-Aldrich (St. Louis, MO, USA). Les expériences ont été menées en utilisant de l'eau non piégée provenant d'un système de purification d'eau Milli-Q (résistivité de 18,2 MΩ/cm, 25 °C, Millipore Corporation, Billerica, MA, USA) et a été filtrée à travers 0,02 m dans un système FEI Strata 201 FIB (FEI Co., Hillsboro, OR, USA), un Zetasizer (Malvern Zetasizer Nano ZS) et un Axopatch 700B (Molecular Devices, Inc., Sunnyvale, CA, USA). Les photos de nos instruments d'occasion ont été ajoutées au matériel supplémentaire (voir Fichier supplémentaire 1 :Figure S1).
Fabrication de nanopores à l'état solide et mesures électriques
Tout d'abord, une fine membrane de Si3 N4 (100 nm d'épaisseur) a été déposé sur un substrat de Si de 300 µm d'épaisseur. Suivi par photolithographie (la taille de la fenêtre ouverte est de 500 × 500 m 2 ). Ensuite, la surface de la membrane a été bombardée d'ions Ga + en utilisant un système FEI Strata 201 FIB (FEI Co., Hillsboro, OR, USA) à un potentiel d'accélération de 30 kV, tandis que le courant était mesuré à 1 pA. Le temps de broyage était de 1,5 s en mode spot. Enfin, les puces de nanopores à l'état solide ont été obtenues et nettoyées dans une solution de piranha fraîchement préparée à 80 ° C pendant 30 min, suivies d'un rinçage à l'eau ultrapure. Après le nettoyage, la puce a été assemblée dans une cellule en téflon sur mesure avec deux joints toriques en Viton pour séparer les deux côtés de la puce et formant deux réservoirs pour assurer le seul chemin du courant ionique à travers le nanopore. Les photos de nos appareils d'occasion ont été ajoutées au matériel supplémentaire (voir Fichier supplémentaire 1 :Figure S2). Des électrodes (Ag/AgCl) ont été connectées à la cellule fluidique et à un amplificateur patch-clamp (Axopatch 700B, Molecular Devices, Inc., Sunnyvale, CA, USA) qui a rendu le courant ionique mesurable sous des tensions constantes, avec un taux d'échantillonnage de 100 kHz pour les signaux . Le filtre de Bessel interne passe-bas à huit pôles de l'amplificateur a été réglé à 10 kHz [3]. L'ensemble de l'instrument a été placé dans une double cage de Faraday.
Résultats et discussion
Immobilisation de Nanopore avec des HRP
Le nanopore sélectionné d'un diamètre d'environ 50 nm a été immergé dans une solution de piranha à 80 ° C pendant 30 min. Après traitement avec une solution de piranha, la surface interne du nanopore a pu prendre des groupes hydroxyle de silicium. Par la suite, la totalité du film mince a été activée avec du (3-aminopropyl)triéthoxysilane (3-APTES). À la suite du traitement avec 3-APTES, l'amino (-NH2 ) des groupes ont été générés à la surface du film.
Après activation au (3-Aminopropyl)triéthoxysilane (3-APTES), la puce nanopore a été amenée dans une solution PBS 0,1 M de N-(3-diméthylaminopropyl)-N'-éthylcarbodiimide (EDC) (10 mM) et de N-hydroxysuccinimide ( NHS) (20 mM). Par la suite, la puce nanopore a été introduite dans de la peroxydase de raifort (HRP) (10 ng/ml). Selon les résultats de recherche antérieurs de notre groupe [3], avec une concentration en sel différente de 0,1 à 2 M KCl, pH 7,0, la HRP ne s'est pas agrégée. En raison du pI la valeur de la peroxydase de raifort étant de 4,3 ± 0,2, nous avons également prouvé que la HRP ne s'agrégeait pas dans 0,1 M KCl pH 6,0 et pH 7,0. Le réactif EDC a activé les groupes carboxyle (-COOH) de HRP en un intermédiaire o-acylisourée hautement réactif. De plus, l'intermédiaire a ensuite été converti en un ester réactif à la succinimidylamine plus stable en présence de NHS [58]. Résultant, en couplage covalent de l'intermédiaire avec le (-NH2 ) générés sur les surfaces internes des nanopores pour former des liaisons amide stables (Fig. 1).
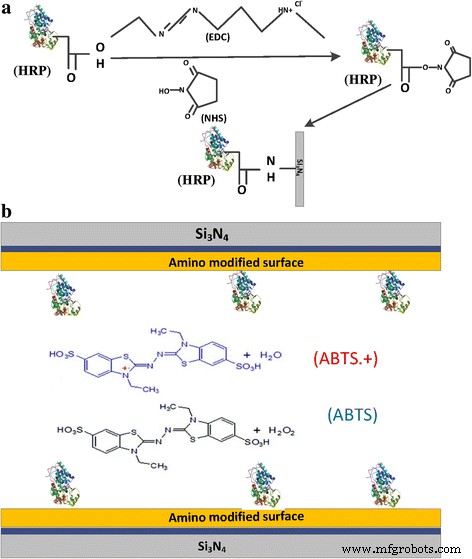
Exécution du processus de modification dans un seul canal nanopore à l'état solide. un Représentation schématique de l'attachement covalent de la peroxydase de raifort (HRP) à un seul canal nanopore via la chimie de couplage carbodiimide. Les groupes carboxyle (-COOH) de HRP ont été activés par une solution d'EDC, permettant au HRP de réagir avec (-NH2 ) généré à la surface d'une puce nanopore. b Schéma du capteur de peroxyde d'hydrogène HRP immobilisé, la surface interne du capteur a été modifiée avec des HRP. Quand H2 O2 et ABTS s'est produit, l'ABTS •+ produit. La structure cristalline de HRP a été utilisée avec la permission de l'auteur [3]
Ces processus nous conduisent vers l'immobilisation des HRP sur la surface interne d'un seul nanopore. La réalisation du processus de fonctionnalisation a été confirmée par la mesure du courant-tension (I-V ) d'un seul nanopore avant et après modification (Fig. 2).
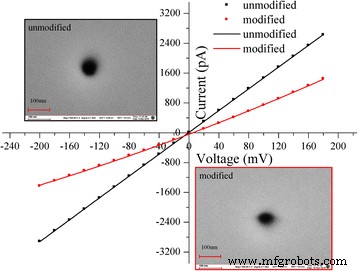
Exécution d'un courant-tension typique (I-V ) courbes du nanopore non modifié (original) et modifié dans 0,1 M de KCl, tamponné à pH 7,0 avec 0,1 M de PBS. La ligne noire est le I-V courbes de nanopore non modifié et ligne rouge est le I-V courbes de nanopore modifié avec des HRP. Les inserts sont la microscopie électronique à balayage (MEB) d'un seul nanopore (diamètre de ~ 50 nm cis) et le capteur nanopore. 100 nm est l'échelle
Caractérisation des nanopores à l'état solide modifiés par HRP
Ici, la forme d'un seul Si3 N4 le canal nanopore est cylindrique. La figure 2 montre le courant-tension typique (I-V ) courbes du nanopore non modifié (original) et modifié dans 0,1 M de KCl, tamponné à pH 7,0 avec 0,1 M de PBS. Après avoir modifié la surface interne du nanopore avec des enzymes HRP, la taille des pores est devenue plus petite.
Selon Wanunu et al, en tenant compte de la conductance externe du nanopore, le diamètre du nanopore à l'état solide peut être calculé par l'équation suivante,
$$ d=\left(1+\sqrt{1+\frac{16\sigma l}{\pi G}}\right) G/2\sigma $$ (1)Où, d et l sont le diamètre et la longueur des pores,G est la conductance à pores ouverts du nanopore, σ est la conductivité de la solution ionique.
Compte tenu des effets géométriques, après la modification du nanopore à l'état solide avec des enzymes HRP, la taille effective peut être calculée. Le diamètre d'un seul nanopore peut être calculé sur la base de l'équation (1). Où, la valeur de la conductance (G non modifié ) est ~15 nS peut être obtenu à partir de I-V courbes du nanopore à l'état solide non modifié. La conductivité (σ ) d'une solution d'ions 0,1 M KCl (25 °C), tamponnée à pH 7,0 avec 0,1 M de PBS est d'environ 1,28 S/m. Par conséquent, le diamètre du nanopore non modifié est d'environ 51 nm, il est similaire au diamètre mesuré. En utilisant la même méthode, la valeur obtenue de la conductance (G modifié ) est d'environ 7,5 nS et le diamètre (environ 34 nm) du nanopore modifié peut être calculé. La réduction du diamètre est possible pour les deux raisons suivantes, la première consiste à traiter la surface interne du nanopore avec du (3-aminopropyl)triéthoxysilane (3-APTES), permettant à la surface du nanopore de prendre (-NH2 ) groupes aminés. La deuxième raison est que le diamètre hydrodynamique (D h ) de l'enzyme HRP est d'environ 8 nm [3], les HRP immobilisées pourraient réduire le diamètre des pores. Ici, le nanopore à l'état solide modifié par HRP d'un diamètre d'environ 34 nm est utilisé comme canal de détection du peroxyde d'hydrogène.
Le principe de la réaction redox
La réaction d'oxydoréduction a été menée à l'intérieur d'un seul nanopore modifié, et le processus de réaction présenté suivant est bien en accord avec la réaction d'oxydoréduction proposée [58]. En présence de H2 O2 (0,5 mM), les enzymes HRP immobilisées sur la surface interne du nanopore ont été immédiatement converties en composé 1. Ensuite, le composé 1 a accepté un électron de la molécule de substrat réductrice ABTS (1,5 mM) pour générer le composé 2. Par la suite, le composé 2 a été ramené à l'enzyme au repos via un transfert d'électron d'une autre molécule de substrat ABTS.
Les produits cationiques (ABTS •+ ) des réactions redox se sont accumulées dans un seul nanopore. La translocation des molécules accumulées du canal nanopore modifierait la conductance (G ), et donc le changement de courant (ΔI b ) peut être trouvé.
$$ \mathrm{H}\mathrm{R}\mathrm{P}\left({\mathrm{Fe}}^{3+}\right)\mathrm{Porp} + {\mathrm{H}}_2{ \mathrm{O}}_2\à \mathrm{H}\mathrm{R}\mathrm{P}\left({\mathrm{Fe}}^{4+}=\mathrm{O}\right){\ mathrm{Porp}}^{\cdotp +}\left(\mathrm{Compound}\ 1\right) + {\mathrm{H}}_2\mathrm{O} $$ $$ \mathrm{H}\mathrm{ R}\mathrm{P}\left({\mathrm{Fe}}^{4+}=\mathrm{O}\right){\mathrm{Porp}}^{\cdotp +} + \mathrm{ABTS} \to \mathrm{H}\mathrm{R}\mathrm{P}\left({\mathrm{Fe}}^{4+}=\mathrm{O}\right)\mathrm{Porp}\left(\ mathrm{Composé}\ 2\right) + {\mathrm{ABTS}}^{\cdotp +} $$ $$ \mathrm{H}\mathrm{R}\mathrm{P}\left({\mathrm{Fe }}^{4+}=\mathrm{O}\right)\mathrm{Porp} + \mathrm{ABTS}\to \mathrm{H}\mathrm{R}\mathrm{P}\left({\mathrm {Fe}}^{3+}\right)\mathrm{Porp} + {\mathrm{ABTS}}^{\cdotp +} + {\mathrm{H}}_2\mathrm{O} $$Détection des événements de translocation
Des expériences ont été réalisées en utilisant des nanopores modifiés à la peroxydase de raifort (HRP) avec des diamètres de pores modifiés (~ 34 nm) dans 0,1 M de KCl, tamponnés à pH 7,0 avec 0,1 M de PBS. 2, 2'-Azinobis-(3-éthylbenzthiazoline-6-sulfonate (ABTS) (1,5 mM) et peroxyde d'hydrogène (H2 O2 ) (0,5 mM) ont été ajoutés au compartiment trans du nanopore. Après avoir ajouté ABTS et H2 O2 , les expériences utilisant des tensions polarisées de -100 à -800 mV ont été réalisées, et elles ont été échantillonnées à 100 kHz. Il n'y a eu aucun événement de translocation jusqu'à ce que la tension augmente à -400 mV. La figure 3 montre des traces de courant ionique représentatives de l'événement de translocation à différentes tensions de -400 à -800 mV dans 0,1 M KCl, 0,1 M PBS, pH 7,0. Les données d'expériences d'événements de translocation de longue durée de différentes tensions ont été ajoutées au matériel supplémentaire (voir Fichier supplémentaire 1 :Figure S3).
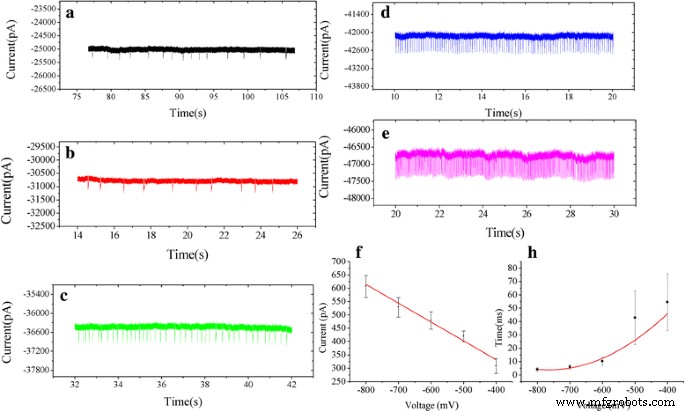
un –e Représentation schématique des événements de translocation à différentes tensions de -400 à -800 mV. La fréquence des événements de translocation augmentait lorsque la tension appliquée passait de -400 mV à -800 mV. f L'amplitude du courant augmente linéairement avec la tension. h Une fonction en décroissance exponentielle (t d ~ e −v/v0 ) a été utilisé pour ajuster le temps de maintien en fonction des tensions appliquées
Les événements de blocage de courant en millisecondes ont été observés, conduits dans 0,1 M de KCl, 0,1 M de PBS, pH 7,0. En ajoutant le réactif H2 O2 et ABTS dans le transcompartiment, les enzymes HRP immobilisées sur la surface interne du canal nanopore unique et une réaction redox s'est produite. Abondance d'ABTS •+ molécules ont été produites, une seule molécule plus petite ABTS •+ peuvent ne pas être détectés à l'aide de notre nanopore à l'état solide, en raison de la résolution du système [3]. Cependant, ces molécules s'agrégeraient après leur production. Par conséquent, il est possible de détecter l'ABTS •+ molécules. Ici, les tensions négatives ont été maintenues et agrégées ABTS •+ molécules ont traversé les nanopores. Il y avait un flux électrophorétique et électroosmotique lorsqu'une tension négative était appliquée. La HRP était chargée négativement dans 0,1 M de KCl, 0,1 M de PBS, pH 7,0 [3], en conséquence, une double couche électrique serait produite et l'électroosmose se ferait dans le sens de l'électrode négative. Pour cette raison, l'électrophorèse et l'électroosmose allaient dans le même sens. L'ABTS agrégé •+ dans le canal nanopore unique transporterait à travers le nanopore à l'état solide, s'écoulerait vers la direction de l'électrode négative.
Analyse statistique des événements de translocation
Étant donné que la tension polarisée a joué un rôle clé dans la translocation des ABTS agrégés •+ , l'influence des blocages actuels des ABTS agrégés •+ le passage à travers les nanopores modifiés par les HRP par rapport aux tensions appliquées a été discuté. La fréquence d'occurrence des événements de translocation a été grandement améliorée avec l'augmentation de la tension (Fig. 3f). Au fur et à mesure que la tension augmente, l'amplitude du courant augmente également. Cependant, les événements de translocation ont progressivement disparu lorsque la tension de polarisation a été maintenue en dessous de -300 mV, ce qui a suggéré que l'ABTS agrégé •+ à travers les nanopores modifiés HRP, il fallait une tension de seuil de -300 mV. La figure 4 montre des histogrammes de l'amplitude actuelle moyenne des événements de translocation mesurés pour l'ABTS agrégé •+ à des tensions différentes. Sur la base des courbes d'ajustement, les valeurs de crête du blocage actuel (ΔI b ) sont de 308,4 ± 27,795 pA, 419,1 ± 20,354 pA, 478,8 ± 32,857 pA, 528,1 ± 36,98 pA, 606,9 ± 40,916 pA à -400, -500, -600, -700 et -800 mV, respectivement, il est probable que la réduction de courant est induite par des ABTS agrégés •+ molécule traversant le nanopore à différentes tensions. Les valeurs de l'amplitude du courant ont été ajustées avec une fonction polynomiale du premier ordre, qui produit une pente de -0,706 et une interception de 49,262. Cependant, sur la base des courbes d'ajustement, les valeurs du temps de maintien sont de 54,5 ± 21,374 ms, 42,8 ± 20,181 ms, 10,3 ± 3,05 ms, 6,0 ± 1,744 ms, 4,0 ± 1,441 ms, à -400, -500, -600, - 700 et -800 mV. La figure 3h montre une fonction en décroissance exponentielle (t d ~ e −v/v0 ) a été utilisé pour ajuster le temps de maintien en fonction des tensions appliquées. Les histogrammes du temps de séjour des événements de translocation ont été ajoutés au matériel supplémentaire (voir Fichier supplémentaire 1 :Figure S4).
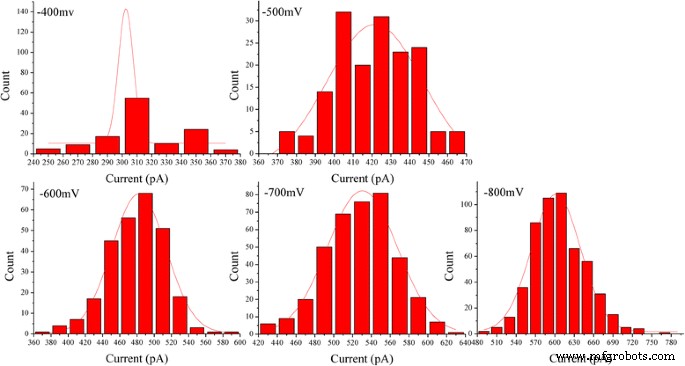
Les histogrammes de l'amplitude moyenne actuelle des événements de translocation mesurés pour l'ABTS agrégé •+ à différentes tensions (-400, -500, -600, -700, -800 mV) dans 0,1 M KCl, 0,1 M PBS, pH 7,0. Tous les histogrammes ont été ajustés avec une distribution gaussienne
Le blocus actuel par rapport au temps de séjour des événements pour chaque ABTS agrégé •+ à différentes tensions ont été installés dans des diagrammes de dispersion à deux dimensions (Fig. 5). Tous les ABTS agrégés •+ montrent un groupe d'événements de -400 à -800 mV, les principaux groupes d'événements sont dus à l'ABTS agrégé •+ passant à travers les nanopores à l'état solide modifiés par HRP.
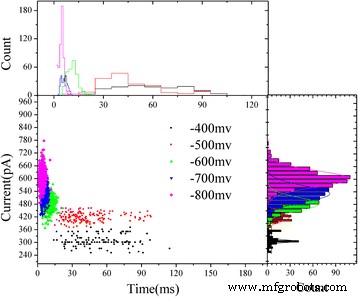
Diagrammes de dispersion bidimensionnels du blocage actuel par rapport au temps de séjour des événements pour chaque ABTS agrégé •+ à des tensions différentes. Ses histogrammes correspondants sont placés à droite et au-dessus. Tous les histogrammes ont été ajustés avec une distribution gaussienne
De plus, l'événement de translocation unique à chaque tension a été analysé et le blocage du courant a été induit par la même taille et la même substance chargée. Ainsi, il est considéré que chaque événement de translocation a été induit par le seul ABTS agrégé •+ . Pour analyser le temps de translocation des ABTS agrégés •+ dans nos expériences. La durée actuelle du blocus t d est considéré comme le temps de séjour d'un seul ABTS agrégé •+ de l'endroit où il s'est produit jusqu'à la sortie du nanopore. Ici, une autre condition a été envisagée, il peut y avoir des enzymes HRP immobilisées à l'entrée du nanopore, et cela pourrait catalyser la réaction redox. Par conséquent, d'autres expériences ont été menées pour vérifier que la réaction redox se produisait à la surface interne d'un seul nanopore plutôt qu'à l'entrée. Pour la vérification, des éléments non modifiés par les HRP ont été appliqués et analysés. Ces nanopores ont été activés avec du 3-APTES. Et la même concentration HRP (10 ng/ml), ABTS (1,5 mM) et H2 O2 (0,5 mM) ont été ajoutés au compartiment trans du nanopore, la tension de polarisation négative a été appliquée dans 0,1 M de KCl, 0,1 M de PBS, pH 7,0, en raison de la force d'électrophorèse, les HRP n'ont pas pu traverser le nanopore. En raison de la réaction redox, l'ABTS •+ agrégé produit, mais aucun événement de translocation n'a été trouvé. Il est possible que l'ABTS agrégé •+ provoquer un effet électrostatique avec les HRP et empêcher l'ABTS •+ agrégé passant à travers le nanopore.
La figure 6 montre les diagrammes de dispersion bidimensionnels du changement de conductance (ΔG ) par rapport au temps de séjour des événements pour chaque ABTS agrégé •+ à des tensions différentes. On peut constater que le changement de conductance (ΔG ) principalement concentré dans 0,8 nS. La forme des événements de translocation est presque la même. La valeur moyenne de ΔG est de ~0,8 nS à différentes tensions. On peut supposer que l'exclusion de volume de chaque ABTS agrégé •+ molécule est presque la même. Il est possible que les effets électrostatiques et stériques des ABTS agrégés •+ les molécules peuvent modifier le courant ionique. Après l'analyse, deux formes typiques de traces de courant avec l'ABTS agrégé chargé positivement •+ des translocations ont été observées (Fig. 7). Les événements de translocation à -700 mV en tant que représentant. Le pourcentage d'événements de deux types a été analysé, et on peut observer que le pourcentage d'événements de type 1 augmentait avec l'augmentation de la tension, en revanche, le pourcentage d'événements de type 2 diminuait. Il a été considéré qu'une tension plus élevée rend la translocation plus rapide que la tension inférieure.
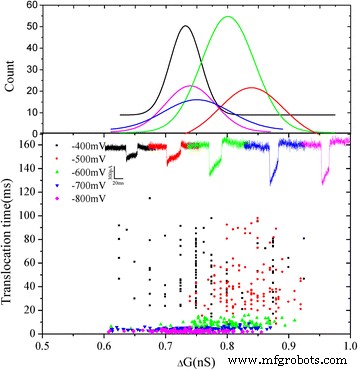
Représentation schématique des nuages de points à deux dimensions de ΔG par rapport au temps de séjour des événements pour chaque ABTS agrégé •+ à des tensions différentes. Les courbes d'ajustement correspondantes ont été positionnées ci-dessus. L'encart est les événements de translocation de différentes tensions (de -400 à -800 mV)
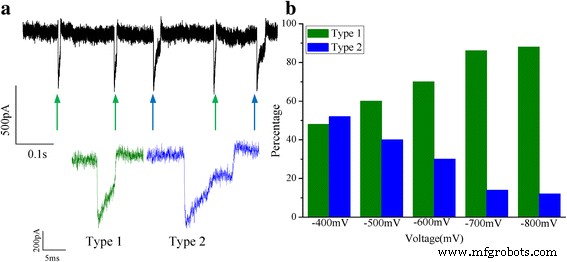
un Schéma de deux événements de translocation de type à une tension de -700 mV. b Le pourcentage d'événements de deux types à des tensions différentes (-400, -500, -600, -700, -800 mV)
Les signaux de blocage actuels ont révélé la taille, la conformation et l'interaction des ABTS agrégés •+ traversant le canal nanopore unique. Pour le changement de forme actuelle, le processus des changements a été spéculé. Pour l'événement 1, les signaux de courant ont une partie de fluctuation typique avec une intensité profonde et un temps de séjour court. Il est possible que l'ABTS agrégé •+ traversé le nanopore depuis l'endroit où il est produit. Lorsque l'ABTS agrégé •+ passé à travers le nanopore, le courant ionique du nanopore restauré au niveau d'origine (Référence) (I 0 ). Pour l'événement 2, les signaux de courant ont une partie fluctuante avec une intensité profonde puis ont un étage horizontal. Cette forme de signaux peut être attribuée à l'interaction électrostatique des ABTS agrégés •+ avec les HRP à la sortie du nanopore, et le courant a été lentement récupéré jusqu'à la ligne de base. Pour une meilleure compréhension du changement actuel, nous devons commencer par le changement de conductance à pores ouverts (G pores ) à concentration saline (0,1 M KCl). Comme discuté dans les études précédentes, une équation de la conductance à pores ouverts d'un nanopore chargé négativement avec un diamètre de d et une longueur de l à faible concentration en sel peut être décrit comme
$$ {G}_{p ore}=\frac{\pi {d^2}_{p ore}}{4{l}_{p ore}}\left[\left({\mu}_{ K^{+}}+{\mu}_{C{ l}^{-}}\right){n}_{K Cl}\cdot e+{\mu}_K\frac{4{\sigma}_p }{d_{p ore}}\right] $$ (2)où μ K et μ Cl sont les motilités électrophorétiques de K + et Cl − , n KCl est la densité numérique de K + et Cl − , la charge élémentaire est e, σ p est la densité de charge de surface des surfaces des nanopores. Dans cette expérience, le nanopore à l'état solide a été modifié chimiquement et le diamètre du nanopore a été modifié. La densité de charge de surface de la surface des nanopores (σ p ) ne peut pas être obtenu exactement. Par conséquent, la conductance à pores ouverts (G pores ) a été calculé sur la base de l'équation (1). En raison de l'équation (1), la conductance à pores ouverts (G pores ) est d'environ 7,5 nS. On suppose que le changement de conductance peut être attribué à deux raisons [15]. La première raison est que l'exclusion volumique des ions dans les nanopores était occupée par les ABTS agrégés •+ molécules. En conséquence, la conductance des nanopores à l'état solide a été diminuée (ΔG - ). La deuxième raison est que certains ions ont été apportés du nanopore par l'ABTS •+ agrégé molécules qui ont augmenté la conductance des nanopores à l'état solide. Dans ces expériences, l'ABTS •+ produit à l'intérieur du nanopore, et aucun ion n'a été apporté. Par conséquent, le changement de la conductance des nanopores à l'état solide (ΔG ) n'a été induite que par l'exclusion volumique. Ainsi, le changement total de la conductance peut être décrit comme
$$ \varDelta G=\varDelta {G}^{-} $$ (3)La diminution de la conductance des nanopores à l'état solide est induite par l'exclusion volumique et peut être calculée par l'équation suivante
$$ \varDelta {G}^{-}=\sigma \frac{\gamma \varLambda}{{\left( l+0.8 d\right)}^2} $$ (4)où γ est le facteur de forme des particules qui est le rapport des surfaces du même volume sphérique et de la particule. Dans ce travail, l'ABTS agrégé •+ molécule a été simplifiée en un objet global, donc la valeur de γ est 1 et Λ est l'exclusion de volume. La conductivité de la solution en vrac σ est de 1,28 S/m, 0,1 M de KCl (25 °C).
Pour l'exclusion de volume (Λ ), on peut déduire des événements de translocation de certaines autres molécules. Pour connecter le changement de conductance (ΔG ) à la propriété physique des molécules, la loi d'Ohm peut être appliquée au changement de volume de la solution électrolytique basée sur le nanopore à l'état solide [59]. Lors d'un événement de translocation d'une molécule dans un nanopore cylindrique à l'état solide, le courant diminue instantanément. Lorsque la résistance du nanopore à l'état solide est la résistance du circuit entier, la conductance change (ΔG ) peut être décrit par l'équation suivante
$$ \varDelta G(t)=-{G}_{p ore}\frac{\varLambda (t)}{H_{eff}{A}_p}\left[1+ f\left({d}_m /{D}_p,{l}_m/{H}_{eff}\right)\right] $$ (5)Dans cette équation, A p H eff = V p est le volume du nanopore à l'état solide, f (d m /D p , lm/H eff ) est le facteur de correction (il a ignoré l'effet de charge de surface), dans nos expériences, nous avons simplifié l'ABTS agrégé •+ molécule à un objet global; par conséquent, le facteur de correction est 1. Le d m /D p est le rapport du diamètre de la molécule et du diamètre des nanopores, le lm/H eff est le rapport de la longueur efficace de la molécule et de la longueur efficace du naopore. L'expression (5) peut être simplifiée comme
$$ \varDelta G/{G}_{p ore}\approx \varLambda /{V}_p $$ (6)La valeur moyenne de la conductance (G pores ) a été analysée des événements de translocation. A partir de l'équation (5), la valeur moyenne de l'exclusion de volume (Λ ) à différentes tensions (-400, -500, -600, -700, -800 mV) peuvent être obtenues. Pendant ce temps, la taille du nanopore utilisé est connue, le volume de nanopore (V p ) est de ~90746 nm 3 . En raison de l'équation (4), la valeur de la conductance change (ΔG - ) peut être calculé comme ~0,6 nS. La valeur moyenne du changement de conductance obtenue à partir des expériences d'événements de translocation à différentes tensions (-400, -500, -600, -700, -800 mV) est d'environ 0,784 nS. On constate que la valeur calculée est proche de la valeur expérimentale.
Dans certaines recherches antérieures, des molécules de peroxyde d'hydrogène ont été obtenues pour être détectées avec différentes technologies. Mais, détecter le peroxyde d'hydrogène par nanocanal est rare. Tan et al. [3] ont différencié des signaux d'événements disparates lorsque les HRP se sont enfilés dans des nanopores, il y avait des ABTS et des H2 O2 en solution de KCl. Les différents types de signaux avec translocation HRP ont été considérés comme ABTS •+ passant à travers les nanopores. Six événements typiques de la translocation du produit des substrats de catalyse enzymatique ont été analysés. Ils ont spéculé sur le processus probable de chaque type. Cependant, pas assez de preuves pour en témoigner. Moubarak Ali et al. have accomplished to detect the redox reaction products inner single conical nanochannels [58]. They found that the cationic radical ABTS •+ reduced the ion current in the HRP-nanochannel in a voltage-dependent fashion, consistent with voltage-dependent concentrations of ions in conical nanochannels. The magnitude of the current blockage was correlated with the H2 O2 concentration in the solution.
Conclusions
In conclusion, we fabricated a Si3 N4 nanopore employing a FIB successfully, a single naonopore system whose surface was modified with covalently linked HRP enzymes. The effect of the immobilized HRPs enzymes in a single solid-state nanopore as a hydrogen peroxide (H2 O2 ) sensor was affirmed by investigating products (ABTS •+ ) of the redox reactions occurring in presence of the substrates H2 O2 and ABTS. The aggregated cationic radical ABTS •+ produced inside the solid-state nanopore and reduced the ionic current in the HRPs modified solid-state nanopore, are consistent with voltage-dependence. The current blockade trends showed linear dependence for applied biased voltages. The relationship between the dwell time versus applied biased voltage was the exponentially decaying (t d ~ e −v/v0 ). Meanwhile, the aggregated ABTS •+ passed through the HRPs modified nanopores needed a −300 mV threshold voltage. The change of conductance (ΔG) has been calculated analytically and compared to the measured experimental values. The translocation events were produced by the certain size aggregated cationic radical ABTS •+ . We expect that using solid-state nanopores will allow lowering the detection limit and improve the system sensitivity. For our solid-state nanopore system, the structure is simple; it is not susceptible to fouling and can be used multiple times.
Abréviations
- 3-APTES:
-
(3-Aminopropyl)triethoxysilane
- ABTS:
-
3-ethylbenzothiazoline-6-sulfonic acid
- EDC :
-
N-(3-dimethylaminopropyl)-N’-ethylcarbodiimide
- FIB:
-
Focused ion beam
- HRP:
-
Horseradish peroxidase
- KCl:
-
Potassium chloride
- NHS:
-
N-hydroxysuccinimide
- SEM :
-
Microscopie électronique à balayage
- SNR:
-
Signal to noise ratio
Nanomatériaux
- Le LiDAR à semi-conducteurs offre une solution de détection automobile plus simple
- Nanosilicium pour produire de l'hydrogène
- Les nanocristaux semi-conducteurs aident à produire de l'hydrogène comme carburant
- Nano graphème, mémoire transparente flexible à base de silicium
- Nanodots de carbone comme nanocapteurs bimode pour la détection sélective du peroxyde d'hydrogène
- Détection de peroxyde d'hydrogène basée sur la modification des surfaces internes de nanopores à l'état solide
- Capteur plasmonique basé sur des nanoprismes diélectriques
- Estimation du stockage d'énergie d'un supercondensateur basée sur des équations différentielles fractionnaires
- Ambarella, Lumentum et ON Semiconductor collaborent sur la détection 3D basée sur le traitement de l'IA pour les appareils AIoT de nouvelle génération



