Contrôle de l'agrégation par des dérivés poly(N-vinylamide) réactifs à plusieurs stimuli dans un système aqueux
Résumé
Copolymère thermique et photosensible à base de N -Le squelette vinylamide a été conçu. Le groupe méthoxyéthyle et l'azobenzène ont été sélectionnés pour améliorer respectivement l'hydrophilie et les fractions photosensibles. Le N -(méthoxyéthyle)-N -vinylformamide a été synthétisé et copolymérisé avec N -vinylformamide par polymérisation radicalaire. Afin de contrôler les structures nanométriques, poly(N -vinylformamide) dérivés portant de l'azobenzène au niveau N -position proche de la chaîne principale du polymère vinylique ont été synthétisés par réaction polymère avec le poly(N -vinylformamide-co -N -(méthoxyéthyle)-N -vinylformamide) et azobenzène. La taille d'agrégation du polymère multi-stimuli a été contrôlée par la préparation de l'interaction hydrophobe à environ N -position.
Contexte
Dans le développement de matériaux polymères, l'ajout d'un comportement multi-stimuli-réactif est impératif [1,2,3], par exemple, thermo-redox [4], thermo-sel [5], thermo-pH [6,7 ,8] entre autres [9, 10]. Le comportement à température critique inférieure de la solution (LCST) est l'une des propriétés thermosensibles qui a été étudiée de manière intensive [11,12,13,14,15,16]. De plus, certains chercheurs ont rapporté que des polymères multi-stimulants étaient synthétisés à partir de polymères thermosensibles et de composés photosensibles, par exemple, des dérivés d'azobenzène en tant que composés photosensibles [17,18,19,20,21,22]. Parmi ceux-ci, une agrégation contrôlée des polymères dans l'eau a été réalisée [23,24,25,26,27,28]. Par exemple, des inclusions moléculaires contrôlées par reconnaissance supermoléculaire et libération contrôlée de médicaments ont été étudiées à l'aide de polymères multi-stimuli [29]. A travers ces exemples, le contrôle de l'agrégation dans l'eau est souhaitable et doit être mieux compris.
En revanche, poly(N -vinylamide) ont été étudiés depuis le développement de la nouvelle voie de synthèse de poly(N -vinylacétamide) (PNVA) a été rapportée [30] De plus, des voies de synthèse plus simples vers les monomères ont été développées [31]. Poly(N -vinylamide) ont plusieurs propriétés intéressantes. Par exemple, le PNVA est un polymère amphiphile [32], poly(N -vinylisobutylamide) (PNVIBA) est un polymère thermosensible [33], et poly(N -vinylformamide) (PNVF) est un précurseur de polycation. De plus, le PNVF peut être hydrolysé dans des conditions alcalines et converti en poly(N cationique -vinylamine) sans libérer d'amine toxique de bas poids moléculaire [34]. De plus, poly(N -vinylamide) étaient stables pendant une longue période vis-à-vis des UV irradiés [35]. Cela motive cette recherche à utiliser ces polymères pour une éventuelle application en tant que matériaux photosensibles. Cependant, la recherche en poly(N -vinylamide) fait défaut par rapport aux dérivés de poly(acrylamide) qui sont des isomères de structure de poly(N -vinylamide) [36, 37]. C'est parce que N -les dérivés de vinylamide sont des monomères de faible réactivité tels que le monomère vinylique non conjugué [38].
Dans cette étude, nous avons synthétisé le monomère de N -dérivés de vinylamide portant un groupe méthoxyéthyle en N -position de NVF (MOENVF :M w = 129) afin d'améliorer l'hydrophilie à la place des substituants alkyles hydrophobes [39]. Dans le travail précédent, nous avons montré la longueur et les isomères de structure des substituants alkyle au N -position de N -les copolymères vinylamides, conduisant à diverses LCST. Poly(NVF-co -MOENVF) (1 ) a été synthétisé par polymérisation radicalaire, donnant un polymère hydrophile (Fig. 1). Quand 1 avaient des unités hydrophobes photosensibles, telles que N -vinylformamide portant des dérivés d'azobenzène au niveau N -position (NVFazo), où le M w de l'unité monomère est 295, 1 est devenu un polymère amphipathique photosensible et thermosensible en fonction de son hydrophobie. Ensuite, poly(NVF-co -MOENVF-co -NVFazo) (2 ) a été synthétisé par réaction polymère (Fig. 1). En utilisant les copolymères, des nanoparticules à base de poly(N -vinylamide)s ont été préparés, et les agrégats ont été contrôlés par la température et l'irradiation UV.
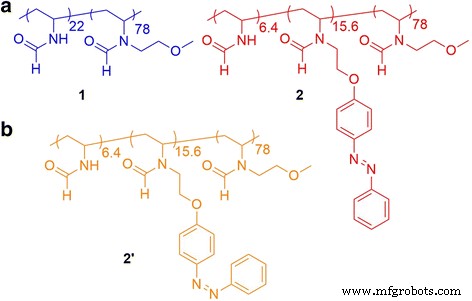
Structures chimiques de 1 (un ) et 2 et 2' (b )
Méthodes
Matériaux
N Le -vinylformamide (NVF) a été acheté auprès de Tokyo Chemical Industry Co., Ltd. (Japon) et a été distillé. L'hydrure de sodium (NaH) 60 % dans l'huile, le 2-bromoéthylméthyléther, le 1,2-dibromoéthane et le 4-(phénylazo)phénol et le tétrahydrofurane (THF) anhydre ont été achetés auprès de Tokyo Chemical Industry Co., Ltd. (Japon) et utilisé tel que reçu. N,N anhydre -diméthylformamide (DMF), acétone, toluène, acétate d'éthyle et sulfate de magnésium ont été achetés auprès de NACALAI TESQUE, INC. (Japon). L'azobisisobutyronitrile (AIBN) et l'hexane ont été achetés auprès de Wako Pure Chemical Industries Ltd. (Japon). L'éther diéthylique a été acheté auprès d'AZBIO CORP. (Japon).
Polymérisation
Le mode opératoire de la copolymérisation radicalaire typique du MOENVF et du NVF était le suivant. MOENVF (1,03 g, 8 mmol), NVF (0,14 g, 2 mmol), toluène (5 ml) et AIBN (0,044 g, 0,25 mmol) ont été combinés dans un réservoir en verre de 50 ml. Le réacteur était coiffé de septa; puis, N2 le bullage a été effectué pendant 2 min. Le mélange réactionnel a été chauffé jusqu'à 60 °C pour démarrer la polymérisation. Après 24 h, il a été refroidi à température ambiante et le mélange réactionnel a été versé dans 500 ml d'éther diéthylique. Le polymère a été lavé deux fois par de l'éther diéthylique et récupéré par centrifugation. Le polymère poly(NVF-co -MOENVF) a été obtenu (0,69 g, rendement 59 %) après séchage sous vide à 30 °C pendant 12 h.
Le poly(NVF-co -MOENVF) (0,20 g, solide) et NaH (0,4 mmol, 0,011 g, solide) ont été combinés dans un réservoir en verre de 50 ml. Le réacteur était coiffé de septa; puis, N2 a été infusé après quoi, du DMF (1 ml) a été lentement ajouté à l'aide d'une seringue à 100 °C. Après agitation pendant 15 min à 100 °C, du 1-bromoéther azobenzène (0,4 mmol, 0,12 g, solide) a été ajouté lentement pendant N2 éructations. Après agitation pendant 12 h, de l'eau (1 ml) a été ajoutée lentement à la seringue à température ambiante. Ensuite, du DMF (2 ml) a été ajouté et versé dans 500 ml d'acétone. Le polymère a été lavé cinq fois à l'acétone et récupéré par centrifugation. Le polymère poly(NVF-co -MOENVF-co -NVFazo) a été obtenu (0,29 g, rendement 43 %) après séchage sous vide à 30 °C pendant 12 h.
Mesures
La chromatographie d'exclusion stérique (SEC) a été réalisée à l'aide d'un système Chem NAV avec des étalons de polystyrène à 40 °C, équipé d'AS-2055, CO-2065, PU-2080, UV-2075 et RI-2031 (JASCO Corporation, Japon) . TSKgel SuperH4000 et TSKgel GMHXL (Tosoh Corporation, Japon) ont été connectés et le diméthylformamide (DMF) a été utilisé comme éluant. Résonance magnétique nucléaire du proton ( 1 Les spectres RMN H) ont été mesurés par JEOL JNM-ECX 400 (400 MHz). Transmission vs. la température a été contrôlée par UV-2600 (Shimadzu Corporation). La lumière UV (330 nm) a été irradiée par MAX-303 avec un filtre de 330 nm à une lampe au xénon de 300 W (ASAHI SPECTRA USA Inc.) pendant 10 min. Le DLS a été mesuré par le ZEN3600 Zetasizer Nano ZS (Malvern Instruments Ltd.) avec un laser He-Ne à 633 nm.
Résultats et discussion
Premièrement, 1 a été synthétisé par polymérisation radicalaire en utilisant AIBN. Le NVF et le MOENVF ont été copolymérisés dans du toluène à 60 °C et le produit a été purifié par reprécipitation avec de l'éther diéthylique. Le tableau 1 présente les données analytiques pour 1 et 2 . La partie insoluble a été filtrée et séchée sous vide, et une poudre blanche a été obtenue à un rendement de 59 % (tableau 1, essai 1). Ce résultat est cohérent avec les recherches antérieures [39]. 2 a ensuite été préparé par la réaction du polymère entre 1 et 1-bromoéthyl azobenzène avec NaH dans DMF. Les unités photosensibles d'azobenzène ont été introduites dans 1 avec synthèse de monomères. Le produit a été purifié par reprécipitation avec de l'acétone à un rendement de 42 % (tableau 1, essai 2). Ratios unitaires en 1 et 2 ont été calculés pour l'intensité intégrale de 1 Spectres RMN H (Fichier supplémentaire 1 :Figure S2). Unités de comonomère dans 1 correspond au taux d'alimentation de la polymérisation (NVF:MOENVF = 20:80). Comme estimé, 72 % des unités NVF dans le copolymère se sont converties en NVAazo, bien que toutes les unités de NVF n'aient pas réagi (16/22 unités ont été converties).
La figure 2 montre les traces SEC de 1 et 2 . La trace RI de 1 n'a qu'un seul large pic (Fig. 2a) ; cependant, la trace RI de 2 en a deux (Fig. 2b). Le pic à environ 9 min n'a pas été calculé car il était hors de la plage du poids moléculaire standard. De plus, la trace RI de 2 élargi tout autour. C'est probablement parce que 2 comprend diverses unités comonomères dans les copolymères, en raison de la réaction polymère entre 1 et azobenzène. Poids moléculaires de 1 et 2 montrés dans le tableau 1 ont été déterminés par SEC avec détecteur RI (Fig. 2a, b). Le poids moléculaire de 2 a été calculé uniquement à partir du pic latéral à faible poids moléculaire (Fig. 2b, 14,2 min) car le pic latéral à poids moléculaire élevé n'a pas pu être utilisé car il était trop élevé (Fig. 2b, 8,1 min). Généralement, la réaction du polymère pour la modification des substituants entraînerait une légère augmentation du poids moléculaire; cependant, nous avons reconnu le pic séparé de SEC dans la région de poids moléculaire très élevé (Fig. 2b).
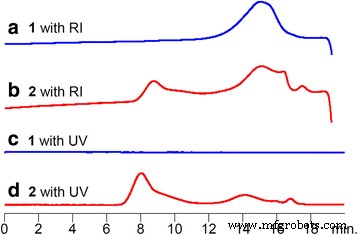
Traces SEC de 1 (un ) et 2 (b ) avec détecteur RI. SEC tracé de 1 (c ) et 2 (d ) avec détecteur UV à 500 nm
Afin de clarifier les pics de 2 en tant qu'unités d'azobenzène, traces SEC de 1 et 2 ont été observés à l'aide du détecteur d'absorbance UV de 500 nm (Fig. 2c, d). Naturellement, aucun pic n'a été détecté pour 1 (Fig. 2c) ; cependant, les pics pour 2 étaient apparentes par l'absorbance UV (Fig. 2d). La différence entre 1 et 2 est la présence ou l'absence des unités azobenzène. Par conséquent, tous les pics affichés par le détecteur UV pour 2 sont dérivés d'unités d'azobenzène. En fait, le détecteur RI pour 2 ont détecté des polymères à environ 0,5 min après avoir détecté l'absorbance UV. Le pic de 1 à environ 15 min détectée par la trace RI déplacée vers le côté de faible poids moléculaire après la réaction du polymère (Fig. 2b).
De plus, la distribution du poids moléculaire a été élargie de 3,8 à 4,8 (tableau 1, série 2). Ceci indique que le rapport d'introduction des unités azobenzène au copolymère a une large gamme. En bref, il a été estimé que la chaîne polymère de 2 (M n = 4000) possède quatre unités d'azobenzène, estimées par SEC et 1 RMN H. Fait intéressant, l'intensité maximale de 2 à environ 9 min détectées par UV (Fig. 2d) est beaucoup plus importante que celle détectée par RI (Fig. 2b), lorsqu'elles sont comparées au pic de 2 à environ 15 min. Compte tenu du fait que les unités d'azobenzène n'ont été détectées que par absorbance UV, cela suggère que la fraction de haut poids moléculaire (Fig. 2d, 8,1 min) est composée d'une sorte d'agrégat enrichi en azobenzène, probablement en raison des interactions π–π [40 ,41,42].
La figure 3 montre le facteur de transmission de la lumière pour les solutions aqueuses 1 et 2 contre la température pendant le processus de chauffage. La transmission lumineuse de 1 (copolymère hydrophile) était constante à toutes les températures. En comparaison, la transmission lumineuse de 2 décliné à haute température en raison de l'interaction hydrophobe dérivée de la chaîne polymère et/ou des unités azobenzène. En outre, les unités d'azobenzène ont été attirées non seulement par l'interaction hydrophobe, mais aussi par l'interaction π–π. En revanche, une différence de 10 % a été observée dans la transmission lumineuse de 2 entre 20 et 90 °C.
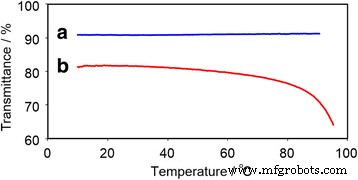
Dépendance à la température de la transmission lumineuse de solutions aqueuses à 0,2 % en poids de 1 (un ) et 2 (b ) dans les processus de chauffage
La figure 4 et le tableau 2 présentent les données DLS pour les tailles de nanoparticules avec une solution aqueuse à 0,2 % en poids à l'aide de 2 et UV irradiés 2 (2' ) à 20 et 60 °C. Les tailles de particules de 2 et 2' ont été observés :210 nm(2 à 20 °C), 250 nm(2 à 60 °C), et 330 nm(2' à 60 °C). La plus grande taille d'assemblage était de 2' à 60 °C. Pour 2' à 20 °C, l'assemblage n'a pas pu être observé car aucun des polymères n'était concentré ou les tailles d'assemblage n'étaient pas conformes à l'échelle. L'isomère de structure de cis - et trans -la configuration de l'azobenzène pourrait avoir une influence. Quand les unités d'azobenzène deviennent trans -configuration, leurs unités étaient probablement attirées par l'interaction π–π, et donc, les polymères comprenant des unités azobenzène se sont assemblés quelle que soit la température. Cependant, cis -configuration les unités d'azobenzène n'ont pas été agrégées peut-être à cause de l'interaction π–π plus faible à basse température. De plus, les deux 2 et 2' les pics de tailles d'assemblage à 60 °C étaient plus marqués que le pic de 2 à 20 °C. Les assemblages ont probablement été formés par interaction π–π entre les unités d'azobenzène et l'interaction hydrophobe des chaînes polymères et des unités d'azobenzène à 60 °C. Par conséquent, les assemblages de polymères ont été compressés avec une interaction hydrophobe. De plus, les tailles moyennes des nanostructures 2' étaient plus grands que 2 à environ 80 nm, indiquant que les assemblages de 2' étaient plus comprimées en raison de la différence de barrière stérique de l'isomère structurel cis-trans par rapport aux unités azobenzène. En revanche, des assemblages se sont formés entre des unités d'azobenzène à 20°C; ensuite, une variabilité des tailles d'assemblage de polymères a été observée, comme le large pic dans les données DLS. Tailles d'assemblage de 2 étaient de 40 nm différents entre 20 et 60 °C, ce qui correspondait au changement de transmission de la lumière.
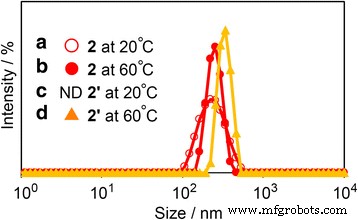
Données DLS de solutions aqueuses à 0,2 % en poids de 2 et UV irradiés 2 pour des montages de 15 min à différentes températures. 2 à 20 °C (a ) et à 60 °C (b ). UV irradié 2' à 20 °C (c ) et 60 °C(d )
Conclusions
1 a été synthétisé avec succès par polymérisation radicalaire en utilisant AIBN après un polymère photosensible et thermosensible de 2 a été obtenu. À l'avenir, la synthèse facile de polymères sensibles aux stimuli est réalisable et le développement accéléré de ces polymères est prévu. Surtout, un polymère multi-stimuli thermosensible et photosensible 2 a été agrégé dans des assemblages de quatre tailles par des stimuli thermiques et UV dans l'eau, qui ont été observés par mesure DLS. Nous supposons deux raisons :premièrement, les interactions hydrophobes entre les chaînes polymères et les motifs azobenzène se renforcent à mesure que la température augmente. Par conséquent, les tailles d'assemblage des polymères ont été modifiées en fonction de la température. Deuxièmement, la structure chimique était dérivée différemment de l'isomère structurel cis-trans des unités d'azobenzène lorsqu'elles étaient irradiées par UV. En résumé, l'interaction π–π entre les unités d'azobenzène était peu susceptible de disparaître et l'effet de l'encombrement stérique était diminué. En conséquence, le processus d'agrégation a été transmuté et les tailles d'assemblage étaient différentes. Plus précisément, les assemblages n'ont pas pu être observés car ni les polymères n'étaient rassemblés, ni les tailles d'assemblage n'étaient trop faibles lors de l'exposition aux UV irradiés à basse température. Il est révélé que les agrégations de 2 changé en plusieurs structures d'agrégation par la lumière UV et la température. Nous sommes motivés à utiliser ces structures agrégées et à obtenir un contrôle plus sensible de la taille de l'agrégation.
Abréviations
- AIBN :
-
Azobisisobutyronitrile
- LCST :
-
Abaisser la température critique de la solution
- MOENVF :
-
N -Méthoxyéthyle-N -vinylformamide
- NVFazo :
-
4-(2-N -Vinylformamide)éthoxyazobenzène
- PNVA :
-
Poly(N -vinylacétamide)
- PNVF :
-
Poly(N -vinylformamide)
- PNVIBA :
-
Poly(N -vinylisobutylamide)
Nanomatériaux
- Déplacement de votre système de contrôle industriel vers le sans fil
- Système de contrôle d'appareil basé sur la température utilisant LM35
- ISA publie un livre sur la sécurité et la fiabilité des systèmes de contrôle
- JMP Solutions obtient une nouvelle certification d'intégration de système de contrôle
- Sécuriser votre système de contrôle industriel
- Survivre à un projet de migration du système de contrôle
- Intégration du système de contrôle
- L'appareil rajeunit le système de contrôle hérité
- Comment atteindre une haute disponibilité dans les systèmes de contrôle modernes



