Comment gérer la vaporisation dans les systèmes d'échantillonnage

Comment gérer la vaporisation dans les systèmes d'échantillonnage
Jon Kestner
Il n'est pas facile de vaporiser un échantillon, et ce n'est pas toujours possible. Cependant, si l'analyseur de votre système d'échantillonnage analytique nécessite du gaz, mais que l'échantillon est liquide, la seule option consiste à convertir le liquide en gaz. Ce processus est appelé vaporisation ou vaporisation flash. L'objectif est de convertir un échantillon de tout liquide en vapeur instantanément sans en changer la composition.
Si vous procédez à la vaporisation, il est important de comprendre la différence entre l'évaporation et la vaporisation. L'évaporation se produit progressivement avec une augmentation de la température. La vaporisation se produit instantanément avec une chute de pression.
Il n'est pas possible de vaporiser un échantillon en augmentant la température. La chaleur provoque l'évaporation, et ajouter plus de chaleur accélère simplement l'évaporation. Dans un échantillon mixte, l'évaporation permettra à certains composés de s'évaporer avant d'autres, entraînant un fractionnement. La vaporisation, lorsqu'elle est effectuée correctement, garantit que tous les composés se vaporisent en même temps, préservant ainsi la composition de l'échantillon.
Les choses pourraient mal tourner lors de la vaporisation. Au lieu de transformer tout l'échantillon en vapeur, vous pourriez involontairement provoquer une combinaison de vaporisation et d'évaporation, entraînant un fractionnement. Une fois qu'un échantillon de composés mélangés se fractionne, il n'est plus adapté à l'analyse.
Avec le fractionnement, un scénario courant est que les molécules plus légères s'évaporent en premier et se dirigent vers l'analyseur, tandis que les molécules plus lourdes restent dans la phase liquide. Même si, à un stade ultérieur du processus, un échantillon fractionné semble être entièrement gazeux, le mélange n'aura pas les mêmes proportions moléculaires qu'avant le fractionnement. Il ne représentera plus avec précision le produit prélevé sur la ligne de traitement. L'ajustement des variables de processus (température, pression et débit) peut aider à garantir une vaporisation appropriée et un résultat analytique précis.
Comprendre la vaporisation
Pour vaporiser un échantillon, on utilise typiquement un régulateur de vaporisation, également appelé vaporisateur. Un vaporisateur est un régulateur de réduction de pression capable de transférer de la chaleur à l'échantillon au bon endroit. La vaporisation consiste en un processus en trois étapes, comme le montre le schéma ci-dessous. Tout d'abord, l'échantillon entre dans le régulateur de vaporisation sous forme liquide. À ce stade, le liquide ne doit pas bouillir.
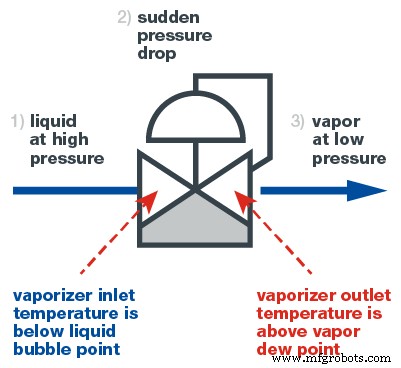
Deuxièmement, le liquide passe à travers la cavité de régulation dans le régulateur de vaporisation, ce qui entraîne une chute de pression sévère et soudaine vaporisant le liquide. En même temps, de la chaleur est appliquée, permettant au liquide vaporisé de rester sous forme de vapeur.
Troisièmement, l'échantillon, maintenant un gaz, sort du régulateur de vaporisation et se dirige vers l'analyseur pour être lu. En raison du passage immédiat à la phase vapeur, la composition du gaz est inchangée par rapport à celle du liquide, assurant une lecture précise.
Dans ce processus délicat, il existe de nombreuses variables ou intrants qui déterminent le succès ou l'échec. Pour les besoins de cette discussion, nous nous concentrerons sur deux principaux ensembles d'entrées.
Le premier ensemble d'entrées concerne la composition de l'échantillon. Selon sa composition, l'échantillon commencera à bouillonner et finira de se vaporiser à différentes pressions et températures. Nous aurons besoin de savoir quelles sont ces pressions et ces températures pour gérer avec succès le processus.
Le deuxième ensemble d'entrées concerne les paramètres que vous contrôlez dans votre système d'échantillonnage :pression, température et débit. La pression et la température sont contrôlées au niveau du vaporisateur, tandis que le débit est contrôlé en aval au niveau d'un rotamètre (débitmètre à section variable) et d'une vanne à pointeau. Ces entrées sont définies en fonction de ce que nous savons du premier ensemble d'entrées. Une bonne vaporisation nécessite un équilibre délicat de chaque apport. Même en abordant la vaporisation d'une manière systématique comme celle-ci, le processus nécessite quelques essais et erreurs.
Comprendre l'exemple
La meilleure façon de comprendre le premier ensemble d'entrées est d'utiliser un diagramme de phase. Un diagramme de phase trace la pression et la température, montrant à n'importe quelle paire de conditions si une substance sera vapeur, liquide ou solide. Les lignes indiquent les interfaces entre deux phases.
Le graphique ci-dessous représente un diagramme de phase pour 20 % d'hexane dans le pentane. Lorsque l'échantillon est au-dessus du point de bulle (ligne bleue), tout est liquide. L'échantillon doit être entièrement liquide lorsqu'il entre dans le vaporisateur. Lorsque le mélange est en dessous du point de rosée (ligne dorée), tout est vapeur. L'échantillon doit être entièrement vapeur lorsqu'il quitte le vaporisateur.
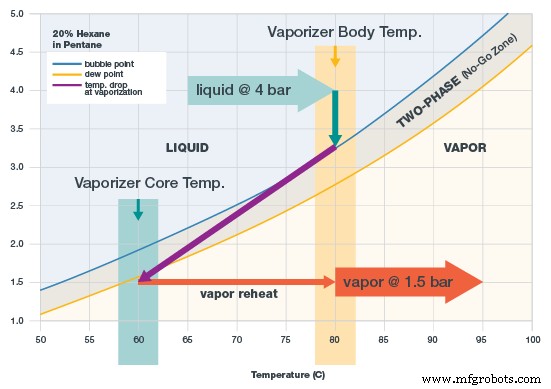
Diagramme de phase montrant 20 % d'hexane dans du pentane, avec réglages de température
Entre les lignes du point de bulle et du point de rosée se trouve la plage d'ébullition, ou «zone interdite» de l'échantillon. Ici, le mélange est en deux phases - une partie liquide et une partie vapeur. Une fois qu'un échantillon tombe dans cette plage, il est fractionné et ne convient plus à l'analyse.
Avec des échantillons purs et presque purs, il y a peu ou pas de plage d'ébullition. Les lignes de point de bulle et de point de rosée sont presque superposées l'une sur l'autre. Les échantillons purs et presque purs se convertiront en vapeur de même composition, que ce soit par évaporation ou vaporisation. Certains échantillons industriels approchent ce niveau de pureté et se convertissent facilement.
D'autre part, certains échantillons ont une plage d'ébullition si large qu'ils ne peuvent pas être vaporisés avec succès. Il n'y a aucun moyen de passer du côté liquide au côté vapeur de la plage d'ébullition. Les variables - température, débit et pression - ne peuvent pas être modifiées pour éviter le fractionnement.
La plupart des échantillons se situent entre ces deux extrêmes. Par exemple, dans le diagramme de phase de l'échantillon, la bande entre le point de bulle et le point de rosée est suffisamment étroite pour qu'avec les réglages appropriés, l'échantillon puisse effectivement passer du côté liquide au côté vapeur de la plage d'ébullition. En même temps, la bande est suffisamment large pour que les variables doivent être soigneusement modifiées pour éviter d'avoir un échantillon dans la plage d'ébullition.
Réglage de la température, de la pression et du débit
La vaporisation est un acte d'équilibre entre les variables. Ce qui suit est un processus en quatre étapes pour régler les entrées pour votre température, votre pression et votre débit.
- Déterminer la pression d'entrée au niveau du vaporisateur. Cette pression, qui est fixe, est la pression de process, à condition que le vaporiseur soit situé à proximité du robinet de prélèvement. Une pression plus élevée est préférable car elle permet une température de vaporisation plus élevée, sans faire bouillir le liquide entrant.
-
Régler la température d'entrée. Il y a deux objectifs lors du réglage de la température. Tout d'abord, la température doit être suffisamment basse pour que lorsque l'échantillon entre dans le vaporisateur, il soit entièrement liquide et ne bouillonne pas. Dans le diagramme de phase à 20 % d'hexane dans le pentane, le point de bulle à 4 bar est de 88 °C. Pour permettre une marge d'erreur dans le maintien de l'état liquide, choisissez 80°C.
Le deuxième objectif est que la température doit être suffisamment élevée pour contribuer à la vaporisation de l'échantillon. Lorsque vous vaporisez l'échantillon, la température chute, conformément aux lois de la conservation de l'énergie. La température de l'échantillon doit être suffisamment élevée au départ pour qu'après la chute de pression, l'échantillon ne soit pas dans la plage d'ébullition.
- Réglez la pression de sortie au niveau du vaporisateur. L'objectif est de faire chuter la pression en dessous de la ligne de point de rosée de l'or. Dans l'exemple de diagramme de phases, la pression de sortie est réglée sur 1,5 bar. Si la pression de sortie était plus élevée dans cet exemple, l'échantillon ne se vaporiserait pas entièrement et ne se fractionnerait pas.
- Définir le flux. Le débit est réglé en aval au niveau d'une vanne et d'un rotamètre, pas au niveau du vaporisateur. Dans un système d'échantillonnage, un débit de vapeur élevé est souhaitable car il déplace l'échantillon vers l'analyseur plus rapidement. Cependant, un débit élevé peut également être problématique, car il faut plus de chaleur pour vaporiser l'échantillon. En d'autres termes, un débit élevé entraîne une baisse de température plus importante au moment de la vaporisation. Dans l'exemple de diagramme de phase, la ligne violette illustre la chute de température. À mesure que le débit augmente, la ligne violette s'incline plus fortement vers la gauche.
Une autre variable influençant la chute de température est la capacité de transfert de chaleur du vaporisateur. Certains vaporisateurs sont construits de manière à ce que la chaleur soit transférée plus efficacement à l'échantillon. Lorsque l'échantillon liquide se transforme en vapeur et que sa température baisse, il tire la chaleur de l'acier inoxydable qui l'entoure. La question cruciale est de savoir avec quelle efficacité le vaporisateur peut remplacer cette chaleur et la maintenir dans l'échantillon. Plus l'échantillon peut tirer de chaleur, moins sa température chute pendant la vaporisation.
Dans certains cas, il est possible que le vaporisateur soit chaud au toucher à l'extérieur mais froid à l'intérieur. C'est parce que l'échantillon vaporisé attire beaucoup de chaleur et que le vaporisateur ne peut pas transférer suffisamment de chaleur pour suivre le rythme. La meilleure solution est de réduire le débit.
La vaporisation implique une certaine approximation. Les ingénieurs du service sur site Swagelok peuvent aider votre équipe à déterminer les vaporisateurs adaptés à votre système d'échantillonnage spécifique. En règle générale, maintenez le débit aussi bas que possible sans provoquer de retard inacceptable dans le temps de trajet de l'échantillon vers l'analyseur. Il est préférable de commencer avec un faible débit et d'essayer de l'augmenter plutôt que de commencer avec un débit plus élevé.
Dépannage
Les diagrammes de phase aident à approximer les réglages de température, de pression et de débit, mais un dépannage sera toujours nécessaire. Une mauvaise répétabilité des résultats de l'analyseur est une indication certaine d'un problème. Ci-dessous, nous évoquons deux possibilités lorsque l'échantillon se fractionne au lieu de se vaporiser, le problème n° 1 étant le plus courant :
Problème 1
Seule une partie de l'échantillon est vaporisée. Le liquide traverse le vaporisateur et reste dans la tubulure du côté aval. Finalement, il s'évapore et attire la chaleur du tube environnant, ce qui rend le tube froid au toucher ou provoque la formation de givre ou de glace. Le liquide en aval du vaporisateur peut passer au-delà de la zone du régulateur et dans d'autres composants, tels que les débitmètres et les filtres, où il peut causer des dommages considérables.
Solution n° 1
Pour résoudre ce problème, la meilleure option serait de réduire le débit. Une autre option serait d'abaisser la pression de sortie du vaporisateur, si cela est possible. Une troisième option serait d'augmenter la chaleur vers le régulateur, mais avec le risque supplémentaire de réduire la durée de vie du vaporisateur et de causer potentiellement le problème #2 (voir ci-dessous).
Problème 2
L'échantillon est en ébullition à l'entrée du vaporisateur. Il se fractionne avant de pouvoir être vaporisé. Un indicateur de ce problème est que le tube d'entrée du vaporisateur se contracte, parfois violemment, et que les valeurs de mesure oscillent. Les molécules plus légères s'évaporent et produisent un grand nuage de molécules de vapeur. Certaines de ces molécules plus légères passent à l'analyseur, donnant une analyse imprécise. Le reste crée un « mur de vapeur », qui repousse le liquide dans le processus. Une partie de ce mur de vapeur se refroidit et se condense. Enfin, l'échantillon liquide se déplace à nouveau vers le vaporisateur, où les molécules plus légères s'évaporent, recommençant le cycle à zéro. Finalement, les molécules les plus lourdes atteignent le vaporisateur et se dirigent vers l'analyseur donnant une analyse entièrement différente.
Solution #2
Pour résoudre ce problème, baissez la température du vaporisateur.
Conclusion
La vaporisation d'un échantillon liquide est un défi. Dans de nombreux systèmes d'échantillonnage à travers le monde, les vaporisateurs fractionnent constamment les échantillons et envoient des échantillons non représentatifs à l'analyseur. Vous pouvez augmenter considérablement vos chances de succès en utilisant un diagramme de phase du mélange particulier de composés de votre système. Vous pouvez encore augmenter votre taux de réussite en comprenant ce qui se passe dans le processus, plus précisément en connaissant les variables (température, pression et débit) et en comprenant leur rôle dans l'influence du résultat du processus. Avec ce cadre en place, vous pouvez atteindre les bons paramètres, en ajustant en fonction des signes et des symptômes que vous observez.
Technologie industrielle
- Comment les fabricants bénéficient de la convergence IT et OT
- Comment gérer un arrêt d'usine
- Comment les données permettent la chaîne d'approvisionnement du futur
- Comment gérer votre service achats à distance
- Comment fonctionnent les systèmes SCADA ?
- Comment atteindre une haute disponibilité dans les systèmes de contrôle modernes
- Comment utiliser l'IA de pointe pour mieux gérer votre entreprise
- Comment les directeurs d'usine peuvent-ils gérer efficacement leurs déchets ?
- Comment atténuer et gérer votre usine après un accident



