Substrat de carbone poreux améliorant les performances de détection des nanoparticules de cuivre vis-à-vis du glucose
Résumé
Un capteur précis pour déterminer rapidement la concentration de glucose est d'une importance significative pour la santé du corps humain, car le diabète est devenu une incidence très élevée dans le monde. Dans ce travail, des nanoparticules de cuivre logées dans des substrats de carbone poreux (Cu NP@PC), synthétisées par calcination des papiers filtres imprégnés d'ions cuivre à haute température, ont été conçues comme matériaux actifs d'électrode pour la détection électrochimique du glucose. Lors de la formation du carbone poreux, les nanoparticules de cuivre se sont spontanément logées dans les vides formés et ont constitué les composites à moitié recouverts. Pour l'oxydation électrochimique du glucose, les composites Cu NP@PC préparés présentent une activité catalytique bien supérieure avec une densité de courant de 0,31 mA/cm 2 au potentiel de 0,55 V en présence de 0,2 mM de glucose. Sur la base de l'activité d'oxydation électrochimique élevée, les présents composites Cu NP@PC présentent également une performance de détection du glucose supérieure. La sensibilité est déterminée à 84,5 μA /(mmol . L) avec une plage linéaire de 0,01 ~ 1,1 mM et une limite de détection basse (LOD) de 2,1 μmol/L. Comparé à celui des nanoparticules de cuivre supportées par du carbone non poreux (Cu NP/C), cela peut être justifié par le transfert de masse amélioré et l'effet synergique renforcé entre les nanoparticules de cuivre et les substrats de carbone poreux.
Introduction
Ces dernières années, le diabète a suscité une grande attention dans le monde entier, favorisant la détermination rapide et précise de la concentration de glucose [1]. Différentes techniques ont été développées [2]. Avec les avantages d'une utilisation facile, d'une réponse rapide et d'une sensibilité élevée, les méthodes électrochimiques sont particulièrement intéressantes pour la détection du glucose, et les matériaux actifs des électrodes sont de la plus haute importance pour les capteurs [3, 4]. Jusqu'à présent, les matériaux rapportés avec une bonne activité de réponse au glucose incluent les métaux nobles (or [4], argent [5], platine [6], palladium [7]), les métaux non nobles (cuivre [8], nickel [9] ), les oxydes métalliques (oxyde de zinc [10], oxyde de manganèse [11], oxyde de nickel [12], oxyde de fer [13]) et les matériaux carbonés (nanotubes de carbone [14], nanodots de carbone [15], carbone mésoporeux [16 ]), etc. Parmi ces matériaux, les composites à base de cuivre présentent un grand potentiel pour la construction d'une plate-forme de détection efficace du glucose, en raison du faible coût [3], de la bonne conductivité électrique [17], de la surface spécifique contrôlée. Pendant ce temps, il est rapporté que les performances électrochimiques des matériaux à base de cuivre seront considérablement améliorées en formant des composites avec des substrats carbonés tels que le graphème [18, 19], les nanofibres de carbone [20], les nanotubes de carbone [21] et les carbones mésoporeux [22] . Par exemple, Zhang et al. préparé les nanoparticules de cuivre sur des composites de graphène induits par laser et développé avec succès un biocapteur ampérométrique de glucose flexible sans enzyme. Bénéficiant de sa simplicité et de sa haute sensibilité, le capteur devait être utilisé dans des biocapteurs portables ou implantables [23]. En utilisant la méthode de décharge à l'arc, les matériaux composites de CuO et de nanotubes de carbone à paroi unique ont été synthétisés par le groupe de Wang. Le réseau hautement conducteur facilité par les nanotubes de carbone a conduit à une sensibilité élevée et une bonne sélectivité dans la détection du glucose [21]. En raison de la bonne conductivité des nanofils de cuivre et du transfert rapide des électrons dans les couches d'oxyde de graphène réduit (rGO) bidimensionnelles, Ju et al. synthétisé un composite de nanofils de cuivre unidimensionnels et de nanofeuilles rGO bidimensionnelles, montrant une sensibilité de 1625 \(\upmu\)A/(mM·cm 2 ) et une limite de détection de 0,2 \(\upmu\)M pour la détection du glucose [3]. Les nombreuses améliorations des performances des matériaux à base de cuivre ont été obtenues, cependant, elles ne suffisent toujours pas pour les applications réelles des appareils portables. Cela signifie qu'il est nécessaire de rechercher de nouveaux modèles ou correspondances pour les nanoparticules de cuivre.
Avec la structure de charpente tridimensionnelle spéciale [24], les carbones poreux possèdent non seulement des sites de liaison abondants pour favoriser la dispersion des centres actifs métalliques, mais fournissent également une plus grande surface spécifique qui améliore l'accessibilité des électrons et des substances réactives [25,26 ,27]. Ces dernières années, les carbones poreux ont été reconnus comme un type de matériaux de modification et de substrat prometteurs, qui peuvent grandement améliorer l'activité de détection électrochimique des matériaux métalliques. Par exemple, Li et al. étudié les composites de Co7 Fe3 nanoparticules d'alliage noyées dans des nanofeuillets de carbone poreux (Co7 Fe3 /NPCSs). Les résultats ont montré une gamme linéaire très large pour la détection du glucose (de 0,001 à 14,00 mM), en raison de l'effet nanoconfiné du carbone poreux [28]. En utilisant les structures métallo-organiques (MOF) comme modèles auto-sacrificiels pour préparer des matériaux de carbone poreux, les nanoparticules de nickel intégrées sur des nanotiges de carbone nanoporeuses préparées par Jia et al. ont présenté de bonnes propriétés de détection du glucose avec des temps de réponse rapides (moins de 1,6 s) [29]. Song et al. construit un composite (Cu@C-500) constitué d'un lit de carbone poreux de nanoparticules de cuivre uniformément intégré en utilisant Cu MOF comme matière première. En raison de la porosité hiérarchique, il présentait une sensibilité élevée et une limite de détection faible, et présentait un grand potentiel dans les dispositifs de capteur de glucose [30]. Par conséquent, avec les effets structurels et électroniques uniques, le matériau de carbone poreux devrait être un excellent partenaire pour améliorer davantage les performances électrochimiques des nanomatériaux de cuivre dans la détection du glucose.
Ici, dans ce travail, les composites de nanoparticules de cuivre logées dans des substrats de carbone poreux ont été conçus et synthétisés en calcinant les papiers filtres bon marché imprégnés d'ions de cuivre à haute température. Au cours du processus de synthèse, la formation de carbone poreux et l'accommodation de nanoparticules de cuivre se sont produites simultanément, ce qui peut être démontré par microscopie électronique à balayage et microscopie électronique à transmission. Pour les mesures électrochimiques, les résultats montrent que les échantillons préparés (Cu NP@PC) présentent une activité électrocatalytique élevée pour l'oxydation du glucose avec la densité de courant de 0,31 mA/cm −2 au potentiel de 0,55 V en présence de 0,2 mM de glucose, ce qui est bien meilleur que celui du Cu NP/C. Pour la détection du glucose, la sensibilité est déterminée à 84,5 μA (mmol/L) −1 et la limite de détection est calculée à 2,1 μmol/L, bien supérieure à celles de la plupart des matériaux rapportés précédemment. De plus, la bonne sélectivité des matériaux présents a également été démontrée par l'expérience anti-interférence.
Expérimental
Réactifs
Nitrate de cuivre (Cu(NO3 )2 ·3H2 O, AR), éthanol (C2 H5 OH, 99,8%), glucose (C6 H12 O6 , 96%), urée (CH4 N2 O, AR, 99%), acide citrique (C6 H8 O7 , AR, 99,5 %), acétate d'ammonium (CH3 COONH4 , AR), chlorure de sodium (NaCl, AR, 99,5 %), hydroxyde de potassium (KOH, AR, 85 %). Tous les réactifs mentionnés ci-dessus ont été achetés chez Aladdin. La solution de Nafion D520 à 5 % obtenue auprès de DuPont et le papier filtre ont été achetés auprès de Hangzhou Fuyang BEIMU Pulp Co., Ltd. Papier carbone auprès du papier carbone conducteur Toray du Japon (TGP-060). L'eau utilisée dans l'ensemble de l'expérience est ultrapure avec une conductivité de 18,25 MΩ⋅cm.
Instruments
Les spectres de diffraction des rayons X (XRD) ont été obtenus à partir du diffractomètre à rayons X sur poudre polyvalent X'Pert PRO MPD. Spectres infrarouges à transformée de Fourier (FT-IR) dans la plage de 1000 à 4000 cm −1 ont été enregistrés à partir du spectromètre IS50 FT-IR. Les spectres Raman ont été mesurés dans le système inVia Qontor (Renishaw, Royaume-Uni) à une longueur d'onde de 532 nm. Les mesures de spectroscopie photoélectronique aux rayons X (XPS) ont été effectuées sur un spectromètre Thermo ESCALAB 250XI fonctionnant à 120 W. Les morphologies de l'échantillon ont été caractérisées par un microscope électronique à balayage (MEB) Hitachi S4800 avec une tension d'accélération de travail de 20 kV. Les images de microscopie électronique à transmission (MET) ont été collectées à partir du Tecnai G2 F20. Les mesures de Brunauer-Emmett-Teller (BET) ont été effectuées sur l'appareil d'adsorption physique à surface spécifique (ASAP2020M).
Synthèse de Cu NP@PC et Cu NP/C
Typiquement, la synthèse de Cu NP@PC a été complétée par une pyrolyse à haute température en deux étapes. Tout d'abord, les papiers filtres commerciaux ont été prétraités à 250 °C pendant 1 h dans un four tubulaire sous atmosphère d'azote. Ensuite, un morceau de papier filtre jaune pâle traité d'une taille de 10 mm \(\times\) 50 mm a été trempé dans une solution de nitrate de cuivre transparent bleu avec une concentration de 0,1 M, et a été retiré après 10 min. Après séchage à température ambiante, le papier filtre a été placé dans une nacelle en porcelaine propre et traité successivement à 180 °C, 240 °C, 900 °C pendant 2 h, 2 h et 1 h dans un four tubulaire sous protection à l'azote, respectivement. . Enfin, le produit Cu NP@PC a été collecté lorsque le système a été refroidi à température ambiante, et a été broyé avant les tests électrochimiques. Pour les échantillons témoins, la synthèse de Cu NP/C et de carbone pur a été réalisée par la même procédure, sauf que la concentration de nitrate de cuivre était respectivement de 0,2 M et 0 M.
Mesures électrochimiques
Dans ce travail, tous les tests électrochimiques ont été effectués sur un poste de travail électrochimique CHI 760E avec un système standard à trois électrodes à température ambiante. Avant l'expérience, plusieurs morceaux de papier carbone (5 mm x 5 mm) servant de collecteurs de courant ont été rincés avec de l'eau, de l'éthanol et séchés pendant une nuit à 60 °C. Pour la préparation de l'encre catalytique, un échantillon de 10 mg (Cu NP@PC, Cu NP/C ou poudres de carbone pur) a été mélangé avec de l'éthanol, de l'eau et une solution de Nafion (5%) dans une certaine proportion de 10:10:1 à former une dispersion uniforme. Ensuite, l'encre catalyseur de 40 L a été déposée sur un papier carbone propre avec une charge de 1,6 mg/cm 2 , qui a été utilisé comme électrode de travail. Une électrode Ag/AgCl (KCl saturé) et une tige de graphite ont été utilisées comme électrode de référence et contre-électrode, respectivement. Pour les expériences électrochimiques, la voltamétrie cyclique et la voltamétrie à balayage linéaire ont été adoptées pour examiner qualitativement les performances potentielles du matériau préparé pour l'oxydation du glucose. La chronoampérométrie a été utilisée pour évaluer quantitativement les performances de détection du matériau préparé. Dans l'ensemble du processus, une solution de KOH 0,1 M a été sélectionnée comme électrolyte.
Résultats et discussion
Comme le montre la figure 1a, pour la synthèse des matériaux cibles, le traitement de préchauffage a permis d'éliminer les impuretés instables et l'humidité du papier filtre avec la couleur passant au jaune clair. Ensuite, pour supporter les nanoparticules métalliques, les papiers filtres traités ont été infiltrés dans la solution d'ions cuivre. Au cours du processus de calcination à haute température dans un four tubulaire, des atomes de cuivre et de minuscules cristallites se sont formés. Parce que le taux de nucléation et de croissance des nanoparticules de cuivre est inférieur au taux de pyrolyse du carbone, ces microcristaux de cuivre initiaux peuvent catalyser la décomposition et l'évaporation du carbone, conduisant à la formation de trous [31]. Enfin, les échantillons Cu NP@PC brun-noir ont été préparés. Notez que la concentration excessive d'ions cuivre augmentera le taux de nucléation, provoquant la formation de matériaux carbonés non poreux. Pour identifier les composants de l'échantillon préparé, des diagrammes de diffraction des rayons X (XRD) ont été collectés, comme le montre la figure 1b. Les échantillons Cu NP@PC et Cu NP/C présentent les pics de diffraction du cuivre et du carbone. Les trois pics caractéristiques aigus situés à des angles de diffraction de 43,2°, 50,3° et 73,9° peuvent être respectivement attribués aux plans de réseau de (111), (200) et (220) des nanoparticules de cuivre (PDF#04-0836) [32, 33]. Le pic large avec le centre autour de 25° correspond à la face cristalline (002) du carbone graphitisé, qui favorisera le transport des électrons dans les réactions électrochimiques ultérieures [3, 25, 34]. Pour analyser les compositions spécifiques du carbone, les spectres Raman de Cu NP@PC et Cu NP/C ont été collectés. Comme le montre la figure 1c, la bande D et la bande G peuvent être déterminées sans ambiguïté par le pic autour de 1350 cm −1 et 1600 cm −1 , respectivement [35]. Comme indiqué, la bande G est causée par le mouvement relatif de sp 2 atomes de carbone, tandis que la bande D est liée au mode de respiration des anneaux de carbone [36]. Ici, le rapport de bande D/G calculé de Cu NP@PC était de 0,899, le même avec la valeur de Cu NP/C. Par conséquent, la distribution du carbone amorphe et du graphite nanocristallin est similaire dans deux échantillons. Cela indique presque les mêmes composants de deux matériaux préparés, c'est-à-dire que Cu NP@PC et Cu NP/C sont constitués de nanoparticules de cuivre et de charpentes de carbone. Pour révéler davantage les informations sur la microstructure, les spectres FTIR de Cu NP@PC et Cu NP/C ont été étudiés. Comme présenté sur la Fig. 1d, on peut voir que les signaux situés à 1734 cm −1 et 1628 cm −1 apparaissent dans Cu NP@PC qui peuvent être attribués à la vibration d'étirement de C=O [39] et à la vibration d'étirement de C–O [40]. Par rapport au Cu NP/C, la bande à 2363 cm −1 du Cu NP@PC est attribué au dioxyde de carbone dans l'air. Une légère bande d'absorption a été observée à 3466 cm −1 du Cu NP@PC et du Cu NP/C pourraient être attribués à la vibration d'étirement de la liaison O-H dans la molécule d'eau [37].
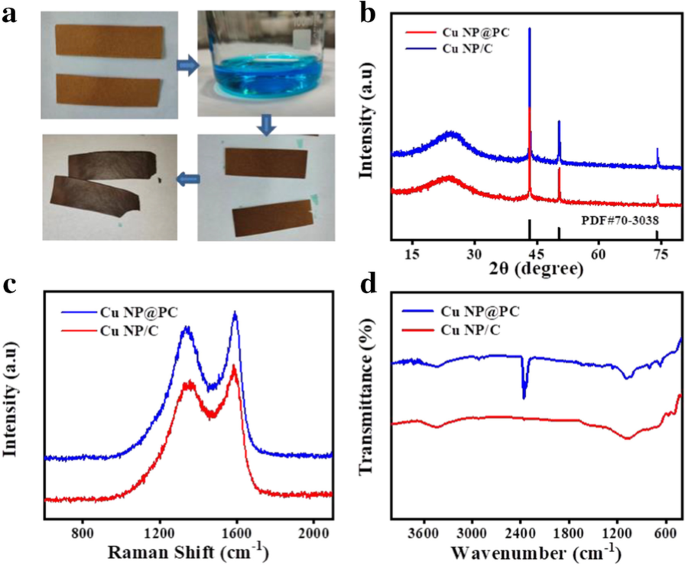
un Illustration schématique de la préparation d'échantillons de Cu NP@PC et Cu NP/C; b Le diagramme de diffraction des rayons X (XRD) de Cu NP@PC et Cu NP/C ; c spectres Raman de Cu NP@PC et Cu NP/C; et d Spectres FTIR de Cu NP@PC et Cu NP/C
Pour observer les morphologies et les structures des matériaux préparés, des expériences au microscope électronique à balayage (MEB) ont été menées. Pour l'échantillon Cu NP@PC, l'image SEM de la figure 2a montre que des trous abondants sont répartis de manière aléatoire à la surface de la couche de carbone et que les nanoparticules de cuivre résident simplement dans ces trous. La figure 2b montre que presque toutes les nanoparticules de cuivre sont à moitié à l'intérieur et à moitié à l'extérieur. Comme il est rapporté, la réaction électrochimique implique généralement un transport d'électrons et de masse. Ainsi, la moitié à l'intérieur sera propice au transfert d'électrons avec le substrat carboné, tandis que la moitié à l'extérieur pourra agir comme des sites actifs, interagissant avec les substances. Cela améliorera à terme l'efficacité des réactions électrochimiques. Sur la figure 2c, aucun carbone poreux n'a été trouvé et toutes les nanoparticules de cuivre sont supportées à la surface du carbone dans l'échantillon Cu NP/C. Certaines agglomérations se sont même produites sur la figure 2d. De plus, la taille des nanoparticules de cuivre de deux échantillons était respectivement de 0,406 et 0,398 µm, sur la base d'une centaine de nanoparticules métalliques. Ainsi, la taille des nanoparticules de cuivre cultivées sous deux concentrations différentes d'ions cuivre n'est pas très différente, ce qui indique que l'augmentation de la concentration d'ions cuivre ne peut contrôler que la morphologie du carbone. De plus, on peut voir à partir de l'image MET de la figure 2e que les nanoparticules de cuivre agrandies ont une taille similaire à ces trous et partiellement encapsulées dans ceux-ci, indiquant à nouveau que la formation réussie des composites cibles. Pour révéler davantage les propriétés poreuses des matériaux préparés, les isothermes d'adsorption d'azote de Cu NP@PC et Cu NP/C ont été étudiées. Comme le montre la figure 2f, la surface BET calculée des nanomatériaux Cu NP@PC était de 309,95 m 2 /g, bien supérieur à celui de Cu NP/C. Ceci est cohérent avec les résultats du SEM et du TEM.
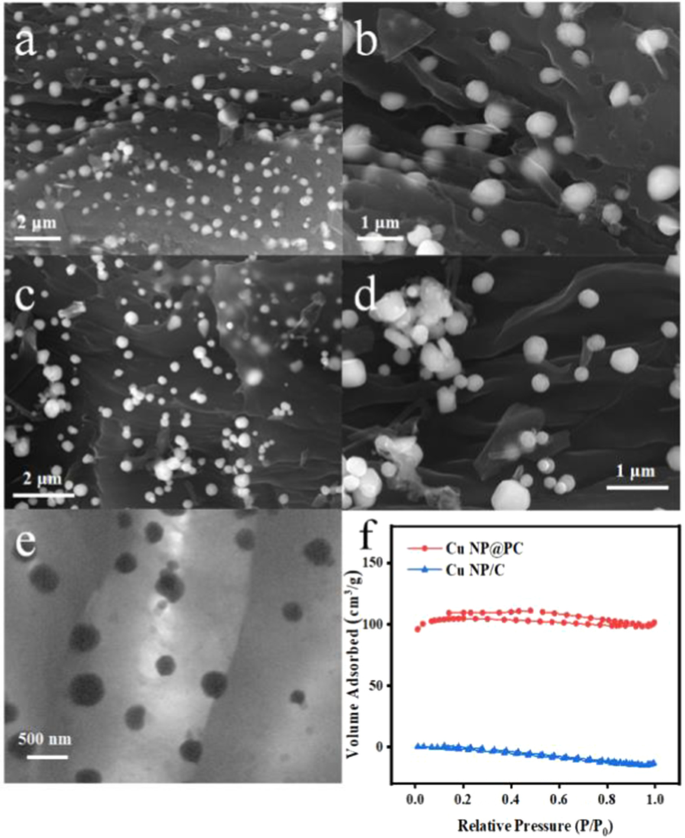
un , b Les images au microscope électronique à balayage (MEB) de Cu NP@PC à différents grossissements ; c , d Les images au microscope électronique à balayage (MEB) de Cu NP/C à différents grossissements ; e L'image en microscopie électronique à transmission (MET) de Cu NP@PC ; et f Analyse de surface Brunauer–Emmett–Teller (BET) de Cu NP@PC et Cu NP/C
Pour étudier la structure électronique des échantillons, une spectroscopie photoélectronique à rayons X (XPS) a été réalisée. Les figures 3a et b affichent les spectres de relevé XPS complets de Cu NP@PC et Cu NP/C, respectivement, qui montrent l'existence de Cu, C et O. Pour l'élément Cu, la figure 3c présente le Cu 2 déconvolué p Spectres XPS des Cu NP@PC et Cu NP/C. Les deux signaux ont été produits aux mêmes positions de pic, suggérant la même composition de deux échantillons. Deux pics évidents à 952,5 eV et 932,8 eV sont attribués au Cu 2p 3/2 et Cu 2p 1/2 de Cu (0), suggérant la présence de cuivre métallique [38]. Les énergies de liaison à 953,7 eV et à 934,8 eV sont attribuées au Cu 2p 3/2 et Cu 2p 1/2 du Cu(II)[39,40,41]. La présence de Cu(II) peut également être confirmée par des pics satellites faibles à 944,2 eV et 941,4 eV[10]. A partir des pics d'ajustement correspondant à Cu(0) et Cu(II), les rapports de Cu(0)/Cu(II) dans Cu NP@PC et Cu NP/C sont estimés à 2,2 et 1,8, respectivement. Cela peut s'expliquer par le fait que les atomes de cuivre de surface dans Cu NP@PC ne sont pas faciles à oxyder en raison de l'encapsulation d'une couche de carbone poreuse. Pendant ce temps, davantage d'atomes de cuivre métalliques peuvent jouer un rôle important pour la détection du glucose. Pour les C1s spectre des deux échantillons de la Fig. 3d, trois signaux situés à 289 eV, 286 eV et 284,8 eV correspondent respectivement aux C=O, C–O, C–C/C–H, indiquant l'existence de groupes fonctionnels tels que le groupe carboxyle [42, 43] et en accord avec les résultats du FTIR.
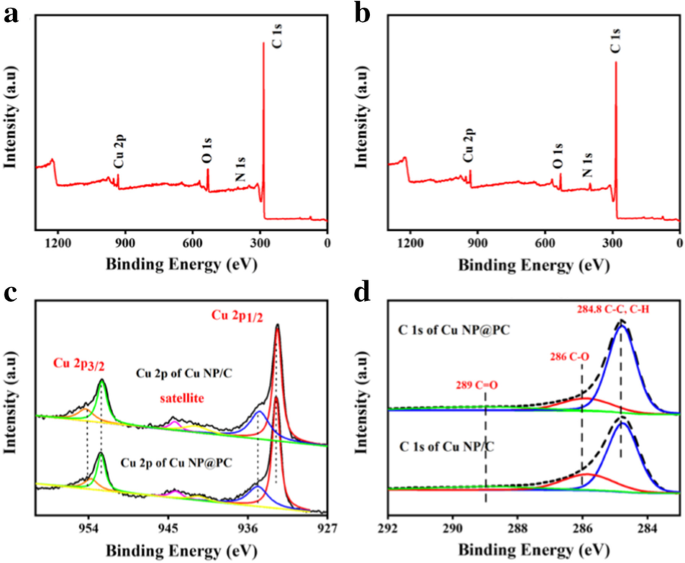
un Spectre de relevé XPS de Cu NP@PC ; b Spectre de relevé XPS de Cu NP/C; c Cu 2p spectres XPS de Cu NP@PC et Cu NP/C; et d Spectres C 1 XPS de Cu NP@PC et Cu NP/C
Sur la base des avantages du carbone poreux, les propriétés de détection électrochimique de Cu NP@PC et Cu NP/C vis-à-vis du glucose ont été étudiées dans une solution de KOH 0,1 M. Le matériau de carbone pur sans nanoparticules de cuivre est utilisé comme échantillon de référence. Comme le montre la figure 4a, les courbes voltamétriques cycliques (CV) montrent la plus grande réponse de courant de Cu NP@PC avec la présence de 0,2 mM de glucose dans l'électrolyte, par rapport à celle de Cu NP/C et de l'échantillon de carbone pur. Plus précisément, la densité de courant de 0,31 mA/cm −2 a été obtenu au potentiel de 0,55 V. Cela indique que le Cu NP@PC préparé est le meilleur catalyseur pour l'oxydation du glucose, ce qui peut être raisonnable par sa propre structure poreuse. Comme il est rapporté, la porosité peut favoriser le transport de masse [29]. Ici, pour démontrer le transport de masse amélioré, l'effet des taux de balayage sur l'oxydation du glucose a été étudié sur une électrode modifiée Cu NP@PC. Comme le montre la figure 4b, la densité de courant augmente selon un gradient avec la vitesse de balayage passant de 20, 40, 60 à 80 mV/s. La figure 4c montre la courbe d'ajustement entre la densité de courant (J p ) et la racine carrée du taux de balayage (v 1/2 ). La relation linéaire peut être exprimée comme :J p = 0.00254 v 1/2 − 0,00359 (coefficient de corrélation :R 2 = 0.995), indiquant un processus contrôlé par la diffusion de l'oxydation du glucose sur l'électrode modifiée Cu NP@PC [44]. De plus, sur la figure 4d, les spectres d'impédance électrochimique (EIS) montrent que la résistance de transfert de charge de Cu NP@PC est inférieure à celle de Cu NP/C. Par conséquent, en combinant le transport de masse favorisé et le processus de transfert d'électrons amélioré, l'oxydation catalytique du glucose sur l'électrode modifiée Cu NP@PC peut être esquissée sur la figure 4e. Le Cu(II) a d'abord été oxydé en Cu(III), qui a ensuite accepté un électron et a été réduit en Cu(II). Au cours de ce processus, la molécule de glucose a donné un électron et a été oxydée en gluconolactone. Bénéficiant de la porosité des matériaux, la gluconolactone formée peut être rapidement transférée dans la solution puis hydrolysée en acide gluconique [3, 45].
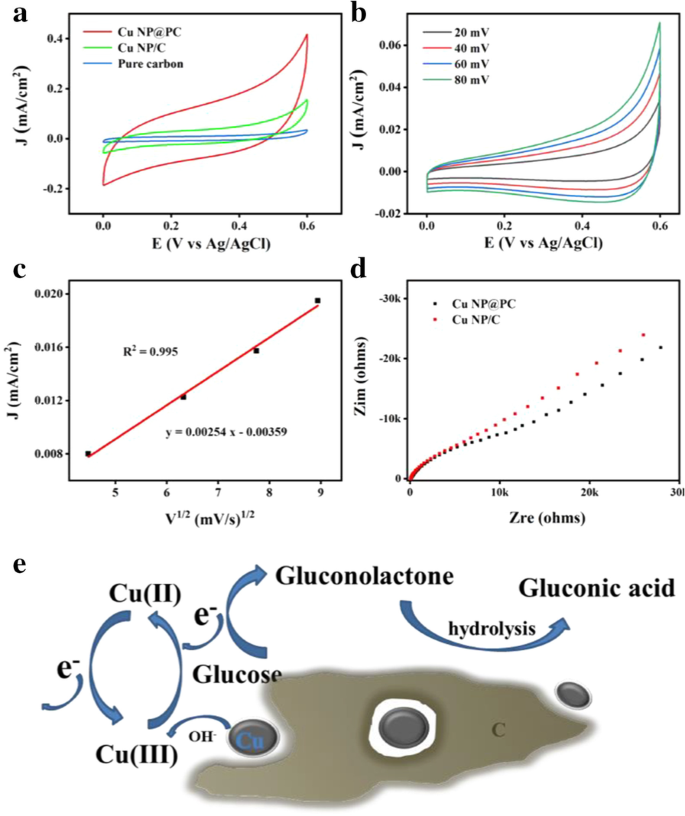
un Courbes CV de Cu NP@PC, Cu NP/C et échantillon de carbone pur pour la réaction d'oxydation du glucose ; (0,2 mM de glucose, 0,1 M de KOH, vitesse de balayage :100 mV/s.) b Courbes CV de Cu NP@PC dans 0,1 M KOH à différentes vitesses de balayage (20, 40, 60, 80 mV/s) ; c Tracé de la densité de courant à 0,4 V par rapport à la racine carrée de la vitesse de balayage ; d Les spectres d'impédance électrochimique de Cu NP@PC et Cu NP/C; et e Le schéma de principe du mécanisme de conversion du glucose sur le Cu NP@PC
Selon les performances d'oxydation catalytique électrochimique supérieures, les performances de détection potentielles de Cu NP@PC vis-à-vis du glucose ont été examinées. Pour étudier qualitativement la réponse actuelle de Cu NP@PC vis-à-vis de la concentration de glucose, une voltamétrie cyclique a été réalisée aux concentrations de 2, 4, 6, 8 et 10 mM. Comme le montre la figure 5a, la densité de courant de l'électrode modifiée par Cu NP@PC augmente progressivement avec l'augmentation de la concentration de glucose, suggérant l'excellente performance de détection potentielle. Pour révéler de manière quantitative les propriétés de détection du glucose de Cu NP@PC, la chronoampérométrie (I-t) a été réalisée et le potentiel de 0,55 V a été choisi. Comme le montre la figure 5b, la densité de courant provenant de l'électrode modifiée par Cu NP@PC augmente progressivement avec la concentration en glucose passant de 0,01 à 1,1 mM. À partir des courbes I-t, sur la figure 5d, la courbe d'étalonnage ajustée entre les concentrations de glucose et les courants de réponse peut être exprimée comme suit :y = 0.3378 x + 0,0077 (coefficient de corrélation :R 2 = 0.997). Pendant ce temps, la sensibilité a été déterminée à 84,5 μA (mmol/L) −1 . D'après la formule de LOD = 3σ /q [46] (σ fait référence à l'écart type de la réponse à blanc et q est la pente de cette courbe de régression linéaire), la limite de détection a été calculée à 2,1 mol/L. Ces deux indices sont bien meilleurs que ceux de la plupart des rapports précédents, comme le montre la figure 6b [47,48,49,50,51,52]. À titre de comparaison, la densité de courant de la courbe I-t de l'électrode modifiée par Cu NP/C montre également un changement de gradient avec l'augmentation de la concentration de glucose, comme le montre la figure 5c. Cependant, l'ampleur du changement a été considérablement réduite. Comme le montre la figure 5d, la courbe linéaire d'ajustement entre les concentrations de glucose et le courant de réponse était représentée par :y = 0.007 x + 0.0017 (coefficient de corrélation R 2 = 0.998). La sensibilité était de 1,75 μA (mmol/L) −1 et la limite de détection a été estimée à 10 μmol/L. Par conséquent, par rapport aux résultats de Cu NP/C, les performances de détection de l'échantillon Cu NP@PC ont également été améliorées par le substrat de carbone poreux.
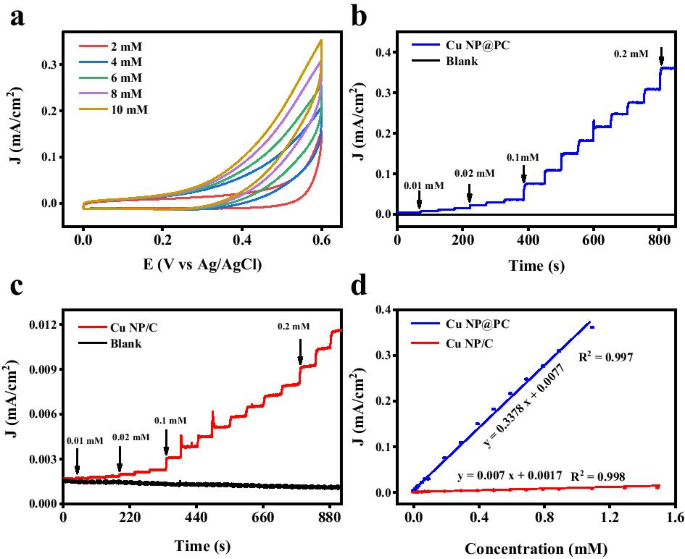
un Courbes CV de Cu NP@PC dans 0,1 M KOH avec présence de glucose à différentes concentrations de 2, 4, 6, 8 et 10 mM. Taux de balayage :100 mV/s; b Les réponses ampérométriques de Cu NP@PC lors de l'ajout successif d'une solution de glucose dans 0,1 M KOH à 0,55 V (vs Ag/AgCl); c Les réponses ampérométriques de Cu NP/C lors de l'ajout successif d'une solution de glucose dans 0,1 M KOH à 0,55 V (vs Ag/AgCl); et d Les courbes d'étalonnage correspondantes du Cu NP@PC et du Cu NP/C pour la détection du glucose. Les barres d'erreur ont été obtenues sur la base de trois répétitions de l'expérience
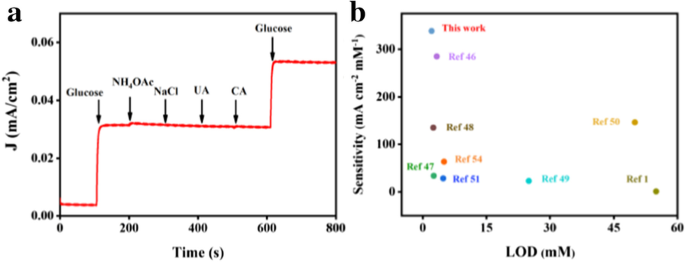
un Les courants de réponse de Cu NP@PC après injection de solution de glucose 0,01 mM, acétate d'ammonium 0,01 mM (NH4 OAc), 0,01 mM de chlorure de sodium (NaCl), 0,01 mM d'urée (UA), 0,01 mM d'acide citrique (CA), respectivement ; et b La compassion du LOD et la sensibilité entre Cu NP@PC et les matériaux précédemment rapportés
Comme on le sait, la capacité anti-interférence est un autre facteur clé pour évaluer les performances de détection des matériaux. Dans ce travail, pour étudier la sélectivité de l'électrode modifiée par Cu NP@PC vis-à-vis du glucose, plusieurs substances interférentes dont l'acétate d'ammonium (NH4 OAc), chlorure de sodium (NaCl), urée (UA), acide citrique (AC) à la concentration de 0,01 mM ont été choisis et injectés successivement dans l'électrolyte [53]. De toute évidence, les changements de densité de courant provoqués par les substances interférentes peuvent être négligeables. Ce n'est que lorsque 0,01 mM de glucose a été injecté que la densité de courant a augmenté de manière significative quelles que soient les interférences ci-dessus, comme le montre la figure 6a. De plus, en utilisant l'urine comme substrat, ce système proposé peut encore réaliser la détection de sensibilité du glucose, comparable au papier test commercial (Fichier supplémentaire 1 :Figure S3 et S4). Par conséquent, les matériaux Cu NP@PC possèdent une excellente capacité d'oxydation catalytique électrochimique et de détection du glucose.
Conclusion
Un composite constitué de nanoparticules de cuivre et de substrats de carbone poreux a été conçu et synthétisé par calcination des papiers filtres commerciaux imprégnés d'ions de cuivre. Avec les avantages de la porosité, le Cu NP@PC préparé a montré une excellente capacité pour l'oxydation et la détection électrochimiques du glucose. La sensibilité a été déterminée à 84,5 μA mM −1 et la limite de détection a été calculée à 2,1 M, ce qui est bien supérieur à ceux de la plupart des rapports précédents. De plus, l'électrode modifiée Cu NP@PC présentait également une bonne sélectivité pour le glucose. Par conséquent, le composite préparé dans ce travail fournira non seulement un nouveau candidat pour la construction de capteurs de glucose portables, mais également une nouvelle idée pour la préparation de matériaux carbonés poreux.
Disponibilité des données et des matériaux
Les données et les conclusions de ce travail sont toutes présentées dans cet article.
Abréviations
- LOD :
-
Limite de détection
- rGO :
-
Oxyde de graphène réduit
- MOF :
-
Charpente métallo-organique
- XRD :
-
Diffraction des rayons X
- SEM :
-
Microscope électronique à balayage
- TEM :
-
Microscopie électronique à transmission
- PARI :
-
Brunauer–Emmett–Teller
- XPS :
-
Spectroscopie photoélectronique aux rayons X
- CV :
-
Courbes voltampérométriques cycliques
- I-t :
-
Chronoampérométrie
- UA :
-
Urée
- CA :
-
Acide citrique
Nanomatériaux
- Comment améliorer les performances de l'alliage de cuivre tungstène ?
- Les nanotubes de carbone repoussent les limites de l'électronique flexible
- En accord avec le cœur d'un atome de cuivre
- Ocean Carbon imagé à l'échelle atomique
- Les avantages d'une prothèse en fibre de carbone
- Les performances de la fibre de verre
- Détection photo-électrochimique améliorée de l'acide urique sur une électrode de carbone vitreuse modifiée par nanoparticules d'Au
- Améliorer la précision et les performances de votre machine de découpe au jet d'eau
- Les propriétés antimicrobiennes du cuivre



